基團貢獻法估算離子液體的摩爾電導率1
張瑞雪,楊代瓊,趙 楠,2,李茂寬,焦夢青
(1.河北地質大學水資源與環境學院,河北 石家莊 050031;2.河北省水資源可持續利用與開發實驗室,河北 石家莊 050031)
離子液體(ILs)是由較大體積的有機陽離子和較小體積的無機或有機陰離子組成的,在小于100 ℃的溫度下呈液態的物質。常見的離子液體陽離子通常有咪唑離子、吡啶離子、季銨離子、季鏻離子等;常見的陰離子通常有六氟磷酸鹽、四氟硼酸鹽、硫酸鹽等。離子液體,作為一類特殊的離子化合物,具有電導率高、蒸氣壓低、電化學窗口寬、穩定性好等諸多特性[1]。通過組合不同的陰、陽離子和支鏈,離子液體可“按需”設計具有特定功能,以滿足不同應用領域的需要。而想要獲得具有特定功能的離子液體,必須先要獲得離子液體的物性數據,研究其構效關系,進而設計出合適的結構。
電導率是離子液體電化學應用的重要指標之一。只有在較高電導率的情況下,離子液體才能達到較高的電流密度,從而保證電解經濟性。一般來說,電解質溶液的導電性是溶液中所有離子貢獻的,但一些離子液體的摩爾電導率卻比電解質溶液的摩爾電導率低很多,即使在所允許的黏度誤差范圍內,還相差很大[2]。因此,深入研究離子液體摩爾電導率是其應用于電化學工業的關鍵理論基礎。對于研究人員來說,實驗測量如此龐大物系的物理化學性質耗時費力,所以開發估算離子液體摩爾電導率的方法很有必要的。
目前,對于預測離子液體摩爾電導率的報道較少。SLATTER等[3]提出離子液體的電導率與其分子體積之間存在緊密關聯。基于這種關系,擬合了含4種陰離子的離子液體電導率數據,但是所用數據個數很少,不具有廣泛性。GARDAS等[4]將基團貢獻法和Vogel-Fulcher-Tammann(VFT)方程結合,對15種離子液體的307個數據點進行擬合,平均相對偏差為4.57 %。GHARAHEIZI等[5]將最小二乘支持向量機法與基團貢獻法結合,對54種離子液體的1077個數據點進行擬合,平均相對偏差為3.3 %。ZHAO等[6,7],采用一種空穴理論估算24種離子液體、共計24個數據點的電導率,估算誤差為11.87 %。本文對兩種單一離子液體及其二元混合物進行基團劃分,建立基團貢獻模型;基于最小二乘法,分三步確定模型參數的最優解;并進一步預測了不同組分濃度的二元離子液體混合物的摩爾電導率,為其他離子液體摩爾電導率性質的研究提供理論參考。
1 計算部分
1.1 實驗數據的選取
選取的實驗數據來自離子液體數據庫(NIST)。其中,單一離子液體有:1-乙基-3-甲基咪唑硫氰酸鹽([C2mim][SCN])、1-乙基-3-甲基咪唑二氰胺鹽([C2mim][DCA]);二元離子液體有:[C2mim][SCN]和[C2mim][DCA]的混合物。陰、陽離子結構詳見圖1。考慮到摩爾電導率隨溫度變化的關系,首先將搜集到的2種單一離子液體的摩爾電導率數據在不同溫度下的變化進行作圖,由圖2可以看出,離子液體摩爾電導率隨溫度呈冪指數形式變化,都隨溫度的升高而升高。還發現,對于陽離子相同的離子液體,隨著離子液體陰離子摩爾質量的增加,其摩爾電導率增大。

圖1 離子液體陰、陽離子的結構
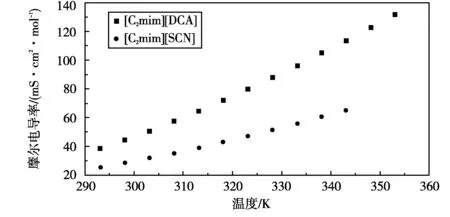
圖2 離子液體摩爾電導率隨溫度的變化
1.2 基團的劃分
本文按照課題組成員ZHAO等[7]預測其他傳遞性質時所定義的方法進行基團劃分,即將構成離子液體的不同種類陰、陽離子分別定義為一種基團,不再細分基團。此種方法可簡化模型計算過程。
1.3 基團貢獻模型的建立
該模型的核心公式(即摩爾電導率的表達式)如下:
(1)
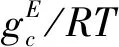
基團貢獻法的基本假設為某物質的某性質相當于該物質各個基團對該性質提供的貢獻值加和[8]。此模型把離子液體陰陽離子的混合看作是理想狀態,即離子液體的摩爾體積為陰陽離子有效摩爾體積之和。而陰陽離子的有效摩爾體積依據JACQUEMIN等[9]提出的方法計算:
(2)
式中:T*=T-298.15,pref=0.1 MPa,ai為有效摩爾體積參數。
陰陽離子的有效摩爾電導率可由Vogel-Fulcher-Tamman(VFT)方程表示:
Λi=A·exp[-B/(T-T0)]
(3)
式中:A,B,T0為離子有效摩爾電導率的參數。
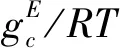
(4)
式中:θi和φi分別為基團的表面積分數和體積分數,ri和qi分別為分子范德華體積和表面積。離子基團的體積和表面積常數Rk和Qk用熱力學軟件COSMOthermX模擬計算確定。
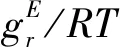
(5)
(6)
式中:N是離子液體中基團種類的總數(N= 2),lnγm是離子液體中m基團剩余活度系數,lnγm,i是只包括i離子參考溶液中m基團的剩余活度系數,Θm為基團表面積分數,Ψmn為基團之間的相互作用參數。
1.4 確定模型參數
本項目中需要優化的是基團之間的相互作用參數αmn和陰陽離子的VFT參數A、B、T0。以MATLAB軟件為載體,以式(7)為目標函數,采用最小二乘法擬合摩爾電導率的文獻實驗值,得到模型參數的最優解。
(7)
式中:M為實驗數據的數目;Λexp為離子液體摩爾電導率的文獻測量值,Λcal為離子液體摩爾電導率的計算值。
在擬合過程中,參數的初始賦值直接影響迭代次數、收斂速度以及結果精度。在一個模型中,同時對多個參數隨機賦初始值,那么尋找到所有參數的最優解是非常困難的。本文分三步確定模型參數:
(1)選擇離子液體[C2mim][DCA],對離子[C2mim]+和[DCA]-的參數賦初始值,根據公式(7)對[C2mim][DCA]的摩爾電導率進行擬合,得到[C2mim]+和[DCA]-的參數值;(2)選定另外1種離子液體[C2mim][SCN],與第1種離子液體[C2mim][DCA]具有相同的陽離子或陰離子,對離子[SCN]-的參數賦初始值,將上一步擬合得到的[C2mim]+和[DCA]-參數值作為本步驟其初始值,根據公式(7)對這2種單一離子液體的摩爾電導率進行一起擬合,得到[C2mim]+、[DCA]-和[SCN]-的參數值;(3)選擇上述兩種離子液體組成的二元混合物x1[C2mim][DCA]+x2[C2mim][SCN](x1=0.4888)的電導率文獻測量數據,對離子[DCA]-和[SCN]-之間的相互作用參數賦初值,將上步擬合得到的[C2mim]+、[DCA]-和[SCN]-參數值作為本步其初始值,根據公式(7)對該二元混合物的摩爾電導率進行擬合,從而確定模型所有參數值。運用上述方法對陰陽離子模型參數所賦初始值更加合理、貼近參數的最優值,有利于減少迭代次數和加快收斂速度。
2 結果與討論
2.1 標準差和相對偏差的計算
為說明此方法的回歸效果,用公式(8)計算了估算結果的標準差。結果顯示參與估算的摩爾電導率數據的標準方差為0.254。
(8)
用公式(9)計算文獻測量值與計算值的相對偏差,進而求出估算結果的平均相對偏差(RAD)為0.333%,具體分布情況見圖3。由圖3可以看出,數據點的相對偏差均小于1%,說明該方法是比較精確的。
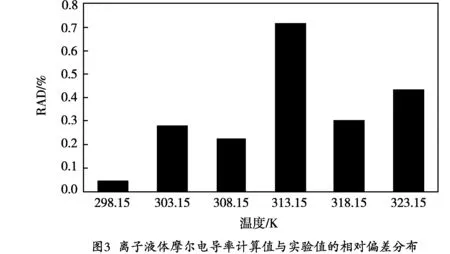
RAD=|Λcal-Λexp|/Λexp
(9)
2.2 驗證基團貢獻模型
為了更好地檢驗該基團貢獻模型的準確性,利用該方法估算其他組分含量的二元混合物(x1[C2mim][DCA]+x2[C2mim][SCN])摩爾電導率,不同溫度下的預測結果見表1。不同組分濃度混合物摩爾電導率的預測值與實驗值的平均相對偏差分別為0.313%(x=0.2397)、0.544%(x=0.7415),圖4顯示該二元混合體系摩爾電導率的估算值、預測值相較于文獻測量值的偏離情況,結果表明該方法是可靠的。
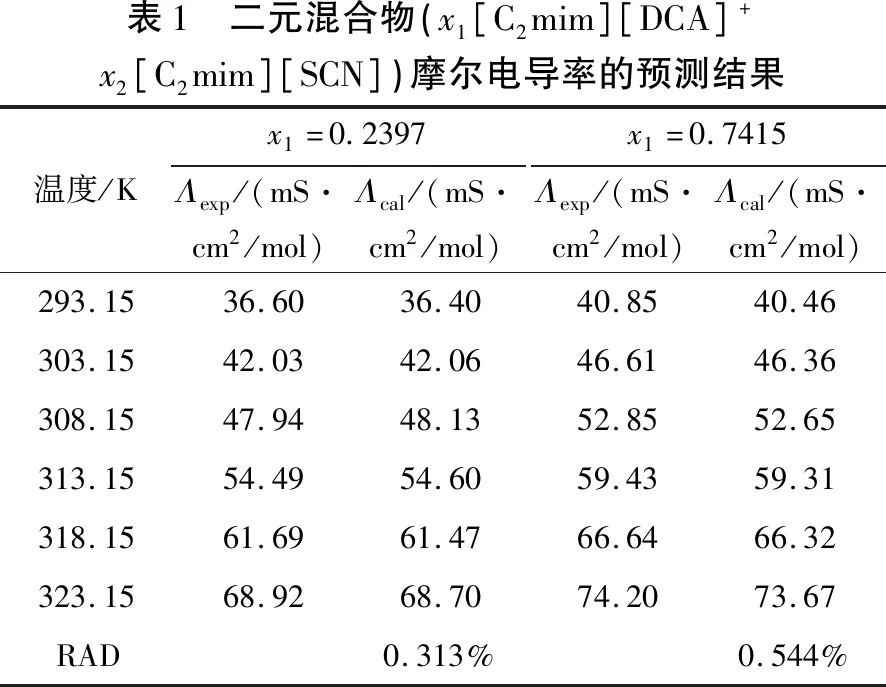
表1 二元混合物(x1[C2mim][DCA]+x2[C2mim][SCN])摩爾電導率的預測結果溫度/Kx1=0.2397Λexp/(mS·cm2/mol)Λcal/(mS·cm2/mol)x1=0.7415Λexp/(mS·cm2/mol)Λcal/(mS·cm2/mol)293.1536.6036.4040.8540.46303.1542.0342.0646.6146.36308.1547.9448.1352.8552.65313.1554.4954.6059.4359.31318.1561.6961.4766.6466.32323.1568.9268.7074.2073.67RAD0.313%0.544%
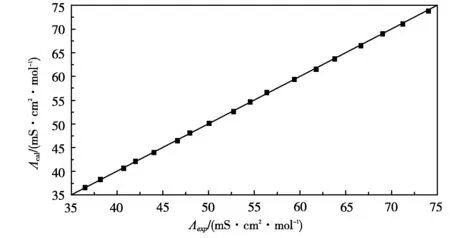
圖4 離子液體摩爾電導率的計算值相較于實驗值的偏差
3 結論
本文提出了一種新的基團貢獻法,搜集單一離子液體[C2mim][DCA]、[C2mim][SCN],及其二元混合物的摩爾電導率文獻實驗數據,分為三步逐步增加模型的參數個數,基于最小二乘法確定模型參數最優解,模型的回歸標準差和平均相對偏差分別為0.254和0.333%。使用該模型預測二元離子液體混合物的摩爾電導率,得到的平均相對偏差分別是0.313%(x=0.2397)、0.544%(x=0.7415),說明該基團貢獻法是準確、可靠的,能夠預測不同組分含量的離子液體二元混合體系。

