雞新城疫微量紅細胞凝集抑制試驗檢測結果不確定度評定
張 寧,宋善道,王書麗,李志娟
(1.河南省獸藥飼料監察所,河南 鄭州 450003;2.河南國康檢測技術有限公司)
測量不確定度,簡稱不確定度,是指根據所用到的信息,表征賦予被測量值分散性的非負參數(JJF 1059.1-2012)或表示與測量結果相關聯的參數,表征合理地賦予被測量值的分散性。其結果為表征結果的分散性,根據計算結果,其結果必然為非負數。具體而言,不確定度包括由系統影響引起的若干分量。測量結果包括估計值和測量不確定度,而不確定度反映了測量結果的可信程度。
本研究利用HI 試驗測定雞新城疫病毒(NDV)抗體,并對測量不確定度進行了評定和計算,提供了測量過程中各分量的組成和計算方法,科學評定了此方法的準確性,以期為獸醫實驗室測量不確定度評估提供參考。
1 材料與方法
1.1 試驗材料
1.1.1 樣品 8份待檢雞血清,均來自河南省獸藥飼料監察所,均為留樣樣品。
1.1.2 試劑 PBS(0.1mol/L,pH 7.0~7.2),自配;1%雞紅細胞懸液,采自河南省獸藥飼料監察所飼養的無新城疫SPF 雞血清配制;新城疫標準抗原,購自哈爾濱國生生物科技股份有限公司,批號:20210412;新城疫標準陽性對照,購自哈爾濱國生生物科技股份有限公司,批號:20210412;新城疫標準陰性對照,購自哈爾濱國生生物科技股份有限公司,批號:20210412。
1.2 主要儀器與設備
電熱恒溫培養箱(DH-420AB),購自北京中興偉業世紀儀器有限公司;高速臺式冷凍離心機(TGL-16MC),購自湘儀離心機儀器有限公司;移液器(八通道),5~50 μL,購自大龍興創實驗儀器(北京)股份公司;移液器,10~100 μL、100~1 000 μL,購自大龍興創實驗儀器(北京)股份公司。
1.3 試驗方法
1.3.1 血凝素工作液配制
血凝素凝集價測定:按照表1,對96孔微量板法布局,用PBS(0.1 mol/L,pH7.0~7.2,下同)將血凝素稀釋成不同倍數,加入與抑制試驗中血清量等量的PBS,再加入1%雞紅細胞懸液。將96 孔微量板在振搖器上搖勻,置室溫20~40 min 或置2~8℃40~60 min,當對照孔中的紅細胞呈顯著紐扣狀時判定結果。以使紅細胞完全凝集的最高稀釋度作為判定終點。
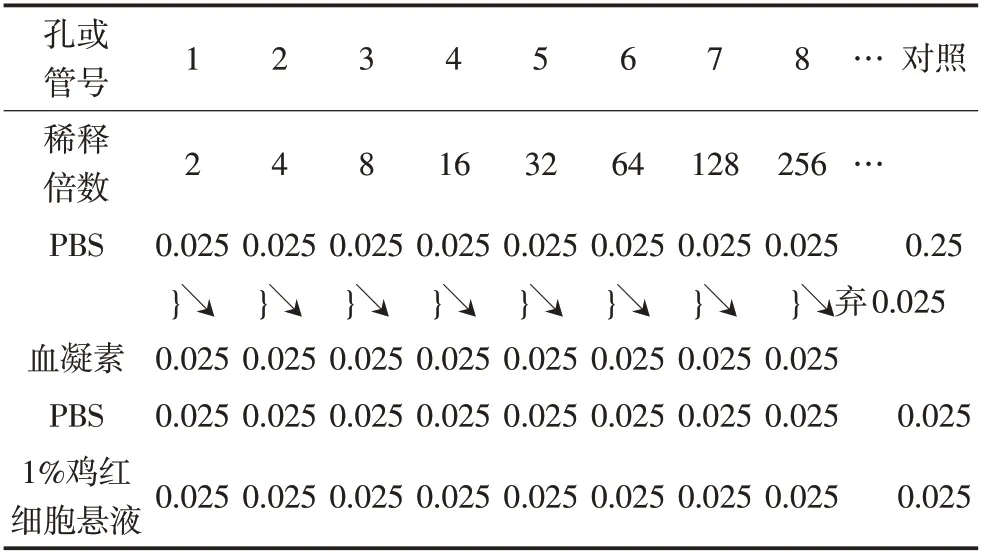
表1 96孔微量板法測定凝集價 (單位:mL)
1.3.2 血凝素工作液配制及檢測
1.3.2.1 四單位HAU血凝素的配制
如果血凝素凝集價測定結果為1:1024(舉例),4個血凝單位(即4HAU)=1024/4=256(即1:256)。取PBS 9.0 mL,加血凝素1.0 mL,即成1:10稀釋,將1:10稀釋液1.0 mL加入24.6 mLPBS中,使最終濃度為1:256。
1.3.2.2 檢測
檢查4HAU 的血凝價是否準確,應將配制的1:256 稀釋液分別以1.0 mL 的量加入PBS 1.0 mL、2.0 mL、3.0 mL、4.0 mL、5.0 mL 和6.0 mL 中,使最終稀釋度為1:2、1:3、1:4、1:5、1:6 和1:7。然后,從每一稀釋度中取0.25 mL,再加入1%雞紅細胞懸液0.25 mL,混勻。
如果用微量板,方式相同。即從每一稀釋度中取0.025 mL,加入PBS 0.025 mL,再加入1%雞紅細胞懸液0.025 mL,混勻。
將血凝板置室溫40 min 或置2~8℃60 min,如果配制的抗原液為4 HAU,則1:4 稀釋度將給出凝集終點;如果4 HAU 高于4 個單位,可能1:5 或1:6 為終點;如果較低,可能1:2或1:3為終點。應根據檢驗結果將血凝素稀釋度做適當調整,使工作液確定為4 HAU。
1.3.3 血凝抑制試驗(HI)
按照表2,對96孔微量板法布局,PBS將本血清做2倍系列稀釋,加入含4 HAU 的血凝素液,并設PBS 和血凝素對照,充分振搖后,置室溫下至少20 min 或在2~8℃下至少60 min,再加入1%雞紅細胞懸液,置室溫20~40 min 或置2~8℃40~60 min,當對照孔中的紅細胞呈顯著紐扣狀時判定結果。以使紅細胞凝集被完全抑制的血清最高稀釋度作為判定終點。

表2 96孔微量血凝抑制試驗 (單位:mL)
2 結果及分析
2.1 數學模型
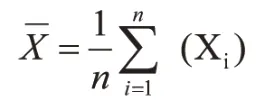
式中, Xi—同一血清樣本單次檢測的新城疫抗體HI效價(log2);
n—平行樣數量;
2.2 測量結果
對8份雞血清進行HI重復性測定,結果見表3。

表3 8份雞血清HI重復測定結果表
2.3 不確定度評定
2.3.1 測定方法重復性導致的不確定度ua
對血清樣品新城疫HI抗體效價進行8次重復測定,平均HI效價為:
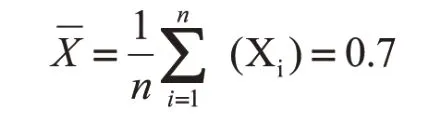
實際標準差為
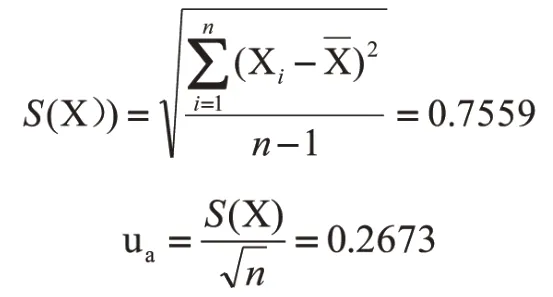
2.3.2 由測量儀器和測定過程導致的不確定度ub1
測定一個血清樣本需采用200 μl 移液槍進行多次操作,其中在96 孔V 型板中加入25 μl PBS 需重復操作10次,血清的稀釋需用移液器進行10 次重復操作,添加4 HAU抗原需移液槍進行10次重復操作,添加1%雞紅血球移液槍進行10次重復操作。主要考慮以下分量:200 ul移液槍經檢定合格,按照《JJG 646-2006移液器檢定規程》吸取25 μl液體,允許最大誤差為±1 μl,該量為均勻分布,包含因子k=

移液器重復帶來的不確定度ub2,取移液槍,精密量取水200 uL,稱重,重復10次,結果見表4。

表4 移液器重復10次檢測結果
稱重的標準偏差為Sm=0.7559 g,故S移=0.7559 mL。
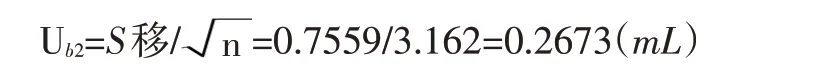
溫度效應引入的不確定度ub3,整個實驗過程中環境溫度變化2℃,考慮其對體積的影響。

整個過程需進行40 次移液器的重復操作,所以由測量儀器和測定過程導致的不確定度ub。
2.3.3 人員讀數導致的不確定度uc
檢測人員在觀察讀數時,因受觀察時間、操作經驗以及1%紅血球溶血度等因素的影響,會產生讀數誤差。估計該差a=0.1(log2),為均勻分布,包含因子k=
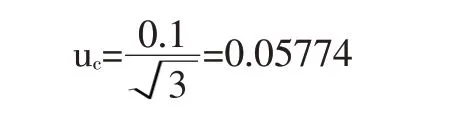
2.4 合成標準不確定度
計算雞新城疫微量紅細胞凝集抑制試驗測定的合成標準不確定度。
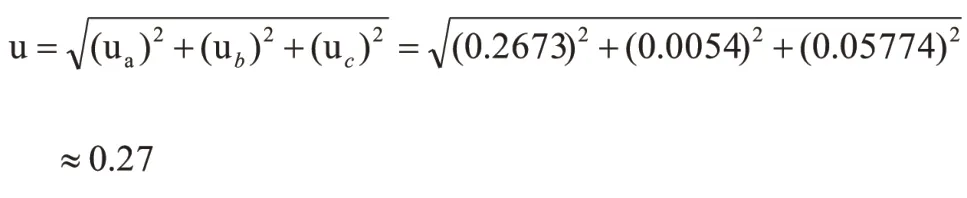
2.5 擴展不確定度
取包含因子k=2,擴展不確定度U=k×u=0.27×2=0.54≈0.6,新城疫微量紅細胞凝集抑制試驗HI 效價為(7.0±0.6)log2,(k=2)。
3 討論
通過對構成不確定度的各分量進行詳細分析,并分析各分量在整體不確定度值中所占的比例,可直觀了解對檢測結果質量影響最大的因素,在對這些因素針對性地改進后,可以有效提高檢測質量。
本研究評估結果顯示,標準不確定度為0.27,擴展不確定度為0.6,置信水平P=95%,k=2。試驗表明,該檢測不確定度的主要來源為測定方法重復性、移液器、溫度環境、人員讀數帶來的不確定度。在樣品測量值處于陽性判定值附近時,需要考慮不確定度的存在。該方法可有效評定雞血清中雞新城疫病毒抗體檢測結果的不確定度,可為實驗室在今后的血凝抑制試驗檢測中提供參考。□

