生物硫鐵復合物的合成及分布特性
胡 璇 鄭志勤1,,3 周 磊1, 宋英澤 翟帆帆 郭芊宏 謝李平
(1.西南科技大學核廢物與環境安全國防重點學科實驗室 四川綿陽 621010;2.西南科技大學生命科學與工程學院 四川綿陽 621010;3.國家衛生健康委員會核技術醫學轉化重點實驗室 四川綿陽 621010;4.西南科技大學環境友好能源材料國家重點實驗室 四川綿陽 621010)
硫酸鹽還原菌(SRB)是一類獨特的功能多樣化的異養厭氧細菌,它主要是把周圍環境中的通過一系列的反應還原為S2-。地球上97%的硫化物由硫酸鹽還原菌通過代謝活動產生[1]。硫鐵復合物在淡水河海洋沉積物中含量豐富,且其來源主要是對硫酸鹽的生物還原[2]。在自然界中,硫鐵化合物常以混合物的形式在沉積物中存在,主要是結晶性較差的四方硫鐵礦(Fe1+xS)、硫復鐵礦(Fe3S4)以及黃鐵礦(FeS2)[3-4],其中更為穩定且結晶性良好的四方硫鐵礦在水溶液中需要長達兩年的時間來形成[5-6]。
隨著科技的發展,納米材料的應用受到廣泛關注,其合成方法也逐漸多樣化。生物合成納米材料作為一種清潔、無毒、環境友好的方法在納米材料的研究中逐漸脫穎而出[7-9]。生物硫鐵復合物納米顆粒因其具有較強的還原性可作為除氧劑應用于重金屬污染的水體或土壤中[10-12]。硫酸鹽還原菌合成硫鐵復合物,其良好的吸附性能與硫酸鹽還原菌共同作用可將有重金屬污染的水體中的重金屬含量降至一個較低的水平[13-14]。為探究其應用化,關于硫酸鹽還原菌對硫酸鹽代謝的影響已有一定的研究[15-17],但硫化物的合成機理還有待進一步研究。本研究使用脫硫弧菌(Desulfovibrio vulgaris)合成硫鐵復合物,對其形成機理進行了探討,為微生物形成納米材料的機理研究以及利用脫硫弧菌處理重金屬污染提供參考依據。
1 實驗部分
1.1 材料、試劑與儀器
1.1.1 菌種
脫硫弧菌菌種由西南科技大學固體廢物處理與資源化教育部重點實驗室提供。
1.1.2 主要試劑與儀器
脫硫弧菌液體培養基按照DSMZ的Medium_63要求 配 制[18]:K2HPO40.5 g/L,Na2SO41 g/L,CaCl2·2H2O 2 g/L,MgSO4·7H2O 2 g/L,乳酸鈉2 g/L,酵母膏1 g/L,抗壞血酸0.1 g/L。
高速冷凍離心機,型號5805 R,Eppendorf AG;真空冷凍干燥機,美國LABCONCO公司;超級凈化手套箱,Universal,上海米開羅那有限公司;X-射線衍射光譜儀(XRD),荷蘭帕科公司;傅里葉紅外光譜儀(ATR-FT-IR),美國珀金埃爾默有限公司;高分辨冷場發射掃描顯微鏡(FSEM),UItra55,德國Carl zeissNTSGmbH公司;透射電子顯微鏡(TEM),JEM-1400PLUS,日本電子(JEOL);徠卡組織處理機,EM TP,徠卡生產;玻璃制刀機,EM KMR3,徠卡生產;超薄切片機,EM UC7,徠卡生產。
1.2 方法
1.2.1 脫硫弧菌生長曲線的測定
在超凈工作臺中,將活化好的菌液接種至3組平行培養基中,接種質量分數為10%,充N220 min,于30℃,120 r/min恒溫搖床中培養,每隔1 h取樣,紫外分光光度計在600 nm波長下測定其OD值。
1.2.2 硫鐵復合物的制備
按照基礎培養基配方溶于990 mL去離子水中,121℃下高壓滅菌30 min。待冷卻后,將2 g/L FeSO4·7H2O和0.1 g抗壞血酸溶于10 mL去離子水中,于超凈工作臺通過0.22μm濾膜緩慢加入培養基。接種質量分數10%的對數生長期的菌液,培養瓶中通N220 min后密封,35℃,120 r/min搖床培養至溶液變黑。約3 d后,將黑色液體培養基10 000 r/min,5 min離心取沉淀后真空冷凍干燥24 h,保存至手套箱。
1.2.3 產物表征
用X-射線衍射光譜儀在N2保護下分析樣品物相,Cu靶,Kα工作電壓40 kV,管流40 mA,掃描范圍10°~80°;采用高分辨冷場發射掃描顯微鏡觀察樣品顆粒形態;利用能譜儀測試產物元素組成;采用傅里葉紅外光譜儀確定樣品的化學成分,分辨率4 cm-1,光譜范圍400~4 000 cm-1,累計掃描64次,鏡面速度為0.632 9 cm/s;利用JEM-1400PLUS透射電子顯微鏡分析產物合成位置及其結構。
2 結果與分析
2.1 脫硫弧菌生長曲線測定及硫鐵復合物合成過程
脫硫弧菌生長曲線如圖1所示。由圖1可以看出,脫硫弧菌在0~4 h處于生長遲緩期,菌體數量增長緩慢;4 h后,脫硫弧菌生長進入對數生長期,生長速率明顯加快,代謝旺盛,菌體數量呈對數增加,消耗大量營養物質;至36 h后脫硫弧菌的OD600nm值趨于基本穩定,進入生長穩定期,活菌數保持相對穩定,總菌數達到最高水平。圖1內嵌圖為硫鐵復合物合成過程中培養基顏色變化。向滅菌后的培養基加入2 g/L FeSO4·7H2O,溶液呈黃綠色,1 d后溶液變成黑綠色,可明顯看出有黑色的顆粒懸浮于溶液中;第3天溶液變成黑色,有大量的黑色顆粒懸浮其中。硫鐵復合物的合成轉化率約為40%。
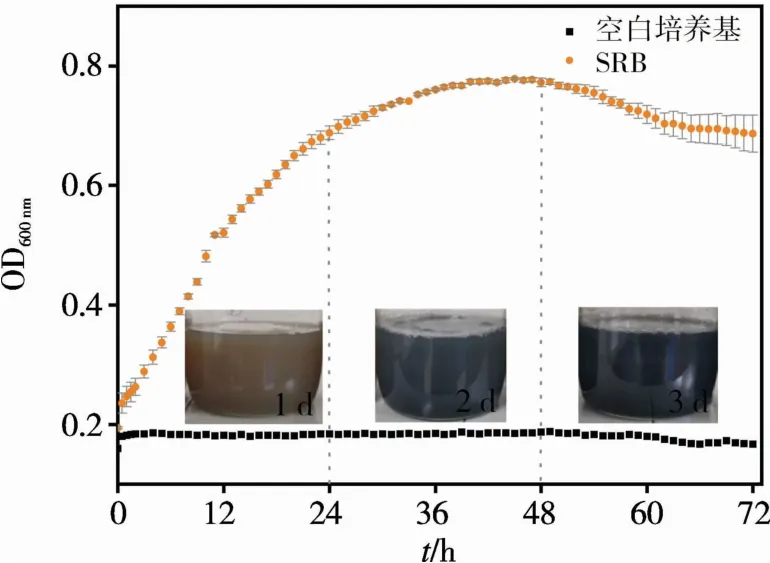
圖1 脫硫弧菌生長曲線及硫鐵復合物合成過程中培養基顏色變化Fig.1 Growth curve of Desulfovibrio vulgaris and color change of culture medium during the synthesis of sulfur-iron complex
2.2 硫鐵復合物特性
自然界中,由脫硫弧菌通過生物礦化形成的硫鐵復合物主要以無定型及微晶型狀態存在,且結晶性較差。圖2(a)和圖2(b)是生物硫鐵復合物中的菌體部分以及脫硫弧菌細胞壁附著產物的透射電鏡圖;圖2(c)和圖2(d)為生物硫鐵復合物的掃描電鏡圖。圖2(e)是生物硫鐵復合物部分EDS圖。從圖2(a)、圖2(b)和圖2(d)可以看出,生物合成的硫鐵復合物的粒徑尺寸為納米級別,形態不規則,以鱗片狀疊加形式存在,且因其不規則疊加的原因會形成一些孔隙狀的形態,這種形態大大提高了生物硫鐵復合物的比表面積以及表面粗糙度,表現更高的活性。這一結果與文獻[19-20]的研究結果一致。從圖2(a)可以看出,生物硫鐵復合物合成會將脫硫弧菌包裹其中,生物硫鐵復合物顆粒均勻附著在菌體的表面。由圖2(c)的掃描電鏡圖可以看出,脫硫弧菌的菌體表面包裹的生物硫鐵復合物是層狀疊加形態,一層層的將脫硫弧菌包裹其中。EDS檢測表明硫鐵復合物的主要元素組成有Ca,O,Fe和S 4種元素。因為制備及儲存過程中Fe2+在空氣中易被氧化,所以材料中含有大量的氧原子,鈣元素為培養基添加。

圖2 硫鐵復合物TEM,FSEM,EDS圖Fig.2 TEM,FSEM,EDSdiagrams of sulfur-iron complex
根據樣品XRD可知(圖3),生物硫鐵復合物有8個明顯的衍射峰,分別位于17.55°,25.94°,28.58°,31.80°,34.45°,35.50°,39.73°,49.51°。其中:17.55°,34.45°,35.50°,49.51°對應四方硫鐵礦(PDF#240073,FeS0.9)標準衍射圖譜;25.94°和28.58°分別對應黃鐵礦(PDF#240074,011295,FeS2)標準衍射圖譜;34.45°對應硫化鐵(PDF#491632,FeS)標準衍射圖譜。因此,推斷脫硫弧菌礦化形成的硫鐵納米顆粒主要是由結晶度較差的四方硫鐵礦組成,且脫硫弧菌形成的硫鐵復合物并不是均一的,是一種硫鐵的混合物[21]。周繼梅[22]使用菌JF-5和脫硫弧菌合成的黑色礦物的組成主要是四方硫鐵礦且其結晶狀態差。王寧[23]利用希瓦氏菌合成無定型狀態且結晶性差、鐵硫原子比為3.93的FeS礦物,通過XPS證明其為四方硫鐵礦。Schoonen等[24-25]對生物合成硫化鐵進行研究,發現生物合成的硫鐵復合物為結晶性差的四方硫鐵礦(FeS)和灰輝石(Fe3S4),并提出這兩類是形成沉積黃鐵礦中的主要固相。Rickard等[26]表示,在環境中四方硫鐵礦通常被認為是黃鐵礦的前體,并且在25℃下形成結晶良好的四方硫鐵礦可能需要長達2年的時間,所以推測脫硫弧菌可以加速礦化形成生物硫鐵復合物,但在短時間內形成的生物硫鐵復合物會以一種非晶形為主存在且無法快速形成完整的微晶體。
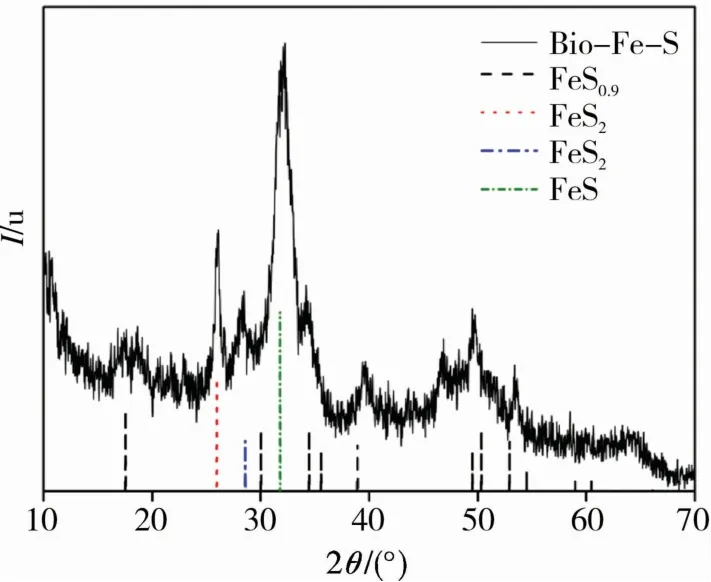
圖3 硫鐵復合物粉末XRD圖譜Fig.3 XRD pattern of sulfur-iron complex powder
對菌體切片,用TEM對比觀察正常培養基與含Fe2+培養基里的菌體切面。從圖4可以看出,在無Fe2+培養基培養的菌體內有明顯的染色質等胞內遺傳物質(圖4(a)、圖4(b)),EDS測試表明菌體內有O,P等元素分布(圖6),皆為生物體內的固有元素。

圖4 脫硫弧菌超薄切片TEM圖Fig.4 TEM diagram of ultrathin sections of desulfovibrio vulgaris
從圖4(c)、圖4(d)可以看出,硫鐵復合物顆粒分布在菌體表面及菌體內部。根據EDS面掃圖可知(圖5(b)、圖5(d)、圖5(e)),菌體內的S,Fe元素均勻分布,根據EDS分析顯示(圖6),其中硫元素的原子數百分比為12.31%,鐵元素原子數百分比為14.06%,Fe與S的原子比約為1∶0.88,結合XRD結果,印證了脫硫弧菌生成的硫鐵顆粒并不是均一的,是一種硫鐵的混合物。
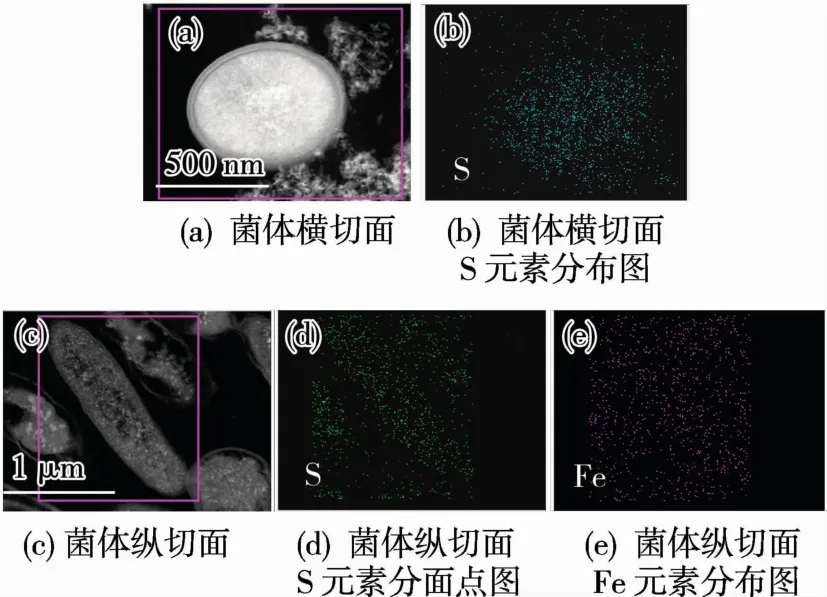
圖5 脫硫弧菌超薄切片EDS圖Fig.5 EDSdiagram of ultrathin sections of desulfovibrio vulgaris
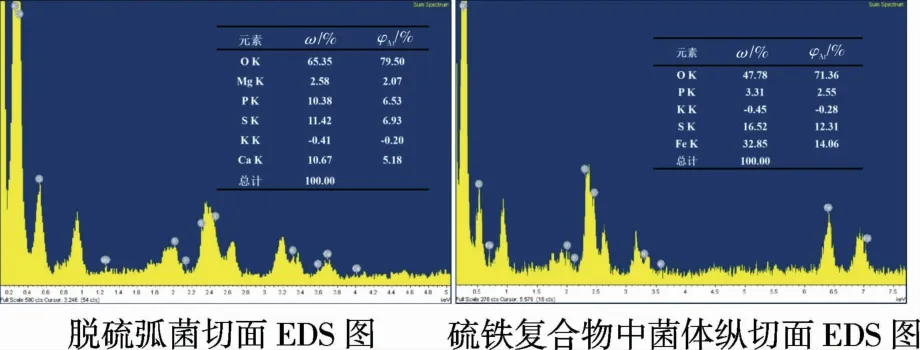
圖6 脫硫弧菌切面EDS圖Fig.6 EDSdiagram of desulfovibrio vulgaris section
生物合成硫鐵復合物的紅外光譜如圖7所示。從圖7可以看出,特征峰425~412cm-1有一段較為微弱的頻帶,是Fe(Ⅱ)-S2伸縮振動的結果[22]。564 cm-1處的特征峰為C-Cl的伸縮振動所致。618 cm-1處特征峰的出現可能與Fe-S的振動有關。波數為1 045 cm-1處的特征峰是S=S伸縮振動所致。1 156~1 120 cm-1處微弱的頻帶與Fe=S有關[27]。1 541 cm-1處的特征峰由自酰胺的N-H彎曲振動產生。1 650 cm-1處的特征峰為產物中水分子的羥基(-OH)發生變形產生。2 359 cm-1處的特征峰由-C=C=C引起。2 880,3 410 cm-1處的特征峰分別來自化合物中C-H的伸縮振動和水分子里-OH的伸縮振動,-OH的出現說明生物基硫鐵納米材料在處理過程中可以通過物理吸附作用對水分子進行吸附[19]。
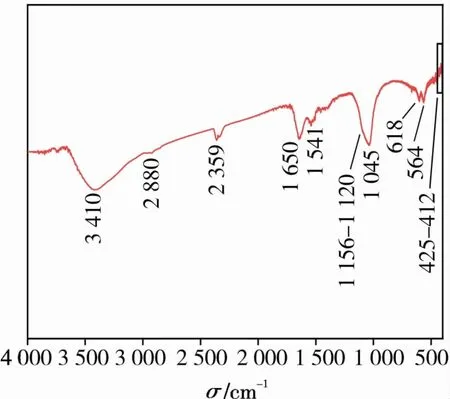
圖7 硫鐵復合物的FT-IR譜圖Fig.7 FT-IR spectrum of sulfur-iron complex
2.3 脫硫弧菌礦化形成硫鐵復合物機理
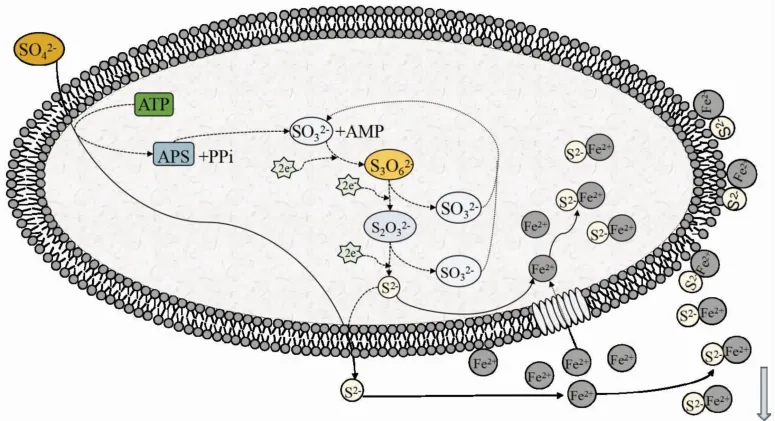
圖8 合成硫鐵復合物機理圖Fig.8 Diagram of the mechanism of sulfur-iron complex synthesis
3 結論
本文探究了脫硫弧菌(Desulfovibrio vulgaris)生物礦化形成的生物硫鐵復合物的微觀形貌、組成和形成位置,得到以下結論:(1)脫硫弧菌通過生物礦化作用形成生物硫鐵復合物,其最佳合成時間為3 d,復合物是一種以四方硫鐵礦為主、與黃鐵礦和硫化鐵組成的混合物。(2)生物硫鐵復合物的形貌主要是微晶型與非晶型的納米級結構,以無定型狀態、鱗片層狀疊加形式存在。Fe,S原子比約為1∶0.88。(3)脫硫弧菌在其胞內、胞外均可合成硫鐵復合物,且部分合成的硫鐵復合物包裹在菌體外部。

