在體跨尺度雙光子顯微成像技術
陳 帥,任 林,周鎮喬,李 敏,賈宏博
(1. 廣西大學 物理科學與工程技術學院和腦與智能研究中心, 廣西 南寧 530004;2. 中國科學院 蘇州生物醫學工程技術研究所, 江蘇 蘇州 215163)
1 引 言
1930年,物理學家Maria Goeppert-Mayer在其博士論文《研究原子的雙光子吸收之可能性》中指出雙光子的吸收是介質吸收兩個光子的過程,該過程中單個光子能量無法使介質中的分子從其基態變成激發態,只能使兩個光子在極短的時間內(ps量級)同時被吸收,從基態通過一個虛態最后達到激發態,過程中將有兩個光子被吸收,所以稱為雙光子吸收。基于該理論,1990年,博士生Winfried Denk提出了一種成像技術:雙光子激光掃描顯微鏡,該技術的出現對神經科學研究產生了革命性影響[1]。相比于單光子熒光激發,雙光子熒光激發需要更長波長和更高光子密度的激光。這些紅外激發光在生物組織中散射小,且只有焦點附近小體積的熒光分子能被激發,因此提高了成像深度和信噪比,并使得雙光子在厚生物組織中仍能具有極高的三維空間分辨率(~0.5 μm),結合雙光子光毒性小等優點,雙光子顯微鏡非常適合用來對腦神經細胞活動進行在體成像[2-4]。
自1997年,Winfried Denk等人首次將雙光子顯微成像技術用于在體觀測小鼠大腦的錐體神經元的感官刺激修道樹突鈣離子動態以來,雙光子顯微鏡在神經科學研究領域的潛能完全凸顯[5-6]。但是初代雙光子顯微鏡存在成像視野小、成像通量低、鏡體體積較大的問題,限制了其獲取生物圖像信息的能力。尤其是其主要適用應用場景暨腦科學在體神經細胞形態和功能研究,特別需要跨尺度成像技術的發展。因為神經細胞具有與身體其他器官細胞完全不同的形態和功能。神經細胞互相連接組成全腦范圍的復雜網絡,一個皮層單個神經元的軸突投射范圍就幾乎可以從大腦皮層的一側半球直接到達另一側半球,大腦神經活動信息傳遞的距離(小鼠:cm量級;人類:dm量級),相比于釋放神經遞質的突觸尺寸(μm量級),其尺度至少跨越4~5個數量級,因此對于空間跨尺度成像有很高需求[7-8]。在深度維度上面,雙光子顯微鏡激發光的波段集中在600~1 100 nm,該波段的光子最容易被水吸收而不易被組織中的其他物質吸收,因此有較強的穿透能力,雙光子顯微鏡的探測深度可達700~1 000 μm,而小鼠腦皮層的厚度約為1 mm,因此雙光子顯微技術剛好可以觀測小鼠腦皮層各層的神經元及其信號。而小鼠腦皮層以下的區域如下丘腦、海馬等,其深度在皮層下大于1 mm處,因此深層腦區域成像也對雙光子顯微鏡在擴展成像深度的尺度上提出了新需求[9-10]。在時間維度上,神經突觸間的信號傳遞時間在10 ms量級,為了能更高效地探測到神經元信號,需要更快的掃描速度對信號進行捕獲。目前基于共振鏡掃描的雙光子圖像刷新頻率為10~30 Hz,在該頻率下通常只能滿足記錄反映神經功能活動的鈣火花信號(~100 ms量級)的需求,目前最新發展的反映膜電位活動和谷氨酸等化學信號的新型熒光探針,響應速度更快,記錄的信號能更直接真實地反映神經動作電位的活動情況,但是要求雙光子顯微鏡的掃描成像速率達到100~1 000 Hz量級,即在時間尺度上需要提高1~2個數據級[11-13]。雙光子顯微鏡實現了實驗動物處在活體狀態下的腦神經結構與功能成像,但是需要對實驗動物的頭部(通常是顱骨)進行固定,并放于顯微鏡鏡頭下進行成像,動物的行為依然受限且經常需要全程麻醉處理。當前腦功能研究通常需要結合動物行為學實驗,許多行為學實驗設計要求實驗動物能在m級范圍內自由清醒活動,而傳統的固定臺式顯微鏡幾乎不可能做到在這樣大的范圍中仍保持μm級顯微分辨率,因此最近頭戴式雙光子成像探頭也是一個重要的發展方向,其需要雙光子顯微鏡在自身體積尺度下進行減縮,同時增加實驗動物在成像過程中可自由活動的尺度范圍。
本綜述將在介紹雙光子顯微鏡工作原理的基礎上,詳細介紹近年來雙光子顯微鏡在成像視野、成像通量、成像深度、分辨率等方面取得的跨量級技術指標突破,并討論跨尺度雙光子在體顯微成像技術發展的難點及未來挑戰。
2 雙光子顯微成像基本工作原理
2.1 雙光子熒光激發原理
熒光團分子中最外層的電子軌道決定了其作為熒光化合物的熒光量子產率以及吸收和發射光子的波長。當熒光化合物在其所謂的“基態”中吸收光能(光子)時,分子的電子態、振動態和旋轉態就會發生改變。吸收的能量有時會將電子移動到離原子核更遠的軌道,其與原子核間的距離會隨時間發生變化,最終這些被吸收的能量都會被釋放。而振動弛豫和熒光發射是熒光團回到其低能基態的主要方式[14],如圖1(a)(彩圖見期刊電子版)所示。熒光成像技術以及共聚焦顯微鏡,都是從光和物質的相互作用中產生對比度,由于單光子熒光效應是線性的,因此信號強弱與入射光強度呈線性關系。而在雙光子激發等非線性熒光效應中,熒光信號大小與入射光強度呈非線性關系,如雙光子激發中熒光信號大小與入射光強度的平方有關,因此其對激光強度的敏感度更高。激光強度在時空分布上未達到基態電子躍遷所需條件時,電子躍遷的概率極低。為了產生足夠的信號,激發光必須空間和時間上高度集中[15-16]。高空間密度是通過高數值孔徑(NA)物鏡聚焦激光束產生的。時間上的高集中則需要使用激光器,發射“超短”脈沖(不到 1 ps)和相應的高峰值強度。對于寬度為τ、 頻率為fR的激光脈沖,與連續波照明相比,非線性效應產生的熒光信號增強了1 /(τfR)n-1倍 ,n為激發過程中參與的激發光子總數,對于雙光子熒光效應,n=2。由此可知,激發光子在時間上越集中,熒光信號越強[17]。以上兩點使得基態的電子短期內(ps范圍內)吸收多個光子后擁有足夠的能量可以躍遷到更高能級上去,如圖1(b)(彩圖見期刊電子版)所示。
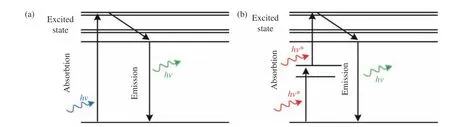
圖1 (a)單光子和(b)雙光子熒光激發原理Fig. 1 Excitation principles of (a) single photon and (b) two-photon fluorescence
相比于線性熒光顯微鏡,雙光子熒光顯微鏡的優勢主要有以下兩點:(1)激發光的波長范圍為670~1 070 nm,屬于近紅外光。由于在大多數組織中缺乏顯著近紅外光的內源性(單光子)吸收劑,因此,近紅外光對生物組織的穿透性更強,其光毒性更小。而對于產生熒光而言,其主要分布在可見光波段,易于探測[18]。(2)當激光束通過顯微鏡物鏡聚焦時,多光子吸收在空間上局限于焦點區域,非焦點區域被激發的可能性極低,因此,產生的熒光信號只會出現在目標區域,大大增加了信號的信噪比,減少了光損傷,增加了組織活力,便于對組織進行長期探測[19]。線性激發時在激光束會聚的整個過程里都容易激發出熒光,焦外熒光干擾嚴重;非線性激發情況只有在焦點附近才發出熒光,因此非線性顯微鏡具有更高的空間分辨率和信噪比。
2.2 雙光子激光掃描顯微鏡
雙光子顯微鏡結構如圖2所示,雙光子顯微鏡的結構與共聚焦顯微鏡類似,但相比于共聚焦顯微鏡,雙光子顯微鏡與其主要區別在于激發光源和熒光檢測路徑。雙光子顯微鏡主要包括6部分;飛秒激光器、光強調制器、激光掃描器、顯微物鏡、光電探測器、中央控制器和上位機軟件,掃描器目前主流部件為機械振鏡和聲光偏轉器[20]。雙光子顯微鏡的激光器多為鈦-藍寶石振蕩器,其重復頻率(~100 MHz)與典型的熒光壽命相匹配,從而平衡了激發效率和飽和現象。該類激光器可以發射670~1 070 nm范圍的激光,因此可以激活多種生物熒光物質[16]。激光的脈沖展寬需根據需求進行設置,通常為100 fs。小于該脈寬的脈沖相對更容易被光路上的色散光學玻璃加寬。而大于該脈寬的激光脈沖激發效率低,需要傳遞的能量更大,容易對樣品造成熱損傷[21-22]。共聚焦熒光顯微鏡在收集熒光的時候需要在探測器前放置一個針孔光闌來減少焦外熒光對目標區域信號的串擾。而對于雙光子顯微鏡,其熒光信號幾乎只在焦點產生,焦外熒光很少,因此不需要額外的輔助器件(如共焦小孔)來限制焦外熒光,從而顯著增強了熒光收集效率。
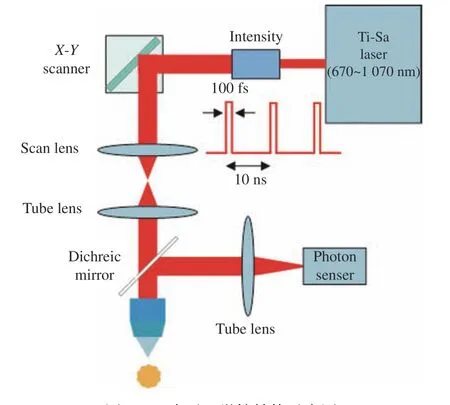
圖2 雙光子顯微鏡結構示意圖Fig. 2 Schematic diagram of two-photon microscope structure
3 雙光子顯微鏡跨尺度技術發展方向
3.1 成像視野
雙光子激光掃描顯微鏡已被廣泛應用于在體研究哺乳動物大腦中亞細胞分辨率的神經網絡結構,雙光子顯微鏡結合基因可編碼鈣指示劑(GECIs)已經成為在散射腦組織中進行神經元功能成像的標準技術[1,17]。然而,此類研究的范圍通常僅限于大腦的單個功能區域。而解剖和功能觀察表明,復雜的大腦功能來自于高度平行的計算[23-24],其中感覺信息和行為參數被映射到全腦神經元種群,其范圍超出了傳統顯微鏡的視場(<1 mm2),因此近年來出現了多種大視場的雙光子顯微鏡系統。
多區域實時雙光子成像技術(Multiarea Twophoton Real-time in vivo Explorer,MATRIEX),在傳統單光束掃描雙光子顯微鏡的基礎上將物鏡替換為雙層復合物鏡結構,上層使用空氣物鏡(DO)實現大視野成像,下層采用微型物鏡陣列(MOs)起到二次聚焦放大的作用,將分辨率提高到μm量級,而且同時實現了多個分離區域的同時成像(圖3(a),彩圖見期刊電子版)。如中國科學院蘇州生物醫學工程技術研究所賈宏博課題組,使用MATRIEX實現了軸向和橫向超過1 mm的成像視場,并同時記錄了小鼠的初級視覺皮層、初級運動皮層和海馬 CA1 區單神經元活動的實時功能成像,探測區域橫向跨度最大可達12 mm,軸向最大跨度超過1 mm[25]。其另外一個優點是僅對物鏡部分進行了模塊替換,而沒有改變雙光子顯微鏡的其他硬件模塊和控制時序,容易實現快速推廣應用。缺點是雖然區域可選范圍直徑達到12 mm,但只能成像若干離散區域,沒有實現大視野連續覆蓋成像。
Mark J Schnitzer研究組開發一種離散多區域成像方法,其將兩個顯微鏡(獨立的掃描采集系統)放置在同一動物的大腦上(圖3(b),彩圖見期刊電子版)。這種雙軸顯微鏡,因為使用的是完全獨立的兩套掃描、激發和探測系統,因此其不同區域可以同時被記錄,成像面積可提升為傳統雙光子顯微鏡成像面積的兩倍[26-27],并且兩個成像區域可以間隔較大距離,實現兩個不同腦功能區的同時成像。然而,用這種方法對兩個以上的大腦區域成像會大幅增加裝置的成本和復雜性。
實現連續覆蓋大視野腦皮層成像,首先需要設計并制作大視野高分辨的介觀物鏡[28-29]。如Spencer L Smith設計了一款大視野介觀物鏡(圖3(c),彩圖見期刊電子版),在保持μm級分辨率的同時將成像視野增加到25 mm2[30]。同時為了提高成像通量,通過偏振光學器件(PBS)將入射激光分為兩束光路,同時使其中一路光的光程增加了1.87 m,比另一束光延遲6.25 ns到達腦表面。通過控制機動轉向鏡(SM1、SM2)和XY掃描鏡(XYscan lens)改變光束在鼠腦XY平面的位置,再通過控制液體變焦透鏡(ETL)來改變激發光在鼠腦Z軸方向上的位置,被調控的激發光通過物鏡聚焦在指定位置。因為兩束激光到達腦表面的時間不一樣(同一脈沖相差6.25 ns),因此每束激光產生的熒光可以利用時分多路復用技術,對不同區域的熒光信號分開記錄,有效提升了信號采樣率。
Karel Svoboda研究組設計了大口徑大視野介觀物鏡,成像視野直徑達到5 mm(圖3(d),彩圖見期刊電子版)。在掃描方案上,他們通過共振鏡串聯一組大孔徑振鏡(20 mm),該共振鏡組由3個振鏡組成,兩個振鏡負責X-Y面掃描,另一個振鏡管控掃描區域的選擇。通過振鏡組掃描和切換成像區域,共振鏡提供高速掃描,實現了在視野跨度為5 mm×5 mm×1 mm范圍對4個任意0.6 mm×0.6 mm的區域同時成像[31]。

圖3 大尺度成像視野雙光子顯微鏡。(a)多區域實時雙光子成像技術[25];(b)雙掃描系統雙光子顯微鏡[26];(c)雙掃描區域同步成像雙光子顯微鏡[28];(d)多區域隨機掃描雙光子顯微鏡[31]。Fig. 3 Two-photon microscope with large-scale imaging field of view. (a) Multi-area real-time two-photon imaging technology[25]; (b) dual scanning system two-photon microscope[26]; (c) two-photon microscope with dual scanning area simultaneous imaging[28]; (d) two-photon microscope with multi-region follow-on scanning[31]
基于介觀物鏡,可以實現連續覆蓋(非離散)的大視野腦皮層雙光子成像[32-33]。但是目前在全視野和細胞分辨率(通常~1 μm)下進行連續覆蓋成像,時間分辨率仍然低于1 Hz。若降低空間采樣率要求(如5 μm),時間分辨率能提高到2~3 Hz,勉強達到鈣離子功能成像的需求。更常用的應用成像模式仍是選定2~4個腦區的離散子區域,在不犧牲空間采樣率下實現10~20 Hz的時間分辨率。
3.2 成像通量
雙光子顯微鏡的成像通量決定了獲取腦神經結構與功能信息的效率。腦神經網絡機理研究越來越需要對大規模的神經元群落同時獲取實時的功能信息,或者需要精準捕捉單細胞高精度樹突網絡中的高速神經動作電位信號,因此對雙光子顯微鏡成像通量的提高提出了迫切的需求。
成像通量可以定義為每秒獲取圖像像素的總數,即為圖像像素數乘以成像幀率。如果是三維體成像,還要乘以同時成像的深度方向層數,用三者的乘積對雙光子顯微鏡的成像通量進行評估。
雙光子顯微鏡非線性激發特點導致其每個激光脈沖所激發的體積受限,進而導致其常規成像通量在百萬量級[21,30-31]。即使是上述的大視場雙光子顯微鏡系統,仍然受限于點掃描激發速度,雖然成像視野或可選范圍極大,但在實時成像條件下也只能對若干少量局部區域進行掃描成像,像素通量也僅勉強達到千萬量級。
提高雙光子顯微鏡成像通量的一種傳統方式是采用寬場照明結合時間聚焦(Temporal Focusing,TF)方法[34],但這一定程度減弱了雙光子點激發的高空間選擇性,令圖像分辨率和信噪比下降。下面將介紹幾種最新雙光子高通量成像方法,它們通過多焦點或線掃描的方法實現億級的成像通量,對分辨率的影響小于寬場照明結合時間聚焦方法。
一個發展方向是提高雙光子體成像的通量[35-37]。Alipasha Vaziri研究組開發的光珠顯微鏡[37],是一種基于多焦點掃描和時分復用技術的顯微鏡,像素通量僅受熒光壽命的限制,其特點是軸向上產生的多個存在脈沖延時的焦點覆蓋了500 μm的軸向范圍,可實現高通量的體成像。該套儀器的原理是將激光重復頻率大幅降低(4.7 MHz),這么做的目的是在一個脈沖周期內產生足夠多個焦點間的脈沖延時,相鄰脈沖延時(6 ns)大于熒光壽命(~3 ns),足夠區分各焦點產生的熒光信號,降低信號串擾。使用多重軸向多路復用模塊將輸入的激光分成N份,產生脈沖延時的同時改變激光發散度,令各個焦點聚焦在不同深度,形成“光珠”柱,并通過調整分光比令每束激光能量不一,使焦點能量分布與成像深度呈指數關系,以抵消成像深度對熒光信號強度的衰減作用(圖4(a),彩圖見期刊電子版)。該技術可以在鼠腦中最多同時追蹤100萬個神經元,成像通量可達億級(1.41×108),最大幀率為9.8 Hz。
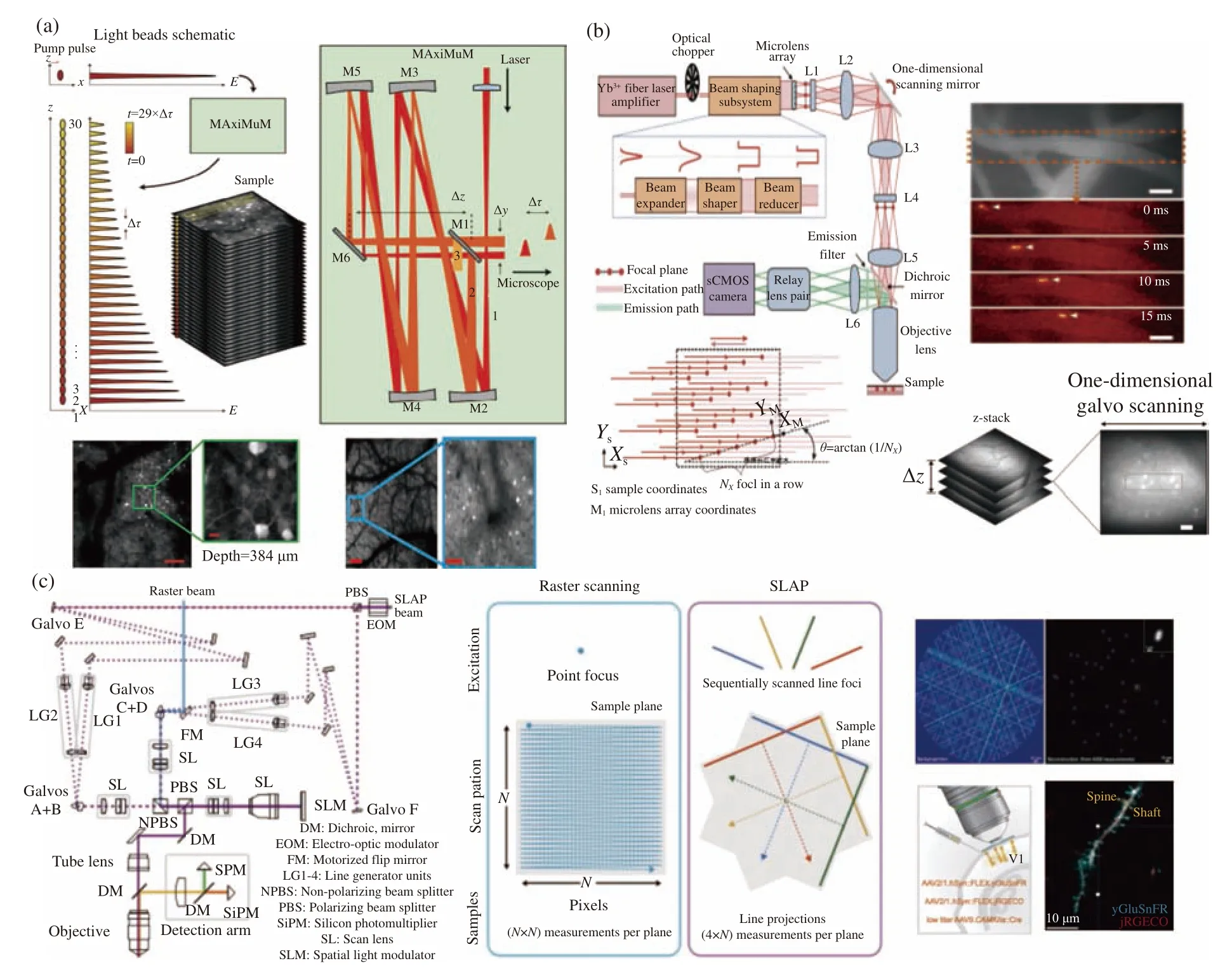
圖4 快速掃描雙光子成像技術。(a)光珠雙光子顯微鏡[37];(b)多焦點快速掃描雙光子顯微鏡[38];(c)快速線掃描雙光子顯微鏡[39]Fig. 4 Fast scanning two-photon imaging technology. (a) Light beads two-photon microscope[37]; (b) multi-focus fast scanning two-photon microscope[38]; (c) fast line scanning two-photon microscope[39]
另外一個發展方向是使雙光子二維成像的幀率高于1 kHz[38-42]。Mark J. Schnitzer研究組設計的平面多焦點雙光子顯微鏡,通過微透鏡陣列(20×20陣列)產生400焦點,進行同時掃描(圖4(b),彩圖見期刊電子版),其通過將焦點陣列傾斜一個角度,結合一維振鏡掃描,同時形成400行掃描線,并用sCMOS相機進行熒光探測。這個方法的成像通量可達兩億,最大幀率為1 kHz[38]。Karel Svoboda研究組利用線掃描加快掃描速度。該顯微鏡以4個不同的角度掃描二維樣本平面上的焦線(圖4(c),彩圖見期刊電子版),視野內每個點在每次線掃描過程中均被探測到,每個點對應一個時間位點,但同一個時間位點包含線內多個空間點的熒光信息,在樣品熒光點稀疏程度較低時,通過壓縮感知算法可以實現熒光圖像的重建而且真實性較高。該方法的優點是僅用4次行掃描就完成了二維圖像掃描,圖像幀率達到1 kHz,缺陷是當視野內的熒光物質密集程度較高時,重建圖像的真實性將降低。該方法可以使成像通量達到十億[39]。此外,通過自由空間角啁啾增強延遲器件(Free-space Angular-Chirp-Enhanced Delay,FACED)對小鼠視皮層進行快速成像,圖像幀率最快可達3 kHz,成像通量可達6.25億[40-41]。另一種基于掃描焦點的光譜時間編碼是通過掃描源的主動調制來產生頻譜編碼的皮秒脈沖序列,然后通過衍射光柵以線掃描方式依次照射到圖像平面上,形成焦點線性陣列,該方法成像通量可達0.88億,最快掃描幀率可達2 kHz[42]。
3.3 成像深度
Mark J Schnitzer課題組開發出一種使用光學器件梯度折射透鏡(Gradient-index (GRIN) lens)配合雙光子掃描顯微鏡的裝置。該裝置理論上可以在任意深度對細胞進行成像[43]。梯度折射率材料之前常用在自聚焦光纖當中,對于實驗中用的梯度折射率透鏡,從截面看,材料折射率隨著距圓心的距離增加而減少,其圓心位置的材料折射率最高。入射光在透鏡切線方向的分量隨著透鏡折射率的減少逐漸減小,直到達到全反射邊界條件后,光切線的方向將發生變化,光線第一次到達軸線時,光線與軸線的夾角等于光線剛入射進透鏡時與軸線的夾角,同理,當光線第二次達到光軸時,此時光線的方向與入射時的方向相同,將其稱為光線在透鏡中的空間頻率。由于透鏡很細,可以認為滿足傍軸條件,因此所有的光線都會以該空間頻率在透鏡中傳播,在1/2周期整數倍時匯聚[44-45]。如圖5(a)(彩圖見期刊電子版)所示(參考Mark J Schnitzer課題組相關技術成果)[43]。該技術大量應用于小鼠腦深處神經信號的探測,Yeka Aponte課題組使用該技術對小鼠腦深5 mm處的外側下丘腦神經元進行16天的熒光成像(圖5(a))[44]。Jianan Y Qu課題組將該技術和自適應光學相結合,用于觀測小鼠海馬神經元可塑性[46]。
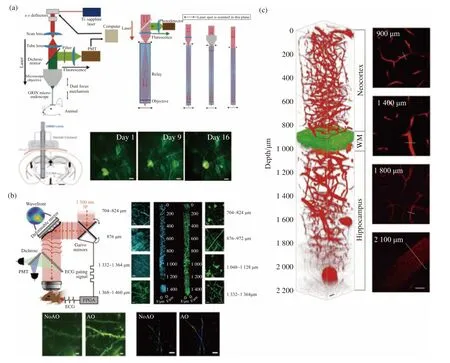
圖5 超深度探測顯微成像技術。(a)梯度折射率透鏡雙光子顯微鏡[44];(b)三光子小鼠神經元成像[49];(c)三光子小鼠腦血管成像[51]Fig. 5 Ultra depth detection microscopic imaging. (a) Gradient refractive index lens two-photon microscope[44]; (b) threephoton neuron imaging in mice[49]; (c) three-photon cerebral vascular imaging in mice[51]
雙光子成像中,最大可實現的成像深度與散射平均自由程成正比,并與所用的激光功率、雙光子的脈沖時間、頻率的倒數以及收集效率的對數成正比[47]。目前在最理想情況下,雙光子的探測深度也只能達到1 mm, 再往下焦斑逐漸惡化[48]。而三光子熒光顯微鏡在對小鼠神經元活體成像時,最深探測深度可以達到1.4 mm。三光子顯微鏡和雙光子顯微鏡類似,都屬于非線性光學,激發過程中,熒光分子吸收3個光子,經過兩個虛擬態分子由基態升至激發態。入射光的波前隨著組織深度的增加產生畸變,導致系統成像質量下降,可通過自適應光學對入射光進行波前補償,使得系統在組織深處也可以得到良好的光學分辨率[49-50]。Robert Prevedel課題組利用三光子技術呈現了小鼠腦皮層下1.4 mm處的海馬樹突精細結構和單個神經元活動情況(圖5(b),彩圖見期刊電子版)[49]。Wang Ke課題組利用三光子技術,將1 700 nm波長的光作為激發光,獲得小鼠皮層下2.1 mm處血管的結構圖像[51](圖5(c),彩圖見期刊電子版)。
3.4 成像分辨率
大部分熒光顯微鏡的光學分辨率都在μm量級,這對于觀測人體細胞(10~20 μm)可以滿足需求,但是對于亞細胞結構,如中心體、高爾基體、線粒體、細胞骨架,細胞間的信號傳導等,還遠遠不夠。為了滿足生物醫學研究與發展的需求,超分辨率光學顯微鏡應運而生。超分辨率光學顯微鏡主要分為3類:(1)單分子定位顯微鏡(Single-Molecule Localization Microscopy, SMLM);(2)受激輻射耗盡熒光顯微鏡(Stimulated Emission Depletion, STED);(3)結構光照明顯微鏡(Structured Illumination Microscopy,SIM)[52-54]。目前未發現有關SMLM和雙光子技術結合的研究報道,而STED和SIM已被證明能與雙光子成像技術結合并提高其成像分辨率。
STED顯微鏡的原理,熒光分子在激光照射下將從基態變成激發態,經過振動弛豫,熒光分子躍遷至激發態的最低振動能級,在無干擾情況下,處于激發態最低能級的熒光分子將通過發射熒光的方式退激發至基態。但熒光分子處于激發態,外界又給予激光照射時,則處于激發態的熒光分子會產生與外界激光相同頻率、偏振、相位的輻射[55]。因此可以將輻射光以光圈的形式對激發光光斑進行照射,通過控制光圈內環的大小調整熒光激發區域,該技術實現了5.8 nm的分辨率[56]。
STED技術可以配合雙光子顯微鏡使用,在進行深度探測的同時也保證了極佳的分辨率[57-59]。對于大多數STED-雙光子顯微鏡來說,將同時應用兩束不同波長的光,光路設計需要考慮光束畸變的問題[59]。最近,Alberto Diaspro課題組開發了一種單一光源的STED-雙光子顯微鏡。原理如圖6(a)所示。其選用特殊染料使耗盡光和激發光為同一波段的光。該技術可以實現80 nm的分辨率,遠優于普通雙光子顯微鏡的分辨率(0.5~1 μm量級)[57-58]。
SIM成像技術是一種改變照明光空間結構的照明方式,其將樣品中不可見的高頻信息攜帶到顯微鏡的可見低通頻帶;通過改變圖案方向和相位,記錄熒光結果并得到多個圖像數據集,再對數據集進行空間域和頻域的傅立葉變化,提取攜帶的高頻信息并重建出超分辨率圖像。該技術原理如圖6(b)所示[54]。
SIM結合雙光子技術,使用電光調制器改變入射結構光的相位和角度,利用雙軸振鏡對樣品進行逐點掃描。Qionghai Dai課題組采用對每個像素點取3個入射方向的結構光對樣品進行照射(相鄰方向角度差值為120°),每個方向的結構光中又包含3個等間距的相位角(相鄰相位角差值為120°),每個像素點需要拍攝9張圖,該方法所得重建結果,橫向分辨率可達141 nm[60]。還有一種方法使用聲光調制器形成5個相位角(相鄰相位角差值為72°),再通過衍射光柵產生結構光,結構光的入射方向保持固定。該裝置主要對樣品進行線掃描,對小鼠神經元成像結果如圖6(b)所示,其橫向分辨率可達208 nm[61]。該技術除了具有優異的成像分辨率外,相對于STED,其成像速度快,使用低強度光源就可以產生足夠的熒光信號,減少了光漂白的可能性[60]。SIM也可配合自適應光學方法使用。該設備對果蠅大腦和斑馬魚胚胎探測的橫向分辨率可達170 nm左右[62]。
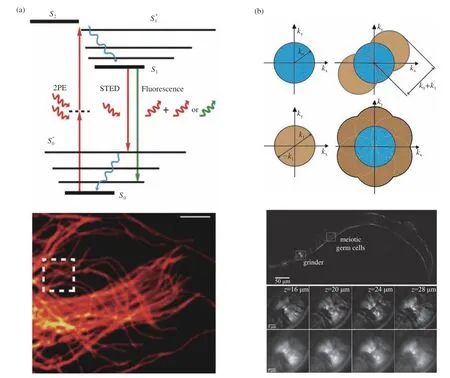
圖6 超分辨率雙光子顯微鏡。(a)STEM成像原理和實驗數據[58];(b)SIM結構光生成方法和結構光與均勻光照射探測精度對比[60]Fig. 6 Super-resolution two-photon microscope. (a) STEM imaging principles and experimental data[58]; (b) SIM structured light generation method and comparison of structured light and uniform light irradiation detection accuracy[60]
以上技術主要針對雙光子熒光顯微鏡橫向分辨率的提升,也有課題組通過液體透鏡配合自適應光學以及使用空間調制器來改善雙光子熒光顯微鏡的軸向分辨率,他們可以將軸向分辨率提升至普通雙光子顯微鏡軸向分辨的3倍[63-64]。
3.5 設備微型化
使用雙光子顯微成像設備探測動物的神經生理活動狀態時,通常需要對小鼠頭部進行固定。但一些科學問題,例如對空間導航和記憶的研究,不應束縛實驗動物行為,才能得到更切合實際生理條件的結果。為了使實驗結果更接近自然行為狀態,科學家們研制了頭戴式微型雙光子顯微鏡[65-68]。程和平團隊研制的微型化雙光子顯微鏡探頭質量只有2~3 g,和實驗小鼠頭部固連在一起,可以長時間記錄小鼠在劇烈運動下的神經元活動(圖7)[65]。該設備通過光纖傳導激發光和熒光,結合微型化振鏡(MEMS),電潤濕可調透鏡以及微型物鏡等器件將雙光子成像設備進行了微型化改造。Emily A Gibson使用微型化頭戴式雙光子顯微鏡對小鼠腦血管進行連續17天的觀測[66]。最近,諾貝爾獎獲得者Edvard I Moser團隊在此基礎上改進了微型光學系統和微型變焦透鏡,開發了不足3 g的微型化雙光子MINI2P系統,可以對自由小鼠多平面實現1 000個神經元鈣成像,成功揭示了不同腦區細胞的空間聯系[68]。

圖7 超分辨率雙光子顯微鏡實驗結果[65-66]Fig. 7 Experimental results of super-resolution two-photon microscope[65-66]
4 跨尺度雙光子在體顯微成像技術的難點及未來挑戰
綜上所述,近年來雙光子顯微鏡在多個維度上均獲得了快速的發展,表1是本文介紹的新型雙光子在體顯微成像技術的一個簡單匯總。在成像視野方面,通過改善單光軸大視野介觀物鏡或多光軸二級成像物鏡結構,雙光子成像視野直徑由~1 mm提升至~10 mm,實現了一個量級的提升;成像通量方面通過多焦點或線焦斑掃描,實現了近兩個量級的提升,達到數億像素每秒,局部圖像幀率提高到1~3 kHz;通過三光子或自適應光學方法,成像深度提升程度超過100%,采用侵入式的梯度折射率透鏡可以將成像深度提高數倍,但對腦組織有一定損傷;通過結合STED技術,雙光子成像極限分辨率達到了80 nm;微型化雙光子顯微鏡的重量僅數克,遠小于常規雙光子顯微鏡數十公斤的重量,能被小鼠頭部攜帶并在數米范圍自由活動并同時成像。顯然,相比初代雙光子顯微鏡,當前雙光子在體顯微成像技術已獲得了跨尺度的發展。
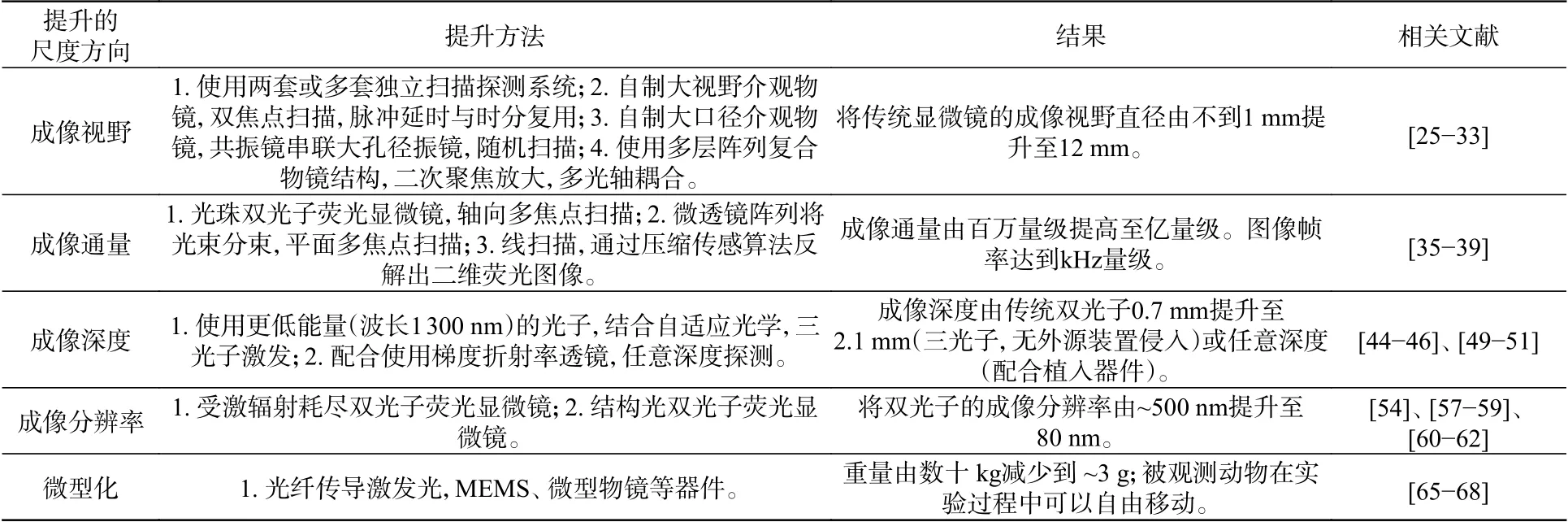
表1 雙光子顯微鏡在多個尺度方向的性能提升進展現狀Tab. 1 Progress in performance improvement of two-photon microscopy in multiple scale directions
但是需要看到的共性問題是,上述多光子顯微成像技術都是僅在1~2個維度實現了跨尺度跨量級的技術指標突破,這可能與技術的應用場景需求有關,通常是集中針對某一、兩個關鍵點進行巧妙設計或參數平衡,但目前還未能在多個尺度同時實現跨量級提高。
譬如使用梯度折射率透鏡雖然能提高成像深度,但一方面是有損植入,另一方面自身視野有限,采用多個分離元件組合的方式也難以實現成大視野面積連續覆蓋的成像[25,44]。而三光子技術無需破損皮層就能對超過1 mm深度的區域進行成像,三光子激發對單脈沖能量的要求比雙光子激發要高,往往采用低重復頻率高脈沖能量的飛秒激光器。低重復頻率通常會限制成像通量,不過與時分復用多焦點技術對重復頻率的需求一致,兩種技術有結合的可能性,但如果焦點數量很多,則分到每個焦點的單脈沖能量仍然有限,簡單增加激光器功率又容易對生物組織產生較大的熱損傷,因此需要合理選取焦點數量[48-51]。
在提高通量方面,線掃描結合壓縮傳感進行圖像重建要求樣品滿足一定稀疏性,故對其應用場景有所限制[39]。采用多焦點同時掃描是目前最佳的方案,其在焦點熒光信號區分方面,一方面可以與時分復用技術結合,但提高倍數有限,最終受熒光探針探測壽命限制;另一方面可以使用CMOS等面陣探測器,但隨著成像深度的增加,散射程度提高,面陣探測器成像分辨率將急劇下降。前述提到的高通量雙光子成像方法,在小視野范圍內的生物應用中已經取得了不錯的成果,典型應用場景是記錄單神經元樹突網絡的動作電位活動圖譜,結合目前最新發展電壓敏感探針或谷氨酸熒光探針,能以1 kHz成像幀率捕捉細小的樹突棘上快速的動作電位信號[38]。在大規模神經元群落成像方面,目前一些高通量體積成像方法,如“光珠”軸向多焦點、貝塞爾軸向焦深擴展等,已經與大視野介觀物鏡技術相結合,并取得了一定成果,但其在進行全視野體成像的時候,為了達到鈣成像的速度門檻,還是通過降低橫向空間采樣率(5 μm)的方式進行掃描成像,采樣率雖勉強達到細胞直徑(~10 μm)的奈奎斯特采樣要求,但其較粗的空間采樣率使神經元結構和功能解析精度降低了不少[37]。
微型化雙光子顯微鏡的重量和體積大幅減小,但由于使用了MEMS掃描鏡、微型物鏡等小型光學器件,元件口徑限制了成像視野直徑,目前局限在1 mm以內(通常僅數百微米),如需在多個腦區域同時成像,勢必需要使實驗動物頭戴多個微型化雙光子成像探頭,這又會增加動物的負重,更適合應用于體型較大的動物。除了成像視野,應用這些微型光學器件進一步提高成像速度和通量也極為困難,結合微型電潤濕可調透鏡進行軸向掃描或體成像擴展是不錯的選擇[65-68]。
結合STED技術雖然可以大幅提高雙光子成像分辨率,但大視野范圍內保持耗盡圓環光斑與激發圓斑對齊比較困難,因此目前未見該超分辨方法與大視野介觀雙光子成像相結合的研究。雙光子技術與SIM結合可以將分辨率提高近1倍,但SIM技術需要對多幅經調制的圖像進行算法解調,重建所需的圖像數量很大,進一步降低了雙光子的成像速度[57-62]。
綜上所述,跨尺度雙光子在體顯微成像技術仍有許多難點需要攻克,仍有待進一步發展。而腦神經網絡研究對于跨尺度在體成像的需求在很長一段時間內仍將為雙光子成像技術發展提供強大動力。當前很多基于單光子激發熒光的成像技術,如光場顯微鏡,得益于單光子高的熒光激發效率,在實現高通量大視野體積成像方面有很大優勢,但組織散射背景干擾等因素仍是其難以克服的障礙,這限制了其對神經結構功能信息的解析精度[69-70]。而多光子成像技術在散射組織內具有高保真的成像能力,獲得的神經結構功能信息更接近真實情況,成像深度更是有3倍以上的優勢,但非線性激發的特性對其通量提高有所限制,也是妨礙其真正實現跨尺度成像的核心因素。
實現大腦在體大視野高分辨率高通量成像,獲得大規模神經元網絡的結構連接與功能活動圖譜,是解決神經環路工作機理的重要一步,目前腦科學領域已達成共識,這離不開跨尺度雙光子在體顯微成像技術的下一步發展。筆者認為,實現該宏偉目標首先需要大視野高分辨介觀物鏡的發展,這是實現大視野高分辨腦皮層連續覆蓋成像的核心器件,但分辨率與視野之間存在天然的制約關系,這對光學設計與制造技術是一個挑戰,而且進一步擴展視野直徑后還需要考慮適配動物腦輪廓形狀,這需要打破傳統的平場顯微光學設計范式[32-33]。其次,可結合三光子技術和自適應光學方法擴展成像深度,但三光子激發需要高單脈沖能量,采用低重復頻率高脈沖能量飛秒激光器往往會導致成像通量有所降低[49]。結合SIM或STED技術提高空間分辨率也會降低成像通量,一方面空間分辨率的提高需要更高的空間采樣率,即更多的采樣點數;另一方面如結合SIM技術需要對多幅圖像進行重建,這會降低有效幀率[59,61]。因此,需要研究提高成像通量的新技術,至少要實現10 Hz附近鈣離子成像所需的幀率,在各方面指標同時提高的情況下,成像通量需要至少提升2~3個量級才能保證實時成像。相比線掃描,采用多焦點技術有利于保持層析效果、信息串擾更少,有利于保證神經結構功能信息的解析精度和保真度[37-38]。最近的研究中使用時分復用技術或其改進技術以降低焦點間的串擾,有效提高成像通量。但時分復用技術的采樣通量受限于熒光探針的熒光壽命,一般為~3 ns,因此僅結合時分復用技術,成像通量的提升上限為2×108~3×108pixel/s,這依然不能滿足cm級大視野和高分辨成像需求。如果需要采用軸向的多個焦點實現體積成像,如“光珠”技術,則對成像通量的需求更高[28,39]。多焦點技術,在結合時分復用技術的同時,可進一步考慮結合在空間上有多個陣元的陣列探測器,在空間上進一步對各焦點產生的熒光進行區分,在時空兩維同時進行焦點區分。這樣一方面可以進一步降低串擾,另一方面將使可容納的焦點數量大幅提高,有望實現2~3個量級的提高。熱效應也是需要考慮的因素,大規模飛秒焦點并行掃描會產生更多熱效應。為了避免動物腦組織產生嚴重熱損傷,一方面可結合外部主動散熱技術,另一方面需要研制更高效的熒光探針,用更少的激光能量得到更多的熒光光子。具有更低熒光壽命以及更長發射光譜的熒光探針有利于通量和成像深度的提高。可以期待,這些方面都在跨尺度雙光子在體顯微成像技術的下一步發展中得到實現。
5 結束語
自雙光子顯微鏡誕生以來,在體腦成像研究的需求促使雙光子顯微鏡在成像視野、成像通量、成像深度、分辨率、微型化等多個維度上性能指標有所提升。本文在介紹雙光子顯微鏡工作原理的基礎上,對近年來雙光子顯微鏡在這些方面的快速發展情況進行了詳細綜述。總的來說,目前雙光子顯微鏡在各個維度上均分別有了跨量級的發展,但仍未實現多個維度同時跨量級突破。量變產生質變,相信在不久的將來,將出現真正意義的在體跨尺度雙光子顯微成像技術,并在突破解析大腦“黑盒子”內部工作原理的過程中起到關鍵作用。