2018~2021年傳染性喉氣管炎在山東商品肉雞中的發生和防控*
秦卓明,馬秀麗,亓麗紅,黃兵,高月花,劉麗萍,黃迪海,秦春芝,徐懷英**
(1.山東省農業科學院家禽研究所,山東 濟南 250100;2.山東省健牧生物藥業有限公司,山東 濟南 250100)
傳染性喉氣管炎(Infectious Laryngotracheitis,ILT)是由傳染性喉氣管炎病毒(Infectious Laryngotracheitis Virus,ILTV)引起雞的一種急性、高度接觸性傳染病,主要侵害雞上呼吸道,同時對眼睛、鼻竇、氣囊和肺等組織產生影響。典型癥狀為呼吸困難、氣喘,咳出帶血分泌物、眼結膜炎和眼簾腫脹等。剖檢可見喉部和氣管黏膜腫脹、出血等,嚴重的病例則具有較高的致死性,死亡率可高達40%以上。除了ILT的典型癥狀外,ILT還可以表現為溫和型,表現為黏液性氣管炎、鼻炎、眼結膜炎、眼流淚等輕微癥狀[1]。傳統認為,該病大多數發生在成年雞和產蛋雞,雛雞感染率較低。但是,近年來,1月齡內商品肉雞發生ILT的病例不斷攀升,呈現出新的發病和流行趨勢[2-3]。
ILT是世界上第一個利用疫苗成功控制的家禽疫病,變異頻率相對較低。盡管如此,ILTV屬于DNA病毒,對外界抵抗力較強,蛋、種雞等廣泛的疫苗接種,使得ILTV野毒株普遍存在,通常每隔3~5年就流行一次[4-5]。
中國ILT最早發生在貴陽(1959)。自20世紀80年代以來,該病伴隨著我國養雞業的蓬勃發展,已逐漸成為我國重要的地方流行性疫病。過去ILT的發病主要是以已開產的蛋雞和種雞為主,雛雞和育成雞較少發生。但自2018年以來,該病在我國江蘇、山東等地的商品肉雞流行普遍[6],造成了極其嚴重的經濟損失。
1 材料和方法
1.1 發病背景
2018~2021年,山東臨沂、濰坊、棗莊等地以及江蘇連云港、徐州等地的規模化商品雞場、蛋雞場等陸續發生了一種以嚴重呼吸困難、咳血、氣管黏膜出血和充血的雞病。主要危害20~50日齡的白羽商品肉雞和地方品種雞,以30~35日齡居多。白羽肉雞的發病較多,且多數未經免疫。雞群一旦感染,則傳播速度較快,感染率在80%以上,死亡率在5%~30%,嚴重的死亡率可高達45%,幾乎無藥可治,嚴重影響雞群的生產和經濟效益。
1.2 病料處理
剖檢具有典型癥狀的發病雞或死亡雞,取其氣管黏膜或刮取黏膜黏液作為病料。病料剪碎后按1:3的比例加入滅菌的PBS溶液,反復凍融3次后,離心取上清,然后加入青、鏈霉素(2 000 U/mL) 置4 ℃冰箱過夜處理, -20 ℃保存備用。
1.3 主要試劑、材料和儀器
Simply P病毒DNA/RNA共提取試劑盒,購自杭州博日科技有限公司;DNA膠回收試劑盒,購自天根生物科技有限公司;2×Premix Taq、DL2000bp DNA Marker,購自寶生物(北京)有限公司;PCR儀,購自Thermo Fisher公司;9~10日齡SPF雞胚由山東省農業科學院家禽研究所提供。
1.4 SPF雞胚接種
將無菌檢驗合格的病料經絨毛尿囊膜(CAM)途徑接種10日齡SPF雞胚,每日照蛋,舍棄48 h內非特異性死亡雞胚,觀察至120 h,死亡胚和120 h活胚及時放置4 ℃冰箱并保存過夜。在生物安全柜內,觀察CAM和雞胚病變。同時將CAM剪碎研磨,加入PBS稀釋,反復凍融3次,離心取上清,置-20 ℃保存備用。取少量樣品提取核酸,進行ILTV鑒定。
1.5 病原核酸鑒定
以ILTV 的ICP4基因為模板,設計ILTV的鑒定用引物,建立相應的反應條件[7]。
1.6 gB基因序列測定
參考GenBank中ILTV經典株的結構蛋白gB基因序列,利用Prime preimer 5.0軟件設計引物,F:5’-TTCGTCTTCGCTTTCTTCTGCC-3’,R:5’-CGCGGTCCTGTATGCAATCC-3’,引物由華大基因合成。
按照病毒基因組DNA/RNA提取試劑盒說明書,提取樣品的DNA,-20℃保存備用。PCR反應體系為:2×Premix Taq 25 μL,待檢DNA模板2 μL,上下游引物(10 mmol/L)各2 μL,最后用RNA-free H2O補足反應體系至50 μL。PCR擴增條件為:94 ℃預變性4 min;進入94 ℃變性35 s, 58 ℃退火 45 s,72 ℃延伸 180 s,共進行33個循環;72 ℃延伸10 min,4 ℃結束反應。將PCR擴增產物在1.5%瓊脂糖凝膠中電泳,選取2 660 bp目的條帶回收后,連接pMD18-T 載體,轉化DH5α,接種LB 固體培養基培養16 h,挑取菌落進行PCR 鑒定。將陽性菌落接種LB 液體培養基增菌,送華大基因進行測序。
1.7 同源性比較和系統發育分析
從GenBank中選擇國內外的ILTV代表毒株gB核苷酸序列,利用Lasergen 7.1和MEGA5.1軟件,比較其核苷酸同源性,并采用鄰接法(Neighbor-Joining)構建支原體的系統發育樹,探討不同ILTV分離株及其與疫苗株間的遺傳距離和系統演化關系。
2 結果
2.1 臨床概況
2.1.1 流行病學 山東省農業科學院家禽研究所禽病診斷中心的檢測數據表明,雞ILT在2018年以后呈現逐年增加趨勢。2018年送檢病例24例,2021年增加到103例。在送檢的疑似ILT的278份病例中,ILT的PCR陽性檢出率高達40%,如圖1。
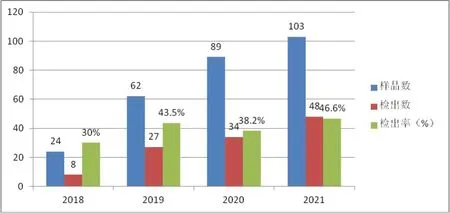
圖1 ILT疑似送檢樣品數、陽性數以及PCR陽性檢出率
2.1.2 典型案例 自2018年10月以來,臨床報導ILT的病例逐漸增多,先是地方品種雞發病。隨后,在2020年5月~2021年4月,商品肉雞發生ILT達到高峰。表1顯示的是2018~2021年間幾次典型的ILT疫情發生概況。調查顯示,首先發生ILT疫情的商品肉雞主要集中在魯南和江蘇連云港等地,該地區蛋雞和麻雞飼養密度大,且大都曾經免疫過ILTV活疫苗。相反,同地域的大部分商品肉雞當時免疫率較低。其中,2019年,魯南地區喉痘疫苗(基因工程疫苗)的免疫率僅為30%;2020年免疫率為50%;2021年,免疫接種率攀升至90%。2021年7月后,該地區商品肉雞的ILT發病率陸續降至冰點。2022年1~9月份,未見ILT發病病例。由此可見,疫苗免疫在ILT疫情的防控方面發揮了決定性作用。
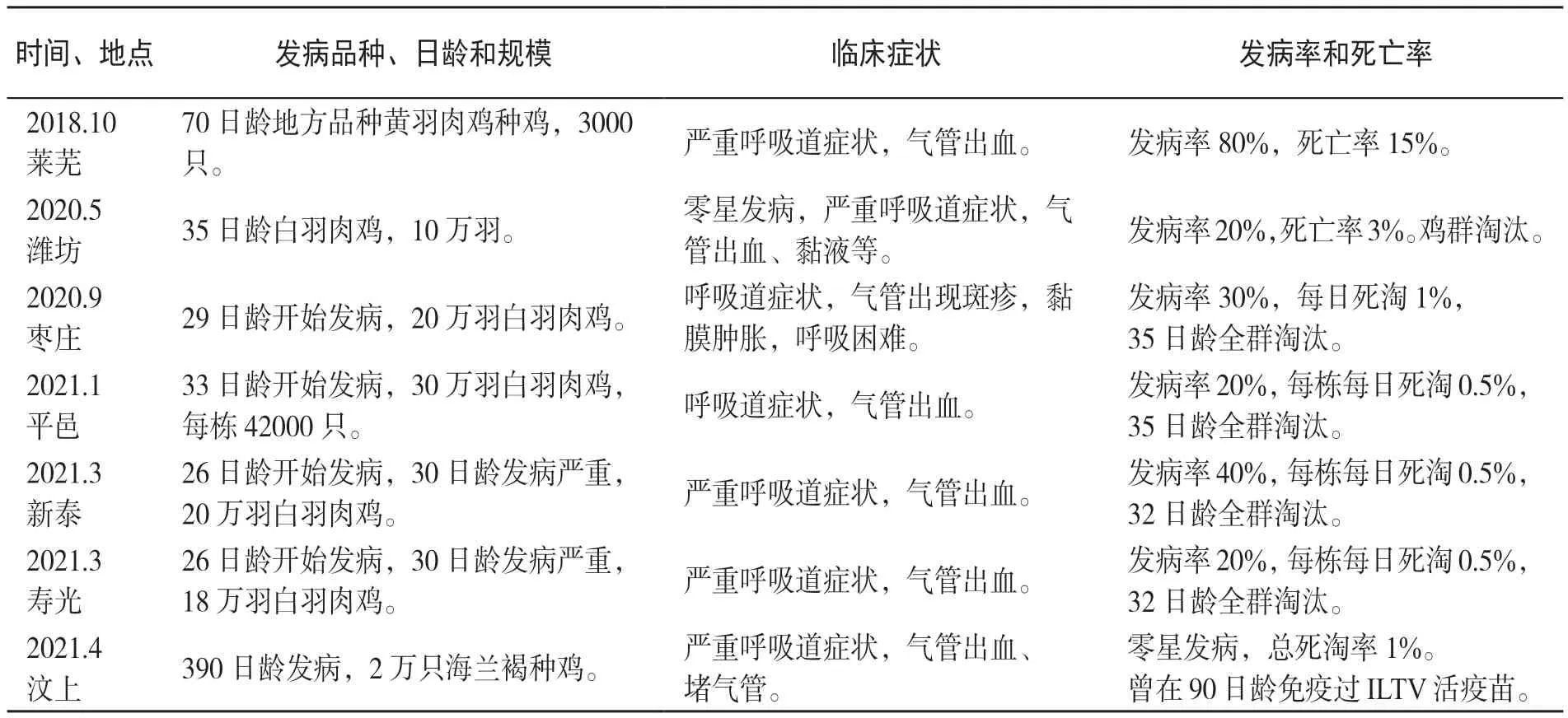
表1 典型的發病案例及其發病概況
2.2 病原分離
篩選25份不同地域、不同日齡的PCR檢測ILTV陽性雞群病料,按常規通過絨毛尿囊膜(CAM)途徑接種SPF雞胚。剖檢雞胚發現:有23份病料接種的SPF胚,其絨毛尿囊膜明顯增厚,接種部位出現典型的痘斑;且接種雞胚與SPF雞胚對照組相比,雞胚明顯發育較小,部分雞胚胚體出血,呈現出典型的ILT雞胚病變。
2.3 PCR核酸鑒定
取發生病變的CAM進行處理,利用ILTV鑒定用引物PCR擴增其ICP4基因,結果有23份有病變的雞胚分離物,其ILTV核酸PCR擴增呈陽性。相反,沒有觀察到病變的2份樣品,其ILTV核酸檢測為陰性
選取10份ILTV核酸檢測為陽性的樣品進行凝膠電泳檢測,結果如圖2。PCR產物片段大小約為570 bp,結果符合預期。對PCR產物進行序列測定,SD.JQ2020等分離株ICP4基因與美國ILTV經典雞胚疫苗株(CEO)、中國ILTV經典強毒王崗株(WG)和澳大利亞CL9毒株的同源性均為100%,證實SD.JQ2020等分離株為ILTV。
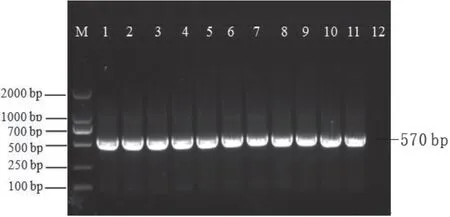
圖2 ILTV ICP4基因PCR擴增特異性鑒定結果
2.4 序列同源性分析
對ILTV 的結構蛋白gB基因的測序測定表明,其片段長度為2 652 bp。核苷酸同源性比較顯示,SD.JQ2020等分離株之間gB基因同源性為99.7%~100%;與我國廣泛使用的疫苗株K317株同源性為99.6%~100%,呈現出較高的同源性;與美國ILTV經典疫苗株CEO和TCO等同源性為99.6%~100%,也具有較高的同源性;與意大利、韓國等ILTV分離株同源性為99.6%~100%;與我國ILTV經典強毒王崗株(WG)及澳大利亞A20和VI-99等同源性為99.5%~99.8%;但與α皰疹病毒亞科馬立克病毒屬MDV(JF742597)的同源性僅為33.9%。
2.5 系統發育樹
系統發育樹(圖3)表明,SD.JQ2020等分離毒株與ILTV CEO疫苗株、我國活疫苗K317株等處于同一分支,顯示出較近的親緣關系;而與我國ILTV經典強毒王崗株(WG)、4株澳大利亞ILTV分離株遺傳距離較遠,處在兩個遺傳演化關系相對較遠的分支。這表明,目前商品肉雞ILTV流行株與我國目前常用的ILTV疫苗株遺傳關系相對較近。
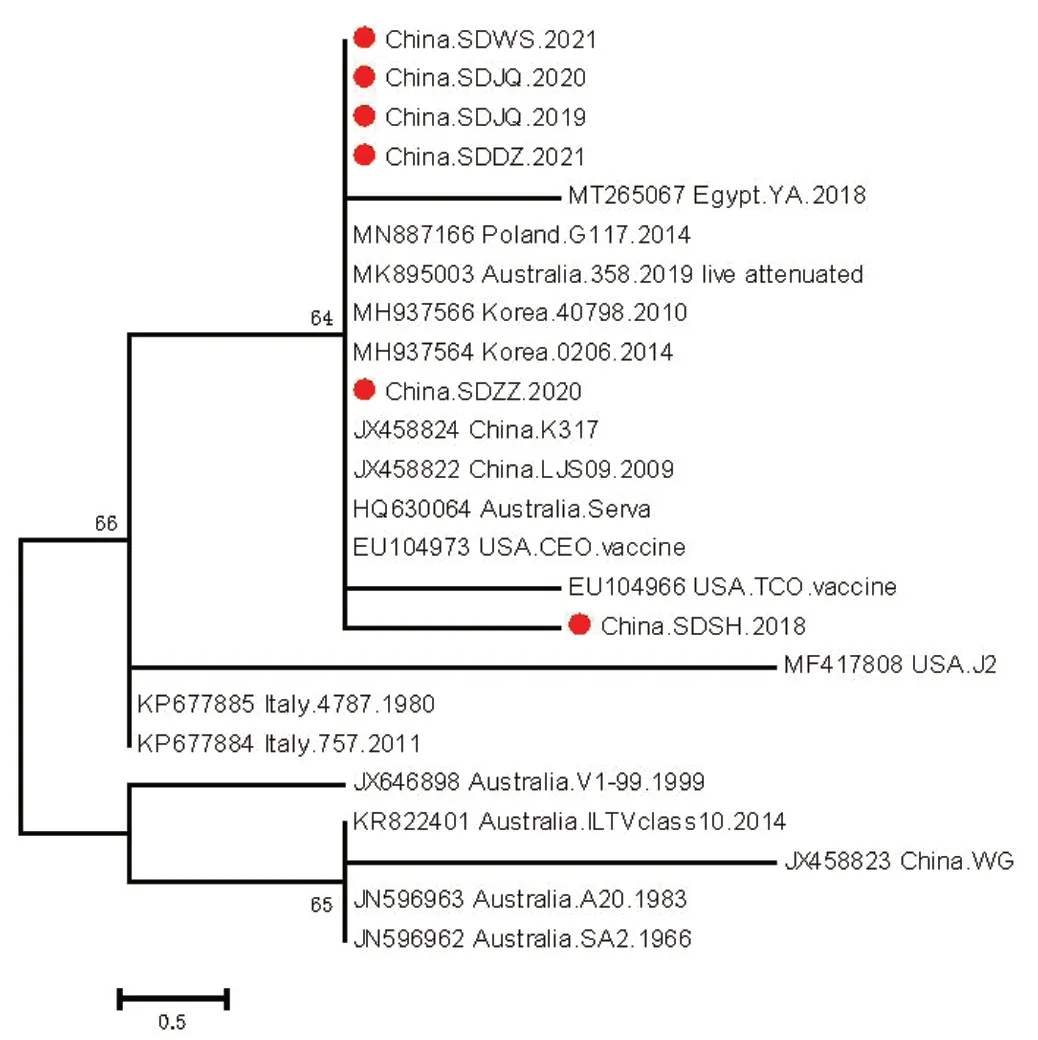
圖3 ILTV毒株gB基因系統發育樹
3 討論
3.1 成功從可疑ILT病料中分離出23株ILTV病毒株,確證了本次發生在商品肉雞、地方品種雞和蛋雞上的疫情為ILT。對ILTV 的結構蛋白gB基因的核苷酸同源性比較顯示,SD.JQ2020等分離株與我國目前在蛋雞、種雞和麻雞等廣泛使用的疫苗株K317株高度同源。這表明,此次疫情與臨床大量使用ILTV疫苗免疫高度相關[8-9]。無獨有偶,2008年美國商品肉雞發生的ILT,也與CEO疫苗免疫高度相關[10-11]。
3.2 針對魯南地區的ILT疫情溯源發現,此次ILT疫情的發生與魯南和蘇北地區家禽飼養模式密不可分。該地區蛋雞、麻雞飼養數量較大,且大都經過了ILTV活疫苗免疫。此外,魯南地區在2018年以后,商品肉雞經歷了高速的發展期,從事養殖的肉雞公司增多,新建立的雞場飼養規模較大,配套的一條龍企業如屠宰加工企業也較多,進而導致整個魯南地域家禽飼養密度較大,蛋雞與肉雞交互飼養,再加上蛋雞糞便、垃圾等清理不及時,導致疫苗毒擴散。此外,值得反思的還有,非洲豬瘟帶來的意外“肉雞火爆”行情,讓大多數養殖者被利潤沖昏了頭腦,盲目擴張,忽視了雞場的生物安全建設和管理。
3.3 疫苗是控制ILT發生最重要的技術手段。ILTV弱毒活疫苗包括雞胚來源疫苗(CEO)和組織來源疫苗(TCO),均屬于中等毒力,存在一定的安全隱患[12]。在4~12周齡(育成雞)免疫接種效果最佳。但一般不能對4周齡以下的雛雞接種,以免造成傷害。在實際生產中,個別養殖者忽視上述常識,對18日齡商品肉雞進行免疫接種,結果導致雞群發病。比較而言,基因工程疫苗似乎更適合于商品肉雞的免疫[13]。
常用的基因工程疫苗通常包括載體疫苗和重組疫苗。王云峰等(2001)利用雞痘病毒(FPV)為載體,成功表達ILTV中國王崗株gB基因,通過動物試驗表明該載體病毒無論對商品雞還是SPF雞的免疫保護均具有較高的保護性[14]。此外,國外有兩個成熟的商業重組ILTV疫苗,在臨床應用較廣[15]:一是由CEVA公司生產(Biomune公司),其以FPV作為載體插入ILTV的gB和UL32基因,特點是見效快,適合于商品肉雞;二是由Intervet公司生產,將ILTV的gI和gD基因克隆到火雞皰疹病毒(HVT)基因[16],特點是維持期長,適合于蛋種雞。上述兩種疫苗均適合于胚胎接種或1日齡雛雞接種,安全系數較高。
3.4 經歷了2020~2021年的ILT疫情后,不同的家禽飼養企業加大了針對ILTV疫苗的免疫[17]。以魯南地區為例,至2021年6月份,90%以上的魯南雞場分別采用CEVA公司生產的喉痘疫苗進行了ILTV的疫苗接種。同時,各公司加大了各飼養廠區的生物安全管理[18]。具體表現在:一是強化疫苗接種;二是將雞舍空舍時間延長10 d以上,重視空舍期間的衛生消毒;三是合理布局新雞場,最大限度地規避與蛋雞場、麻雞場等不同雞場的生物安全距離;四是加強了對外來車輛的管理,禁止外來車輛進入;五是加強了對雞場糞便及其污染物的處理。通過以上綜合措施的實施,2021年7月以后的ILT疫情大幅度減少。持續的跟蹤檢測顯示,2021年10月~2022年9月,魯南地區ILT的發病幾乎為零,達到了理想的控制效果。

