矢車菊素-3-葡萄糖苷的生理功能及其穩態化技術研究進展
王 渝,朱千林,楊榮玲,何曉希,畢艷紅,趙祥杰,鄭雙濤
(淮陰工學院生命科學與食品工程學院,江蘇淮安 223003)
花青素是黃酮類化合物的一種,具有C6-C3-C6碳骨架結構,是一種天然無毒的水溶性色素[1],廣泛存在于自然界中各種水果、蔬菜及谷物中,如桑葚、葡萄、紫薯、黑豆等,能夠使植物呈現各種不同的顏色。花青素化學性質活潑,通常以酚羥基糖苷化形式的花色苷存在,根據苷元和糖苷配體的不同可形成多種花色苷。存在于植物中的苷元主要有6 種:天竺葵素、矢車菊素、芍藥素、飛燕草素、牽牛素和錦葵素[2]。其中,矢車菊素-3-葡萄糖苷(cyanidin-3-glucoside,C3G)是一種最常見的花青素,存在于黑米、黑豆、紫薯和許多五顏六色的漿果中,具有抗氧化、抗癌、保護視力、保護胰島、預防糖尿病等作用。但在其應用過程中,往往存在穩定性差、不易儲藏、親脂性低、不易被人體吸收等問題,因此國內外許多研究者對花青素的結構修飾進行了深入研究,以便花青素更好地被應用于化妝品、醫療、保健品等行業。本文對矢車菊素-3-葡萄糖苷的性質和多種生理功能進行了綜述,并展示了多種矢車菊素-3-葡萄糖苷穩態化制備方法,為矢車菊素-3-葡萄糖的進一步研究和利用提供參考。
1 C3G 的性質及提取來源
1.1 C3G 的性質
C3G 是自然界最常見且相對穩定的一種花青素[2]。C3G 具有多種生物活性,但因其性質較為活潑,結構穩定性差,容易受多種因素影響而發生降解,使其生物活性的發揮受到諸多限制[3]。花青素的穩定性主要受pH 值影響,在酸性介質中更穩定。此外,花色苷易受外界環境諸如氧氣、光照、溫度、水活度等的影響而發生結構改變,甚至功能喪失,因此常通過多種方法保持其結構穩定性[4],進而在腸道部位定向釋放[5],從而發揮其最大生物活性,提高其應用價值(圖1)。
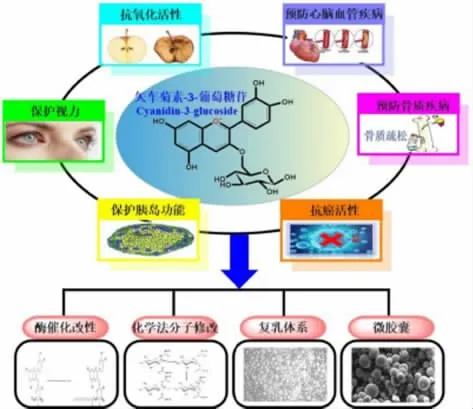
圖1 C3G 的來源、功能與穩態化技術Fig.1 Source,function and steady-state technology of C3G
1.2 C3G 的來源及提取
在自然界中C3G 存在于各種植物中,尤其是深色果蔬及谷物中[6-7],如葡萄、桑葚、藍莓、草莓、紫甘藍、黑米等。此外,目前有許多學者在不同的植物中發現了C3G,如水果中的阿薩伊、黑果腺肋花楸、草莓、藍莓,蔬菜中的紫甘藍,谷物中的黑豆和黑糌粑以及茶葉中等[6-7]。
在進行花色苷提取的過程中,不恰當的提取方法會導致花色苷發生降解,從而降低得率,因此在花色苷的研究中提取工藝是極其重要的環節。有機溶劑提取法是目前提取花色苷應用最多的一種方法,具有操作簡單、成本較低、容易實現等特點[8]。許多學者通過不同的有機溶劑提取了阿薩伊[9]、黑果腺肋花楸[10]、草莓[11]、紫甘藍[13]、黑豆[14]、古茶[15]、黑糌粑[16]、桑葚[17]、楊梅[18]等植物中的C3G,并測定了其中C3G 的含量。研究發現,不同植物來源的C3G 含量范圍在0.001~12.829 mg/g 之間(見表1),其中黑豆中的C3G 含量最高,但不同品種黑豆中C3G含量亦不同,楊梅中含量較低;不同植物來源的C3G在提取過程中,單純溶劑提取法綜合提取效果不理想,多數采用輔助提取技術,增強了提取效果,而超聲處理為當前最有效的輔助手段。因此針對不同植物原料開展專門提取工藝優化以及采用其他溶劑體系和利用其他輔助技術進一步提高C3G 的提取效率也是以后研究的重點。
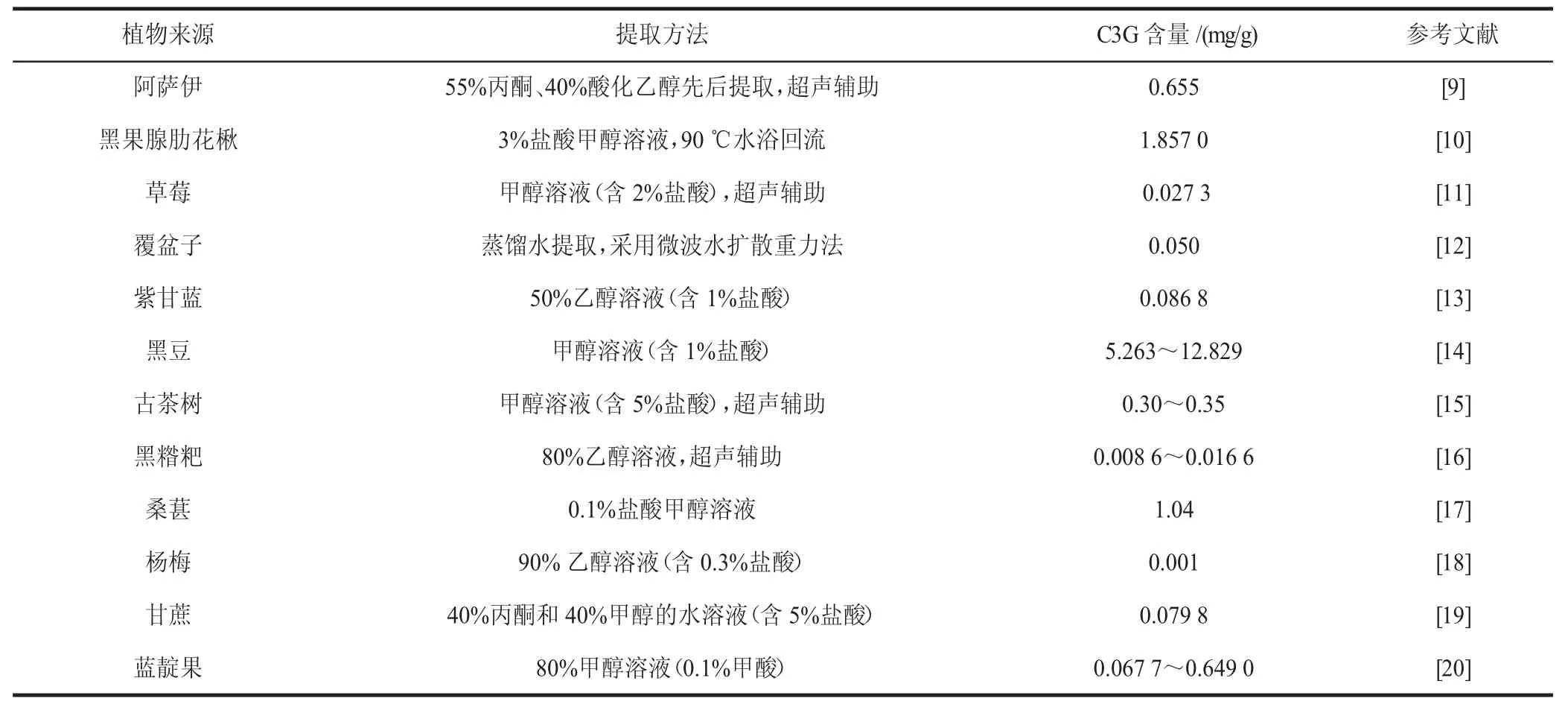
表1 不同植物來源的C3GTable 1 C3G from different plant sources
1.3 C3G 的主要生理功能
1.3.1 抗氧化
C3G 是自然界存在的最普遍的、相對穩定且易于獲得的一種花青素。矢車菊素可通過多種途徑清除自由基,并且清除自由基能力、還原力及抗氧化能力都要優于其它花青素提取物,其抗氧化活性在人類植物膳食以及保健品方面都有極其重要作用,對于保持身體的健康至關重要[19-20]。Sukprasansap 等[21]研究表明,C3G 作為一種天然的抗氧化物質,可以通過抑制谷氨酸誘導的氧化和ER 應激信號以及激活ERK/Nrf2 抗氧化機制途徑而成為一種神經保護劑。此外,重金屬也會對機體發揮正常的抗氧化功能造成干擾,導致體內大量自由基存在,從而對機體造成氧化損傷[22]。研究表明,C3G 可以通過清除自由基來緩解由重金屬引起的性激素分泌紊亂和生殖損傷,從而起到保護作用[23-24]。
1.3.2 保護視力
白內障是全球排名第一位的嚴重致盲性眼病,而導致白內障的關鍵原因是自由基及其引發的氧化應激效應導致了晶狀體生理功能發生改變[25]。矢車菊素及其糖苷具有清除自由基、調節免疫等生物活性,已成為國內外視力保護研究的熱點。其中C3G 在體外糖尿病型白內障模型中顯示出了抗晶狀體渾濁功能[25]。李翔等[26]通過逆相蒸發法制備得到TMC 修飾的C3G 脂質體(TMC-modified C3G-loaded liposomes,C3G-TCL),通過采用乳鼠白內障動物模型對晶狀體渾濁度及生化指標測定,評價了C3G-TCL 對眼部應用的效果,結果表明C3G-TCL 可恢復受氧化損傷眼部細胞的活力。張婧等[27]利用逆相蒸發法制備眼用TMC 修飾的1 脂質體(cyanidin-3-glycoside(1)-title liposomes,1-TCL),利用星點設計-效應面法,以包封率為評價指標,篩選獲得了1-TCL 的優化配方,并考察了1-TCL 對H2O2致氧化損傷的人晶體上皮細胞(human lens epithelial cells,HLECs)的保護效果,結果表明,1-TCL 能顯著提升HLECs 的細胞活力,說明其對HLECs 的保護能力,具有潛在的視力保護功效。綜上所述,C3G 在保護視力和治療白內障方面具有重要的應用效果及開發價值。
1.3.3 保護胰島功能
肥胖是一種全球流行病,會導致2 型糖尿病、高血壓、心血管疾病和某些癌癥的患病率急劇增加。已有研究表明,C3G 具有降低血糖、抑制肥胖及改善胰島素抵抗的作用[28-30]。Qi 等[28]通過建立糖尿病腎病大鼠模型,對其給予C3G 治療56 d,并以賴諾普利治療為陽性對照,研究發現C3G 可降低血糖,預防胰島素抵抗,修復糖尿病大鼠的腎功能,預防糖尿病大鼠腎間質纖維化、腎小球硬化和氧化應激。Sasikumar 等[29]通過細胞培養實驗發現C3G可保護胰腺β細胞免受氧化應激誘導的凋亡,從而起到保護胰島的作用。此外,有研究表明C3G 可以通過改善糖類代謝紊亂狀態,進而降低胰島素抵抗,從而達到預防肥胖、心腦血管等疾病發生的目的[30]。
1.3.4 抗癌
C3G 作為一種黃酮類化合物,具有黃酮類化合物的良好抗癌作用,且對機體的毒副作用較小,能夠抑制結腸炎及結直腸癌的發生和發展[31]。王麗等[32]研究了C3G 對結腸癌的增殖及TOPK 激酶活性影響,結果表明C3G 通過靶向TOPK 抑制結直腸癌的生長。宋柬等[33]研究了不同濃度C3G 對環氧丙酰胺引起的人類乳癌細胞MDA-MB-231 毒性的影響,結果表明C3G 對環氧丙酰胺引起的MDA-MB-231 細胞毒性具有非常明顯的抑制作用。
C3G 具有清除自由基、抗突變等生物活性,能夠抑制多種腫瘤的生長,誘導腫瘤細胞凋亡。Liang 等[34]研究表明,C3G 可以降低三陰性乳腺癌細胞系MDA-MB-231和BT-549 的遷移和侵襲性,還能減弱三陰性乳腺癌的NF-κB 代謝通路,逆轉上皮細胞-間充質惡性轉化,具有抗乳腺癌的作用。Zhao 等[35]研究發現C3G 可以保護HepG2 細胞免受由2-氨基-3-甲基咪唑并[4,5-f] 喹啉(IQ)所誘導的細胞毒性,主要通過與X-連鎖凋亡抑制蛋白(X-linked inhibitor of apoptosis protein,XIAP)的BIR3結構域進行緊密結合,抑制XIAP 靶蛋白引發的細胞凋亡,從而使C3G 具有預防雜環芳香胺的致癌風險。
1.3.5 預防骨質疾病
骨質疏松癥是一種多發于老年人群的慢性疾病,當前大量化學藥物用于骨質疏松癥治療,但長期用藥會對身體產生副作用。有研究顯示花色苷對骨骼健康有促進作用,富含花色苷的食物可以降低骨質疏松癥的發生率[36]。Cheng 等[37]發現C3G 鹽酸鹽能抑制破骨細胞形成、羥基磷灰石吸收以及通過核因子(NF-κB)受體活化因子配體信號通路(RANKL)誘導的破骨細胞標志基因表達,進而抑制RANKL 誘導的NF-κB 活化,并減弱細胞外信號調節激酶的磷酸化,具有治療溶骨性疾病的潛力。Samarpita 等[38]發現C3G 能減弱血清白介素-17A(IL-17A)細胞因子信號介導的單核細胞遷移和向類風濕關節炎成熟破骨細胞分化。C3G 在分子水平上阻斷p38 MAPK 信號通路的激活,從而響應IL-17A 的作用,這為C3G 治療由IL-17A 信號介導的類風濕性關節炎提供了支持。
1.3.6 預防心腦血管疾病
近年來,心血管疾病(cardiovascular disease,CVD)成為工業化國家和發展中國家的主要健康問題,高發病率和高死亡率給社會帶來了沉重的健康和經濟負擔[39]。目前的藥物治療可以使心血管疾病得到一定的控制,然而,很多藥物具有一定的副作用,因此,迫切需要探索新的有效治療方法。已有研究表明,富含植物花色苷食物的攝入與CVD 的發病呈負相關[40],這也為花色苷物質在心腦血管疾病中的應用提供了重要參考。鄧秀娟等[41]研究證實了C3G 能夠抑制高膽固醇血小板顆粒物釋放,從而對心血管具有保護作用,起到預防心血管疾病的作用。姚艷玲等[39]研究證實了C3G 能降低小鼠的血脂水平,顯著降低小鼠頸動脈斑塊面積,并可干預高脂飲食組小鼠血清中趨化因子,使CXCL12 和CCL2 降低水平達到顯著程度,從而對高脂飲食組小鼠的血脂異常和動脈斑塊形成具有明顯的改善作用。Ya 等[42]證明了C3G 在體外可促進活化的血小板凋亡,促進巨核細胞的增殖、分化和原血小板的形成。張莉珂[43]通過小鼠實驗發現花色苷能夠降低高脂血癥引起的小鼠血小板凋亡,并對減少健康小鼠血小板凋亡具有一定的預防作用。此外,C3G對缺血性卒中也具有一定的治療作用。韓旭等[44]研究表明,C3G 能夠通過多種途徑改善缺血性卒中的神經功能轉歸,從而對缺血后的腦損傷具有保護作用。雖然C3G在人體健康中發揮多種生理功能,在食品和醫藥等行業中有巨大發展潛力,但當前藥理活性及功能評價較少在人體中開展,對其毒理學和遺傳影響的研究尚不足,有待于進一步研究。
2 C3G 的穩態化技術
C3G 在功能食品開發中有著巨大的潛在應用價值,但因其性質活潑、結構不穩定,在貯存和加工過程中容易受到外界環境影響而發生降解,使其生物利用度顯著降低。同時,花色苷是非脂溶性物質,較難穿過細胞膜的磷脂雙層結構,大大降低了其應用效果。因此可以通過結構修飾改性和載體包封的方式對C3G 進行穩態化制備,結構修飾后的C3G 在脂溶性和穩定性上得到顯著提升,從而提高其利用率,而載體包封或乳液共溶后的C3G 可以有效抵御機體逆性環境的影響,達到在腸道部位定向釋放的目的,提高其生物活性。到目前為止,生物酶催化改性法、化學法分子修飾改性法、微膠囊法等均是對花色苷進行穩態化制備的重要方法[45-48]。
2.1 結構修飾提升穩定性
2.1.1 生物酶催化改性
花色苷的酶促酰化通常是使用脂肪酶和短鏈到長鏈的脂肪酸作為酰基供體來進行的,有機溶劑是目前非水相酶催化應用和酶學研究最為廣泛的體系[49]。相比于化學法,酶促酰化反應所需的反應條件溫和,具有更高的區域選擇性。Zhang 等[50]采用固定化脂肪酶催化脂肪酸甲酯對C3G 進行酰基化修飾,研究證明C3G 與中鏈脂肪酸的酰化衍生物比C3G 具有更好的穩定性和抗氧化活性。Yan 等[51]以芳香酸甲酯為酰基供體,脂肪酶做催化劑,與黑米花色苷進行酶促酰化反應,反應提高了花色苷的熱穩定性和耐光性。外國學者通過酶促反應增加飽和脂肪酸的鏈長,改善了C3G 的脂溶性,并研究了其在親脂介質不同pH 值下的熱穩定性,與未經修飾的C3G相比,親脂性C3G 衍生物表現出更好的顏色穩定性和更低的熱降解敏感性[52]。與天然的C3G 相比,通過酶促法合成的矢車菊素-3 -葡萄糖苷月桂酯(cyanidin-3-glucoside lauryl ester,C3G-C12)的脂溶性、pH 電阻率和熱穩定性都有顯著提高[53]。
2.1.2 化學法分子修飾改性
在對花青素的化學修飾方面,主要以有機合成技術為基礎,因此選擇適當的酰化劑和催化劑是化學修飾研究改性的關鍵[54]。酰化反應降低了極性,增加了分子尺寸,改變了花色苷的空間結構,從而改變了它們的化學反應性和穩定性。趙立儀[54]通過引入月桂酸的長脂肪鏈對C3G 進行酰化修飾,酰化后C3G 的親脂性和穩定性得到了明顯的提高。C3G的酯交換酯化反應見圖2。李穎暢等[55]將花青素和乙酸進行酰化反應,通過紫外光譜和紅外光譜對酰化反應進行分析確定,結果證明酰化后的花青素穩定性明顯提高。
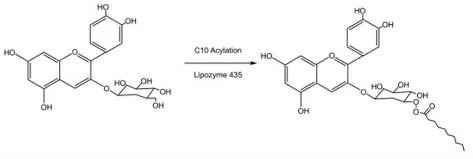
圖2 C3G 的酯交換酰化反應Fig.2 Transesterification of C3G
2.2 遞送系統保持穩態化
穩態化技術除了各類反應讓化合物分子傷筋動骨保持性能穩定外,還可以通過改變溶劑性能使其穩定。隨著技術的不斷進步,除了通過傳統的生物酶法和化學法對C3G 改性外,還出現了許多新的改性方法,如微膠囊包埋和復乳體系。
2.2.1 復乳體系
復乳又稱“多重乳液”“乳中之乳”,指將簡單乳液包裹于另外一種連續相中,包括將水包油型(O/W/O)、油包水型(W/O/W),還包括將固體分散于油相中再分散于連續的水相中(S/O/W),其中W/O/W 型比較常見。W/O/W型復乳是指將內水相分散在油相中,再將這個包有水滴的油相分散在水中,以此形成一個兩面三相的結構[5]。袁麗等[5]以離心保留率、流變性、顯微結構為指標對復乳制備工藝和配方進行優化,利用優化后的W/O/W 體系包埋C3G,發現該體系具有較好的包埋C3G 功能,能夠提高C3G 的穩定性。
2.2.2 微膠囊包埋
微膠囊化是以碳水化合物、蛋白質、多糖、脂類或人工合成高分子材料為壁材包埋小分子活性物質,并可在特定條件下釋放的技術[4,56]。錢柳等[57]利用熱改性方法構建乳清蛋白納米粒子運輸載體,通過納米粒的粒徑電位和載藥性能變化確定WP-C3G 納米的最佳比例,研究發現C3G 和WP 結合后能夠改善其腸胃消化穩定性和貯藏穩定性。Chen 等[58]發現利用微囊化技術,對多酚類化合物進行封裝,可以提高酚類化合物的生物利用度。
雖然微膠囊化可以提高C3G 的穩定性,但操作復雜,可能會對C3G 的生物活性造成一定的損傷。因此,又有學者通過不同的方法來提高C3G 的穩定性。Sun 等[59]研究了殼聚糖(chitosan,CS)、殼寡糖(chitosan oligosaccharide,CSO)和羧甲基殼聚糖(carboxymethyl chitosan,CMC)與離子交聯劑γ-聚谷氨酸(polyglutamic acid,PGA)或氯化鈣結合,制備了負載C3G 的納米顆粒,其中C3G-CMC-CaCl2納米顆粒包封效率和負載效率均為最高,顯著提高了C3G 的穩定性,擴展了其在食品加工中的應用。Li 等[60]利用絲素蛋白多肽與桑椹中的矢車菊素-3-葡萄糖苷結合,從而提高了C3G 的理化穩定性。
3 總結與展望
隨著生活水平的提高,人們對健康食品的要求也越來越高,C3G 作為花色苷中的一種重要成分,也是其主要活性成分,具有多種生理活性,在食品、化妝、醫療等方面具有較大的市場。但由于C3G 穩定性差和生物利用度較低,目前對C3G 的研究還存在許多不足之處,以后的研究應從以下幾個方面進行:(1)加強C3G 穩態化制備技術研究,分別從微膠囊技術、共輔色技術、乳液技術等方面開發新的穩態化工藝;(2)開展C3G 綠色催化介質理性設計及其催化工藝研究,確定酰化產物構效關系,制備具有較高生物活性的酰化產物;(3)含C3G 食品的非熱和熱加工條件下的穩定性研究,考察不同大分子對C3G 的熱降解動力學,同時考慮食品添加劑、營養素、風味物質等對花色苷的影響,尋找穩態化效果更佳的制備工藝和工藝條件,擴大其在食品等產業中應用范圍。花色苷來源廣泛,具有顯著的資源優勢,因此,對C3G 的穩態化進行深入研究具有重要實際意義。

