伊托必利對重癥患者營養不良及腸道屏障功能的改善效果評估
王啟明 劉漢影 陳小云
危重癥患者往往存在營養不良的問題,特別是胃腸道功能紊亂,營養攝入嚴重不足,具有更高的營養不良風險[1]。長期的營養不良可影響機體的組織、器官結構以及功能,容易出現多臟器功能不全,導致肺功能、呼吸肌收縮功能以及免疫功能等損傷或者紊亂,造成患者嚴重感染,從而增加死亡風險[2]。危重癥患者營養不良是病情加重、治療難度增加的關鍵因素,也是影響患者預后的危險因素,因此改善患者消化功能并及時補充營養具有重要意義。目前,臨床上常采用腸內營養治療,同時配合益生菌腸內營養干預可一定程度改善患者免疫功能,糾正體內菌群失衡狀態以及調節營養狀態[3]。研究認為[4],胃動力改變是導致疾病發生、發展的重要因素,通過恢復胃腸道的功能可有效改善患者消化不良、吸收減退等癥狀,為重癥營養不良提供新的治療選擇。伊托必利是常見的胃腸道促動力藥,已廣泛應用于功能性消化不良引起的各種癥狀[5],本文將通過實例進一步探討,旨在為臨床治療提供理論依據。
1 資料與方法
1.1一般資料 選取2020 年1~12 月期間本院收治的108 例重癥患者,根據入組先后順序依次編號,并采用隨機數字表法分為對照組和觀察組,每組54 例。兩組患者的性別、年齡、體重、急性生理學及慢性健康狀況評分系統(APACHE Ⅱ)評分及病因等一般資料比較,差異無統計學意義(P>0.05),具有可比性。見表1。本研究經本院倫理委員會批準。
表1 兩組患者一般資料比較(n,)
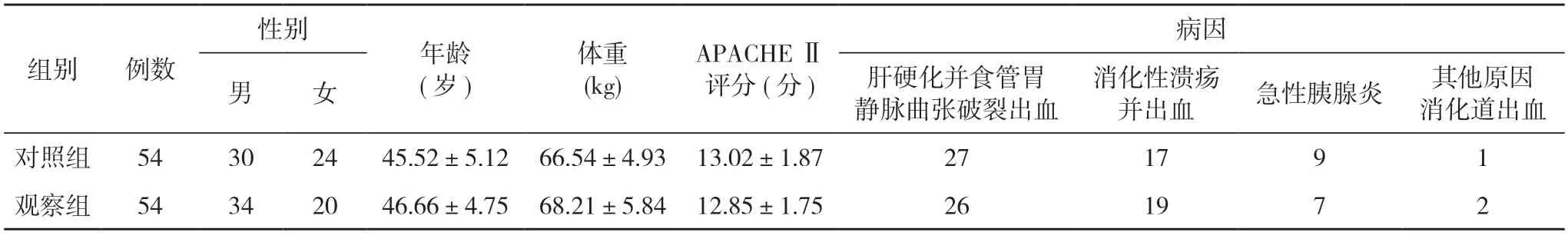
表1 兩組患者一般資料比較(n,)
注:兩組比較,P>0.05
1.2納入及排除標準
1.2.1納入標準 ①MNA-SF 評分<11 分(表明營養不良);②入組前1 d 完成肝腎功能、血糖、血脂等相關檢查;③意識清楚,可以配合治療;④入組患者知情同意。
1.2.2排除標準 ①不能行腸內營養、近期手術、惡性腫瘤;②近期有抗生素應用史;③病程中出現腸穿孔、腸壞死、完全性腸梗阻等腸道不良事件。
1.3方法 在入院后,對所有患者進行基礎性治療,并給予常規腸內營養治療以及益生菌腸內營養干預,包括使用腸內營養粉劑(商品名:安素,美國雅培制藥有限公司)和服用益生菌制劑(規格:0.5 g/片),55.8 g腸內營養粉劑加入到200 ml 涼水中,攪拌溶解,配置成250 ml 營養劑,3 次/d,250 ml/次,服用或管飼;益生菌制劑每片含保加利亞乳桿菌和嗜熱鏈球菌活菌≥0.5×106CFU、長雙歧桿菌活菌≥0.5×107CFU,3 次/d,3 片/次。觀察組在此基礎上口服伊托必利(上海雅培制藥有限公司,規格:50 mg/片),3次/d,1片/次。兩組患者均治療2 周。
1.4觀察指標及判定標準
1.4.1營養狀態 分別于治療前、治療2 周后評估患者營養狀態。檢測血清TP、Alb、Hb 水平,使用全自動生化分析儀進行檢查。采用微營養評估量表(mininutritional assessment,MNA-SF)進行營養狀態評估,包括患者的體質量指數(BMI)、神經疾病、飲食變化、應激狀況、活動能力等情況,總分14 分,分值越高表明營養狀態越好。
1.4.2胃腸功能 分別于治療前及治療2 周后采集所有患者晨起空腹外周靜脈血5 ml,應用酶聯免疫吸附試驗法(ELISA)(武漢博士德生物工程有限公司)檢測腸脂肪酸結合蛋白(intestinal fatty acid binding protein,IFABP)、血管活性腸肽(vasoactive intestinal peptide,VIP)水平。
1.4.3腸道屏障功能 分別于治療前及治療2 周后檢測患者血液D-乳酸、二胺氧化酶及細菌內毒素水平。采用JY-DLT 腸道屏障功能生化指標分析系統進行檢測,聯檢試劑盒購自于北京中生金域診斷技術有限公司,正常值范圍:D-乳酸≤15 mg/dl、二胺氧化酶≤10 U/L、細菌內毒素≤20 U/L。
1.4.4不良事件發生情況 統計治療期間患者不良事件發生情況,如惡心嘔吐、腹痛腹瀉、食欲減退、感染等。
1.5統計學方法 采用SPSS23.0 統計學軟件進行統計分析。計量資料以均數±標準差()表示,采用t 檢驗;計數資料以率(%)表示,采用χ2檢驗。P<0.05 表示差異具有統計學意義。
2 結果
2.1兩組患者營養狀態比較 治療前,兩組患者血清TP、Alb、Hb 水平以及MNA-SF 評分比較,差異無統計學意義(P>0.05);治療2 周后,兩組患者血清TP、Alb、Hb 水平以及MNA-SF 評分均高于本組治療前,且觀察組患者血清TP、Alb、Hb 水平以及MNA-SF 評分均高于對照組,差異具有統計學意義(P<0.05)。見表2。
表2 兩組患者營養狀態比較()

表2 兩組患者營養狀態比較()
注:與本組治療前比較,aP<0.05;與對照組治療后比較,bP<0.05
2.2兩組患者胃腸功能比較 治療前,兩組患者IFABP、VIP 比較,差異無統計學意義(P>0.05);治療2 周后,兩組患者IFABP 低于本組治療前,VIP 高于本組治療前,且觀察組患者IFABP 低于對照組,VIP 高于對照組,差異具有統計學意義(P<0.05)。見表3。
表3 兩組患者胃腸功能比較()

表3 兩組患者胃腸功能比較()
注:與本組治療前比較,aP<0.05;與對照組治療后比較,bP<0.05
2.3兩組患者腸道屏障功能比較 治療前,兩組患者D-乳酸、二胺氧化酶、細菌內毒素比較,差異無統計學意義(P>0.05);治療2 周后,兩組患者D-乳酸、二胺氧化酶、細菌內毒素均低于本組治療前,且觀察組患者D-乳酸、二胺氧化酶、細菌內毒素均低于對照組,差異具有統計學意義(P<0.05)。見表4。
表4 兩組患者腸道屏障功能比較()

表4 兩組患者腸道屏障功能比較()
注:與本組治療前比較,aP<0.05;與對照組治療后比較,bP<0.05
2.4兩組患者不良事件發生情況比較 觀察組患者惡心嘔吐、感染發生率明顯低于對照組,差異具有統計學意義(P<0.05);兩組患者腹痛腹瀉、食欲減退發生率比較,差異無統計學意義(P>0.05)。見表5。

表5 兩組患者不良事件發生情況比較[n(%)]
3 討論
重癥患者的內環境失衡,且處于應激狀態,導致胃腸激素調節紊亂,能量消耗增多,并出現消化功能、胃腸功能障礙。同時,重癥患者往往有意識障礙、吞咽困難、呼吸困難等癥狀,無法自主進食,機體需消耗自身貯存的能量以維持正常的生理機能,導致營養供求失衡,容易出現營養不良,進而引起多器官功能衰竭,增加死亡風險[6,7]。營養支持治療通過提供充足的營養以滿足機體的代謝需求,其中腸內營養支持較為常見,可以抑制腸道細菌移位,維護患者胃腸功能正常,防止因胃腸功能受損而導致的器官衰竭、病情惡化[8]。本次研究發現,治療2 周后,兩組患者血清TP、Alb、Hb 水平以及MNA-SF 評分均高于本組治療前,且觀察組患者均高于對照組,差異具有統計學意義(P<0.05)。表明常規腸內營養干預可改善重癥患者的營養狀態,在此基礎上聯合伊托必利治療效果顯著。丁丞章等[9]及Lu 等[10]研究認為,患者接受益生菌腸內營養干預后,可有效抑制病原菌大量繁殖,改善腸道菌落紊亂狀態,并且維護腸道黏膜的正常功能,進而減少有害物質進入血液循環,故而本次研究發現治療2 周后,兩組患者的血清D-乳酸、二胺氧化酶、細菌內毒素均呈下降趨勢。說明常規腸內營養治療以及含益生菌腸內營養干預可有效促進重癥患者的腸道屏障功能恢復,進而降低細菌內毒素等有害物質對機體的刺激或者損傷,利于患者營養狀態以及生理功能的恢復。
研究認為[11,12],危重癥患者營養不良現象非常多見,與患者機體代謝因素、能量消耗以及胃腸道消化功能狀態有關,在開展營養治療、腸道菌群調節的過程中積極主動恢復患者的胃腸動力學狀態對于疾病的治療具有重要意義。伊托必利具有抑制乙酰膽堿酯酶活性以及阻滯多巴胺D2受體的作用,同時還能刺激乙酰膽堿的釋放,從而增強胃、十二指腸的運動,以及促進胃排空,已成為治療胃動力障礙引起的消化性不良的常用選擇[13,14]。本次研究結果表明伊托必利可改善重癥患者的胃腸功能。伊托必利可通過調節自主神經系統而改善胃腸道功能,進而促進胃腸道動力學,改善消化道不良癥狀,故而本次研究發現觀察組患者經治療后惡心、嘔吐癥狀發生率明顯低于對照組,差異具有統計學意義(P<0.05)。楊勇等[15]研究認為,腸內營養劑可以加快蛋白質合成,增強體內免疫反應,而益生菌腸內營養干預可保護腸道功能的完整性,促進免疫球蛋白A(IgA)的分泌,同時還能促進淋巴細胞分裂以及調控T 淋巴細胞的分泌功能,兩者協同作用改善免疫功能,從而降低感染風險。王石健等[16]通過動物實驗表明,伊托必利可通過抑制MAPK 信號通路(抑制cleaved、Caspase-3、NF-κB 等的表達),以及增加胃黏膜緊密連接蛋白(Occludin、ZO-1)的表達,減少胃上皮細胞凋亡,促進損傷胃黏膜的修復,增強胃黏膜屏障功能。同時,配合使用益生菌,改善腸道菌群以及抑制內毒素釋放,從而減少毒素、病原菌從腸腔釋放入腸壁的淋巴或血液循環中,降低血清細菌內毒素水平以及降低腸源性感染風險,利于疾病的預后。
綜上所述,伊托必利可改善重癥患者的營養不良狀態,促進腸道屏障功能的恢復,糾正胃腸功能紊亂,降低不良事件發生風險,具有良好的臨床應用價值。

