腦-骨交互視閾下應對抑郁癥與骨質疏松癥的運動調節機制研究進展
徐 帥 ,沈 飛
抑郁癥(depression)和骨質疏松癥(osteoporosis)是本屬2個不同體系的疾患形式,亦是重要的合并癥(Bellanti et al., 2020)。現代醫學研究策略中的生物-心理-社會結構融合,為抑郁癥和骨質疏松癥共發病機制提供了新的研究思路。基于整合醫學領域,下丘腦-骨骼信號傳導和骨骼-下丘腦信號傳導的交互機制,為骨-腦信號交互提供了更為深遠的研究(徐帥 等,2021),尤其是在腦和骨骼之間的傳遞機制中,腦-骨交互為抑郁癥和骨質疏松癥的密切相關搭建出腦-骨網絡學說,是抑郁癥和骨質疏松癥相關性研究在現代醫學發展前沿領域的最新理論。運動為二者共同干預的手段,通過運動調節探索腦-骨交互視閾下中抑郁癥與骨質疏松癥之間的聯系,進一步挖掘新視角下應對腦-骨之間雙向信息交流和功能整合的研究機制。
現有抑郁癥和骨質疏松癥的研究基礎存在以下研究認知:其一,抑郁形成的機體內部變化導致骨質疏松的發生,骨質疏松是抑郁癥引發的后果;抑郁誘導的異常行為,導致不良行為習慣,間接引發骨質疏松形成。其二,骨質疏松癥誘導抑郁機制,骨質疏松癥患者多存在悲傷、沮喪和抑郁情緒,其抑郁情緒來源于骨質疏松中機體的功能性退化;骨質疏松引起骨骼內分泌能力減弱,誘發抑郁癥的發展。運動作為非藥物治療手段,對抑郁癥和骨質疏松癥均具有功能改善作用(徐帥 等,2019;薛香莉等,2019)。本研究通過分析抑郁癥的生理功能變化對骨骼質量的影響,以及骨質疏松癥的生理功能變化對抑郁患病機制的影響,探討抑郁癥和骨質疏松癥之間的腦-骨交互機制(Aloumanis et al.,2013)。
1 抑郁癥誘發骨質疏松的生理學基礎及運動干預
抑郁癥導致骨質減少/骨質疏松發生的潛在機制中,可通過刺激促腎上腺皮質激素釋放激素(corticotropin-releas?ing hormone, CRH),誘導促腎上腺皮質激素(adrenocortico?tropic hormone,ACTH)、藍斑(locus coeruleus)、促性腺激素釋放激素(gonadotropin-releasing hormone, GnRH)、生長激素抑制素(somatostatin)和生長激素釋放激素(growth hor?mone releasing hormone, GHRH)等異常性分泌,導致骨代謝惡化,骨形成減少和骨吸收增加,引起骨質疏松癥(圖1)。運動作為非藥物治療抑郁癥方法,可減輕抑郁癥患者癥狀,改善抑郁癥誘導的分子水平變化(Schuch et al., 2019),提高骨形成過程,緩解骨丟失水平,改善骨微結構。

圖1 抑郁癥誘發骨質疏松的潛在機制(Cizza et al., 2009)Figure 1. Underlying Mechanism of Depression-Induced Osteoporosis (Cizza et al., 2009)
1.1 下丘腦-垂體-腎上腺軸傳導對骨質的影響
下丘腦-垂體-腎上腺軸(hypothalamic-pituitary-adrenal axis, HPA)從中樞神經系統(central nervous system, CNS)向周圍介導抑郁情緒信號途徑(Bab et al., 2010)。HPA軸受下丘腦分泌的CRH和加壓素(vasopressin, AVP)調控。在應激作用刺激下,CRH從下丘腦釋放,刺激下游應激反應中ACTH異常分泌,刺激腎上腺皮質分泌皮質激素,包括糖皮質激素(glucocorticoids, GCs)(主要是皮質醇)和鹽皮質激素,GCs調節神經元存活,神經發生、記憶獲取以及情感評價(Pariante et al., 2008),過量GCs對成骨細胞分化起抑制作用,引起骨質流失,被稱為GCs誘發的骨質疏松癥(glucocorticoid-induced osteoporosis, GIOP)(Jiang et al.,2020)。對60歲以上抑郁癥患者CRH、ACTH、皮質醇進行薈萃分析,患抑郁癥人群表現出高度HPA軸活動失調,抑郁對皮質醇水平有顯著影響(Murri et al.,2014)。而對14名參加6周有氧運動訓練的重度抑郁癥患者研究中,皮質醇反應性從基線到干預后均未改變(Gerber et al.,2020)。妊娠期大鼠按每天0.1 mg/kg接受地塞米松(dexamethasone, DXMS)攝入可誘發抑郁樣行為,當采用60 min/天、5天/周、共4周游泳運動后,可緩解胚胎期接觸GCs前暴露于DXMS大鼠的HPA活性并改善其抑郁樣行為(Liu et al.,2012),長期服用DXMS,還會導致松質骨骨量增加,形成GCs誘導鼠類動物骨質疏松癥模型(Liu et al.,2020)。CRH影響HPA軸抑制下丘腦釋放GnRH和GHRH(圖1),生長激素(growth hormone, GH)、胰島素樣生長因子 1(insulin-like growth factor 1, IGF-1)以及性類固醇分泌減少,導致骨形成減少和骨吸收增加(Cizza et al.,2001; Cizza,2009)。
HPA功能障礙與兒童期抑郁癥密切相關,伴隨年齡增長,社交能力增強,抑郁情緒得以緩解,除年齡外,運動對HPA軸的影響亦是重要因素(Budde et al., 2018)。運動可增加HPA軸對應激刺激的適應性,急性運動可刺激ACTH、皮質醇和乳酸分泌,長期運動后機體內激素變化更緩和、恢復更快。運動和振動可預防懸尾大鼠骨骼退化,其中懸尾大鼠的皮質醇血清水平顯著升高,ACTH血清水平沒有顯著升高,經運動干預發現,局部振動對大鼠骨質流失的調節有積極作用,而被動運動影響較弱(Luan et al.,2018)。運動減緩抑郁過程中,外周給予IGF-1與抑郁癥相關行為時,對游泳運動大鼠施加IGF-1,IGF-1在前額葉皮質和海馬部位產生作用,運動抗抑郁效果顯著增強(Duman et al.,2009),IGF-1水平升高,進一步改善骨骼質量,抑制骨質疏松的生理變化。通過2 068名骨質疏松癥患者和2 071名健康對照者的薈萃分析發現,IGF-1基因多態性與骨質疏松癥易感性之間存在顯著相關性(Gao et al.,2018),積極改善骨質減少/骨質疏松的運動效果中,IGF-1分泌水平升高后促進成骨細胞存活,提高成骨作用,通過PI3K/AKT/mTOR信號傳導通路增強成骨細胞前體(osteoblast precursor cells, OBPC)增殖(Bakker et al.,2015),延緩或改善骨質疏松的發生態勢。
1.2 交感神經系統傳輸對骨質的影響
抑郁癥是骨密度(bone mineral density, BMD)減弱的危險因素,可通過刺激交感神經系統(sympathetic nervous system, SNS)影響骨吸收和骨重建過程,導致骨質流失,誘發骨質疏松癥(Bab et al., 2010)。慢性輕度應激(chronic mild stress, CMS)小鼠的實驗研究中,抑郁癥導致的骨質流失與骨骼中去甲腎上腺素(noradrenaline)增加有關,β受體阻滯劑可預防CMS小鼠骨質流失(Bab et al., 2010)。CMS誘導骨質流失伴隨成骨細胞數量減少導致骨形成受阻,抗抑郁療法可抑制對CMS行為反應,完全抑制骨形成減少(Yirmiya et al.,2006),運動干預作為抗抑郁手段,可緩解CMS行為,進一步刺激成骨細胞,提高骨形成過程。此外,5-羥色胺(5-hydroxytryptamine, 5-HT)作為單胺類神經遞質,可在神經元突觸中釋放,對維持骨骼穩態具有重要的調節作用,同時5-HT可改善機體心理和行為功能,如情緒焦慮癥狀。縫核產生5-HT的神經元投射到下丘腦腹膜內側,抑制SNS活性,對成骨細胞表面負性腎上腺作用進行正向調節(Aloumanis et al., 2013)。久坐不動會引發SNS環節中適應機制缺陷,形成情緒衰落、機體運動意向降低等癥狀(Sanches et al.,2016)。運動在刺激SNS過程中,16天跑輪運動可改善永久性大腦中動脈阻塞(permanent middle cerebral artery occlusion, pMCAO)大鼠神經功能,增強神經元可塑性,并上調5-HT、5-HT受體和腦源性神經營養因子(brain-derived neurotrophic factor,BDNF)分泌水平(Lan et al.,2014)。5-HT神經元信號降低SNS活性后,抑制骨量增長,運動可引起血清5-HT水平升高,緩解骨抑制癥狀(Piotrowicz et al.,2019)。
除此以外,SNS進一步介導的兒茶酚胺(catechol?amine)作為應激激素,包括去甲腎上腺素、腎上腺素和多巴胺。心理壓力通過兒茶酚胺誘導的成骨細胞和破骨細胞上的β-腎上腺素受體(β adrenergic receptor)活化,β腎上腺素受體活化可增加NF-κβ受體活化因子配體(recep?tor for activation of nuclear factor kappa β ligand, RANKL)表達,導致破骨細胞分化,β-腎上腺素信號傳導還通過產生活性氧(reactive oxygen species, ROS)促進破骨細胞生成,加劇骨質流失(Kelly et al.,2019)。同時遞增負荷運動中,兒茶酚胺的分泌水平與反應時間和運動時間密切相關(Mcmorris et al.,2003)。
1.3 瘦素調節對骨質的影響
瘦素是脂肪組織中的重要細胞因子,與抑郁癥和骨重塑調節有關,在體質量、食物攝入和能量代謝中起調節作用。研究發現,瘦素在情緒和認知水平有潛在的調節機制,該作用是通過改善大腦突觸變化來進行抗抑郁調節。其中,抑郁癥患者的高瘦素血癥狀比瘦素敏感性受損的肥胖和代謝異常引起的中心瘦素抵抗癥狀更強(Ge et al.,2018)。瘦素與抑郁癥和骨重塑的調節有關,通過直接或間接參與骨骼重塑,抑制破骨細胞生成以控制骨代謝。骨質疏松癥循環瘦素與BMD之間存在顯著相關性,瘦素通過SNS起作用,通過刺激下丘腦可卡因和苯丙胺調節的轉錄表達來抑制骨吸收(Mclarnon,2012)。瘦素通過SNS調節骨代謝,與其下丘腦瘦素受體(leptin receptor,Ob-Rb)結合,對下丘腦腹腔(ventromedial hypothalamus,VMH)中金硫葡萄糖(gold thioglucose, GTG)敏感性神經元調節,誘導交感活動,并通過β2腎上腺素受體(β2adren?ergic receptor, Adrβ2)向骨細胞發出信號。其一,Adrβ2可使轉錄因子cAMP反應元件結合蛋白(cAMP-response ele?ment binding protein, CREB)來調節基因表達,通過CREB抑制c-Myc表達,從而增加細胞周期蛋白D1(cyclin D1)水平,抑制成骨細胞增殖;其二,Adrβ2激活蛋白激酶A(protein kinase A, PKA),引起轉錄激活因子4(activating transcription factor 4, ATF4)磷酸化,上調RANKL表達,促進破骨細胞的吸收作用(Chen et al., 2015)。
瘦素可發揮抗抑郁作用,進而減輕大鼠的抑郁樣行為,刺激GSK3β/β-catenin信號,并通過Ser9磷酸化抑制糖原合酶激酶 3β(glycogen synthase kinase-3β, GSK-3β)活性,表明GSK3β/β-catenin信號通路依賴的神經發生與瘦素的抗抑郁作用有關(Ge et al.,2018; Liu et al.,2017)。瘦素通過抑制破骨細胞形成對去卵巢(ovariectomized,OVX)大鼠起骨保護作用,促進骨髓間充質干細胞(bone marrow mesenchymal stem cells, BMSCs)成骨分化,通過調節RANKL/OPG比率抑制破骨細胞生成(Said et al.,2020),而在RANK/RANKL/OPG路徑與運動關系中,常規性運動鍛煉對RANK/RANKL/OPG途徑具有積極影響,極度劇烈運動(馬拉松運動)會產生負面調節(Keramaris et al.,2013)。運動刺激機體內瘦素水平提高,瘦素敏感性得以緩解,進一步調節抑郁性功能,同時瘦素的調節改善骨骼質量,形成抗骨質疏松作用。
1.4 炎癥細胞因子分泌對骨質的影響
藍斑位于第四腦室底,腦橋前背部。藍斑是腦中合成去甲腎上腺素的主要部位,與應激反應有關,應激時藍斑-交感-腎上腺髓質系統可引起腦橋藍斑的中樞效用,引發興奮、警覺及緊張、焦慮和抑郁等情緒。藍斑去甲腎上腺素神經元中GCs受體缺失可減弱雌性小鼠社交互動能力(Jacobson,2019)。炎癥反應不僅是機體受傷或感染的主要來源,亦是誘導機體患抑郁癥的重要因素,慢性應激會干擾免疫反應,抑郁癥存在促炎性細胞因子的釋放和過量的皮質醇癥狀(Sanches et al.,2016)。Liu等(2017)證實,游泳運動可以改善抑郁癥大鼠代謝和炎癥反應。運動改善細胞功能,緩解炎癥反應。抑郁情緒下,神經內分泌激素會影響骨形成和/或骨吸收,外周(血清)和中央(腦脊液)中白介素 1(interleukin-1,IL-1)、白介素 6(inter?leukin-6,IL-6)、腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α)、干擾素 γ(interferon-γ, IFN-γ)等促炎細胞因子水平升高,誘導全身炎癥性反應導致抑郁樣行為(Mezuk et al., 2008),引發骨骼質量下降,增加破骨細胞活性,增強骨吸收,降低BMD水平(Rosenblat et al.,2016)。
對OVX小鼠進行糖水實驗、曠場實驗和懸尾實驗發現,小鼠抑郁樣行為發生改變,包括興趣缺失、探究性行為減少、絕望情緒增加,產生抑郁樣行為,小鼠體內促炎細胞因子IL-1β、IL-6含量升高,抑炎細胞因子白介素4(interleukin-4,IL-4)、白介素 10(interleukin-10,IL-10)含量降低,進行為期5周、5天/周、40 min/天、15 m/min的運動干預后,可逆轉IL-1β和IL-4表達改變(鮑青悅 等,2015)。OVX是構建骨質疏松的經典模型,可導致大鼠體內IL-1β mRNA和蛋白水平以及脛骨中IL-6和環氧合酶-2(cyclo?oxygenase-2, Cox-2)蛋白水平顯著增加,對OVX大鼠進行 251.2 m/天、6天/周、3個月的跑輪運動,OVX 大鼠IL-1 mRNA和蛋白、IL-6 mRNA、Cox-2 mRNA和蛋白水平下降(Li et al.,2014)。OVX干預可造成抑郁行為和骨質疏松一體化模型,經運動干預后,既可以緩解抑郁和骨質疏松中促炎因子和抑郁情緒,同時抑制骨吸收,增加骨形成和骨質疏松的骨量水平。
1.5 抗抑郁藥攝入對骨質的影響
抗抑郁藥攝入會調節骨骼健康,對1年內有過髖部骨折史的477名受試者(50歲以上)進行隊列分析發現,髖部骨折發生與抗抑郁藥物使用存在顯著相關性(Leavy et al.,2016)。美國國立衛生研究院(National Institute of Health, NIH)將選擇性5-羥色胺再攝取抑制劑(selective serotonin reuptake inhibitor, SSRI)作為抗抑郁的一線治療藥物(Guo et al.,2019)。SSRI能抑制突觸前神經元對5-HT的再攝取,維持突觸間隙更高水平的5-HT并增加突觸后神經傳遞。對60歲以上老年人研究發現,SSRI與跌倒、骨質流失和骨折有關,SSRIs在老年人安全性中存在憂慮,可增加骨質疏松,引起跌倒和骨折風險(Gebara et al.,2014)。其中,SSRI和5-羥色胺去甲腎上腺素再攝取抑制劑(serotonin and norepinephrine reuptake inhibitor, SNRI)使用情況與BMD降低、骨折風險增加等存在相關性。SSRI使用與骨折風險的關聯可能會因劑量、用藥時間、年齡或性別而異,停用SSRI后,骨折風險會迅速降低(Bruyère et al., 2015; Wu et al.,2015)。在抗抑郁藥治療中增加有氧運動會形成明顯的優勢效果(Murri et al.,2018),對15名年輕(20~39歲)和年老(60~79歲)抑郁癥患者進行>20 min/天、>3天/周、12周運動干預,發現運動增強和藥物療法對不同年齡段抑郁人群均可行,并且對與抑郁有關的核心大腦區域具有神經益處(Gujral et al.,2019),尤其是運動形成對骨骼刺激,可形成良性調節骨骼質量手段。在對24月齡老年大鼠有氧運動干預(共6周、5天/周、2次/天 、15 min /次、5~8 m/min)、SSRI攝入干預(10 mg/kg)、SSRI+運動雙重介導干預的3種干預方式研究中,發現SSRI+運動老年大鼠的杏仁核和海馬組織中5-HT水平顯著升高,同時干預會增加海馬、前額葉皮層和杏仁核中細胞數量,減少老年焦慮和抑郁情況,且運動刺激會緩解骨質流失過程(Gokdemir et al., 2020;Stanghelle et al.,2020)。
2 骨質疏松癥誘發抑郁的生理學基礎及運動干預
抑郁對BMD產生不利影響并增加抑郁癥患者骨折風險,且患有骨質疏松癥患者罹患抑郁癥的可能性亦明顯升高(表1),已有研究證實了骨質疏松癥可加劇抑郁癥狀(Carlone et al.,2015)。根據老年抑郁量表(geriatric de?pression scale, GDS)評估報道,患有椎骨骨折絕經女性比無骨折女性存在更多的抑郁癥狀,其中骨折女性抑郁可能性(GDS≥6)會增加至 2.5%(Silverman et al.,2007)。流行病學研究中心抑郁量表(center for epidemiologic stud?ies depression scale, CES-D)在評估與骨質減少/骨質疏松的相關研究中,經過校正協變量(體質量指數、年齡、雌激素、種族、吸煙和飲酒)后,抑郁癥狀中白人女性髖部BMD變量的占比約為2%(Lyles,2001)。研究認為,骨骼質量的下降,帶來生活能力不便必然引發機體情緒波動,誘導抑郁癥發生;有別于傳統醫學對骨骼的認知,骨骼上升為內分泌系統已經得到了廣泛共識,骨骼作為內分泌器官可分泌骨骼因子作用于下丘腦,進而誘導抑郁癥狀。運動對骨質疏松有效改善效果分析認為:運動可緩解骨質疏松癥和脊椎骨折老年女性行走的恐懼心理(Stang?helle et al.,2020),緩解因骨骼質量減弱導致的精神壓力,減輕抑郁癥進一步惡化;運動調節骨骼質量的改善,進一步引起骨骼分泌因子的釋放,通過下丘腦組織,緩解抑郁癥狀的發生。

表1 抑郁癥與骨質疏松癥的關聯性研究Table 1 Correlation Study between Depression and Osteoporosis
2.1 骨質降低誘導的抑郁情緒
成年人進入30歲后骨骼質量將緩慢衰減,患骨質疏松或存在骨折史的患者多存在憂患意識,尤其是面臨再次跌倒風險,長期處于高壓情緒狀態可形成憂郁意識。對患有骨質疏松癥并存在椎骨骨折女性進行12周的抗阻和平衡運動,可以改善肌肉強度和平衡能力,提高骨骼質量,并減少跌倒的恐懼感(Stanghelle et al.,2020)。伴隨增齡性疾病的發生,中老年人機體能力顯著下降,易引發其情緒意識的失調,表現出焦慮不安、抑郁等癥狀。當骨骼質量下降后,會直接誘導跌倒性骨質損傷的發生,在跌倒與抑郁的雙向性調節中,跌倒對抑郁的影響與跌倒后期恐懼心理之間存在必然聯系(Rosenblat et al.,2016),對患有骨質疏松癥的老年人健康教育中,保持良好精神狀態、樂觀情緒進而提高神經反應,同樣可以緩解應激壓力。
高強度漸進式阻力和沖擊訓練(high-intensity progres?sive resistance and impact training, HiRIT)可提高骨骼強度,改善跌倒和骨折風險相關功能,緩解負面心理作用,形成良好的心理機能狀態(Harding et al.,2020)。對日本百歲老人的流行病調查研究發現,定期運動、95歲以后沒有嚴重跌倒、保持基本的日常生活活動,能夠有效維持老年人幸福感和個人機體能力,形成成功的個體衰老機制(Strandberg et al., 2007),使老年人維持在健康的身心健康狀態中。采用運動干預時,針對老年人的活動能力,快步走和階梯行走有助于減輕與年齡有關的自然骨骼質量下降問題,并且可以輕松地融入老年人日常活動中(Mar?telli et al.,2020),采取順其自然的方式進行有效調控,尤其是對骨質疏松患者的運動干預,在認知行為療法中適當采用正念接受時亦可緩解疼痛和負面情緒(Kober et al.,2019),由此形成的健康心理狀態能夠有效預防骨質減少/骨質疏松引起的抑郁情緒。
2.2 骨骼內分泌功能調節抑郁情緒
在骨內分泌系統(bone endocrine system)的視角下,骨鈣素(osteocalcin, OCN)、成纖維細胞生長因子23(Fibro?blast Growth Factor, FGF23)和 脂 質 蛋 白 2(lipocalin-2,LCN2)構成了新型骨內分泌源激素,3種因子可通過血液循環體系進行全身性機能改善,其中OCN和LCN2可對下丘腦進行進一步的調節(徐帥 等,2021)。OCN由成骨細胞分泌,通過羧化后形成有活性的羧化不全骨鈣素(un?carboxylated osteocalcin, ucOCN),ucOCN與機體能量代謝密切相關,可調節脂肪和葡萄糖代謝,在抗阻訓練和有氧間歇訓練中ucOCN循環水平顯著增加(Rahimi et al.,2020)。ucOCN可作用于BDNF和神經生長因子(nerve growth factor, NGF),共同改善下丘腦對神經功能的影響。在“抑郁癥的神經營養蛋白假說”的研究中,壓力或抗抑郁藥治療與BDNF下調或上調相關(Martinowich et al., 2007),BDNF在神經可塑性、神經發生和神經保護中起調節作用,骨骼中的ucOCN能夠作用于BDNF,BDNF的水平與抑郁癥狀的嚴重程度呈負相關(Ge et al.,2018)。運動后血清BDNF、GDNF水平升高(Piotrowicz et al.,2019)。ucOCN經血液循環可增加腦內GH合成,并通過與GPR158受體結合,在記憶增加和減少焦慮/抑郁中起重要作用。另外,參與空間學習和記憶處理的大腦區域OCN水平顯著性升高。值得注意的是,OCN水平低的小鼠大腦體積始終小于OCN水平正常的小鼠大腦體積,OCN缺陷小鼠表現出較高的焦慮樣行為和認知能力下降,OCN注入后,OCN缺陷小鼠癥狀得以糾正(Diaz-Franco,2019)。OCN 穿越血腦屏障(blood brain barrier,BBB)可恢復小鼠記憶力和認知能力,高脂膳食飼養C57BL/6雄性和雌性小鼠8周后,再進行8周的OCN注射或跑步運動干預,后2周完成抑郁樣行為、焦慮樣行為、小鼠解決問題能力和記憶行為測試,在性別差異、飲食結構與運動關系中,高脂飲食僅增加雌性的焦慮樣行為,OCN注射和運動有效降低小鼠抑郁樣行為,OCN注射和運動干預對抑郁樣行為的影響雖然相似但機制效果不同,并且OCN和運動效果存在明顯的重疊作用(Winberg et al.,2020)。
LCN2屬于先天免疫的鐵相關蛋白,由成骨細胞分泌,可參與情緒行為變化和認知功能改善過程。研究發現,10周齡雄性LCN2缺失小鼠表現出焦慮樣行為、抑郁樣行為以及空間學習任務認知障礙,該行為改變與HPA軸過度激活有關,并反映在LCN2缺失小鼠中皮質類固醇水平升高過程中;LCN2缺失小鼠海馬神經元形態分析顯示,海馬腦細胞結構改變,腹側海馬顆粒狀和錐體神經元肥大,該區域與情緒行為有關(Ferreira et al.,2013)。在慢性應激反應抑郁模型(unpredictable chronic mild stress,UCMS)的研究中,LCN2與慢性應激反應誘導的抑郁癥發病有密切關系,其機制與中樞系統小膠質細胞活性有關。對小鼠顱骨成骨細胞進行模擬微重力分析時發現,與單位重力條件相比,LCN2水平顯著上調(Rucci et al.,2015)。運動刺激LCN2分泌水平,通過血液循環進入腦內,改善抑郁癥狀。除此以外,LCN2與肥胖癥、Ⅱ型糖尿病和代謝綜合征的相關調節密切相關(Moghadasi et al.,2014)。總之,運動通過改善抑郁癥,提高骨骼質量,抑制或緩解骨質疏松的惡化。通過改善骨質疏松,提高行動能力,緩解抑郁情緒;同時骨骼分泌OCN和LCN2作用于腦內組織,緩解抑郁癥的發生(圖2)。
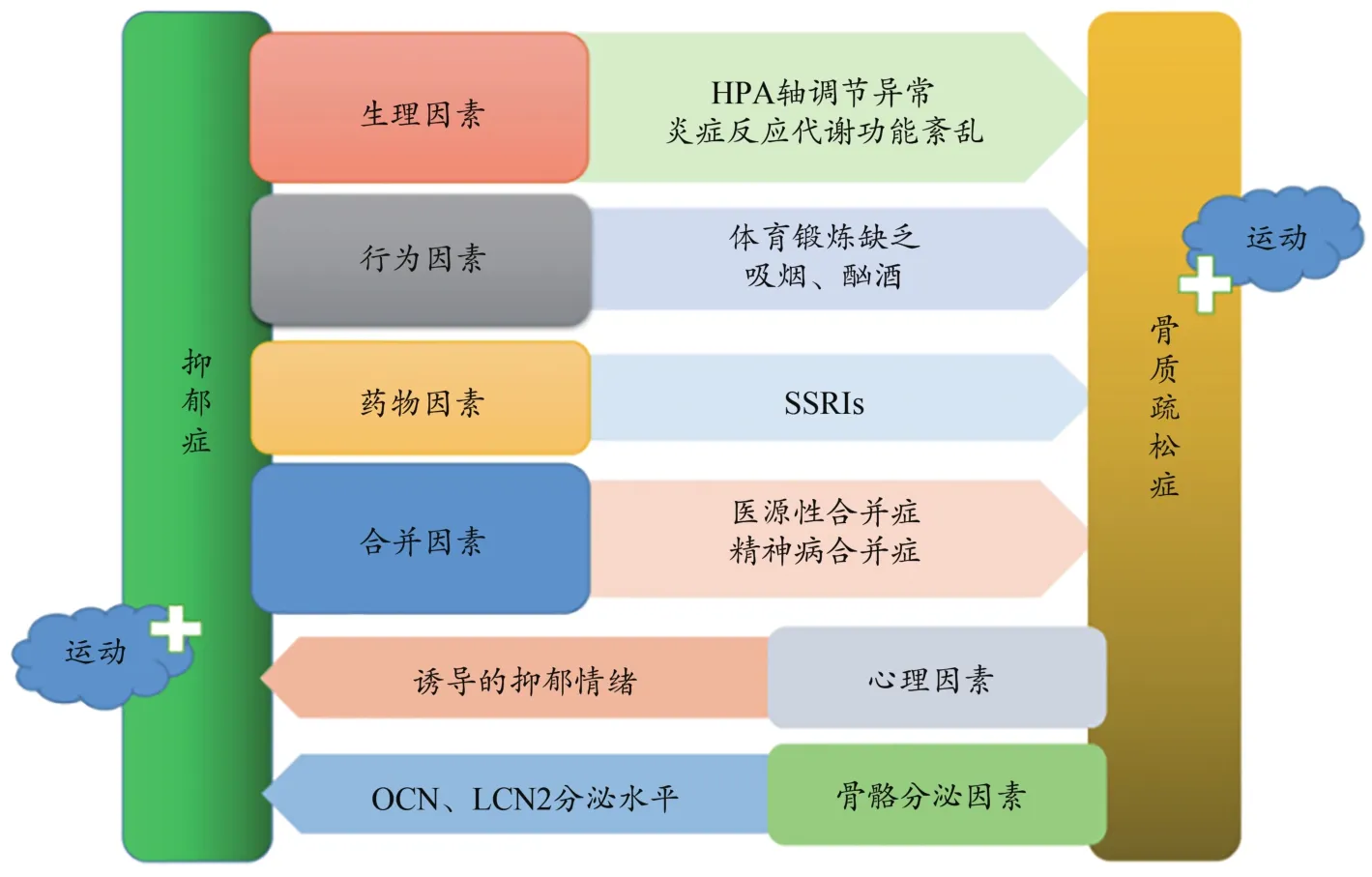
圖2 運動貫穿抑郁癥和骨質疏松癥路徑分析示意圖(Rosenblat et al., 2016)Figure 2. Schematic Diagram of Path Analysis of Exercise Running through Depression and Osteoporosis (Rosenblat et al., 2016)
3 小結與展望
腦-骨交互是應對抑郁癥和骨質疏松癥共病的新機制,在罹患抑郁癥或骨質疏松癥的獨立研究中,抑郁癥是機體罹患骨質疏松和骨折的危險因素,及時對患有抑郁癥的患者進行骨骼質量檢測,有助于骨質流失或骨質疏松的早期篩查。骨質疏松癥中出現BMD降低和骨骼分泌能力下降后,一方面由于骨骼質量的下降,生活質量受到干擾,可引發患者情緒化;另一方面骨骼內分泌因子OCN和LCN2水平下降,亦可誘導抑郁癥的發生發展,及時對患有骨質疏松癥的患者進行抑郁情緒檢測,有助于及時解決患者情緒化問題。
本研究旨在將腦-骨交互進一步延伸到整合生物學的整體角度提供新靶向,更深入的研究方向在于:1)中青年抑郁癥患者的骨量是否會完全達到峰值;抑郁癥中骨質減少/骨質疏松的發生幾率需要進一步確定,對抑郁癥誘發骨折進行及時有效的前瞻性評估;2)絕經女性特有的身體變化,雌激素水平下降可誘導骨質下降,同時伴有情緒變化可能引發抑郁風險,在總體研究中需考慮性別差異性;3)運動干預抑郁癥和/或骨質疏松癥中具有顯著效果,而采用的運動方式卻存在差別,抑郁癥多采用有氧運動干預,骨質疏松癥多采用直接應力刺激,如何進一步選取有效的運動模式來緩解共發病的過程,尤為重要。

