外泌體miRNAs
——運動促進心血管健康的新靶點
馬春蓮,柳 華,熊曉玲,楊 翼
心血管疾病(cardiovascular disease,CVD)致死、致殘率較高。美國心臟協會(Amer?ican Heart Association, AHA)統計顯示,2015—2018年全球≥20歲的成年人患CVD的幾率達49.2%,2019年一年內全球因CVD死亡的人數約87.5萬(American Heart Associa?tion,2022)。《中國心血管健康與疾病報告2020》顯示,我國各類CVD患者達3.3億,因CVD死亡的人數占全國死亡人數的43%以上,CVD依然是我國居民的首要死因(國家心血管病中心,2021)。盡管心血管研究和臨床護理的進步提高了CVD患者的生存率,但鑒于持續較高的死亡率,仍需要良好的預防、治療策略。運動可以為身體多個系統帶來益處,降低CVD和2型糖尿病(type 2 diabetes,T2D)35%~55%的發病風險(American Association of Diabetes Educators,2012),已經成為預防及緩解CVD的有效措施之一。
外泌體(exosomes,EXO)是由不同類型細胞分泌的直徑在40~150 nm的細胞外囊泡(extracellular vesicles,EVs),可將其包裹的 microRNAs(miRNAs)、蛋白質、脂質等物質傳遞到受體細胞(Pluchino et al.,2019),在細胞之間、細胞與組織之間發揮重要的信息傳遞作用,參與多種生理和病理過程。EXO具有內分泌、旁分泌和自分泌的特性,不同細胞來源及細胞微環境會影響EXO的分泌及功能(Kalluri et al.,2020)。運動作為機體強烈的刺激可調控EXO的分泌及其內含物,體內75%的運動因子存在于EXO中(Safdar et al.,2016)。
miRNAs是一種長度為22~25個核苷酸,通過與mRNA的3’端結合,在轉錄后調控基因表達的非編碼單鏈RNA(Henning,2021)。miRNAs通過降解mRNA或抑制mRNA的翻譯,在生物發育、代謝調節、腫瘤發生發展等方面發揮重要調控作用。單個miRNA可以靶向數百個mRNA,而單個mRNA也可以被多個不同miRNAs靶向(Romao et al.,2014),體現出miRNA強大、復雜和靈活的調控潛力。哺乳動物超過60%的蛋白編碼基因直接被miRNAs調控(Friedman et al.,2009)。exomiRs是EXO中重要的內含物,由于受脂質雙層的保護,免于RNA酶分解(Shelke et al.,2014),從而能更有效地調控細胞轉錄后過程。
研究表明,EXO尤其EXO內含的miRNAs(exomiRs)參與了心血管健康的調控。運動促進心血管健康或許是EXO作為細胞間通訊媒介,介導運動產生了多系統效應。基于此,本研究對exomiRs介導運動在促進心血管健康方面的作用進行綜述。
1 exomiRs的來源及去路
exomiRs的形成是復雜而精密的調控過程。細胞核內miRNA基因在RNA聚合酶的作用下生成前體miRNA(pre-miRNA),pre-miRNA出核后在細胞漿內經過進一步加工,形成成熟的miRNA(Michlewski et al.,2019)。EXO在生成過程中對細胞漿內成熟的miRNAs進行分選及包裹。細胞膜的內陷形成早期內體(early sorting endosome,ESE),ESE的膜內陷選擇性地包裹細胞漿內的miRNAs、脂質、蛋白質等物質(Henning,2021),形成含有腔內小泡(intraluminal vesicles,ILVs)的晚期內體(late sorting endosome,LSE),隨著ILVs的逐漸積累,LSE形成多泡體(multivesic?ular bodies,MVBs)。溶酶體調控MVBs的降解及EXO的釋放。MVBs生成后可以與溶酶體融合,被降解供細胞循環利用,也可以與細胞膜融合將ILVs釋放到細胞外,即為含特定miRNAs的EXO(Kalluri et al.,2020)。EXO被釋放后可以通過受體細胞內吞、受體-配體介導的胞吐、與受體細胞膜融合3種形式將exomiRs釋放到受體細胞(Wang et al,2019)。進入受體細胞的exomiRs與mRNA靶基因結合(Achkar et al.,2016),從而調控靶基因的降解或抑制其翻譯過程(圖1)。
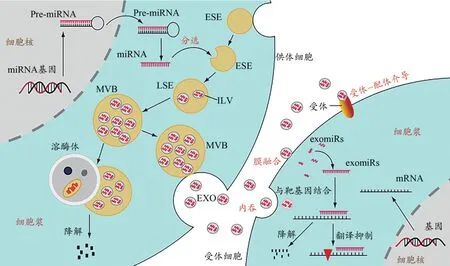
圖1 exomiRs的來源及去路示意圖Figure 1. Schematic Diagram of the Source and Destination of exomiRs
2 運動對EXO分泌及exomiRs表達的調控
2.1 一次性運動對EXO分泌及exomiRs表達的調控
Fruhbeis等(2015)對12名運動愛好者(每周運動超過3 h)進行研究發現,在一次性遞增強度自行車運動至力竭(起始負荷50 W,每3 min增加50 W)過程中,運動強度達到個體乳酸閾強度前EXO的分泌就已經開始了。運動后即刻循環EXO的水平顯著高于運動前,并在運動結束90 min后恢復到靜息水平。男性大學生進行遞增強度的自行車運動至力竭(起始負荷60 W,每1 min增加30 W),運動后即刻血漿中血小板和中性粒細胞來源的EVs顯著升高,運動后2 h血漿中EVs的水平仍顯著高于靜息狀態(Chaar et al.,2011)。Sossdorf等(2011)對 16名健康男性(根據運動水平分為訓練組與久坐組)進行最大攝氧量和個體乳酸閾水平的測試發現,兩組受試者分別以80%個體無氧閾強度進行90 min自行車運動后血小板、單核細胞、內皮細胞(endothelial cells,ECs)來源的EVs數量顯著增加,但訓練組血漿EVs峰值出現在運動后45 min,久坐組則出現在運動后2 h。有研究發現,運動員進行遞增強度自行車運動至力竭(起始負荷40 W,每3 min增加40 W),運動后即刻ECs、血小板、各種類型白細胞來源的EVs顯著增加(Brahmer et al., 2019)。以上研究結果顯示,一次性運動能促進EXO的分泌,并且不同運動水平的受試者體內EXO產生與清除的代謝動力學不同。一次性運動促進心血管細胞來源EXO的分泌,由于EXO具有母細胞的某些特性,提示,運動誘導的心血管細胞來源EXO水平的變化可能與運動改善心血管功能、免疫調節、炎癥有關。
exomiRs是EXO參與機體生理和病理過程調控的重要內含物。近年研究發現,運動參與了exomiRs生成過程的調控,并促進了特定exomiRs的表達。Whitham等(2018)研究發現,1 h自行車運動(30 min 55%O2max強度,20 min 70%O2max強度 ,10 min 80%O2max強度)可以促進包括EXO和ILVs結構蛋白在內的超過300種蛋白質表達增加,并且促進EVs向肝臟轉移蛋白質。一次性有氧+抗阻運動(雙腿以55%O2max強度進行45 min自行車運動+3組55% 1RM強度的單腿8~12次的伸膝運動,組間間歇2 min)上調了健康男性股外側肌MVBs合成相關蛋白Clathrin和Alix的mRNA表達,同時促進了miRNA加工相關蛋白Dicer和Exportin 5的mRNA表達,并且運動誘導的MVBs合成相關蛋白基因表達量與miRNA加工相關蛋白基因表達量呈正相關(Garner et al.,2020)。提示,一次性運動促進了與EXO生成相關蛋白質的合成。
雖然,還沒有直接證據證明一次性運動促進miRNAs分選并包裹進EXO,至少說明在運動中EXO和miRNAs的生物合成途徑遵循著類似的時間軸,提示一次性運動可能促進miRNAs分選并包裹進EXO的動態過程。Lovett等(2018)發現,倍增跳躍聯合下山跑的訓練(10組10次90%最大跳躍高度,組間間隔1 min,跳躍完成5 min后以10 km/h的速度進行5組4 min的下山跑,坡度為10%,組間間隔2 min),可以選擇性地改變健康男性循環EVs中的miR?NAs,而這些EVs中表達改變的miRNAs參與了骨骼肌損傷后的內源性修復。D’Souza等(2018)發現,一次性高強度間歇運動(10組60 s最大輸出功率的自行車運動,組間間歇75 s)使血漿EXO內含miR-126-3p、miR-23a-3p、miR-208a-3p等9種exomiRs表達顯著上調,并且發生變化的exomiRs與運動誘導的骨骼肌及血漿中發生變化的miR?NAs并不完全一致,提示,運動調控了EXO生成過程中miRNAs的分選,選擇性地促進特定exomiRs的表達。
2.2 長期運動對EXO分泌及exomiRs表達的調控
長期規律性運動可以提高人體免疫力,緩解代謝綜合征,提高生活質量(孫海波 等,2020)。長期運動是否能影響EXO分泌及exomiRs表達備受學者關注。Bertoldi等(2018)研究發現,相比于3月齡大鼠,21月齡及26月齡老年大鼠EXO特異性標志蛋白CD63的表達顯著降低,2周中等強度的跑臺運動(60%O2max,每天20 min)顯著上調了老年大鼠循環EXO中CD63的蛋白表達,下調了循環EXO內活性氧(reactive oxygen species,ROS)水平。Wang等(2020)研究發現,4周中等強度的跑臺運動(10 m/min)可增強小鼠循環內皮祖細胞(endothelial progenitor cells,EPCs)來源EXO的分泌,上調EPCs來源exomiR-126的表達水平,減少中動脈阻塞誘導的細胞損傷。前期研究發現,db/db糖尿病小鼠進行4周跑臺運動(低強度5 m/min,中等強度10 m/min,每天60 min,每周5天)可強度依賴性地促進EPCs來源EXO的分泌,上調exomiR-126的表達水平(Ma et al.,2018)。此外,8周中等強度的有氧運動(7 m/min,每天300 m,每周5天)促進了db/db糖尿病小鼠心源性EXO中exomiR-455、exomiR-29b、exomiR-323-5p和exomiR-466的表達(Chaturvedi et al.,2015)。
相比于久坐者,周期性運動的老年人基礎狀態下血清exomiR-486-5p、exomiR-215-5p、exomiR-941的水平顯著上調,兩組受試者一次性運動后血清exomiRs的表達譜也不相同,周期性運動者血清中產生變化的exomiRs主要與代謝激活的信號轉導有關(Nair et al.,2020),提示,長期運動通過調控循環exomiRs的表達譜調節老年人的代謝能力。Hou等(2019)對經過1年以上團體賽艇訓練(每天1~2 h,每周6天)的運動員和未訓練者進行研究發現,在最后一次運動24 h后血漿EXO大小、濃度未見顯著差異。值得注意的是,長期運動者血漿EXO對心肌細胞有保護作用,而未訓練者EXO則無此效應,EXO對心肌細胞的保護作用通過 exomiR-342-5p實現(Hou et al.,2019)。以上研究提示,長期規律性運動或許并不能改變基礎狀態下循環EXO的大小及濃度,但可以選擇性地促進體內某些特定細胞來源EXO的分泌。更重要的是,長期運動能調控exomiRs的表達譜,運動通過調控特定exomiRs的表達變化發揮健康促進的有益效應。
3 exomiRs介導運動促進心血管健康
3.1 exomiRs介導運動促進心臟健康
研究發現,exomiRs參與了心血管健康的調控。Ruan等(2018)研究發現,速效救心丸(心絞痛和冠心病的常用藥物)可以促進小鼠心肌間充質干細胞(mesenchymal stem cells,MSCs)來源EXO的分泌,抵抗缺血/再灌注(ischemia/reperfusion,I/R)產生的心肌損傷。心肌祖細胞(cardiac progenitor cells,CPCs)來源的exomiR-133a可以降低心肌肥厚,抑制細胞凋亡,促進心臟收縮功能(Izarra et al.,2014)。CPCs來源的exomiR-451可以保護心肌細胞緩解氧化應激性損傷(Chen et al.,2013)。干細胞移植能促進壞死心臟區域心肌及血管再生,是心血管疾病治療中非常有應用前景的治療手段。造血干細胞(hematopoietic stem cells,HSCs)由骨髓向外周的運轉活力是影響移植效果的重要因素。富含miR-126的EVs能抑制骨髓HSCs血管細胞粘附分子1(vascular cell adhesion molecule1,VCAM1)的表達,促進HSCs向外周血的運轉(Salvucci et al.,2012)。Shao等(2017)研究發現,在心肌梗死(miocardial infarc?tion,MI)的治療中,胚胎干細胞(embryonic stem cells,ESCs)來源的EXO能抑制心肌纖維化、炎癥,改善心臟功能,治療MI比ESCs移植更有效,該研究發現,ESCs來源的exomiR-15、exomiR-21顯著富集是產生良好治療效果的原因。小鼠I/R前5 min注射MSCs來源EXO可增強心肌細胞活力,減少45%的梗死面積,保護心室的結構及收縮功能(Arslan et al.,2013),提示,EXO作為MI治療劑具有巨大潛力。MI發生后21天心臟疤痕組織已經形成,此時向心肌注射心肌球樣細胞(cardiosphere-derived cells,CDCs)來源EXO,可增加心肌細胞的存活、減少心臟的疤痕、改善心室射血功能,CDCs來源的exomiR-146a的抗氧化應激效應在緩解MI損傷,保護心臟功能中發揮了關鍵作用(Ibrahim et al.,2014)。以上研究證實,多種細胞來源的EXO通過特定exomiRs的調控緩解了病理狀態下心肌細胞的損傷,改善了心臟功能。
體育運動可以減少心肌梗死面積,促進CVD患者的心肺功能(石曉明 等,2017;Hou et al.,2019)。有研究證實,exomiRs參與了運動對心臟功能的調控。Brahmer等(2019)研究發現,中等強度的有氧運動引起血小板、白細胞、ECs等細胞來源EVs的釋放。急性MI發生后,運動康復誘導心臟分泌富含抗纖維化作用的exomiR-29b、exomiR-323-5p、exomiR-455、exomiR-466,上述exomiRs可以下調基質金屬蛋白酶 9(matrix metalloproteinase 9,MMP9),從而降低MI后的不良重塑(Chaturvedi et al.,2015)。Hou等(2019)建立大鼠MI模型并將長期運動者血漿EXO進行大鼠心外注射,發現運動誘導的血漿exomiR-342-5p可以靶向抑制caspase 9和c-Jun氨基末端激酶2(c-Jun N-terminal kinase enzyme,JNK2)基因的表達,降低心肌梗死面積,提高心室射血分數,對心肌產生保護效應。細胞實驗發現,長期運動者血漿EXO能抑制細胞凋亡,降低乳酸脫氫酶(lactate dehydrogenase,LDH)的分泌,增加細胞活力,緩解心肌細胞因缺氧/復氧(hypoxia/reoxygenation,H/R)刺激而產生的損傷(Hou et al.,2019)。缺氧預處理可模擬機體運動中缺氧的特性,研究發現,缺氧預處理可以促進CPCs來源EXO的分泌,并使CPCs來源的exomiR-103、exomiR-15b、exomiR-292等7種exomiRs表達上調,參與ECs血管生成以及心肌成纖維細胞(cardiac fibroblasts,CFs)分化相關的調控,將CPCs來源EXO通過心肌注射應用于I/R大鼠,可促進血管生成,減少心肌纖維化,改善心臟射血功能(Gray et al.,2015)。綜上,運動可以選擇性地促進特定細胞來源exomiRs的表達,運動以及模擬運動特性的刺激所誘導的exomiRs表達變化在促進心血管健康中發揮了關鍵作用(表1)。
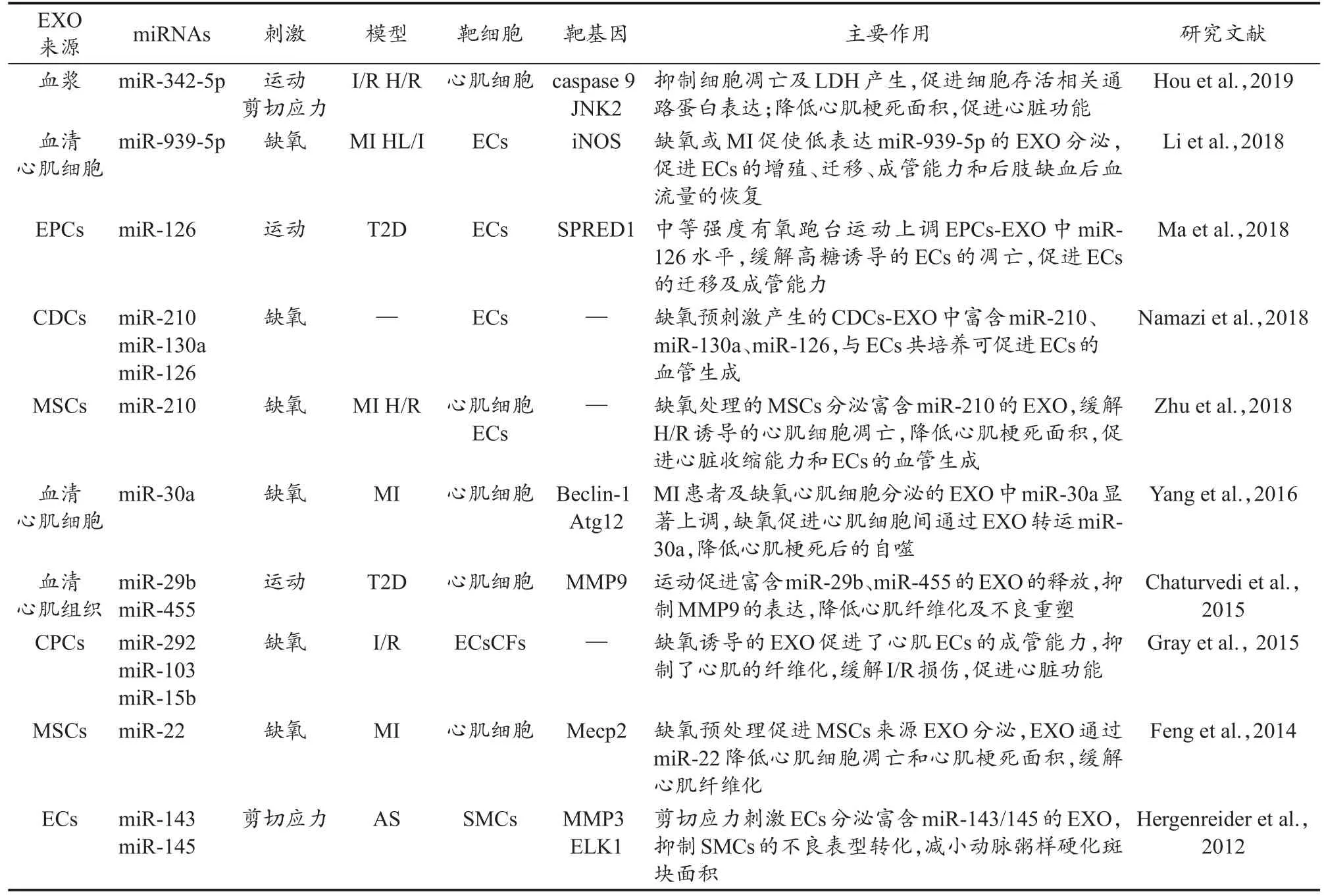
表1 運動及模擬運動特性的實驗中exomiRs促進心血管健康的主要研究Table 1 The Main Research on the Promotion of Cardiovascular Health by exomiRs in the Experiments of Exercise and Simulated Exercise
3.2 exomiRs介導運動促進血管健康
伴隨老齡化的發展,高血壓、動脈粥樣硬化(athero?sclerosis,AS)等血管疾病高發。有研究發現,EXO以及exomiRs參與了血壓及血管鈣化的調節。Otani等(2018)將自發性高血壓大鼠(spontaneously hypertensive rats, SHR)血漿EXO腹腔注射入正常大鼠體內能引起收縮壓升高、胸主動脈壁增厚、膠原減少和心室肌纖維化,相反將正常大鼠血漿EXO注射進SHR大鼠體內,能使收縮壓降低,心室肌纖維化得到緩解。骨髓MSCs來源EXO的運用可以降低高磷共孵育平滑肌細胞(smooth muscle cells, SMCs)的鈣含量和堿性磷酸酶活性,抑制SMCs的鈣化(Guo et al.,2019)。骨髓 MSCs來源 exomiR-146a可以靶向抑制SMCs硫氧還蛋白相互作用蛋白(thioredoxin-interacting protein,TXNIP)的活性,降低ROS的產生及SMCs的成骨樣分化,緩解糖基化終產物對血管SMCs的損傷(Wang et al.,2018)。MSCs來源EXO與CDCs共培養改變了CDCs中miRNAs的表達譜,在MI后促進CDCs的存活,降低心肌纖維化,增加毛細血管密度(Zhang et al.,2016)。當將人體CD34+干細胞EXO注入小鼠缺血后肢(hind-limb ischemia,HL/I)時,可通過exomiR-126-3p抑制ECs出芽相關蛋白1(sprouty-related protein-1,SPRED1)的表達,改善缺血后肢毛細血管密度,促進后肢運動能力(Mathiyalagan et al.,2017)。Van Balkom等(2013)研究發現,ECs通過exomiR-214以自分泌的方式促進ECs的遷移、血管生成,改善毛細血管擴張失調。
運動可以促進血管的順應性,緩解動脈硬化,逆轉SMCs的不良表型轉化,提高其收縮功能(陳金鰲 等,2014;廖靜雯 等,2018;王帝之 等,2019)。有證據表明,exomiRs參與了運動對心血管調控的有益效應。少年男子自行車運動員急性運動中和運動后,調控血管功能的miR-126顯著增加(Kilian et al.,2016),而miR-126主要來自ECs并大量存在于循環EVs中(Jansen et al.,2014)。4周中等強度的跑臺運動(10 m/min,每天60 min,每周5天)可以上調EPCs來源exomiR-126水平,緩解高糖誘導的ECs凋亡,促進ECs的遷移及成管能力(Ma et al.,2018)。運動可以造成體內缺血、缺氧,能量需求及血流剪切應力增加等急性應激反應。用能量剝奪的體外實驗模擬在體運動狀態的研究發現,能量剝奪促進ECs分泌EVs,并將其富含的miR-126、miR-21轉運到 SMCs(Wahl et al.,2016),提示,在運動狀態下,EVs充當了ECs和SMCs之間信息交流及物質轉運的媒介,調控運動對血管的有益效應。另一項研究發現,能量剝奪促進心肌細胞釋放富含葡萄糖轉運蛋白1(glucose transporter 1,GLUT1)、葡萄糖轉運蛋白4(glucose transporter 4,GLUT4)、LDH和甘油醛-3-磷酸脫氫酶(glyceraldehyde-3phosphate dehydrogenase,GAPDH)的EXO,這些EXO被鄰近的ECs攝取,參與ECs的能量代謝調節(Garcia et al.,2016)。剪切應力增加是運動中血流產生的重要變化。體外研究發現,剪切應力刺激促進久坐者血小板來源EVs的釋放(Chen et al.,2010)。以剪切應力刺激人血管ECs可以促進EXO的分泌并上調exomiR-143、exomiR-145的表達,將EXO與SMCs共培養誘導了SMCs基因表達變化及表型轉化,緩解了載脂蛋白E(apolipopro?tein E, ApoE)基因敲除小鼠動脈粥樣硬化的形成(Hergen?reider et al.,2012)。心肌缺血時供血供氧能力受損,而血管生成對于促進缺血心臟的再灌注和功能恢復至關重要。缺氧預處理可以促進CDCs來源EXO中exomiR-210、exomiR-130a和exomiR-126的表達上調,用CDCs來源EXO與血管ECs共培養后,可促進ECs的血管生成(Namazi et al.,2018)。以上在體及離體研究提示,多種細胞來源的EXO通過exomiRs在心血管細胞功能調控中發揮了關鍵作用(圖2)。exomiRs介導運動促進了體內多個系統的信息交流及物質轉運,在病理狀態下發揮對心血管系統的保護效應。

圖2 不同細胞來源exomiRs對心血管細胞的調控Figure 2. Regulation of Cardiovascular Cells by exomiRs from Different Cells
4 exomiRs在CVD中的未來應用展望
4.1 exomiRs作為CVD預測和診斷的生物標志
exomiRs表達譜受身體健康狀況影響,特定疾病會誘導體內產生特異性exomiRs(Garcia-Contreras et al.,2017)。在心肌病的診斷中,患者循環exomiR-133a在肌酸激酶、肌鈣蛋白等傳統生物標志物升高之前就發生了顯著升高(Kuwabara et al.,2011),提示,特定exomiRs在預測心肌病發病中具有很高的敏感性。在所有MI患者中,大約25%會在1年內發生心力衰竭而面臨死亡(Velagaleti et al.,2008)。Matsumoto等(2013)研究發現,急性MI后2~3周患者血清exomiR-194和exomiR-34a顯著增加,而這些exomiRs的水平增加更易于使患者在后期發展成心力衰竭。穩定型冠心病患者循環exomiR-199a、exomiR-126的水平與心血管不良事件發生風險呈負相關,而循環miR-199a和miR-126與心血管不良事件發生風險并無相關性(Jansen et al.,2014)。加之被脂質膜包裹免受RNA酶的降解(Cheng et al.,2014),循環exomiRs相比循環miRNAs能更加敏感而穩定地預測心血管健康狀態。此外,長期運動能上調循環exomiR-342-5p以及心源性exomiR-29b、exomiR-323-5p、exomiR-455、exomiR-466的表達,產生心血管保護效應(Chaturvedi et al.,2015;Hou et al.,2019),提示,在心肌梗死患者的運動康復中,可以通過測試上述exomiRs的表達判斷疾病進展及運動康復效果。相比臨床指標,exomiRs在CVD的診斷、病理發展、不良心血管事件發生風險預測中具有較高的敏感性,有望發展為CVD風險預測、臨床診斷以及運動康復效果評定的生物標志物。
4.2 exomiRs成為CVD靶向治療的新方法
運動通過調控EXO的代謝動力和exomiRs表達譜對心血管產生保護作用。干細胞來源的EXO具有母細胞的某些特性,可以降低心肌纖維化和不良重塑,促進血管增生,提高心血管功能,在CVD的治療中比母細胞產生更好的效果(Davidson et al.,2018)。加之EXO的純化、輸送和儲存比干細胞制備和輸送更加簡單和快捷。所以,收集健康年輕人或長期運動者的血液并制備EXO,將其注入CVD患者體內,有望成為治療CVD的新方法。EXO是轉運核酸的天然載體,相比現有的核酸載體具有更加優越的循環穩定性、生物相容性和較低的毒性(Lin et al.,2020)。隨著對EXO生物生成、包裝機制、生理特性的了解,未來通過基因技術將某些特定miRNAs裝載到EXO制備納米藥物,利用EXO歸巢能力強、靶外效應小的特點(Floriano et al.,2020;Tomasetti et al.,2017)實施無細胞靶向治療CVD,將成為可能。
5 結語
EXO分泌是體內存在的基本生理過程,分泌缺乏將誘發病理過程(Alexander et al.,2017)。運動促進了特定EXO的分泌,調控了exomiRs的表達譜,exomiRs介導運動在促進心血管健康方面發揮了重要作用,在臨床CVD的預防、診斷及治療中具有很好的應用前景。但是,目前的研究與臨床應用還有一定距離,某些問題尚待進一步闡釋:1)EXO的粒徑范圍與EVs中微囊泡的粒徑范圍出現重疊(Lawson et al.,2016),不同研究中EXO粒徑的界定也有分歧(Lawson et al.,2016;Pluchino et al.,2019),需在未來研究中規范EXO的粒徑范圍,確保研究結果的準確性。2)鮮見exomiRs介導運動調控心血管健康的研究,尤其是在體研究。后期尚需加大研究力度,期望臨床實現運動處方科學指導運動來調控exomiRs的表達,從而達到內源性非藥物治療CVD的目的。3)不同細胞來源EXO的半衰期不同(Saunderson et al.,2014;Takahashi et al.,2013),不同注射途徑也會影響EXO在體內的分布(Zhou et al.,2020)。因此,后期在EXO的代謝動力學方面還需深入研究,以便能在臨床應用中尋找治療CVD的最佳注射時間和注射途徑。

