具有主導晶面的BiOIO3/BiOCl異質結制備與光催化性能
黃宗益 鄭遺凡 楊 娥 宋旭春*,
(1福建師范大學化學與材料學院,福州 350007)
(2浙江工業大學分析測試中心,杭州 310014)
0 引 言
作為一種能夠解決環境污染持續惡化和能源短缺的綠色技術,半導體光催化引起了人們的廣泛關注[1?2]。BiOCl晶體結構由[Bi2O2]2+層及兩層 Cl?組成的片層相互交織而構成,使得BiOCl可以阻礙來自[Bi2O2]2+及Cl?之間靜電場形成的載流子的復合,還可以降低兩片層之間表面缺陷所引起的表面電子俘獲。由于這種特殊的層狀結構,BiOCl具有優良的光催化性能,因而得到了廣泛的研究[3?5]。但是,迄今為止BiOCl光催化活性仍然存在量子效率低等問題。因此,還需進一步的調控其微結構來提升其光催化性能以滿足當前的需求。光催化反應是典型的基于表面的過程,所以光催化效率也和材料的表面微觀結構密切相關[6]。半導體表面暴露的不同晶面有著不同的本征配位和表面原子排列,而本征配位和表面原子排列決定了表面底物與光生電子間的轉移能力和對底物的吸附強度,因而半導體的表面特定晶面暴露率對于光催化性能至關重要[7?8]。構造和調控具有高活性面取向生長的光催化劑一直是研究人員關注的問題。Hu等[9]通過添加或不添加檸檬酸鈉,采用水熱法調控合成了具有(001)和(102)主導晶面的納米BiOCl。研究結果表明,隨著(001)主導晶面百分比的增加,其光催化降解甲基橙(MO)的活性也隨之增強。Pan等[10]制備了具有高(001)和(110)主導晶面的納米BiOI,在可見光照射下,具有(110)晶面的BiOI比(001)晶面有更好的光催化降解雙酚A活性。
近年來,碘酸氧鉍(BiOIO3)作為一種新型的光催化劑,由于其潛在的光催化效果而被廣泛的關注[11]。BiOIO3半導體的實際應用受到光響應范圍小和光生電子?空穴對的快速復合的負面影響。通過結合具有合適電子能帶結構的一種以上的半導體光催化劑,可形成復合的異質結光催化劑體系,有利于促進電子和空穴的有效分離,可顯著提高光催化活性[12]。目前報道的幾種半導體在和BiOIO3形成異質結之后,都呈現出比單一半導體光催化劑更優異的光催化性能,如BiOIO3/RGO(RGO=還原氧化石墨烯)[13]、g?C3N4/BiOIO3[14]、AgI/BiOIO3[15]和BiOI/BiOIO3[16]等。
我們通過乙二醇(EG)溶劑熱法和簡單水熱法調控制備了具有(110)主導晶面的BiOCl與BiOIO3復合的異質結(BiOIO3/{110}BiOCl)和具有(001)主導晶面的BiOCl的異質結(BiOIO3/{001}BiOCl)。在可見光的照射下,通過降解羅丹明B(RhB)和苯酚測試其光催化性能,并探討了BiOIO3/{110}BiOCl具有更高光催化活性的機理。
1 實驗部分
1.1 試 劑
實驗中所用試劑未經進一步純化直接使用。五水合硝酸鉍(分析純)、碘酸鉀(分析純)、氯化鉀(分析純)、EG(分析純)、無水乙醇(分析純)、苯酚和二甲基亞砜(分析純)購自國藥集團上海化學試劑有限公司;RhB(分析純)和氯化硝基四氮唑藍(NBT,分析純)購自Aladdin公司。
1.2 光催化劑的制備
BiOIO3的制備:分別將5 mmol KIO3和5 mmol Bi(NO3)3·5H2O溶于20 mL的去離子水中,隨后將KIO3溶液加入Bi(NO3)3溶液中,攪拌30 min。將上述溶液轉移到50 mL高壓反應釜中,130℃水熱反應12 h。自然降至室溫后,收集產物,并用去離子水和無水乙醇分別洗滌,在60℃的溫度下干燥即得BiOIO3。
BiOIO3/{110}BiOCl和 BiOIO3/{001}BiOCl異質結的制備:將 1.667 mmol BiOIO3和 5 mmol Bi(NO3)3·5H2O分散在20 mL EG中攪拌形成懸浮液A。同時,將5 mmol KCl溶解于20 mL EG中形成溶液B。在攪拌下將懸浮液A加入溶液B中。攪拌30 min后,將上述混合物轉移到50 mL的高壓水熱釜中160℃下反應。經過12 h后,冷卻至室溫,用去離子水和無水乙醇分別洗滌產物,離心收集產物并在60℃下干燥,即得到BiOIO3物質的量分數為25%的異質結(25% BiOIO3/{110}BiOCl)。通過調節投料比,合成x% BiOIO3/{110}BiOCl(x%=15%、35%)。用類似方法,將上述步驟中EG更換為去離子水,合成x% BiOIO3/{001}BiOCl(x%=15%、25%、35%)。
{001}BiOCl和{110}BiOCl的制備:在反應中不添加 BiOIO3,其余步驟同 BiOIO3/{110}BiOCl和BiOIO3/{001}BiOCl異質結的制備。
1.3 光催化劑的表征
X射線衍射(XRD)分析在Thermo ARL SCINTAG X′TRA型X射線衍射儀上進行,Cu靶Kα輻射(λ=0.154 056 nm),管電壓為40 kV,管電流為40 mA,掃描范圍10°~80°。形貌分析通過Hitachi S?4700型場發射掃描電鏡(SEM)表征,工作電壓為15 kV。通過能量色散譜(EDS,Thermo Noran VANTAG?ESI)對產物進行成分分析。通過Lambda 850紫外可見漫反射光譜儀測定樣品的UV?Vis DRS譜圖。用X射線光電子能譜儀(XPS,Thermo ESCALAB250)分析樣品的價帶位置。樣品的N2吸附?脫附測試所用儀器為Micromeritics ASAP 2000型N2吸附?脫附儀,用Brunauer?Emmett?Teller(BET)法計算比表面。光電流測試在CHI?660E電化學工作站進行。采用三電極體系,將催化劑超聲分散在Nafion溶液,并均勻地涂覆在ITO導電玻璃上作為工作電極,鉑絲電極為輔助電極,飽和Ag/AgCl電極為參比電極,0.1 mol·L?1的Na2SO4溶液為電解液。
1.4 光催化活性測試
通過在可見光照射下光催化降解RhB和苯酚溶液來評估樣品的光催化活性。將0.1 g光催化劑樣品分散在100 mL濃度20 μmol·L?1的RhB溶液或50 mL質量濃度50 mg·L?1的苯酚溶液中。在光照射前,先將懸浮液避光攪拌30 min,達到吸附平衡。然后,接通氙燈(300 W,帶有420 nm濾光片,1 900 mW·cm?2)電源。在光催化降解過程中,每隔一定時間取樣,每次3 mL懸浮液,離心除去催化劑,通過紫外可見分光光度計(UV1902)測定光催化降解后RhB或苯酚溶液的濃度。
1.5 超氧自由基(·O2-)檢測
將 0.1 mmol·L?1的 NBT 溶液和 0.1 g·L?1的催化劑懸浮液各取20 mL置于反應器中,在300 W氙燈光源照射下,每隔5 min取樣,離心分離,用二甲基亞砜溶解沉淀物,通過UV1902在680 nm處測量吸光度。
2 結果與討論
2.1 光催化劑的晶相組成
圖1為制備的BiOIO3/{110}BiOCl和BiOIO3/{001}BiOCl異質結的XRD圖。由圖可見,所制備的2 種異質結在 2θ=12.03°、25.89°、32.57°、33.55°、40.98°、46.74°、55.25°、58.72°的衍射峰,分別與四方晶系的 BiOCl(PDF No.06?0249)的(001)、(101)、(110)、(102)、(112)、(200)、(104)、(212)晶面相吻合。位于 2θ=27.54°、31.35°、44.79°處的衍射峰分別與斜方晶系BiOIO3(PDF No.64?0028)的(121)、(002)、(202)晶面相吻合。由此可見,所制備的2種異質結催化劑都由BiOIO3和BiOCl組成。并且沒有發現其他雜質衍射峰,表明在制備過程中沒有形成雜質相。值得注意的是,BiOIO3/{110}BiOCl和 BiOIO3/{001}BiOCl異質結的XRD圖略有差異。圖1a顯示,15% BiOIO3/{110}BiOCl、25% BiOIO3/{110}BiOCl和 35% BiOIO3/{110}BiOCl異質結中 BiOCl的(110)晶面與(001)晶面的衍射峰強度比分別為2.15、2.26和2.32。圖1b中,BiOIO3物質的量分數為15%、25%、35%的異質結中BiOCl的(110)晶面與(001)晶面的衍射峰強度比分別為1.07、1.25、1.19。結果表明,在EG溶劑中通過溶劑熱制備的BiOCl(110)晶面生長占優,形成了(110)晶面主導的BiOIO3/{110}BiOCl異質結。而通過水熱法合成的BiOCl則(001)晶面生長占優,得到的是(001)晶面主導的BiOIO3/{001}BiOCl異質結。

圖1 (a)BiOIO3/{110}BiOCl和(b)BiOIO3/{001}BiOCl的XRD圖Fig.1 XRD patterns of(a)BiOIO3/{110}BiOCl and(b)BiOIO3/{001}BiOCl
2.2 光催化劑的形貌
通過 SEM 對所制備的 BiOIO3、{110}BiOCl、{001}BiOCl、BiOIO3/{110}BiOCl和 BiOIO3/{001}BiOCl的形貌進行表征。圖2a顯示,純的BiOIO3是粒徑為50~200 nm的納米顆粒。合成的具有(110)主導晶面的純BiOCl的SEM顯示在圖2b。由圖可見,{110}BiOCl是由納米片聚集而成的直徑大約為5μm的微球結構。圖2c給出了25% BiOIO3/{110}BiOCl異質結的SEM照片,可以觀察到顆粒狀的納米BiOIO3附著在{110}BiOCl微球的表面,形成BiOIO3/{110}BiOCl異質結。圖2d呈現的是水熱法合成的(001)晶面主導的純{001}BiOCl形貌圖,顯示{001}BiOCl納米片交錯堆積組裝成類似花狀結構。25% BiOIO3/{001}BiOCl異質結SEM圖像顯示在圖2e。可以看見BiOIO3納米顆粒片黏附在花狀的{001}BiOCl上,表明形成了BiOIO3/{001}BiOCl異質結。通過EDS對25% BiOIO3/{110}BiOCl進行成分分析。圖2f顯示了Bi、O、I、Cl的元素峰,其中Cu元素來自背景銅網,表明BiOIO3/{110}BiOCl復合物由BiOIO3和 BiOCl所組成。
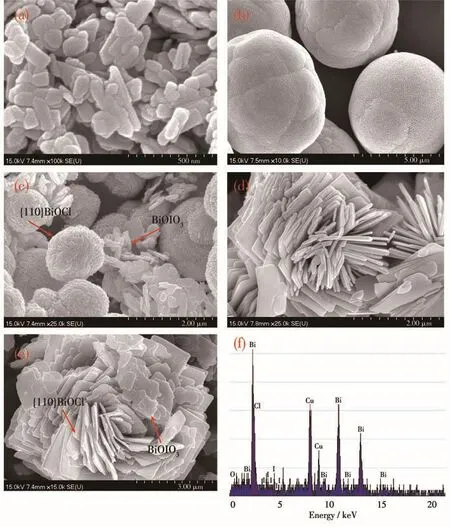
圖2 (a)BiOIO3、(b){110}BiOCl、(c)25% BiOIO3/{110}BiOCl、(d){001}BiOCl、(e)25% BiOIO3/{001}BiOCl的 SEM圖;(f)25% BiOIO3/{110}BiOCl的EDS譜圖Fig.2 SEM images of(a)BiOIO3,(b){110}BiOCl,(c)25% BiOIO3/{110}BiOCl,(d){001}BiOCl,(e)25% BiOIO3/{001}BiOCl,respectively;(f)EDS spectrum of 25% BiOIO3/{110}BiOCl
2.3 UV?Vis DRS表征
通過UV?Vis DRS技術表征光催化劑對光的吸收性能。從圖3a中可見,純BiOIO3在紫外光區表現出強吸收,其吸收帶邊大約在380 nm,并且在400~600 nm的可見光區域也表現出一定吸收能力。純{110}BiOCl微球的吸收帶邊大約在430 nm,而且在可見光區也表現出較高的吸光度。對于35% BiOIO3/{110}BiOCl、25% BiOIO3/{110}BiOCl和 15% BiOIO3/{110}BiOCl異質結,隨著BiOIO3的含量減少,光吸收帶邊略微向長波長位移,表現出紅移現象。同時異質結對可見光的吸收強度明顯高于純BiOIO3,但較純{110}BiOCl微球有所降低。圖3b顯示了純{001}BiOCl的吸收帶邊約在360 nm處,在可見光區僅有微弱的吸收,表明{110}BiOCl比{001}BiOCl具有更優良的光吸收性能。在BiOIO3/{001}BiOCl異質結中,隨著BiOIO3的物質的量分數增加,其吸收邊從370 nm移動到376 nm,表現出較小的紅移現象。與BiOIO3/{110}BiOCl異質結不同,BiOIO3/{001}BiOCl異質結在可見光區域的光吸收很弱。暗示相比于BiOIO3/{001}BiOCl異質結,BiOIO3/{110}BiOCl異質結將具有較高的光催化活性。利用下式可以計算出{110}BiOCl、{001}BiOCl和 BiOIO3的帶隙能[17]:

其中α、h、ν、A和Eg分別為吸收系數、普朗克常數、光的頻率、比例常數和帶隙能,間接半導體的n的取值為4。圖3c顯示的是(αhν)n/2對hν所作的曲線圖。通過切線計算出{110}BiOCl、{001}BiOCl和BiOIO3的帶隙能分別為2.70、3.25和3.05 eV。圖4所示為通過小結合能范圍的XPS掃描而確定的BiOIO3、{001}BiOCl和{110}BiOCl的價帶位置(EVB)。通過測定和計算得出BiOIO3的EVB和導帶位置(ECB)分別為2.50和?0.55 eV;{110}BiOCl的EVB是2.00 eV,其比{001}BiOCl的 EVB(2.30 eV)小。{110}BiOCl的 ECB為?0.70 eV,比{001}BiOCl的ECB(?0.95 eV)大。
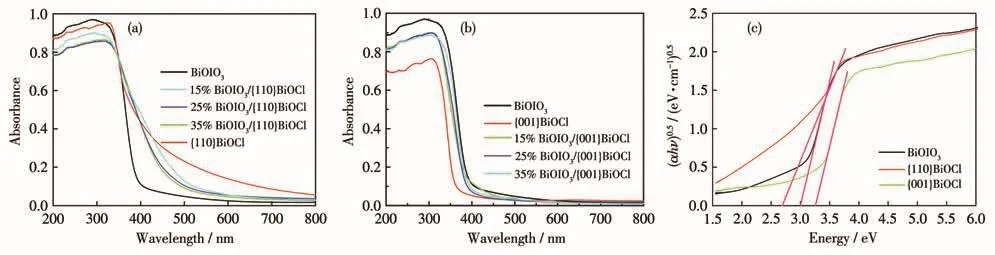
圖3 (a)BiOIO3/{110}BiOCl和(b)BiOIO3/{001}BiOCl的UV?Vis DRS譜圖;(c)BiOIO3、{001}BiOCl和{110}BiOCl的(αhν)1/2?hν圖Fig.3 UV?Vis DRS spectra of(a)BiOIO3/{110}BiOCl and(b)BiOIO3/{001}BiOCl;(c)Plots of(αhν)1/2?hν for BiOIO3,{001}BiOCl,and{110}BiOCl
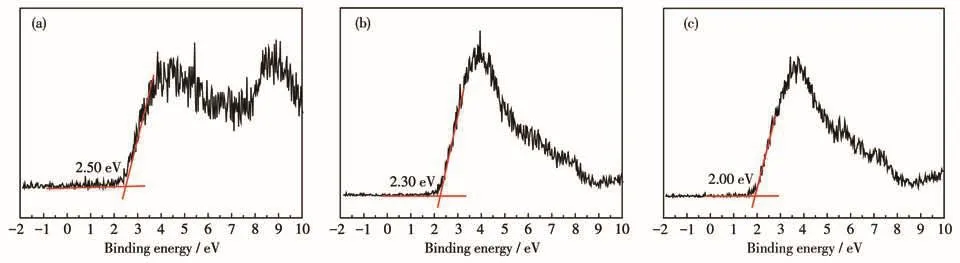
圖4 (a)BiOIO3、(b){001}BiOCl和(c){110}BiOCl的VB?XPS譜圖Fig.4 VB?XPS spectra of(a)BiOIO3,(b){001}BiOCl,and(c){110}BiOCl
2.4 光電流
光電流用于評估催化劑在光照下激發產生光生電子和空穴的分離效率。圖5a為BiOIO3、{110}BiOCl和25% BiOIO3/{110}BiOCl異質結的瞬態光電流響應曲線。25% BiOIO3/{110}BiOCl異質結相較于純的BiOIO3和{110}BiOCl,呈現出高的光電流強度,表明25% BiOIO3/{001}BiOCl異質結具有更有效的光生電子?空穴分離能力。圖5b同樣顯示25% BiOIO3/{001}BiOCl異質結的光電流強度高于純的BiOIO3和{001}BiOCl。結果表明,異質結結構的形成,有利于提高光生電子和空穴的分離效率。值得注意的是,{110}BiOCl和25% BiOIO3/{110}BiOCl異質結的光電流密度均顯著高于{001}BiOCl和25% BiOIO3/{001}BiOCl異質結。表明{110}BiOCl和25% BiOIO3/{110}BiOCl異質結中的(110)主導晶面有利于抑制光載流子的復合,從而有利于提高其光催化性能。
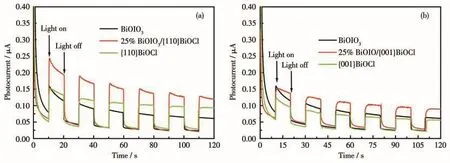
圖5 (a)BiOIO3、{110}BiOCl和 25% BiOIO3/{110}BiOCl的光電流響應圖;(b)BiOIO3、{001}BiOCl和 25% BiOIO3/{001}BiOCl的光電流響應圖Fig.5 (a)Photocurrent response diagrams of BiOIO3,{110}BiOCl,and 25% BiOIO3/{110}BiOCl;(b)Photocurrent response diagrams of BiOIO3,{001}BiOCl,and 25% BiOIO3/{001}BiOCl
2.5 催化活性評價
通過在可見光下催化降解RhB來評估所合成光催化劑的光催化活性。圖6a是在光催化劑BiOIO3、{001}BiOCl和 BiOIO3/{001}BiOCl參與下的RhB降解率(c/c0)隨照射時間變化曲線圖。由圖可見,不同物質的量之比的BiOIO3/{001}BiOCl均表現出比BiOIO3和{001}BiOCl高的光催化活性。隨BiOIO3含量的增加,BiOIO3/{001}BiOCl異質結光催化活性呈現出先增加后降低的趨勢,25% BiOIO3/{001}BiOCl異質結表現出最高的活性,光照15 min后RhB溶液的降解率為43.4%。光催化劑BiOIO3、{110}BiOCl和BiOIO3/{110}BiOCl的光催化降解RhB活性如圖6b所示。對于純BiOIO3和{110}BiOCl,在可見光照射催化反應15 min后,RhB的降解率分別為12.3%和84.4%,{110}BiOCl的光催化活性遠高于{001}BiOCl(降解率 13.8%)。25% BiOIO3/{110}BiOCl顯示出了最高的光催化活性,在可見光照15 min后,降解率高達98.7%。
通過擬一級動力學模型求出RhB光降解反應速率常數,方程式(2)為ln(c/c0)=?kt,其中k是表觀降解速率常數,t、c和c0分別是降解時間、t時的RhB濃度和光照開始時RhB濃度。由圖6c可得,BiOIO3、{001}BiOCl、15% BiOIO3/{001}BiOCl、25% BiOIO3/{001}BiOCl和35% BiOIO3/{001}BiOCl的降解速率常數分別是0.006 3、0.009 2、0.024 1、0.037 5和0.024 4 min?1。 通 過 圖 6d 可 知 ,{110}BiOCl、15% BiOIO3/{110}BiOCl、25% BiOIO3/{110}BiOCl和 35% BiOIO3/{110}BiOCl的光催化降解RhB的速率常數分別為 0.112 3、0.234 2、0.313 1 和 0.149 2 min?1。25% BiOIO3/{110}BiOCl的光催化速率常數是25% BiOIO3/{001}BiOCl的8.35倍。
圖6e顯示了在可見光照條件下,25% BiOIO3/{110}BiOCl異質結對苯酚溶液的光催化降解活性。在光照射150 min后,苯酚的降解率接近100%,表明25% BiOIO3/{110}BiOCl對光催化降解苯酚同樣表現出優異的活性。通過對25% BiOIO3/{110}BiOCl的多次循環使用實驗,考察其穩定性。如圖6f所示,催化劑在3次循環使用后,其對RhB光催化降解率為91.3%,表明其具有較好的穩定性。
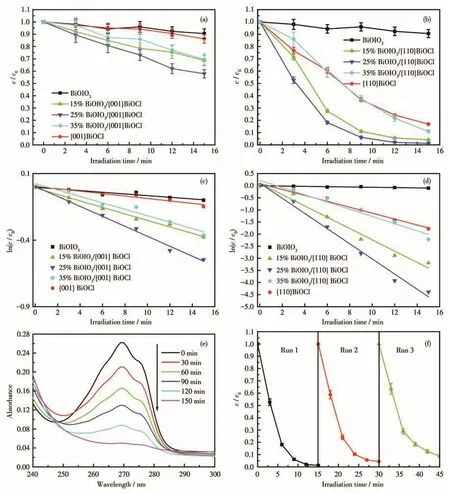
圖6 (a)BiOIO3、{001}BiOCl和BiOIO3/{001}BiOCl光催化降解RhB性能曲線;(b)BiOIO3、{110}BiOCl和BiOIO3/{110}BiOCl光催化降解RhB性能曲線;(c)BiOIO3、{001}BiOCl和BiOIO3/{001}BiOCl光催化降解RhB的動力學線性擬合;(d)BiOIO3、{110}BiOCl和BiOIO3/{110}BiOCl光催化降解RhB的動力學線性擬合;25% BiOIO3/{110}BiOCl光催化(e)降解苯酚的UV?Vis吸收光譜圖和(f)降解RhB的循環實驗Fig.6 (a)Photodegradation efficiencies of RhB by BiOIO3,{001}BiOCl,and BiOIO3/{001}BiOCl;(b)Photodegradation efficiencies of RhB by BiOIO3,{110}BiOCl,and BiOIO3/{110}BiOCl;(c)Linear fitting of the kinetics of photocatalytic degradation of RhB by BiOIO3,{001}BiOCl,and BiOIO3/{001}BiOCl;(d)Linear fitting of the kinetics of photocatalytic degradation of RhB by BiOIO3,{110}BiOCl,and BiOIO3/{110}BiOCl;(e)UV?Vis adsorption spectra for photodegradation of phenol and(f)cycling experiment of degrading RhB by 25% BiOIO3/{110}BiOCl
2.6 催化反應機理
以苯醌(BQ,2 mmol·L?1)、異丙醇(IPA,15 mL)、乙二胺四乙酸二鈉(EDTA?2Na,2 mmol·L?1)、L?組氨酸(L?HIS,2 mmol·L?1)和 AgNO3(2 mmol·L?1)分別作為·O2?、羥基自由基(·OH)、空穴(h+)、單線態氧(1O2)和電子(e?)的捕獲劑,確定 BiOIO3/{110}BiOCl光催化降解RhB過程中的活性物種,結果如圖7所示。添加BQ后RhB的光催化降解效率下降最大,表明·O2?是光催化降解反應中最重要的活性物種。在光催化反應體系中加入EDTA?2Na后,RhB的光降解速率也顯著降低,表明h+也是參與光催化反應的主要活性物種。加入AgNO3后,RhB的光降解速率略有下降,這可能與加入電子捕獲劑影響光生電子與O2反應生成·O2?有關。而添加IPA和L?HIS后,RhB的光降解速率沒有明顯下降,表明·OH和1O2對該光催化過程影響較小。圖8顯示NBT顯色法探究催化劑在光照下生成·O2?的測試。隨著光照時間延長,NBT被還原為甲臜后的吸光度逐漸升高,表明25%BiO?IO3/{110}BiOCl和25% BiOIO3/{001}BiOCl溶液中生成的·O2?增多,并且25% BiOIO3/{110}BiOCl產生的·的量大于 25% BiOIO3/{001}BiOCl。
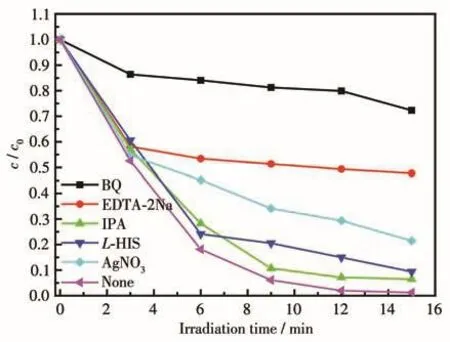
圖7 25% BiOIO3/{110}BiOCl光催化降解RhB的捕獲實驗Fig.7 Trapping experiments for the photodegradation of RhB by 25% BiOIO3/{110}BiOCl
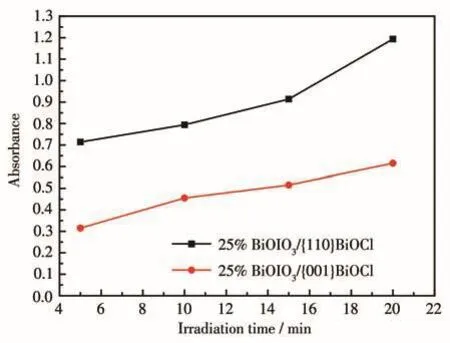
圖8 25% BiOIO3/{110}BiOCl和25% BiOIO3/{001}BiOCl光催化反應中·O2?產生量的對比Fig.8 Comparison in amount of·O2?in photocatalytic reaction by 25% BiOIO3/{110}BiOCl and 25% BiOIO3/{001}BiOCl
BiOIO3/BiOCl異質結的光催化機理如圖9所示。根據先前的分析結果,{110}BiOCl和{001}BiOCl的EVB和ECB比BiOIO3更小。因此,無論是{110}BiOCl還是{001}BiOCl,都能和BiOIO3形成一個交錯型的異質結構,通常交錯型異質結被認為在光催化反應中能夠有效地促進光生電子和空穴對的分離,從而提高光催化活性。光催化測試也證明了BiOIO3/{001}BiOCl和BiOIO3/{110}BiOCl異質結相對于各自組成中的純半導體,其光催化性能都顯著提高。BiOIO3/{110}BiOCl比BiOIO3/{001}BiOCl異質結具有更高的光催化活性,應歸結于不同的主導晶面:其一,具有(110)主導晶面的BiOCl比{001}BiOCl具有更高的可見光吸收性能,并且{110}BiOCl與BiOIO3復合后形成的BiOIO3/{110}BiOCl異質結保持了可見光吸收性能,提高了催化活性。其二,由光電流測試可知,{110}BiOCl的光電流密度顯著高于{001}BiOCl,表明(110)主導晶面有利于抑制光生電子和空穴對的復合,這一因素提高了BiOIO3/{110}BiOCl異質結的光催化性能。另外,催化劑的表面積可能也影響光催化性能。25% BiOIO3/{110}BiOCl和25% BiOIO3/{001}BiOCl的BET比表面積分別為 11和7 m2·g?1,表明BET比表面積也是增強25% BiOIO3/{110}BiOCl光催化活性的因素之一。在可見光照射下,半導體BiOIO3和{110}BiOCl受光的激發,其價帶中的電子被激發到導帶。{110}BiOCl的ECB上光生電子轉移到BiOIO3半導體上,BiOIO3的光生空穴轉移到{110}BiOCl上,這就抑制了光生載流子的復合。BiOIO3導帶中的光生電子與O2反應生成·O2?(O2/·O2?:?0.284 eV),·O2?進一步與有機分子發生氧化還原而使其降解。同時,{110}BiOCl價帶中的h+也可以直接和有機污染物發生氧化還原反應。而{110}BiOCl的EVB(2.00 eV)比·OH/H2O的能級(2.27 eV)低,很難產生·OH。
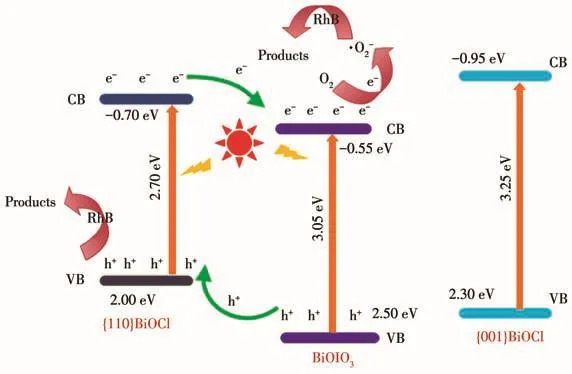
圖9 25% BiOIO3/{110}BiOCl光催化降解RhB的機理Fig.9 Mechanism of the photocatalytic degradation of RhB by 25% BiOIO3/{110}BiOCl
3 結論
通過水熱/溶劑熱法調控合成了具有(110)和(001)主導晶面的BiOIO3/{110}BiOCl和BiOIO3/{001}BiOCl異質結。BiOIO3/{001}BiOCl和BiOIO3/{110}BiOCl均表現出比純BiOIO3和BiOCl高的光催化活性。與BiOIO3/{001}BiOCl異質結相比,BiOIO3/{110}BiOCl在可見光下對RhB的光降解效率顯著提高,在光照15 min后,降解率高達98.7%。形成異質結在光催化反應中能夠有效促進光生電子和空穴對的分離,是提高光催化活性的原因之一。此外,具有(110)主導晶面的BiOIO3/{110}BiOCl比BiOIO3/{001}BiOCl具有更高的可見光吸收性能、更強的抑制光生電子和空穴對復合能力和更大的比表面積,提高了催化活性。

