榮筋拈痛方調控LncRNA H19/miR-675延緩大鼠膝骨關節炎軟骨退變的作用機制
戴雨婷,鄭若曦,王 鶴,陳 俊,陳振沅,吳廣文
(1.福建中醫藥大學中西醫結合研究院,福建 福州 350122;2.福建中醫藥大學中西醫結合學院,福建 福州 350122;3.中醫骨傷及運動康復教育部重點實驗室,福建 福州 350122)
骨關節炎(osteoarthritis,OA)是一種常見的退行性疾病,膝關節因其承載全身負重而最為多發[1-2]。膝骨關節炎(knee osteoarthritis,KOA)的形成與人口老齡化、肥胖、不良生活習慣、錯誤運動方式、職業、外傷史、家族史等因素密切相關,在女性中更為多見,且發病群體出現年輕化趨勢[3]。以軟骨基質進行性丟失為典型表現的軟骨退變是KOA發病的關鍵,軟骨基質主要由以Ⅱ型膠原(CollagenⅡ)為主的各種膠原蛋白和以聚集蛋白聚糖(Aggrecan)為主的蛋白多糖構成[4-5],因此有效調控CollagenⅡ與Aggrecan 的合成和分解代謝是延緩軟骨退變的關鍵。研究發現長鏈非編碼RNA(long non-coding RNA,LncRNA)不但調控癌癥等疾病的發生,而且在OA 相關細胞中的表達存在差異性,對延緩KOA 發病具有重要調節作用[6-7];微小RNA(micro RNA,miRNA)可通過調控膠原蛋白表達影響軟骨細胞的衰老與修復,這被認為是有效治療OA 的新工具[8-9]。研究表明,LncRNA H19 通過調控miR-675 可促進參與合成軟骨細胞相關蛋白的分泌,從而減緩KOA 進程[10]。榮筋拈痛方是挖掘陳可冀院士《清宮配方集成》基礎上擬定而成,前期研究發現榮筋拈痛方可通過多靶點、多途徑對KOA 大鼠起到一定的治療作用[11],但其是否可通過調控LncRNA H19/miR-675 治療KOA 尚不明確。本研究構建KOA 模型,通過觀察榮筋拈痛方對軟骨組織中LncRNA H19/miR-675 及下游CollagenⅡ、Aggrecan 表達水平的影響,旨在探討榮筋拈痛方延緩大鼠KOA 軟骨退變的作用機制,為其臨床應用提供實驗依據。
1 實驗材料
1.1 實驗動物 SPF 級8 周齡雄性SD 大鼠46 只,購自上海斯萊克實驗動物有限責任公司,實驗動物許可證號:SCXK(滬)2007-0011。
1.2 實驗藥物 榮筋拈痛方顆粒劑由江陰天江藥業有限公司生產(批號:2006001);鹽酸氨基葡萄糖膠囊由香港澳美制藥公司生產(批號:4170135)。參照“人和動物間按體表面積折算的等效劑量比值”[12]計算,大鼠給藥量是成人的6 倍。按照大鼠灌胃量為10 mL/kg,將1 袋榮筋拈痛方顆粒劑溶解于0.9%生理鹽水后定容至100 mL;將1 粒鹽酸氨基葡萄糖膠囊溶解于0.9%生理鹽水后定容至100 mL。
1.3 實驗試劑 Trizol(美國Thermo Fisher 公司);無水乙醇(美國Sigma 公司);氯仿(西隴科學股份有限公司);異丙醇(中國國藥集團化學試劑公司);Mir-XTMmiRNA 逆轉錄試劑盒、PrimeScriptTMRT mRNA 逆轉錄試劑盒、TB GreenTMPremix ExTaqTMⅡ試劑盒(日本Takara 公司);AceQqPCR SYBR Green Master Mix 試劑盒(南京諾唯贊生物科技股份有限公司)。
1.4 實驗儀器 全自動樣品快速研磨儀(上海凈信實業發展有限公司);高速冷凍離心機(德國Eppendorf 公司);NanoDrop 2000 超微量分光光度計(美國Thermo 公司);PCR 儀(美國Bio-Rad 公司);7500 Fast實時熒光定量基因擴增儀(美國ABI公司)。
2 方 法
2.1 分組與造模 46 只SD 大鼠適用性喂養1 周后,隨機分為空白組(13 只)與造模組(33 只)。空白組進行假手術處理,將膝關節內側切開1 cm 左右的皮膚與肌肉后隨即縫合,不打開關節腔;造模組采用改良Hulth 法構建大鼠KOA 模型[13],同時連續3 d 肌內注射20 萬U 青霉素防止感染。造模2周后,隨機選擇2組中各3只大鼠拍攝膝關節MRI,鑒定造模是否成功。造模成功后,隨機將造模組大鼠分為模型組、治療組和對照組,每組各10 只。
2.2 藥物干預 治療組按1.9 g/(kg·d)予榮筋拈痛方顆粒藥液灌胃,對照組按0.15 g/(kg·d)予鹽酸氨基葡萄糖膠囊藥液灌胃,空白組與模型組予等量0.9%生理鹽水灌胃。每日灌胃2次,連續灌胃12周,每周稱取1 次體質量調整灌胃量。
2.3 取材 連續干預12 周后,用2%戊巴比妥鈉腹腔注射麻醉后,打開膝關節腔,剝離膝關節周圍的肌肉、韌帶等組織,分離右側脛骨平臺后迅速投入液氮中,隨后放入-80 ℃冰箱保存。
2.4 Real-time PCR 法檢測LncRNA H19、miR-675、CollagenⅡ、Aggrecan 基因表達水平
2.4.1 總RNA 提取 將各組右側脛骨平臺樣本從-80 ℃冰箱取出,收集軟骨組織并加入液氮研磨,采用Trizol 試劑盒提取各組總RNA,并于分光光度計檢測總RNA 濃度。
2.4.2 miRNA 的逆轉錄與檢測 配置miRNA 逆轉錄體系10 μL:mRQ Enzyme Mix 1.25 μL,mRQ Buffer(2×) 5 μL,1 μg 總RNA 與DEPC 水共3.75 μL。反應條件:37 ℃ 1 h,85 ℃ 5 min,4 ℃保存。以逆轉錄成的cDNA 為模板,配置Real-time PCR 反應體系。① U6 反應體系:Mix(2×) 5 μL,ROX(50×)0.2 μL,U6-F 0.4 μL,U6-R 0.4 μL,cDNA 2 μL,DEPC水2 μL。② miR-675反應體系:Mix(2×) 5 μL,ROX(50×) 0.2 μL,miR-675 引物0.4 μL,mRQ3” Primer 0.4 μL,cDNA 2 μL,DEPC 水2 μL。擴增反應條件:95 ℃預變性30 s,95 ℃變性10 s,60 ℃退火34 s,共40 個循環,最后95 ℃ 15 s,60 ℃延伸1 min。以U6 為內參,采用2-ΔΔCt法分析miR-675 相對表達水平,引物序列見表1。
2.4.3 LncRNA/mRNA的逆轉錄與檢測 配置mRNA逆轉錄體系20 μL。① gDNA去除:gDNA Eraser 1 μL,gDNA Eraser Buffer (5×) 2 μL,1 μg總RNA與DEPC水共7 μL,離心后室溫靜置5 min。② Prime Script RT Enzyme MixⅠ1 μL,Prime Script Buffer (5×) 4 μL,RT Primer Mix 1 μL,DEPC 水4 μL。反應條件:37 ℃15 min,85 ℃ 5 s,4 ℃保存。以逆轉錄成的cDNA為模板,配置Real-time PCR 反應體系:Mix(2×) 10 μL,ROX(50×) 0.4 μL,各指標正向引物(F)與反向引物(R)各0.4 μL,cDNA 1 μL,DEPC 水7.8 μL。擴增反應條件為:95 ℃預變性10 min,95 ℃變性10 s,60 ℃退火34 s,共40 個循環,最后95 ℃ 15 s,60 ℃延伸1 min。以β-actin 為內參,采用2-ΔΔCt法分析LncRNA H19、CollagenⅡ、Aggrecan 基因相對表達水平。引物序列見表1。
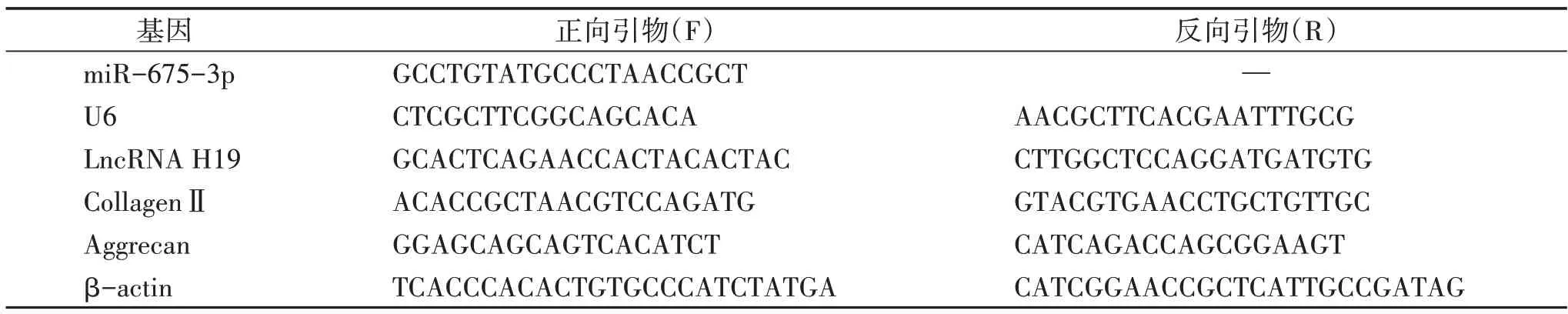
表1 PCR 相關擴增引物序列
2.5 統計學方法 運用SPSS 23.0 統計軟件對數據進行統計學分析。計量資料符合正態分布采用(±s)表示。當滿足正態分布時,運用單因素方差分析,若方差齊則運用LSD-t檢驗進行組間兩兩比較,若方差不齊則運用Games-Howell 檢驗進行組間兩兩比較。P<0.05 為差異有統計學意義。
3 結 果
3.1 實驗動物飼養情況 治療組有2 只大鼠在灌胃過程中可能因肺栓塞死亡。
3.2 膝關節MRI 結果 空白組大鼠膝關節整體結構完整且無腫脹,內外側半月板形態完好,關節腔間隙正常無積液,脛骨平臺與股骨髁軟骨的表面平整。造模組大鼠膝關節整體結構不完整,腫脹明顯,內側半月板缺失,關節腔間隙變寬且有積液累積,脛骨平臺與股骨髁軟骨的表面不平整,局部缺如,伴有結締組織增生與骨贅形成,以上結果表明大鼠KOA 模型建立成功。見圖1。
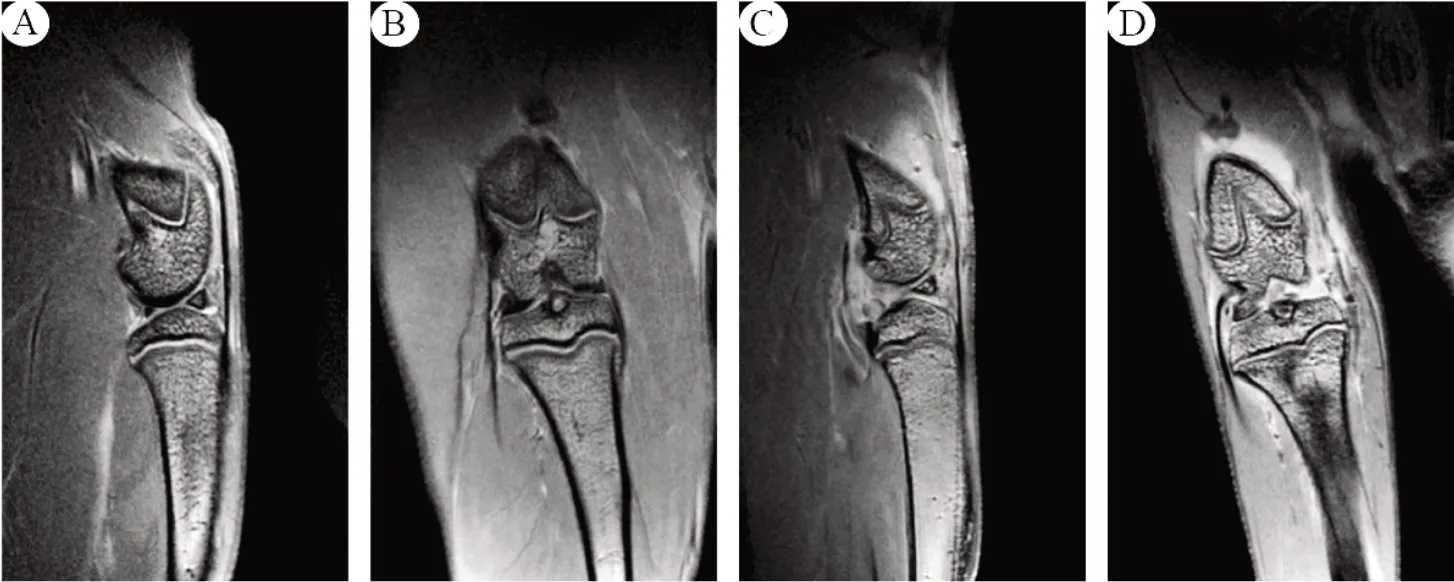
圖1 大鼠膝關節MRI 影像圖
3.3 4 組 大 鼠 軟 骨 組 織LncRNA H19、miR-675、CollagenⅡ和Aggrecan 基因表達水平比較 與空白組比較,模型組軟骨組織LncRNA H19、miR-675、Collagen Ⅱ和Aggrecan 基因水平均明顯降低(P<0.05);與模型組比較,治療組和對照組軟骨組織LncRNA H19、miR-675、CollagenⅡ和Aggrecan 基因水平均明顯升高(P<0.05)。見圖2。
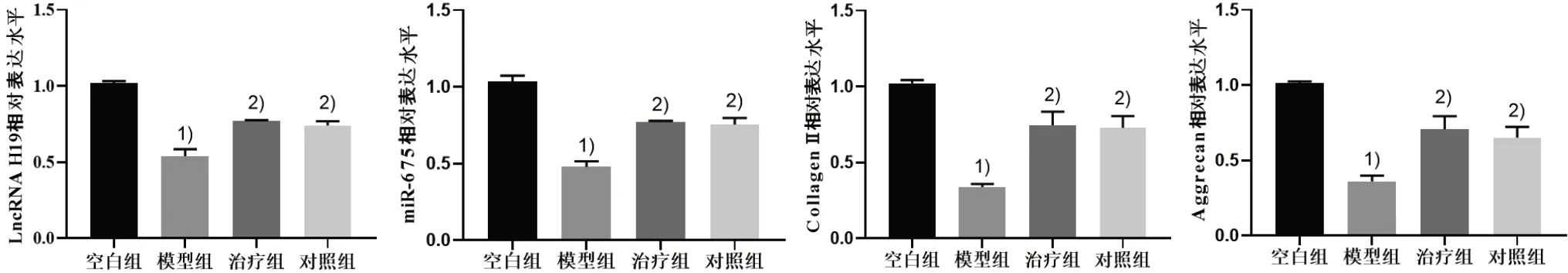
圖2 4 組大鼠軟骨組織LncRNA H19、miR-675、CollagenⅡ和Aggrecan 基因水平比較
4 討 論
KOA 臨床常表現為疼痛、腫脹、僵硬、關節屈伸不利、活動受限等,嚴重者會致畸、致殘,給患者和社會帶來嚴重的經濟損失與生活負擔[14]。流行病學調查數據發現,40、60、80 歲以上人群患病率分別為38%、50%、80%[15-16]。局部使用非甾體類抗炎藥為目前KOA 的一線治療方法。與口服相比,關節腔內注射配合糖皮質激素治療是臨床常用的選擇,療效顯著且副作用小[17]。但是非甾體類抗炎藥的廣泛使用存在患有心肌梗死的弊端,除此之外還存在胃腸道出血的毒副作用,具有一定程度的死亡率,嚴重危害患者的生命安全。手術治療因其較高的手術置換費用、術后并發癥、康復時間長等缺點不被晚期患者所采納[18-20]。因此,KOA 的防治已然成為公共健康的重大課題,研發療效明確,毒副作用少,能夠緩解甚至阻斷KOA 發展的新藥具有重大意義。
KOA 歸屬于中醫學“骨痹”范疇,骨痹實則為“虛證”“痿證”,治療的關鍵為扶正祛邪[21]。榮筋拈痛方由牛膝、當歸、獨活、羌活、防風、甘草組成,具有補肝腎、壯筋骨、祛風濕、止痹痛之功效。牛膝、當歸君臣相伍,補肝腎、壯筋骨,又兼活血,寓“治風先治血,血行風自滅”之意;獨活治下,羌活治上,與防風共行祛風、除濕、止痛之效,三者皆為佐藥;甘草緩急止痛,調和諸藥為使藥。榮筋拈痛方標本兼顧,對痹證日久、肝腎俱虛的膝骨關節炎具有治療作用[22]。前期研究可知,榮筋拈痛方具有抗炎鎮痛的效果,臨床可有效緩解KOA 癥狀[23]。其有效成分可通過促進膠原蛋白與蛋白多糖的合成參與軟骨基質的合成,降低基質金屬蛋白酶的表達,參與軟骨基質的分解,進一步利用促進軟骨細胞增殖、延緩軟骨細胞退變、抑制軟骨細胞凋亡的方式改變軟骨結構[24-25]。除此之外,榮筋拈痛方可抑制炎癥因子分泌,對滑膜炎癥也具有一定的緩解作用[26]。
與少量的蛋白質編碼基因不同,非編碼RNA(non-coding RNA,ncRNA)占人類基因組的大部分,研究發現其可參與調控細胞增殖、分化、代謝等全過程,是轉錄及轉錄后修飾的關鍵因子[27]。ncRNAs包括miRNA、LncRNA 和環狀RNA(circular RNA,circRNA)等[28]。miRNA 是一類長約20~22 個核苷酸的單鏈小RNA 分子。其在多種病理生理過程中起關鍵作用,一方面可直接結合靶基因mRNA 并使其降解,另一方面可抑制mRNA 的翻譯以調控基因表達[29]。研究發現在膝關節腔內的滑液中存在miRNA,且其表達穩定,可根據滑液中不同miRNA的表達水平差異區分KOA 患者與正常人[30]。LncRNA 的長度>200 nt,曾被認為不具有生物學功能,但目前發現其可通過參與修飾染色質、激活或干擾轉錄、核內運輸等過程調控基因表達[31]。LncRNA 可通過多種途徑參與緩解KOA,如LncRNA通過調控MMP 和ADAMTS 影響軟骨機制的合成與分解代謝,LncRNA 參與調控軟骨細胞的增殖與凋亡,LncRNA 通過NF-κB 與MAPK 途徑參與調控炎癥反應,LncRNA 參與調控滑膜關節血管生成,LncRNA 通過調控自噬影響軟骨變性等[32]。通過基因調控網絡的深入研究,發現許多疾病中LncRNA和miRNA 之間存在相互作用和相互調控。LncRNA H19 最早是由Tilghman 實驗室發現的,其在小鼠胎兒肝臟中高表達,出生后下調,在控制細胞壽 命 過 程 中 扮 演 重 要 角 色[33]。LncRNA H19 是miRNA 前體轉錄物,miR-675 是其第1 個外顯子區域加工產生的衍生物,LncRNA 可以通過成為具有調控功能的miRNA 的前體發揮作用[34]。
CollagenⅡ對軟骨修復與再生起到了重要作用,研究者往往通過增加CollagenⅡ的表達或者抑制其降解的角度來延緩KOA 的進展[35]。當Aggrecan 合成受到抑制時,關節軟骨會因失去滋養而出現軟骨基質的損傷,最終發生骨關節退行性病變[36]。miR-675 對關節軟骨合成代謝起促進作用,能有效延緩KOA 進展[37]。研究表明沉默LncRNA H19 或者miR-675 時,CollagenⅡ表達水平顯著下調,過表達時則與之相反,但是否介導Aggrecan 的表達未曾報道[38-39]。可見,LncRNA H19/miR-675 表達水平的變化與軟骨基質合成代謝密切相關[10,40]。
本研究結果顯示,與空白組比較,模型組中LncRNA H19、miR-675 及其調控的CollagenⅡ、Aggrecan 基因表達水平降低;經過榮筋拈痛方與鹽酸氨基葡萄糖治療后,LncRNA H19、miR-675、CollagenⅡ、Aggrecan 基因表達水平升高,提示榮筋拈痛方可能通過上調LncRNA H19/miR-675 促進CollagenⅡ、Aggrecan 表達,從而延緩大鼠軟骨退變,起到治療KOA 的作用。

