空間導航的腦網絡基礎和調控機制*
孔祥禎 張鳳翔 蒲 藝
·研究構想(Conceptual Framework)·
空間導航的腦網絡基礎和調控機制*
孔祥禎1,2張鳳翔1蒲 藝3
(1浙江大學心理與行為科學系, 杭州 310028) (2浙江大學醫學院附屬邵逸夫醫院, 杭州 310058) (3馬克斯·普朗克經驗美學研究所神經科學系, 法蘭克福 60322, 德國)
空間導航在生活中時刻發生, 空間能力衰退是阿爾茲海默癥的重要早期表現。早期關于空間導航神經機制的研究主要關注單個腦區的特異性功能, 但這些腦區如何交互以整合不同模態的信息支持復雜導航行為尚不清楚。腦成像技術、腦網絡建模方法和神經調控手段的發展, 為在腦網絡水平理解人類空間導航的認知神經機制提供了重要研究手段。本研究試圖融合空間導航認知神經機制研究的最新進展, 借助腦網絡建模、大數據分析、微電流刺激等前沿研究手段, 研究空間導航腦網絡的關鍵拓撲屬性特征(如模塊化、核心節點等), 探尋該功能特異性神經網絡的重要影響因素和調控機制, 并構建空間導航的腦網絡理論模型。研究成果將有利于理解人類復雜導航行為的腦網絡基礎, 為阿爾茲海默癥等相關認知障礙腦疾病的篩查和診斷提供重要參考。
空間導航, 腦網絡, 神經調控, 神經機制, 認知地圖
1 問題提出
在熟悉的環境中穿行, 在陌生的環境中尋路, 空間導航活動時刻在我們的生活中發生。對空間的認知被認為是人類認知和智能的“核心知識” (Core Knowledge) (Spelke & Kinzler, 2007)。因此, 研究空間導航的發展、認知神經基礎和遺傳因素, 對我們理解智能的本質和起源, 有著重要的科學意義。英國倫敦大學學院教授John O'Keefe、挪威科技大學教授May-Britt Moser、Edvard Moser通過對老鼠的電生理實驗研究(Fyhn et al., 2004; O'Keefe & Nadel, 1978), 首次發現了構成大腦空間定位系統的功能特異神經元細胞, 開啟了理解人類空間導航神經基礎的大門。憑借這一發現, 他們獲得了2014年諾貝爾生理學或醫學獎。此外, 青少年時期的空間能力與其將來能否在科學、技術、工程和數學等理工科領域(STEM)取得更好的學業及職業成就, 有著直接關聯(Wai et al., 2009); 而且, 空間導航能力的退化, 又是阿爾茲海默癥(Alzheimer's disease, AD)等與記憶有關的神經退行性疾病的核心臨床表現(張家鑫等, 2019; Coughlan et al., 2018)。因此, 對人類空間導航的認知神經和遺傳基礎的研究具有重要的教育意義和臨床價值。
近幾十年來, 空間導航研究領域取得了重要進展, 其研究對象涵蓋不同動物模型、兒童和成年人, 研究方法涉及行為、電生理記錄、功能和結構腦成像等。這些研究成果, 主要集中在對單個腦區特異性功能的刻畫, 比如海馬(hippocampus)中的位置細胞(place cell)和內嗅皮層(entorhinal cortex)的網格細胞(grid cell)等(Fyhn et al., 2004; O'Keefe & Nadel, 1978); 此外就是利用腦影像的方法, 找到不同腦區的特異性功能, 分別對應空間導航的不同認知成分, 比如位于內嗅皮層的類網格細胞功能和位于旁海馬的場景加工腦區(Horner et al., 2016; Zhen et al., 2017)。這些研究, 極大地推進了我們對人類空間導航的認知加工和神經機制的理解(圖1) (王欣等, 2018; 許琴等, 2010; Coughlan et al., 2018; Epstein et al., 2017)。
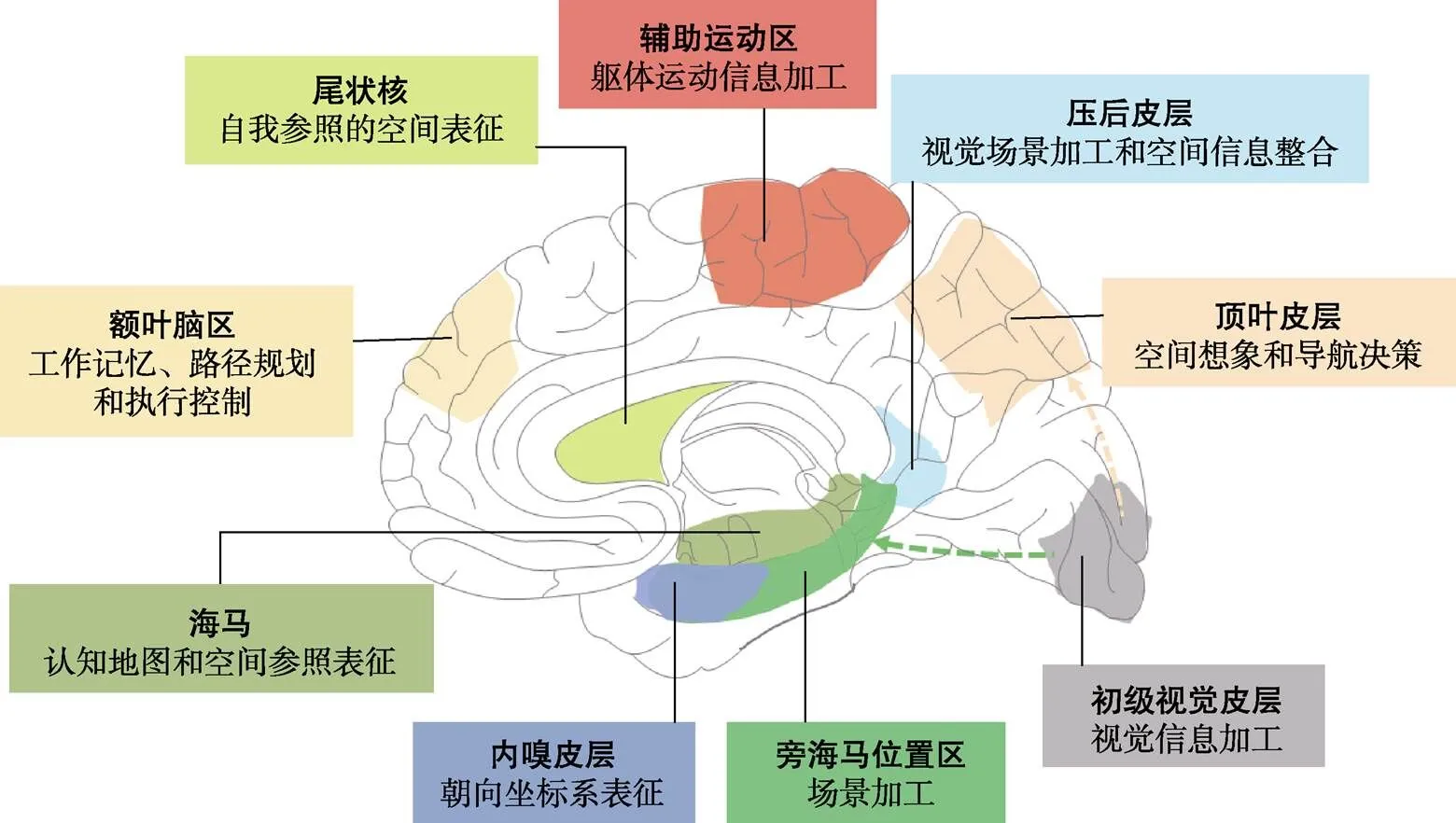
圖1 參與空間導航過程的主要腦結構及相關功能
然而, 空間導航是一個復雜的認知過程, 靈活的導航需要多感知模態整合、視空間編碼、記憶和決策等多個認知成分的共同參與(Wolbers & Hegarty, 2010; Baumann & Mattingley, 2021)。而且,研究者認為, 這些認知過程并非不同表征模塊獨立運作(modular processing), 而是一個高度動態、需要整合不同模態信息的加工過程(heuristic processing) (Ekstrom et al., 2017; Kong et al., 2017)。此外, 研究表明, 對導航至關重要的海馬, 其功能不僅僅是對位置的表征, 它似乎更像是普遍的粘合劑(“the hippocampus as a binding device”) (Pu et al., 2020; Cornwell et al., 2008; Kessels et al., 2001; Mitchell et al., 2000), 聯結了來自其他腦區的不同模態信息, 以支持人類的行為和決策。因此, 研究者指出, 研究空間導航的神經機制不應局限于某個特定腦區(如海馬), 而應該從神經環路或網絡的角度, 研究不同腦區如何交互以支撐復雜導航行為(Ekstrom et al., 2017; Baumann & Mattingley, 2021; Kong et al., 2017)。目前, 我們對人類大腦空間導航腦網絡的架構和運作機制還處于起步階段, 很多關鍵問題尚不清楚。例如, 導航腦網絡的復雜網絡屬性(核心節點和模塊化)是怎樣的?通常被認為對空間導航至關重要的海馬結構, 是導航腦網絡的核心節點嗎?一些與導航和記憶有關的神經退行性疾病, 如阿爾茲海默癥, 是否表現出導航腦網絡異常?如何實現對導航腦網絡的精準調控, 從而改善導航行為表現?
鑒于此, 本項目擬采用跨學科研究手段, 對空間導航的腦網絡基礎和調控機制進行研究。本項目有望為我們理解空間導航在腦網絡水平的神經機制提供新的科學證據, 同時對空間導航腦網絡和調控機制的研究, 為研究AD等認知障礙腦疾病提供了新的重要視角, 為早期診斷和精準治療新方案的提出提供參考。
2 研究現狀
2.1 腦網絡研究方法
隨著神經成像技術的不斷成熟和普及, 彌散加權成像(diffusion weighted imaging, DWI)、功能磁共振成像(functional magnetic resonance imaging, fMRI)和T1加權成像(T1-weighted MRI)等多種腦影像方法, 在考察多個腦區之間的內在交互研究中得到廣泛應用。采用這些成像技術和不同的圖像處理算法, 我們可以從白質纖維連接、功能連接、形態學協變關聯等不同角度, 考察感興趣腦區之間的連接特征和腦網絡拓撲屬性。
白質纖維連接主要采用DWI數據和纖維追蹤方法, 可以量化不同腦區之間的白質纖維連接的路徑和強度信息(Maier-Hein et al., 2017; Tournier et al., 2019)。功能連接主要采用靜息態或任務態fMRI數據, 通過量化不同腦區功能活動相關的時間序列的同步性, 可以用于研究不同腦區之間的功能交互的方向性和強度信息(Kelly et al., 2012; Smith et al., 2013)。結構形態學的協變關聯也是一種常用的結構連接建模方法, 其計算過程往往基于大腦結構形態學測量, 比如通過計算兩個腦區的形態學測量跨個體或跨時間點的相關性來量化腦區間的共變性(He et al., 2007; Evans, 2013); 也有研究者提出, 通過計算不同腦區形態學測量分布的相似性來量化單被試水平的腦區間結構關聯(Kong et al., 2015; Kong et al., 2014)。
基于不同腦連接分析方法可以構建包含多個腦區的連接網絡。基于此, 圖論和腦連接組學方法提供了一系列針對復雜腦網絡整體屬性的量化手段, 包括小世界網絡、核心節點腦區和模塊化等(Zuo et al., 2012; He & Evans, 2010)。結合腦影像技術和腦連接組學方法, 已發表的研究為我們了解人腦全腦水平的網絡架構特征提供了重要數據。相關腦成像技術和腦網絡分析方法的發展, 也為在腦連接和腦網絡水平理解人類空間導航的腦網絡基礎提供了重要研究手段。
2.2 空間導航的腦網絡研究
目前, 僅有較少數研究探索不同腦區如何交互以支持空間導航和記憶, 我們對導航腦網絡的組織架構和拓撲屬性尚不清楚(Ekstrom et al., 2017; Baumann & Mattingley, 2021; Epstein et al., 2017)。
利用皮層腦電圖(electrocortigography, ECoG), Watrous等人研究了顳葉內側、前額葉和部分頂葉腦區如何實現交互以支持空間和時間記憶(Watrous et al., 2015)。他們發現, 相比較不正確記憶的試次,正確記憶的試次所展現出的腦區之間的功能連接更強。雖然, 由于ECoG的電極覆蓋有限, 他們沒能記錄到其他一些與導航和記憶有關的重要腦區,但他們的研究結果極大地表明腦區之間的協同對導航和記憶至關重要。
為了克服上述ECoG電極覆蓋有限的缺點,作者采用大尺度腦影像元分析(meta-analysis) (Yarkoni et al., 2011)對導航相關的腦區進行了全面定位, 并基于此導航腦功能區圖譜, 采用功能連接方法考察了空間導航腦網絡在無任務狀態(靜息態)時的網絡拓撲屬性(如核心節點和模塊化等)及其行為學相關(Kong et al., 2017)。與以往腦網絡研究中所采用的全腦網絡方法不同, 該研究首先利用幾十年關于空間導航的神經影像學研究成果(截止到2014年11月), 基于大尺度元分析定位導航相關的功能腦區, 并以此為節點, 結合靜息態fMRI對空間導航腦網絡進行建模和分析。研究結果顯示, 基于靜息態fMRI的空間導航腦網絡, 表現出小世界和模塊化的組織特征。此外, 近年來, 研究者不斷認識到壓后皮層(retrosplenial cortex, RSC)在空間導航中的關鍵作用, 提出了RSC作為導航網絡核心節點(而非海馬)的理論預測(Ekstrom et al., 2017; Weisberg & Ekstrom 2021)。該理論對于理解人類空間導航腦網絡的認知和計算機制具有重要的意義, 但還尚待進一步驗證。在前期的初步研究中, 我們發現, RSC在基于靜息態fMRI構建的導航腦網絡中表現出最高的中介度(betweenness), 并且RSC的核心程度在個體間的差異與自我報告的導航能力顯著正相關(Kong et al., 2017)。這些研究結果為以RSC作為導航網絡核心節點的理論預測提供了重要實證數據。該研究為我們理解空間導航的腦網絡基礎邁出了關鍵一步。
近十年來, 有更多關于空間導航的腦影像研究發表, 這些最新的研究為我們定位導航相關腦功能區提供了新的重要數據。在本項目中, 將最新的腦影像研究成果整合到元分析中, 從而對導航相關腦功能區進行更新。這些更新后的腦區定位可以幫助我們對導航腦網絡進行更精準地建模和分析。
2.3 直接電刺激調控大腦活動
直接電刺激通過植入的電極將電流施加在大腦的特定區域, 是調控神經活動的新的有效方法(Hescham et al., 2020)。直接電刺激是治療帕金森患者運動失能(Benabid et al., 1991; Bronstein et al., 2011)和確定癲癇發作部位(Fisher et al., 2010; McIntyre & Hahn, 2010)的標準方法, 也被用于探索強迫癥等一些精神障礙疾病的診療方案(Greenberg et al., 2006)。直接電刺激作用效果的底層機制可能與其通過電流刺激打破了腦網絡的失能狀態有關(Ezzyat et al., 2018)。在關于腦功能的基礎研究方面, 研究者利用癲癇病人術前植入的深度電極,采用iEEG和直接電刺激方法調控海馬和內嗅皮層的活動, 考察對導航行為或記憶能力的影響。例如, Suthana等人在導航學習階段, 給5名術前癲癇病人內嗅皮層和海馬連續施加50 Hz的微電流, 他們發現, 相較于沒有電流刺激的條件, 刺激病人的內嗅皮層后導航行為有明顯提高; 然而, 刺激海馬的條件下病人的導航能力卻沒有明顯變化(Suthana et al., 2012)。但在隨后一個更大規模的實驗里, 研究者發現, 不管刺激內嗅皮層還是海馬, 均會使導航行為表現顯著降低(Jacobs et al., 2016)。
在不同研究中, 直接電刺激對行為產生了不同的影響, 其原因也尚不明確(Mohan et al., 2020)。可能的因素包括不同研究中采用的刺激靶點腦區、刺激強度和頻率、行為范式等方面的異質性。因此, 目前我們對如何精準地調控大腦以改善認知功能還知之甚少。這些亟待解決的關鍵核心問題包括:如何選擇直接電刺激的靶點腦區以達到最佳的調控效果、刺激特定腦區對腦認知網絡的動態影響以及刺激引起的腦網絡的變化和行為改變的對應關系等。為此, 本項目將以得到的空間導航腦網絡模型作為指導, 選取導航腦網絡中的核心節點腦區和與之連接的白質纖維作為靶點進行微電流刺激, 結合iEEG腦活動記錄, 探索核心節點腦區對導航網絡動態和導航行為的調控機制。
3 研究構想
本項目將采用行為學測試、多模態磁共振腦成像技術、計算建模與機器學習、腦網絡組學和神經調控技術等跨學科研究方法, 結合大樣本開放數據庫, 研究空間導航的腦網絡基礎及其調控機制。
3.1 研究1:空間導航腦網絡的定位和建模
本部分我們將重點關注空間導航腦網絡的定位、網絡建模和復雜網絡分析, 以揭示空間導航腦網絡的空間分布和核心節點、模塊化等復雜網絡拓撲屬性, 以及不同模態網絡之間的交互關系。具體包括:1) 調研空間導航相關的神經影像研究, 采用大尺度腦影像元分析方法, 對研究文獻中報告的功能激活坐標進行元分析, 形成空間導航的腦功能區分布圖。進而, 參照大腦解剖先驗知識和大腦分割圖譜(atlas), 完成相關腦區的分割和命名, 形成空間導航腦功能區圖譜。2) 基于得到的導航腦功能區圖譜, 結合不同模態磁共振圖像, 建立多模態腦網絡:結合彌散磁共振成像數據和纖維追蹤技術, 量化腦區間白質纖維連接, 構建白質連接網絡; 結合靜息態功能磁共振成像數據和功能連接方法, 量化腦區間功能連接, 構建功能連接網絡; 結合結構磁共振腦成像數據和腦形態學分析方法, 采用作者在已有研究中提出的個體形態學相似性腦網絡算法, 構建空間導航腦網絡的形態學網絡。3).采用復雜網絡研究方法, 考察不同模態空間導航腦網絡的核心節點、模塊化等拓撲特征。采用多元統計方法考察不同模態導航腦網絡的相似性, 考察功能網絡與結構網絡之間的交互關系。
3.2 研究2:空間導航腦網絡的影響因素
本部分我們將采用大樣本公開數據庫(UK Biobank), 通過關聯導航腦網絡的拓撲屬性指標與早期生活經歷、全基因組數據, 探索該功能網絡的早期生活經歷因素和遺傳基礎。具體包括:1) 考察導航腦網絡的拓撲屬性指標與性別和出生地(城市或鄉村)、家庭經濟狀況、飲食和酒精攝入等早期生活經歷之間的關系; 2) 基于全基因組關聯分析和遺傳學功能分析, 考察導航腦網絡的遺傳基礎, 探索導航腦網絡的候選基因和通路。
3.3 研究3:空間導航腦網絡的調控機制
本部分我們將結合前沿的iEEG和直接電刺激技術, 以本項目得到的空間導航腦網絡模型為指導, 探索導航腦網絡核心節點對網絡狀態和導航行為表現的調控作用。具體包括:1) 基于癲癇病人術前植入的深度電極(depth electrode), 記錄導航腦網絡相關腦區的顱內腦電活動, 并采用直接電刺激技術, 考察不同靶點腦區對網絡狀態的調控作用; 2) 基于癲癇病人術前植入的深度電極, 采用直接電刺激技術, 考察不同靶點腦區對導航行為表現的調控作用。在本部分研究中, 刺激靶點腦區的選擇是關鍵。考慮到網絡模型中核心節點的關鍵作用, 該研究中靶點腦區選擇將主要參考上述研究建立的導航腦網絡模型中識別出的核心節點。根據已有實驗數據和相關理論假設, 海馬(“the hippocampus as a binding device”) (Kessels et al., 2001; O’Reilly et al., 2022)和RSC (負責不同子系統的信息整合) (Ekstrom et al., 2017)是目前我們最感興趣的靶點腦區。研究實施過程中, 靶點腦區和其他相關參數將結合最新的研究進展最終確定。
4 理論構建與創新
空間認知是人類認知和智能的“核心知識”, 空間導航能力缺陷被認為是AD的關鍵認知生物學標志物。揭示人類空間導航的認知神經機制和遺傳基礎, 不僅在心理學、認知神經科學、腦科學和醫學等領域具有重要的科學意義, 同時也具有重要的教育意義和應用價值。
已有研究通常關注海馬、內嗅皮質等單個腦區的功能特異性, 因此在傳統理論中多局限于單個腦區在空間導航過程中的功能。空間導航是一個復雜的認知過程, 近年來, 研究者指出, 研究空間導航的神經機制不應局限于某個特定腦區(如海馬), 而應該從神經環路或網絡的角度, 研究不同腦區如何交互以支撐復雜導航行為(Ekstrom et al., 2017; Baumann & Mattingley, 2021; Kong et al., 2017; Weisberg & Ekstrom, 2021)。本項目打破傳統的局限于單個腦區功能特異性的研究視角, 采用跨學科的研究手段和計算方法, 對空間導航的腦網絡基礎進行研究, 有望識別出空間導航腦網絡的關鍵拓撲屬性(如模塊化和核心節點腦區等), 揭示導航網絡中不同模塊的內部結構特征和功能意義, 以及關鍵核心節點的分布特點, 這些結果對于構建空間導航的腦網絡理論模型可以提供重要數據(圖2)。以導航腦網絡核心節點腦區為例, 近年來, 研究者基于RSC在空間導航中的關鍵作用, 提出了RSC作為導航腦網絡核心腦區的理論假設(Ekstrom et al., 2017), 我們預期, 本研究的成果將為進一步檢驗和完善相關理論提供多個方面的實證數據。同時, 在此基礎上, 我們將以導航腦網絡的核心節點腦區為直接電刺激靶點, 結合基于磁共振技術的功能連接和白質纖維追蹤技術, 探索靶點對導航腦網絡的網絡動態和導航行為的調控機制。完善的空間導航腦網絡理論模型的建立, 可以催生大量重要的研究工作, 以解決新的關鍵科學問題。例如, 導航腦網絡中不同功能模塊的具體功能如何?不同模塊之間的交互在不同導航任務下是如何動態變化的?交互動態的異常是否會導致腦疾病的產生?
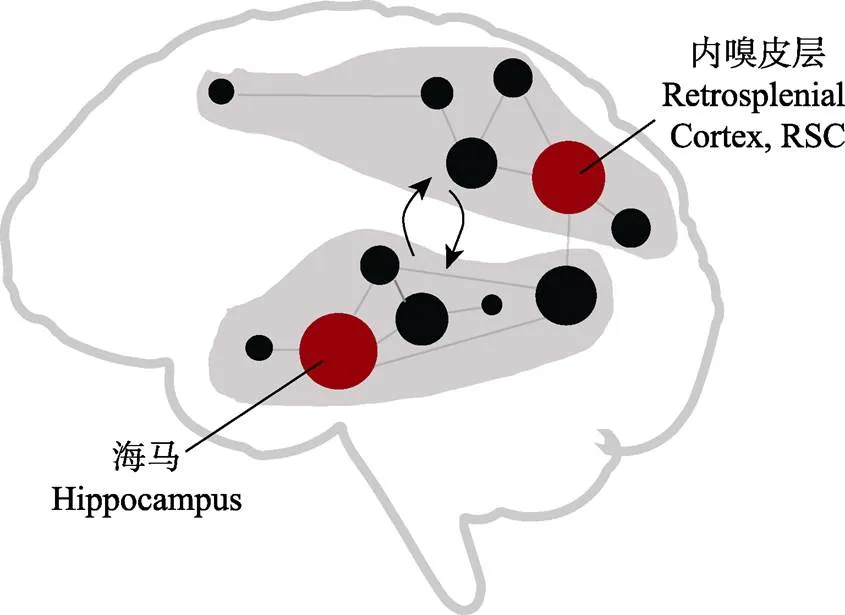
圖2 空間導航的腦網絡模型示意圖(灰色區塊為可能存在的功能模塊, 紅色圓點為可能的核心節點腦區, 灰色箭頭為不同功能模塊間動態交互)
基于諸多細胞水平的研究發現, 研究者提出了整合位于不同腦區的不同類型神經細胞加工的向量編碼理論模型, 試圖揭示空間信息不同要素神經表征的統一機制(Bicanski & Burgess, 2020)。這些模型為我們更好地理解空間導航腦網絡中不同節點腦區、不同功能模塊之間的交互以及這些交互的功能意義, 提供了重要視角; 同時, 導航腦網絡模型的建立, 又可以進一步幫助我們在神經環路和網絡水平驗證和理解這些計算理論。
此外, 大量研究表明, 空間導航能力衰退是AD等認知障礙的重要早期行為表現; 同時, 參與空間導航的重要腦區與早期AD影響的腦區大量重疊。隨著社會老齡化, AD等老年癡呆癥已經成為嚴重的健康、經濟和社會問題。由北京宣武醫院主導的一項最新大規模調查顯示, 在我國60歲以上人群中有約1000萬AD患者, 占比約為4% (Jia et al., 2020)。關于空間導航的腦網絡的研究成果, 將幫助我們從腦認知網絡的角度, 理解老齡化與相關腦疾病的底層神經機制, 幫助我們更好地開發新的診斷和干預策略, 以阻斷或減緩疾病的發展, 推遲并降低發病率。目前, 針對AD的神經調控研究還相對比較初步, 且多采用TMS、tDCS等無創調控技術。這些技術在研究腦網絡的調控機制中, 尤其是以深部腦結構為靶點腦區時, 具有很大的局限性。因此, 本項目選用更為直接、精準的直接電刺激技術, 探索特定腦結構對導航腦網絡的調控機制。雖然, 該神經調控研究在癲癇患者中進行, 相關研究成果一方面將幫助我們理解導航腦網絡的調控機制, 同時將為AD等空間導航損傷相關的腦疾病的干預和治療提供重要參考。
綜上所述, 本項目采用跨學科研究方法, 對空間導航的腦網絡基礎和調控機制進行研究。研究成果將為我們理解空間導航的神經環路機制、影響因素, 以及腦認知網絡與行為之間的因果關系提供重要科學證據; 同時, 導航腦網絡模型及其調控機制為研究AD等認知障礙腦疾病提供了新的重要的視角, 為早期診斷和精準治療新方案的提出提供參考, 符合國家重大戰略需求。
王欣, 武文博, 李竹, 王濤, 張鑫, 青釗, 張冰. (2018). 網格細胞的電生理及腦功能成像研究進展.,(5), 381–385.
許琴, 羅宇, 劉嘉. (2010). 方向感的加工機制及影響因素.,(8), 1208–1221.
張家鑫, 海拉干, 李會杰. (2019). 空間導航的測量及其在認知老化中的應用.,(12), 2019–2033.
Baumann, O., & Mattingley, J. B. (2021). Extrahippocampal contributions to spatial navigation in humans: A review of the neuroimaging evidence.,(7), 640–657.
Benabid, A. L., Pollak, P., Gervason, C., Hoffmann, D., Gao, D. M., Hommel, M., Perret, J. E., & de Rougemont, J. (1991). Long-term suppression of tremor by chronic stimulation of the ventral intermediate thalamic nucleus.,(8738), 403–406.
Bicanski, A., & Burgess, N. (2020). Neuronal vector coding in spatial cognition.(9), 453–470.
Bronstein, J. M., Tagliati, M., Alterman, R. L., Lozano, A. M., Volkmann, J., Stefani, A., ... DeLong, M. R. (2011). Deep brain stimulation for Parkinson disease: An expert consensus and review of key issues.,(2), 165. https://doi.org/10.1001/archneurol.2010.260.
Cornwell, B. R., Johnson, L. L., Holroyd, T., Carver, F. W., & Grillon, C. (2008). Human hippocampal and parahippocampal theta during goal-directed spatial navigation predicts performance on a virtual Morris water maze.,(23), 5983–5990.
Coughlan, G., Laczó, J., Hort, J., Minihane, A. M., & Hornberger,M. (2018). Spatial navigation deficits - overlooked cognitive marker for preclinical Alzheimer disease?,(8), 496–506. https://doi.org/10.1038/s41582- 018-0031-x
Ekstrom, A. D., Huffman, D. J., & Starrett, M. (2017). Interacting networks of brain regions underlie human spatial navigation: A review and novel synthesis of the literature.,(6), 3328–3344. https://doi.org/10.1152/jn.00531.2017
Epstein, R. A., Patai, E. Z., Julian, J. B., & Spiers, H. J. (2017). The cognitive map in humans: Spatial navigation and beyond.,(11), 1504–1513. https://doi.org/10.1038/nn.4656
Evans, A. C. (2013). Networks of anatomical covariance.,, 489–504. https://doi.org/10.1016/j.neuroimage. 2013.05.054
Ezzyat, Y., Wanda, P. A., Levy, D. F., Kadel, A., Aka, A., Pedisich, I., ... Kahana, M. J. (2018). Closed-loop stimulation of temporal cortex rescues functional networks and improves memory.,(1), 365. https://doi.org/10.1038/s41467-017-02753-0
Fisher, R., Salanova, V., Witt, T., Worth, R., Henry, T., Gross, R., ... Group, S. S. (2010). Electrical stimulation of the anterior nucleus of thalamus for treatment of refractory epilepsy.,(5), 899–908. https://doi.org/10. 1111/j.1528-1167.2010.02536.x
Fyhn, M., Molden, S., Witter, M. P., Moser, E. I., & Moser, M. B. (2004). Spatial representation in the entorhinal cortex.,(5688), 1258–1264.
Greenberg, B. D., Malone, D. A., Friehs, G. M., Rezai, A. R., Kubu, C. S., Malloy, P. F., … Rasmussen, S. A. (2006). Three-year outcomes in deep brain stimulation for highly resistant obsessive-compulsive disorder.,(11), 2384–2393. https://doi.org/10.1038/sj.npp.1301165
He, Y., Chen, Z. J., & Evans, A. C. (2007). Small-world anatomical networks in the human brain revealed by cortical thickness from MRI.,(10), 2407–2419.
He, Y., & Evans, A. (2010). Graph theoretical modeling of brain connectivity.,(4), 341–350. https://doi.org/10.1097/WCO.0b013e32833aa567
Hescham, S., Liu, H., Jahanshahi, A., & Temel, Y. (2020). Deep brain stimulation and cognition: Translational aspects.,, 107283. https://doi.org/10.1016/j.nlm.2020.107283
Horner, A. J., Bisby, J. A., Zotow, E., Bush, D., & Burgess, N. (2016). Grid-like processing of imagined navigation.,(6), 842–847.
Jacobs, J., Miller, J., Lee, S. A., Coffey, T., Watrous, A. J., Sperling, M. R., … Rizzuto, D. S. (2016). Direct electrical stimulation of the human entorhinal region and hippocampus impairs memory.,(5), 983–990. https://doi.org/ 10.1016/j.neuron.2016.10.062
Jia, L., Du, Y., Chu, L., Zhang, Z., Li, F., Lyu, D., ... Qiu, Q. (2020). Prevalence, risk factors, and management of dementia and mild cognitive impairment in adults aged 60 years or older in China: A cross-sectional study.(12), e661–e671.
Kelly, C., Biswal, B. B., Craddock, R. C., Castellanos, F. X., & Milham, M. P. (2012). Characterizing variation in the functional connectome: Promise and pitfalls.,(3), 181–188.
Kessels, R. P., de Haan, E. H., Kappelle, L. J., & Postma, A. (2001). Varieties of human spatial memory: A meta-analysis on the effects of hippocampal lesions.(3), 295–303.
Kong, X. Z., Liu, Z. G., Huang, L. J., Wang, X., Yang, Z. T., Zhou, G. F., Zhen, Z. L., & Liu, J. (2015). Mapping individual brain networks using statistical similarity in regional morphology from MRI.,(11), e0141840.
Kong, X. Z., Wang, X., Huang, L., Pu, Y., Yang, Z., Dang, X., Zhen, Z., & Liu, J. (2014). Measuring individual morphological relationship of cortical regions.,, 103–107.
Kong, X. Z., Wang, X., Pu, Y., Huang, L., Hao, X., Zhen, Z., & Liu, J. (2017). Human navigation network: The intrinsic functional organization and behavioral relevance.,(2), 749–764. https://doi.org/ 10.1007/s00429-016-1243-8
Maier-Hein, K. H., Neher, P. F., Houde, J. C., C?té, M. A., Garyfallidis, E., Zhong, J., ... Descoteaux, M. (2017). The challenge of mapping the human connectome based on diffusion tractography.,(1), 1349. https://doi.org/10.1038/s41467-017-01285-x
McIntyre, C. C., & Hahn, P. J. (2010). Network perspectives on the mechanisms of deep brain stimulation.,(3), 329–337. https://doi.org/10.1016/j.nbd.2009. 09.022
Mitchell, K. J., Johnson, M. K., Raye, C. L., & D'Esposito, M. (2000). fMRI evidence of age-related hippocampal dysfunction in feature binding in working memory.,(1-2), 197–206. https://doi.org/10.1016/ s0926-6410(00)00029-x
Mohan, U. R., Watrous, A. J., Miller, J. F., Lega, B. C., Sperling, M. R., Worrell, G. A., … Jacobs, J. (2020). The effects of direct brain stimulation in humans depend on frequency, amplitude, and white-matter proximity.,(5), 1183–1195. https://doi.org/10.1016/j. brs.2020.05.009
O'Keefe, J., & Nadel, L. (Eds.). (1978).. London, Clarendon Press.
O’Reilly, R. C., Ranganath, C., & Russin, J. L. (2022). The structure of systematicity in the brain.,(2), 124–130.
Pu, Y., Cheyne, D., Sun, Y., & Johnson, B. W. (2020). Theta oscillations support the interface between language and memory.,, 1–12.
Smith, S. M., Vidaurre, D., Beckmann, C. F., Glasser, M. F., Jenkinson, M., Miller, K. L., … van Essen, D. C. (2013). Functional connectomics from resting-state fMRI.,(12), 666–682. https://doi.org/10. 1016/j.tics.2013.09.016
Spelke, E. S., & Kinzler, K. D. (2007). Core knowledge.,(1), 89–96.
Suthana, N., Haneef, Z., Stern, J., Mukamel, R., Behnke, E., Knowlton, B., & Fried, I. (2012). Memory enhancement and deep-brain stimulation of the entorhinal area.,(6), 502–510. https://doi. org/10.1056/NEJMoa1107212
Tournier, J. D., Smith, R., Raffelt, D., Tabbara, R., Dhollander, T., Pietsch, M., … Connelly, A. (2019). MRtrix3: A fast, flexible and open software framework for medical image processing and visualisation.,, 116137. https://doi.org/10.1016/j.neuroimage.2019.116137
Wai, J., Lubinski, D., & Benbow, C. P. (2009). Spatial ability for STEM domains: Aligning over 50 years of cumulative psychological knowledge solidifies its importance.,(4), 817–835.
Watrous, A. J., Deuker, L., Fell, J., & Axmacher, N. (2015). Phase-amplitude coupling supports phase coding in human ECoG.,, e07886. https://doi.org/10.7554/ eLife.07886
Weisberg, S. M., & Ekstrom, A. D. (2021). Hippocampal volume and navigational ability: The map (ping) is not to scale.,, 102–112. https://doi.org/10.1016/j.neubiorev.2021.03.012
Wolbers, T., & Hegarty, M. (2010). What determines our navigational abilities?,(3), 138–146.
Yarkoni, T., Poldrack, R. A., Nichols, T. E., van Essen, D. C., & Wager, T. D. (2011). Large-scale automated synthesis of human functional neuroimaging data.,(8), 665–670.
Zhen, Z., Kong, X. Z., Huang, L., Yang, Z., Wang, X., Hao, X., Huang, T., Song, Y., & Liu, J. (2017). Quantifying the variability of scene-selective regions: Interindividual, interhemispheric, and sex differences.,(4), 2260–2275. https://doi.org/10.1002/hbm. 23519
Zuo, X. N., Ehmke, R., Mennes, M., Imperati, D., Castellanos, F. X., Sporns, O., & Milham, M. P. (2012). Network centrality in the human functional connectome.,(8), 1862–1875.
The functional brain network that supports human spatial navigation
KONG Xiang-Zhen1,2, ZHANG Fengxiang1, PU Yi3
(1Department of Psychology and Behavioral Sciences, Zhejiang University, Hangzhou 310028, China) (2Department of Psychiatry of Sir Run Shaw Hospital, Zhejiang University School of Medicine, Hangzhou 310058, China) (3Department of Neuroscience, Max Planck Institute for Empirical Aesthetics, Frankfurt am Main, 60322, Germany)
The system for representing space is one of the core knowledge systems in the human brain. Spatial navigation is emerging as a potential cost-effective cognitive biomarker to detect Alzheimer’s disease (AD) in the preclinical stages. Previous work has revealed multiple regions across the brain associated with human navigation. However, little is known about how these regions work together as a network (referred to as navigation network) to support flexible navigation behaviors. This work presents a conceptual framework for research on how the brain network supports human spatial navigation. Integrative approaches including behavioral testing, computational modeling of brain networks, and brain stimulation were proposed to apply. The results are expected to help elucidate the neural network mechanisms of flexible navigation behaviors in human, and also provide new insights into more efficient prevention and diagnosis of AD.
spatial navigation, brain networks, brain stimulation, neuronal basis, cognitive map
2022-08-19
*國家自然科學基金(32171031)和中央高校基本科研業務費專項資金(2021XZZX006)資助。
孔祥禎, E-mail: xiangzhen.kong@zju.edu.cn
B845.1

