急性膽囊炎的膽囊引流方法及引流后擇期LC的手術時機
吳鋼,蔡端
(復旦大學附屬華山醫院 普外科,上海 200040)
膽囊結石是外科臨床的常見病和多發病,可以導致90%以上的急性膽囊炎(acute cholecystitis,AC),AC的病死率約為1%~10%[1-2]。腹腔鏡膽囊切除術(laparoscopic cholecystectomy,LC)是膽囊良性疾病尤其是有癥狀的膽囊結石和AC的標準治療手術[3]。患者在AC發作72 h內接受LC,可以明顯降低手術并發癥、死亡率、住院時間和費用[4]。膽囊結石的發病率隨年齡的增長而增加,隨著全球預期壽命的增加和人口老齡化,與高齡相關的合并癥也在增多[5]。許多AC高齡患者合并循環和呼吸系統疾病、糖尿病和腎功能不良等基礎疾病,特別是有的患者合并肝硬化、腹水、凝血障礙性疾病、晚期腫瘤等高風險疾病。AC引起的系統性感染會加重這些基礎疾病,而通過保守治療有時難以控制感染。對這一類患者進行急診手術可能導致更多的并發癥和更高的病死率[3-4,6]。《東京指南(2018)》AC治療流程推薦膽囊引流作為中重度AC高危外科患者手術的主要輔助性過渡治療,可以減輕患者的中毒癥狀,改善肝功能和全身狀況,為全身疾病和局部炎癥的緩解提供時間,從而為擇期的LC提供條件,起到重要的橋梁作用[7]。一些經內鏡的膽囊引流還可以作為合并不可逆嚴重合并癥患者的最終治療手段[8]。但是膽囊引流后擇期LC的最佳手術時機,目前還缺乏基于循證醫學的共識和指南。本文就AC的膽囊引流方法及引流后擇期LC的手術時機進行探討。
1 AC膽囊引流的適應證
對急性發作72 h內的Ⅰ級(輕度)和部分Ⅱ級(中度)AC首選早期LC治療。按照《東京指南(2018)》AC患者膽囊引流的處理策略的分級標準,AC患者不適合進行早期或緊急LC而需要膽囊引流的指征主要包括:(1)部分Ⅱ級和Ⅲ級AC,急性發作超過72 h,且通過抗生素和常規支持治療無法緩解癥狀者,尤其是肝、腎功能受損和凝血障礙等的Ⅲ級AC患者;(2)根據美國麻醉師協會的身體狀況分類(American Society of Anesthesiologists Physical Status Classification,ASA-PS)得分≥3分,即患有嚴重甚至對生命構成持續威脅的系統性疾病;(3)查爾森合并癥指數(Charlson comorbidity index,CCI)≥4分。應采用多學科綜合治療(multi-disciplinary team,MDT)模式對膽囊引流的AC患者的全身情況、合并癥、麻醉風險等進行精準的個體化綜合評估,并在膽囊引流后的保守治療期間對患者的全身情況和手術風險再進行反復評估[9-10]。
2 膽囊引流的方法
膽囊引流主要包括經皮和經內鏡兩大類途徑,(1)經皮途徑包括經皮經肝膽囊引流(percutaneous transhepatic gallbladder drainage,PTGBD)、經皮經肝膽囊穿刺(percutaneous transhepatic gallbladder aspiration,PTGBA)和經皮經腹膜膽囊引流(percutaneous transperitoneal gallbladder drainage,PPGBD);(2)經內鏡途徑主要包括內鏡超聲引導下膽囊引流(endoscopic ultrasound guided gallbladder drainage,EUSGBD)和需要經內鏡逆行膽胰管造影(endoscopic retrograde cholangiopancreatography,ERCP)實施的經內鏡經乳頭膽囊引流(endoscopic transpapillary gallbladder drainage,ETGBD)(見圖1)。引流方法的選擇取決于膽囊引流是作為擇期LC的過渡手段還是作為長期治療,并結合醫院的技術、設備條件和醫師的操作經驗等進行綜合考量[11-12]。PTGBD成熟且安全,技術門檻較低,基層醫院亦可熟練掌握,因此運用最為廣泛。而經內鏡引流對技術和設備有較高的要求,一般在一些大醫院的內鏡中心開展。
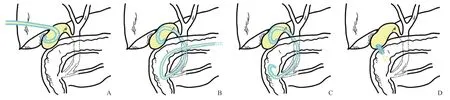
圖1 AC膽囊引流的主要方法
2.1 經皮途徑
2.1.1 PTGBD。PTGBD技術成熟且安全、應用廣泛,是膽囊引流的首選方法,可以在超聲、CT的引導下對腫大的膽囊進行穿刺、置管減壓,引流感染的膽汁,消除敗血癥的病原,緩解膽囊壁和周圍組織的炎癥,從而減輕中毒癥狀,改善肝功能和全身狀況,為擇期LC創造條件[1,6,13]。在擇期LC前和LC術中可以經PTGBD導管進行膽管造影,有助于了解膽管的解剖,降低膽管損傷的幾率[14-15]。
目前尚無關于PTGBD后拔除導管的指征和時機的共識或指南,大部分患者可以帶管至擇期LC。帶管期間有25%~66%的患者出現不良事件(adverse events,AEs),一些患者需要再次干預。對于最終不能接受LC的患者,長期放置或者拔除導管通常會導致22%~47%的患者AC再次發作,PTGBD導管引起的不適明顯影響患者的生活質量[15-16]。
2.1.2 PTGBA。PTGBA相對簡單快捷、成本較低,可以在病床旁反復進行操作,特別是當受時間、人員、設備、患者不宜搬動等客觀條件限制時,更顯其便利[17]。PTGBA的并發癥發生率低于PTGBD,但臨床成功率(clinical success rate,CSR)顯著低于PTGBD。有研究顯示再次實施PTGBA可以提高膽囊引流的有效性。由于PTGBA缺乏導管的擠壓支撐作用,出血和膽漏的風險較高[18]。
2.1.3 PPGBD。PPGBD是經皮穿刺引流的另一種可行的備選方法。與PTGBD相比,PPGBD的導管直接沿腹膜腔內走行,少量膽汁可能溢出到膽囊周圍,從而可能加劇膽囊的炎癥反應。穿刺期間和穿刺后12 h的疼痛指數和寒戰/發熱率均高于PTGBD,且引流后在導管周圍所形成的局部柱狀粘連,增加了后期LC手術分離的難度和范圍[19]。
2.2 經內鏡途徑
2.2.1 ETGBD。ETGBD包括經內鏡鼻膽囊引流(endoscopic naso-gallbladder drainage,ENGBD)和經內鏡膽囊支架(endoscopic gallbladder stent,EGBS),即經過十二指腸主乳頭放置連通膽囊和十二指腸間的鼻膽管(naso-gallbladder drainage tube,NGBT)或者雙豬尾塑料支架。ETGBD具有微創、出血風險較低、無外部引流、可以改善患者的生活質量等優勢,特別適用于存在經皮途徑有禁忌的患者[20]。在ERCP過程中,膽囊管的插管具有較大的技術挑戰性[4,9]。有研究表明膽管內超聲(intraductal ultrasonography,IDUS),SG-ETGBD(SpyGlass DS-assisted ETGBD)可以提高ETGBD的技術成功率(technical success rate,TSR)[21-22]。ETGBD的TSR和CSR分別為64%~100%和75%~95%[23-24]。與ETGBD相關的AEs主要包括胰腺炎、出血、穿孔和膽管炎等,ETGBD特有的AEs包括膽囊管或膽囊穿孔、支架移位等[25]。
放置ENGBD后可以對膽囊進行沖洗和抽吸膽汁,監測引流量,并可檢測致病微生物。但是由于鼻膽管會引起患者鼻咽部不適,并可能意外移位和脫出,因此,一般用于短期引流減壓[20]。而EGBS放置的時間可以比ENGBD和PTGBD更長,因此可以作為始終無法接受LC患者的最終治療[25]。Maekawa等[26]報道31 例老年AC患者放置EGBS,其中30 例(96.7%)無復發,至患者死亡或研究結束(1個月~5年),29例(93.5%)保持無癥狀。
2.2.2 EUSGBD。EUSGBD是指在內鏡超聲引導下,從胃體、胃竇或十二指腸球部穿刺膽囊置入支架,建立膽囊與胃腸之間的內引流。支架主要有NGBT、雙豬尾塑料支架、自膨脹金屬支架(self-expandable metal stent,SEMS)和內腔貼附金屬支架(lumenapposing metal stents,LAMS)等[27]。其中LAMS具有終端法蘭和啞鈴形中央管狀鞍座,可以降低膽漏、穿孔和支架移位的發生率,該支架內徑較大,可最大限度地減少因膽泥或結石導致的支架阻塞,而且放置支架以后可以進行后續的診斷和治療性操作,因此已成為EUSGBD的首選支架[28]。LAMS可長期發揮功能,有研究報告最長隨訪時間3年,支架通暢率為86%[29]。但是,LAMS等支架比較昂貴且不易獲取,所以目前在國內尚未開展。
雖然EUSGBD可以作為過渡性措施,但更適用于始終不能接受LC的高齡、高危患者的最終治療,特別是ETGBD失敗、胃腸Roux-en-Y術后、晚期腫瘤、已放置金屬支架治療惡性膽道梗阻并發AC患者[30]。EUSGBD的TSR和CSR分別為84.0%~100.0%和90.8%~96.7%,長期療效優于ETGBD和PTGBD。相關的AEs包括氣腹、膽汁性腹膜炎/膽汁滲漏、支架移位、十二指腸或膽囊穿孔、支架阻塞等[27-28]。
3 膽囊引流后的手術治療時機
3.1 AC發生后行PTGBD時機對擇期LC的影響
PTGBD對后期LC的手術難度和術后并發癥發生率的影響主要取決于PTGBD操作之前AC本身的嚴重程度分級和從AC癥狀發作到患者接受PTGBD的間隔時間。根據《東京指南(2018)》,AC的嚴重程度分級與術中發現和術后結果顯著相關。PTGBD和后續LC的手術難度和術后并發癥發生率也可能因AC的嚴重程度分級而異[7]。一些研究發現PTGBD后膽囊通常會縮小,膽囊壁及膽囊周圍組織纖維化增厚,膽囊與周圍組織界限不清,從而導致手術相關的技術困難和術后并發癥[13,19]。另外,PTGBD的導管對漿膜和黏膜組織有一定程度的損傷,而炎性細胞有可能浸潤和破壞膽囊壁組織,導致在膽囊和周圍組織之間形成致密的纖維束,難以強行分離,術中可能在外科視野內造成更多出血。另外,導管及少量膽汁對周圍組織的刺激也可以導致粘連,使得常規以漿膜分離為主的LC可能會變得異常困難[8,13]。Lee等[8]的研究結果提示對于I級AC在癥狀出現后3.5 d內進行PTGBD可以減小手術難度。Yamada等[31]的研究表明LC術后的病理結果主要受AC癥狀發作到實施PTGBD的間隔時間的影響:該研究根據Youden指數計算的截止值提示,當患者AC發作到接受PTGBD的間隔時間≤73.5 h時,后期LC的手術時間明顯縮短,嚴重粘連率較低,中轉開腹手術率較低。因為PTGBD可以阻止炎癥的進展,并防止炎癥擴散到周圍組織。反之,在癥狀發作73.5 h后再進行PTGBD則并不能明顯減輕手術的難度。值得注意的是,盡管圍繞PTGBD對LC影響的研究結果不盡相同,但一致公認的是,對于早期LC有禁忌的患者,尤其是Ⅱ級或Ⅲ級AC患者,一旦決定膽囊引流應盡早實施[10]。
3.2 PTGBD后LC的時機選擇
PTGBD后擇期LC的手術時機仍然是一個非常值得探討的問題,相關的研究結果差異較大。Inoue等[32]通過ROC曲線分析得出PTGBD到LC之間的最佳間隔時間為9 d。一些研究表明PTGBD術后4~6周或者更長的時間間隔以后再行LC,可能具有較低的LC中轉開腹率和術后并發癥、較少的術中出血、較短的術后住院時間等[19,33]。如果PTGBD放置時間過短,導管周圍的瘺管并未完整形成,膽囊的急性炎癥還沒有完全消退,因而手術仍然比較困難。Choi等[34]報告PTGBD后72 h內行LC的患者比72 h以后的患者預后差。但過度延長留置PTGBD導管的時間也沒有意義,還會帶來較高的導管相關并發癥和膽囊壁的嚴重纖維化,且長期帶管影響患者的生活質量[35]。因此,PTGBD作為擇期手術的過渡性手段,患者的急性炎癥明顯緩解或者消退后,即可考慮LC[16]。
Sakamoto等[14]對日本9 256例AC進行了限制性立方樣條圖(restricted cubic spline,RCS)回歸分析和多變量回歸分析,研究從PTGBD到LC的間隔時間與手術和術后結果之間的相關性。結果顯示PTGBD與LC的間隔時間與病死率/并發癥發病率和輸血率呈反向“J”型關聯,而與麻醉持續時間和術后住院時間呈“J”型關聯。PTGBD對AC患者急性炎癥的影響可能在PTGBD后的第7天左右明顯減弱,而纖維化的影響出現在PTGBD后第26天左右。因此,該研究最終得出的結論是擇期LC的最佳時間是PTGBD后7~26 d。即PTGBD后擇期LC的時間選擇在膽囊的急性炎癥基本消退之后到膽囊壁及周圍組織形成纖維瘢痕性改變之前的這個“窗口期”。這是迄今最大樣本的相關性研究所得出的結論,值得借鑒,而且很多研究者的結果與上述的結論相符。當然,我們在考慮PTGBD術后擇期LC的手術時機時,還要綜合患者的全身狀況、影像學評估、醫院的硬件和外科醫師的經驗等因素進行綜合決策[8]。PTGBD后LC的最佳時機還需要更多的臨床研究來驗證,以便更準確地指導臨床治療。
3.3 ETGBD對擇期LC的影響
Mu等[9]報告ENGBD和PTGBD兩組在TSR、CSR和安全性方面雖然沒有顯著差異,但是,ENGBD患者疼痛較輕,依從性更好,而且ENGBD由于沿著自然腔道進行操作,不損傷膽囊漿膜和黏膜,膽囊的完整性得以保留,炎癥因子的破壞盡可能局限于黏膜。因此,與PTGBD相比,擇期LC出血量和腹腔引流管放置率顯著降低,手術難度有可能降低。
一項對35例AC患者的研究結果提示EGBS組與ENGBD組的臨床結果無明顯差異[36]。另一項多中心前瞻性研究指出,ETGBD不會干擾后續的LC,其中37例中度AC患者ENGBD后成功進行了擇期LC[37]。與ETGBS相比,ENGBD導管長時間的留置,會影響患者的生活質量,增加導管相關并發癥的發生。ETGBS的導管可能會促使膽囊管內組織增生、膽囊管壁增厚和纖維化,導致Calot三角內翻,并造成手術困難。ETGBS或ENGBD引流后,在LC術中往往無法夾閉膽囊管,有研究報告約50%的患者需要縫合膽囊管殘端[12]。因此,多數研究者認為如果條件允許,應盡量縮短ENGBD患者等待LC的時間[2]。但是,ETGBD也有其有利于手術安全的一面:ETGBD的導管提高了膽囊管的可視性,當Calot三角內膽囊管與周圍組織有明顯的炎性及粘連時,ETGBD可以提高對膽囊管與膽總管的判別能力[29]。
3.4 EUSGBD的后續治療
大多數研究認為EUSGBD更適用于最終無法接受LC的患者。一些研究認為有機會接受LC的患者先行EUSGBD作為過渡性的治療,可能會導致LC更加困難和復雜,因為EUSGBD術后患者的行LC時,首先需要關閉胃或者十二指腸壁的瘺口,并防止術后上消化道瘺。對于外科醫師而言,關閉胃、特別是十二指腸壁的瘺口本身就是一個挑戰,而EUSGBD對周圍組織產生的粘連,膽囊的纖維化、萎縮也會導致手術更加困難。因此,隨著晚期惡性腫瘤、無法耐受全麻的高齡患者的增加,內鏡醫師和外科醫師應該建立共識,嚴格把握EUSGBD的適應證[27]。一項小型多中心研究報告的結果提示EUSGBD置入LAMS,其中經胃9 例、經十二指腸4 例,內引流后2~4個月患者接受LC,EUSGBD組與PTGBD組LC的AEs和中轉開腹率無顯著差異[38]。另有研究報告使用線型切割吻合器分離膽囊和十二指腸(或胃)之間的瘺管是安全的,無上消化道漏發生[39]。
綜上所述,中重度AC不適合進行緊急LC患者,膽囊引流可以減輕中毒癥狀,改善肝功能和全身狀況,為擇期的確定性手術創造條件。引流的方法可根據引流的目標個體化選擇PTGBD、ETGBD或EUSGBD等。PTCD是成熟的一線方法,隨著內鏡的不斷發展,EUSGBD和ETGBD取得了較高的技術成功率和臨床緩解率。膽囊引流后對LC的影響和手術時機是外科臨床的一個值得探討的問題。PTGBD后對LC手術難度的影響主要取決于PTGBD之前AC本身的初始嚴重程度分級。大樣本的研究認為進行LC的最佳時間為PTGBD后7~26 d。EGBS和EUSGBD可作為最終無法接受LC患者的長期治療方案。膽囊引流方法的選擇,引流術后最佳的擇期LC時機尚需更多的前瞻性臨床研究。

