COPD患者腦微出血發病率
王龍龍 張明 許淑娣 馬洪鴿 曹亞娟 成莎 李娜 王警建
(1西安交通大學第一附屬醫院醫學影像科,陜西 西安 710061;2西安市第九醫院)
慢性阻塞性肺疾病(COPD)是一種多系統疾病,與肺部對有害顆粒或氣體的異常炎癥反應有關,主要表現為持續的氣流受限,呈慢性進行性發展,其發病率和流行率呈上升趨勢〔1,2〕。 COPD 不但累及肺臟,而且可引起全身不良反應。近來COPD肺外系統病變也得到了廣泛的重視〔3〕,中樞神經系統是其中廣泛關注的一個。與其他組織器官不同,腦組織一直處于活躍狀態,雖然占人體體重不到2%,但耗氧量占到全身的25%,其血流量占心臟輸出的15%,因此,腦組織對缺氧極其敏感,不可逆的氣流受限可引起動脈血氧飽和度降低,進一步引起腦部供氧不足。COPD造成腦部長期慢性缺氧,最終會導致腦細胞損傷;此外,其全身系統性炎癥也會加劇神經損傷〔4〕。目前尚不明確COPD是否并發腦小血管疾病。對照研究表明COPD會增加腦微出血(CMBs)的風險〔5〕,但是,文獻檢索發現極少關于COPD患者腦病理活檢的相關研究。
腦小血管疾病在老年人中很常見,CMBs是一種評估腦血管病相對較新的指標,是指微量出血后,以含鐵血黃素為主要成分的血液裂解產物在腦微小血管周圍間隙沉積,在磁共振的磁敏感加權成像(SWI)序列上表現為可見的低信號小區域(直徑≤10 mm)〔6〕。CMBs很少消失,使其成為累積腦血管損傷的合適標志物〔7〕。CMBs最常見的危險因素為高血壓,CMBs的位置似乎與其潛在的疾病機制有關,深部或腦室周圍部位的微出血提示高血壓或動脈硬化性微血管病,而那些彌漫性分布于腦葉的微出血提示腦淀粉樣血管病變(CAA)〔8〕。檢測COPD患者的CMBs發病情況并研究其位置可能會大大增加對腦小血管病的病理分析。本研究調查COPD患者CMBs的發病率。
1 資料與方法
1.1研究對象 前瞻性選擇自2018年1月至2020年5月于西安市第九醫院神經內外科及呼吸科行頭顱磁共振成像(MRI)檢查患者為研究對象,根據患者臨床資料將患者分為COPD組、單純高血壓組與正常組。納入標準:(1)符合2013年《慢性阻塞性肺疾病全球倡議》的COPD診治指南患者納入COPD組,有高血壓病史且無COPD患者納入單純高血壓組,其余無COPD及高血壓患者納入正常組;(2)自愿配合本次研究,意識清楚,能正確表達自己的意愿者。排除標準:(1)有其他系統嚴重疾病,如嚴重糖尿病、嚴重肝腎功能不全、嚴重血液系統疾病、惡性腫瘤。(2)合并呼吸系統其他疾病:支氣管哮喘、重度支氣管擴張、肺結核等;(3)精神障礙性疾病,如老年性癡呆、嚴重認知障礙、智力障礙;(4)存在頭顱MRI檢查禁忌證。記錄患者年齡、性別、疾病類型、高血壓時間、血壓最高值、糖尿病、是否合并腦梗死、腦出血、第1秒末用力呼氣容積(FEV1)實測值占預計值的百分比(FEV1%)、FEV1占用力肺活量(FVC)的百分比(FEV1/FVC)、吸煙史等。本研究得到西安市第九醫院醫學倫理委員會批準。對收集患者臨床資料醫師采用盲法(不清楚MRI檢查結果)。
1.2腦MRI檢查 利用飛利浦3.0T MRI采集3D-T1WI序列、T2液體反轉恢復(T2-FLAIR)序列、SWI評估腦白質損傷、檢測CMBs。3D-T1WI序列參數為:重復時間(TR)=8.2 ms,回波時間(TE)=3.8 ms,層厚1 mm,間隔0,激勵次數(NSA)1,掃描范圍(FOV)為240×240×140 mm,掃描矩陣240×222×140,體素1×1×1,回波鏈長222;T2-FLAIR序列參數為:TR=11 000 ms,TE=120 ms,回波鏈長42,反轉時間(TI)=2 800 ms,層厚6 mm,間隔-1,NSA1,FOV為230×184×125 mm,掃描矩陣368×294×18,體素0.96×1.19×6.0;SWI參數為:TR=3.1 ms,TE=7.2 ms,層厚2 mm,間隔0,FOV為219×177×150 mm,掃描矩陣368×294×150,體素0.6×0.6×2.0,NSA 1。
1.3CMBs評價 根據SWI影像結果,相位圖與強度圖均為低信號,評估為出血灶,強度圖低信號,相位圖高信號評估為鈣化灶。依據CMBs的總數將其嚴重程度分為4級:0級:無,1級(輕度):1~4個,2級(中度):5~9個,3級(重度):10個及以上;按照CMBs解剖評分(MARS)量表的標準圖譜將CMBs的部位分為腦葉(額葉、頂葉、顳葉、枕葉、島葉)、深部(基底節、丘腦、外囊、內囊、胼胝體、深部及腦室旁白質)、幕下(腦干、小腦),統計各部位CMBs的發生率。影像結果的判讀由2名經驗豐富的影像科醫師完成,意見不一致時由主任醫師審核,對MRI圖像分析醫師采用盲法(不清楚患者臨床資料及分組)。
1.4統計學分析 采用SPSS24.0軟件及Rversion3.5.3進行H檢驗、χ2檢驗。采用Spearman相關性分析方法分析雙變量間的相關性。
2 結 果
2.1各組一般資料及CMBs影像學表現比較 3組年齡及性別差異無統計學意義(P>0.05),COPD組和單純高血壓組BCMs及3級CMBs發生率顯著高于正常組(P<0.05)。單純高血壓組CMBs及3級MBCs發生率顯著高于COPD組(P<0.05)。見表1。3組CMBs均好發于深部腦實質,CMBs分布見表2。各組典型CMBs影像見圖1。

表1 各組一般資料及CMBs影像學表現比較〔M(P25,P75〕
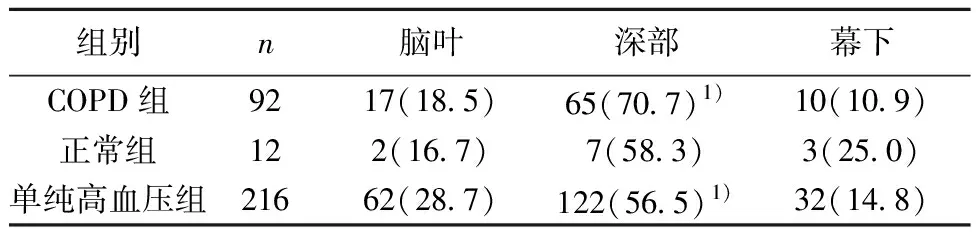
表2 CMBs腦內不同部位分布數量〔n(%)〕

男,78歲,COPD 20年,無高血壓及糖尿病,深部白質3個CMBs

女,88歲,高血壓10年,無糖尿病及COPD,深部白質及腦葉多發CMBs>10個

女,57歲,無高血壓、COPD及糖尿病,右側深部白質(腦室枕角旁)1個CMBs圖1 3組典型MRI
2.2COPD患者是否合并高血壓組CMBs比較 COPD合并高血壓組CMBs〔88.9%(8/9) vs 63.6%(7/11)〕及3級CMBs發生率〔33.3%(3/9) vs 0.0%(0/11)〕顯著高于COPD不合并高血壓組(P<0.05)。
2.3CMBs不同分級與COPD病程、FEV1、FEV1/FVC、收縮壓相關性分析 CMBs不同分級的臨床資料見表3。COPD病程與CMBs分級的Spearman相關性分析顯示,COPD病程與腦內CMBs未發現統計學相關性(r=-0.034,P=0.885);FEV1%、FEV1/FVC%與腦內CMBs未發現統計學相關性(r=-0.114、0.083,P=0.652、0.751);高血壓組中,收縮壓與CMBs數量及分級呈正相關(r=0.531、0.514,P=0.003、0.004)。高血壓病程及舒張壓與CMBs分級無統計學相關性(r=0.253、0.249,P=0.178、0.193)。

表3 CMBs不同分級的臨床資料
3 討 論
近年來,COPD的中樞神經系統相關臨床表現,情緒障礙(抑郁、焦慮)及認知障礙(記憶力、注意力及執行功能等)得到越來越多的重視,神經影像學研究逐漸發現了COPD患者神經系統腦結構和功能的變化,這些研究結果為相關的神經病例機制研究和理解提供了依據〔9〕。然而,對于影響這些癥狀較多的CMBs相關研究較少,很大原因在于以往研究中多采用梯度回波T2自由衰減加權成像(GRE T2*WI)檢測,該序列層厚較厚,部分小的CMBs不能檢出〔10〕。SWI是近年來發展起來的新技術,采用長TE的高分辨三維梯度回波序列,磁共振信號經過傅里葉轉換包含強度圖和相位圖,相位圖通過高通濾波技術去除大范圍磁場不均勻性,可以得到局部體素的磁場不均勻性信息,T2自由衰減(T2*)效應明顯放大,提高了CMBs與周圍組織的對比,更容易顯示CMBs〔11〕。
對于CMBs引起腦實質損傷的機制,不同于急性腦出血形成局部占位性血腫,以壓迫周圍腦組織為主導致的急性神經組織損害〔12〕,CMBs是血漿慢性滲入腦實質,導致持續的局限性炎性反應,進而出現以巨噬細胞浸潤和小膠質細胞增生為特征的炎癥表現,最終引起神經元功能障礙和細胞死亡〔13〕。
由于導致腦內微出血的影響因素較多,因此本研究排除影響CMBs的主要影響因素(腦出血、大面積梗死、嚴重糖尿病、淀粉樣血管變性患者),此外,高血壓作為CMBs的最常見獨立影響因素,且COPD患者多合并高血壓〔14〕,因此,本研究設立高血壓無COPD患者和無COPD及高血壓患者為對照組,探索COPD患者腦微出血的發病率與相關性。對于CMBs的數量與分級,有研究表明CMBs數量≥10個,腦出血的發病風險會顯著增加〔15〕,因此,設立3級CMBs(CMBs數量≥10個)作為相關分析變量。
本研究CMBs結果與既往的一項鹿特丹隊列研究結果一致〔5〕,提示高收縮壓可能是導致CMBs的主要危險因素之一,可能由于較高的壓力傳入末梢微血管易引發CMBs。既往研究表明年齡是CMBs的危險因素,但是隨著年齡增加,高血壓發病率也會明顯升高〔16〕。本研究3級CMBs發病率結果表明COPD患者與高血壓患者較正常人群均有更高的腦出血風險,可能是由于腦葉的CMBs多由腦血管淀粉樣變性造成,其主要累及軟腦膜和皮層的中小動脈、微動脈及靜脈,因此COPD組與高血壓組患者較正常組更容易發生腦血管淀粉樣變性。本研究中3組CMBs均好發生于深部白質,可能由于深部白質深穿支血管較多,更容易發生腦小血管病〔17〕。
本研究局限性,COPD患者肺外合并疾病復雜,疾病等因素都可能影響CMBs的發病率,雖然本研究排除了大面積梗死、腦出血、嚴重糖尿病及血液系統疾病等患者,但是對于輕癥患者、高血壓及年齡等混雜影響因素不能完全排除,希望通過嚴格的大樣本量試驗進一步研究明確;對于COPD合并CMBs相關的機制方面,傳統觀點認為主要有COPD全身炎癥反應造成神經血管組織的損傷及長期慢性缺氧造成的腦組織損傷〔18~20〕,本研究發現COPD患者合并的高血壓也是CMBs的主要危險因素之一,但是有較少相關的病理學研究,期望有更多相關的病理解剖學研究進一步證實。

