高糖上調肺泡上皮細胞大麻素受體1表達加重結核分枝桿菌感染引起的細胞損傷
馬庭喜 唐朦
(西安市胸科醫院結核合并證科,陜西 西安 710061)
肺結核是由結核分枝桿菌(M.tb)引起的一種慢性消耗性人畜共患傳染病,發病后會產生結核結節、鈣化灶或者干酪樣結節等病理性特征〔1〕。結核病早已成為全世界的公共衛生問題,嚴重影響并威脅人類身體健康〔2〕。近年來,糖尿病并發肺結核患者數量增長引發學者們探究兩者之間的關系。世界衛生組織(WHO)已經確定,糖尿病是肺結核重要且容易被忽視的危險因素〔3〕。大麻素受體(CB)1廣泛分布于人體各個系統。CB1在人體很多病理生理調節中發揮重要作用〔4〕。CB1拮抗劑能夠降低胰島素耐受,對糖尿病患者有很好的治療效果〔5〕。有研究表明,CB1拮抗劑能夠通過調節細胞內質網應激減輕高糖誘導的大鼠腎臟系膜細胞損傷〔6〕,在糖尿病腎病中發揮重要作用。但其是否參與糖尿病合并肺結核的病理進程,并沒有相關報道。本文通過構建高糖環境下M.tb感染的肺泡上皮細胞損傷模型,探討CB1對損傷模型細胞生物學的調節作用。
1 材料和方法
1.1材料 人肺泡上皮細胞株A549購自中國科學院上海細胞所。M.tb菌株H37Rv為本實驗保存。利莫那班(WIN55212-2)購自英國Tocris公司;DMEM培養基購自美國Hyclone公司;胎牛血清、雙抗、胰蛋白酶購自美國Gibco公司;Trizol試劑購自美國Invitrogen公司;反轉錄試劑盒、SYBR Premix Ex mixture購自日本TaKaRa公司;二喹啉甲酸(BCA)蛋白定量試劑盒購自上海生工生物工程有限公司;兔多克隆抗CB1抗體、鼠單克隆TLR4抗體和兔多克隆MyD88抗體購自美國Abcam公司;電化學發光(ECL)顯色劑購自北京中杉金橋生物技術有限公司;腫瘤壞死因子(TNF)-α、白細胞介素(IL)-6、IL-8酶聯免疫吸附試驗(ELISA)試劑盒,CCK-8檢測試劑盒,乳酸脫氫酶(LDH)檢測試劑盒均購自江蘇凱基生物技術股份有限公司;活性氧(ROS)檢測試劑盒購自上海前塵生物科技有限公司。
1.2方法
1.2.1細胞培養和處理 肺泡上皮細胞A549使用含有10%的胎牛血清,100 U/ml青霉素,100 μg/ml鏈霉素的DMEM完全培養液,于37℃,5%CO2的恒溫培養箱中常規培養。2~3 d更換1次新鮮培養基,融合度達到80%~90%時傳代培養。取對數生長期A549細胞,按照葡萄糖濃度分為0、5、10、25、50 mmol/L組,按分組處理細胞,置于37℃,5%CO2培養箱中培養24 h后,分別收集細胞培養上清和細胞總蛋白,檢測細胞中CB1蛋白表達;另外收集細胞,進行細胞內ROS檢測。為了構建高糖環境下M.tb感染的細胞模型,用含有25 mmol/L葡萄糖的DMEM培養基培養細胞24 h后,加入感染復數(MOI)為10的M.tb菌株H37Rv,再置于37 ℃,5%CO2培養箱中孵育12 h,收集細胞,進行后續實驗。將A549細胞隨機分為高糖(HG)組,高糖M.tb(HG+M.tb)組,CB1激動劑(WIN55212-2)處理(HG+M.tb+WIN)組和拮抗劑(利莫那班)處理(HG+M.tb+LM)組,按分組處理細胞24 h。收集細胞上清、蛋白等進行后續實驗。
1.2.2體外細胞菌落形成單位(CFU)檢測 高糖作用24 h后,加入M.tb感染12 h,然后收集細胞,檢測細菌載量變化,具體方法如下:磷酸鹽緩沖液(PBS)清洗細胞2遍,每孔加入0.1 % Triton-x-100水溶液裂解20 min。取裂解液稀釋不同濃度進行涂板,檢測CFU。3~4 d后觀察菌落生長狀況并計數。CFU計算方法:CFU/ml=C×10n×20(C:3個培養皿的菌落數均數,n為所計數的培養皿的稀釋倍數)。
1.2.3細胞內ROS檢測 按照試劑盒說明書,用無血清培養基以1∶1 000稀釋DCFH-DA,使其終濃度為10 μmol/L。以H2O2處理組的細胞為陽性對照。按照1∶1 000用無血清培養液稀釋DCFH-DA,終濃度為10 μmol/L。去除各組細胞培養液,加入適當體積稀釋好的2,7-二氯熒光素二乙酸酯(DCFH-DA),充分蓋住細胞,置于37℃,5%CO2培養箱中孵育20 min。用無血清培養液洗滌細胞3次,以充分去除未進入細胞內的DCFH-DA。于激光共聚焦顯微鏡下觀察細胞內綠色熒光情況。
1.2.4Western印跡檢測蛋白表達 收集不同葡萄糖濃度處理之后的肺泡上皮A549細胞,提取細胞蛋白,BCA法測定蛋白質濃度。每孔40 μg蛋白質總量進行電泳,轉膜、5%牛血清白蛋白(BSA)封閉1 h后,4℃下過夜孵育一抗稀釋液。一抗稀釋倍數為:CB1(1∶1 000)和β-actin(1∶10 000)。37℃條件下加入相應二抗(1∶1 000)孵育1 h,漂洗后暗室曝光,ECL顯色,Quantity One軟件分進行灰度值測定。按分組收集CB1激動劑和拮抗劑處理后的A549細胞,按照上述方法檢測TLR4和MyD88蛋白表達。
1.2.5實時熒光定量-聚合酶鏈反應(RT-PCR)檢測mRNA表達 將A549細胞按上述方法處理之后,Trizol法提取細胞總RNA,并檢測其純度以及完整性。反轉錄合成cDNA,以cDNA為模板,進行PCR擴增,2%~3%瓊脂糖凝膠上電泳,依據2-ΔΔCt法計算各組mRNA的相對表達量。引物由上海生工生物工程公司合成,序列如下: MyD88正向:5′-GTG TCT GGT CTA TTG CTA GTG-3′, 反向:5′-CCT TGC TCT GCA GGT AAT C-3′。TLR4正向:5′-CCTGGACCTGAGCTTTAATC-3′,反向:5′-CTGGATTTCACACCTGGATAA-3′。
1.2.6CCK-8檢測細胞活性 取對數生長期A549細胞,按照1×105個/孔接種于96孔板,各組設定3個平行孔,培養24 h之后,按照上述方法處理各組細胞,培養24 h之后加入10 μl CCK-8溶液,37℃下CO2恒溫培養箱中避光孵育3 h。酶標儀檢測各孔450 nm波長下的OD值,按照公式計算各孔的細胞活力:樣本孔讀數=實測數字-空白對照孔的讀數,每孔OD值平均值/對照組OD值的比值作為結果進行分析。
1.2.7LDH檢測細胞毒性 取對數生長期A549細胞,按照1×105個/孔接種于96孔板,各組設定3個平行孔,培養24 h之后,按照上述方法處理各組細胞,24 h之后將細胞培養板置于多孔板離心機中離心5 min,每孔取0.2 ml上清液進行LDH實驗,0.2 ml細胞上清液加50 μl的LDH工作液,室溫下避光反應30 min,在490 nm處檢測OD值。
1.2.8ELISA檢測炎性分子表達 收集經過處理的A549損傷細胞上清液,取出TNF-α、IL-6、IL-8 ELISA檢測試劑盒平衡至室溫,按照需要適當稀釋樣品濃度,按照試劑盒操作說明書繪制標準曲線,根據標準曲線計算TNF-α、IL-6、IL-8的最終濃度。
1.2.9流式細胞儀檢測細胞凋亡 按分組收集CB1激動劑和拮抗劑處理后的A549細胞,按照膜聯蛋白V-異硫氰酸熒光素(Annexin V-FITC)/碘化丙啶(PI)凋亡檢測試劑盒的說明步驟進行操作檢測細胞凋亡水平。胰蛋白酶加入各組細胞中進行細胞消化,經過離心,收集細胞。PBS清洗2次后重懸細胞,加入Annexin V-FITC和PI,室溫避光孵育15 min之后流式細胞儀檢測細胞凋亡水平。
1.2.10試劑盒檢測含半胱氨酸的天冬氨酸蛋白水解酶(Caspases)水平 按分組收集CB1激動劑和拮抗劑處理后的A549細胞,用不含乙二胺四乙酸(EDTA)的胰酶消化并收集細胞,PBS洗滌細胞2次,1 000 r/min離心5 min,去除上清,加入裂解緩沖液(北京索萊寶科技有限公司)吹打均勻,在冰上裂解10 min。4℃下,10 000 r/min離心5 min收集上清液(胞質提取液)并分裝轉移至1.5 ml離心管中,BCA蛋白定量法檢測蛋白濃度;加入含有二硫蘇糖醇(DTT)的反應緩沖液,加入pNA標記的蛋白酶底物,于37℃下避光孵育3 h。酶標儀405 nm處檢測吸光度值(A405),Caspase3/9活化水平以實驗組A405值與對照組A405值的比值來表示。
1.3統計學方法 采用SPSS17.0軟件進行單因素方差分析、SNK-q檢驗。
2 結 果
2.1高糖環境下肺泡上皮細胞中CB1表達 低濃度葡萄糖處理組細胞內ROS水平較低。隨著葡萄糖濃度的升高,綠色熒光陽性細胞數及細胞內熒光強度均增加,說明高濃度葡萄糖處理對A549細胞的損傷加重(圖1)。隨著葡萄糖濃度的升高,細胞中CB1蛋白表達逐漸上升,0、5、10、25、50 nmol/L組CB1蛋白灰度值分別為(1.00±0.09、1.17±0.08、1.49±0.04、2.09±0.12、2.57±0.07)在葡萄糖濃度達到10 nmol/L起,細胞中CB1表達即與正常環境中的表達存在顯著性差異(P<0.05)。見圖2。提示CB1可能參與高糖環境對肺泡上皮細胞A549的損傷。

圖1 不同濃度葡萄糖處理的肺泡上皮細胞系A549中ROS水平(×100)
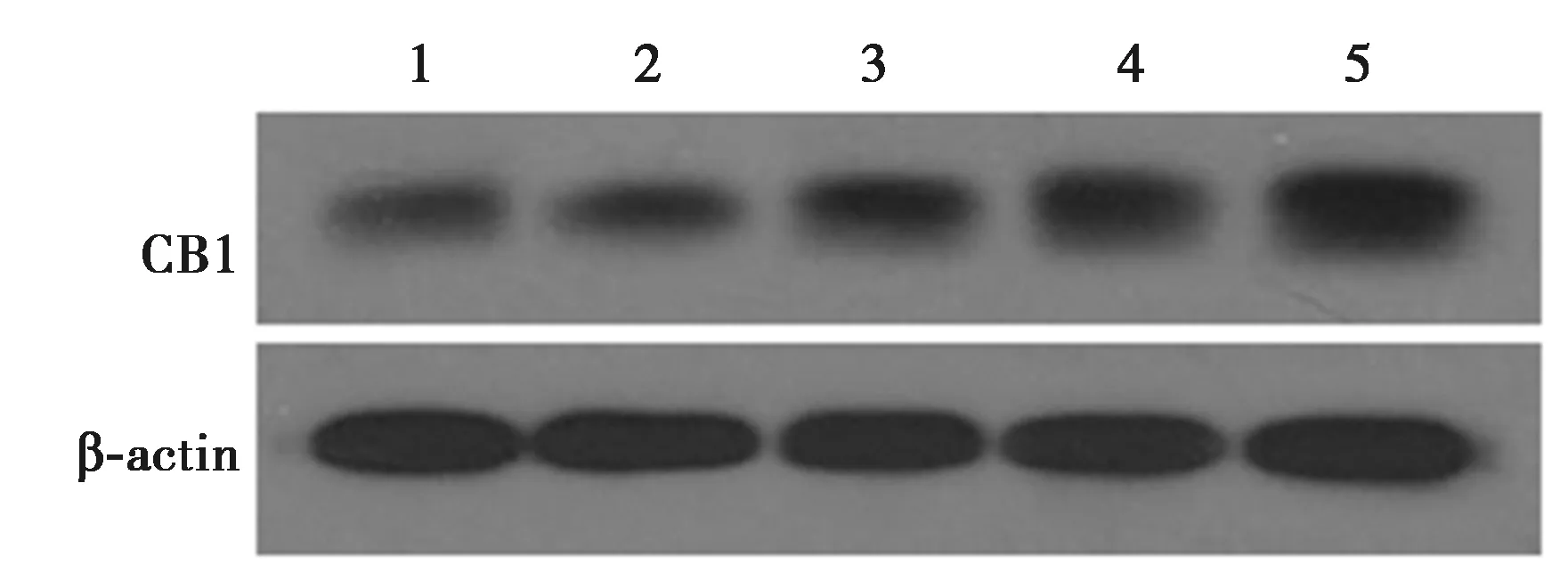
1~5:0 nmol/L組,5 nmol/L組,10 nmol/L組,25 nmol/L組,50 nmol/L組圖2 Western印跡檢測各組細胞中CB1蛋白表達
2.2高糖環境下M.tb感染對肺泡上皮細胞的損傷 將A549細胞在25 nmol/L葡萄糖濃度下培養,隨后用M.tb感染構建高糖環境下的細胞結核分枝桿菌感染模型。感染12 h后,與M.tb組相比,HG+M.tb組細菌存活率明顯降低(P<0.05)。CCK-8結果顯示,與NC組相比,HG組和M.tb組細胞活性均顯著降低(P<0.05);而HG+M.tb細胞活性較HG組、M.tb組顯著降低(P<0.05)。與NC組相比,HG組、M.tb組、HG+M.tb組LDH釋放顯著增加,且HG+M.tb組LDH釋放顯著高于HG組及M.tb組(P<0.05)。ELISA檢測結果顯示,與NC相比,HG組及M.tb組細胞分泌炎性因子TNF-α、IL-6和IL-8水平均顯著升高(P<0.05);與HG組及M.tb組相比,HG+M.tb組細胞炎性因子水平也顯著升高(P<0.05)。提示高糖合并M.tb感染處理細胞顯著降低了A549細胞活性及細菌存活率,并提高了細胞炎性因子的分泌水平。見圖3、表1。
圖3 高糖環境下M.tb感染后A549細胞形態觀察(×100)

表1 高糖環境下M.tb感染后A549細胞活性及分泌的炎性因子水平比較
2.3高糖環境下CB1對M.tb感染的肺泡上皮細胞活性和凋亡的影響 構建高糖環境下M.tb感染肺泡上皮細胞損傷的模型之后,用CB1激動劑(WIN)或拮抗劑(LM)處理細胞,CCK-8結果顯示,CB1激動劑處理之后,損傷細胞活性顯著降低,LDH釋放量顯著升高,細胞凋亡率顯著升高,線粒體凋亡因子Caspase-3/9水平顯著升高(P<0.05);而CB1拮抗劑處理之后,損傷細胞的細胞活性明顯升高,LDH釋放明顯降低,細胞凋亡率顯著升高,細胞凋亡率則顯著降低,Caspase-3/9水平顯著降低(P<0.05)。見圖4、表2。提示高糖環境下造成肺泡上皮細胞的損傷,合并M.tb感染后,細胞損傷加重,細胞活力降低更為明顯,細胞凋亡率更高。CB1激動劑(WIN)對高糖環境合并M.tb感染造成的細胞損傷有促進作用;而CB1拮抗劑(LM)處理能緩解高糖環境合并M.tb感染對細胞的損傷。
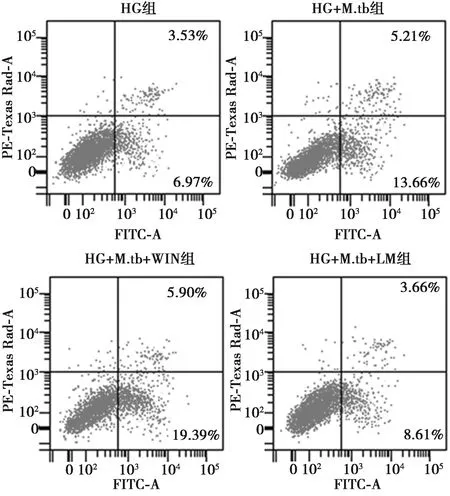
圖4 CB1對高糖環境下M.tb感染之后A549細胞凋亡水平的影響

表2 CB1對高糖環境下M.tb感染之后A549細胞活性及凋亡水平的影響
2.4高糖環境下CB1對M.tb感染的肺泡上皮細胞中TLR通路及炎性分子的調節 CB1激動劑處理損傷細胞模型后,細胞中炎癥反應通路TLR相關分子TLR4、髓樣分化因子(MyD88)蛋白及mRNA表達顯著上升,炎性因子TNF-α、IL-6和IL-8水平顯著上升(P<0.05);而CB1拮抗劑處理后,細胞中TLR4和MyD88蛋白及mRNA表達明顯降低,炎性因子TNF-α、IL-6和IL-8水平,明顯降低(均P<0.05)。見圖4、表3。提示CB1能夠促進高糖環境合并M.tb感染下肺泡上皮細胞TLR炎癥通路的反應及細胞炎性因子TNF-α、IL-6和IL-8水平。

1~4:HG組、HG+M.tb組、HG+M.tb+WIN組、HG+M.tb+LM組圖4 CB1對高糖環境下M.tb感染之后A549細胞中TLR4通路的影響

表3 CB1對高糖環境下M.tb感染之后A549細胞TLR4通路及炎性因子水平的影響
3 討 論
糖尿病合并肺結核患者主要由于營養代謝障礙、機體免疫力低下,容易被各種病原體感染。據報道,糖尿病患者肺結核的概率是正常人群的2~4倍,且兩者之間相互影響。肺泡Ⅱ型上皮是細胞M.tb由呼吸道吸入之后最先侵染的肺部細胞。研究表明,作為肺臟細胞重要組成的肺泡Ⅱ型上皮細胞是M.tb感染的主要靶細胞,也是機體抗M.tb感染的第一道防線〔7〕。
CB包括CB1和CB2,主要分布于腦部、脊髓及外周神經系統中。其中CB1主要存在于中樞神經系統,CB2主要分布于外周組織〔8〕。研究表明,CB1在2型糖尿病小鼠體內誘導浸潤胰島的巨噬細胞的炎癥反應,表明CB1信號通路發揮促進糖尿病進展的作用〔9〕。另外,足細胞中CB1受體過表達加重了糖尿病腎病的病理進程〔10〕。本研究提示CB1可能參與高糖處理對A549細胞的損傷作用。本研究成功建立了研究糖尿病合并肺結核的體外細胞模型。但與文獻報道不同,本研究發現,高糖A549細胞24 h后,M.tb感染合并處理12 h,A549細胞活性即出現明顯下降。而Fine-Coulson等〔7〕報道顯示M.tb單獨感染48 h后,細胞的線粒體組成及分布出現顯著變化。處理時間的差異可能是由于高糖預處理使A549細胞對M.tb感染更敏感。研究表明,CB1拮抗劑能改善脂質代謝從而減輕肥胖〔11〕,而其在胰島細胞中的缺乏能夠保護高糖誘導的胰島功能障礙和炎性損傷〔12〕。提示CB1在糖尿病及糖尿病并發癥的過程中發揮積極的作用。將CB1激動劑或拮抗劑作用于高糖環境下結核分枝桿菌感染的A549細胞,結果表明CB1拮抗劑減輕了高糖環境下M.tb感染造成的細胞活性和凋亡的損傷。
TLRs是生物機體內一類中藥的先天性模式識別受體,廣泛分布于心肌細胞、脂肪細胞、血管內皮細胞、樹突細胞、免疫T細胞等表面。TLRs介導的信號通路中,研究最多的是由TLR2和TLR4介導的通路,可分為MyD88依賴性和MyD88非依賴性的轉導途徑〔13〕。有研究發現,小鼠體內敲除TLR2之后,在感染M.tb后體內固有免疫應答和適應性免疫應答反應受損。而TLR4突變的小鼠與野生型的小鼠比較,前者更易感染M.tb,并出現炎癥增強、粒細胞增多等特征〔14〕,說明TLR4在M.tb感染細胞過程中起防御作用。研究表明,對M.tb感染誘導的TLR4/Myd88通路的調控,是肺結核的臨床治療的新方向〔15,16〕。本研究結果顯示,高糖環境下M.tb感染A549細胞之后,細胞中TLR4和MyD88表達及炎性因子水平顯著上升,而CB1拮抗劑作用之后降低了其表達水平。TLRs作為微生物產生的信號轉導器,在免疫系統中產生局部變化,參與調節細胞及組織敏感性。本研究發現CB1拮抗劑能減輕了細胞模型中的TLR4炎癥通路反應,而CB1激動劑則抑制TLR4炎癥通路反應。CB1可能通過調節TLR通路,進一步影響A549細胞對M.tb的敏感性。但對于CB1如何影響TLR4信號通路,目前缺乏相關報道,有待進一步研究。
綜上,高糖可以促進肺泡上皮細胞表面CB1表達上調,從而增加了對M.tb感染后細胞損傷的易感性,其中與肺泡上皮細胞內TLR4介導的炎癥反應通路活化相關,而使用CB1抑制劑則可以明顯改善肺泡上皮細胞損傷則進一步證明了CB1信號通路活化可能是造成M.tb感染后細胞損傷的機制之一。

