重難點創新題組專練
題組一:有機物結構與性質(融合考查)
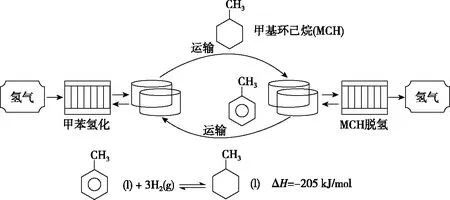
1.國內外關于氫氣的儲運方式有多種:如高壓氣態儲氫、低溫液態儲氫、碳質材料儲氫、金屬合金儲氫以及有機化學氫化法等。下列有關有機化學氫化法的說法不正確的是
( )
A.氫化的過程既屬于加成反應又屬于還原反應
B.氫化反應前后的兩種有機物的一氯代物均為5種
C.減壓和升溫都有利于MCH脫氫
D.工業上常使用脫氫催化劑加快脫氫速率,若在高溫條件下容易使脫氫催化劑失活
【參考答案】B
2.有機物在生產生活中有很重要的應用,有關這些有機物的描述不正確的是
河南省滎陽市高級中學 靳思增 這些有機物的描述不正確的是( )
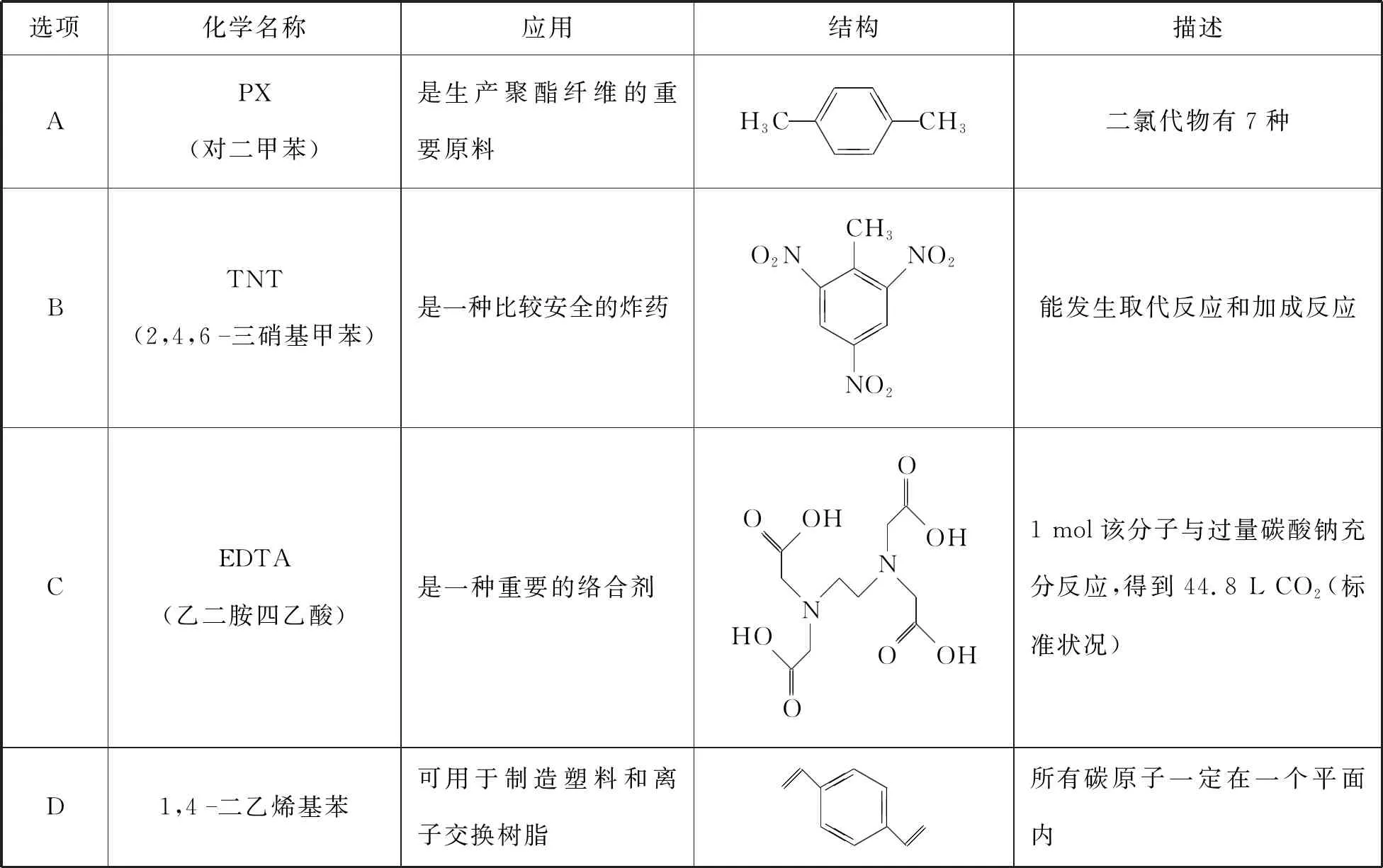
選項化學名稱應用結構描述APX(對二甲苯)是生產聚酯纖維的重要原料H3CCH3二氯代物有7種BTNT(2,4,6三硝基甲苯)是一種比較安全的炸藥NO2O2NCH3NO2能發生取代反應和加成反應CEDTA(乙二胺四乙酸)是一種重要的絡合劑OOHNOHONOOHOOH1 mol該分子與過量碳酸鈉充分反應,得到44.8 L CO2(標準狀況)D1,4二乙烯基苯可用于制造塑料和離子交換樹脂所有碳原子一定在一個平面內
【參考答案】D
河南省滎陽市高級中學 靳思增
3.由W、X、Y、Z原子序數依次增大的四種短周期主族元素組成的一種消毒劑的結構如圖所示。已知:
①X、Y為同周期元素,且核外均有2個未成對電子。
②W、X、Z不在同一周期。
③基態Z原子核外K、L能層上的電子總數是3p能級的兩倍。
下列說法不正確的是
( )
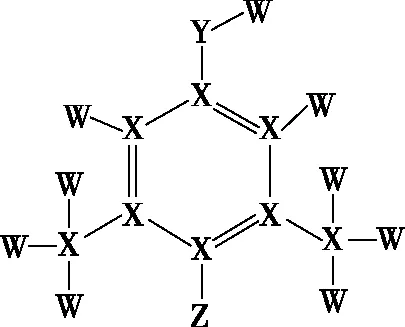
A.該化合物含有2種官能團
B.由W、X、Y組成的離子均能促進水的電離
C.分子中X原子的軌道雜化方式為sp2、sp3的個數之比為3∶1
D.分子中所有的原子不可能共平面
【參考答案】B
湖南省郴州市湘南中學 戴儒儉
題組二:化學實驗
4.室溫下,通過下列實驗探究H2O2溶液的性質。
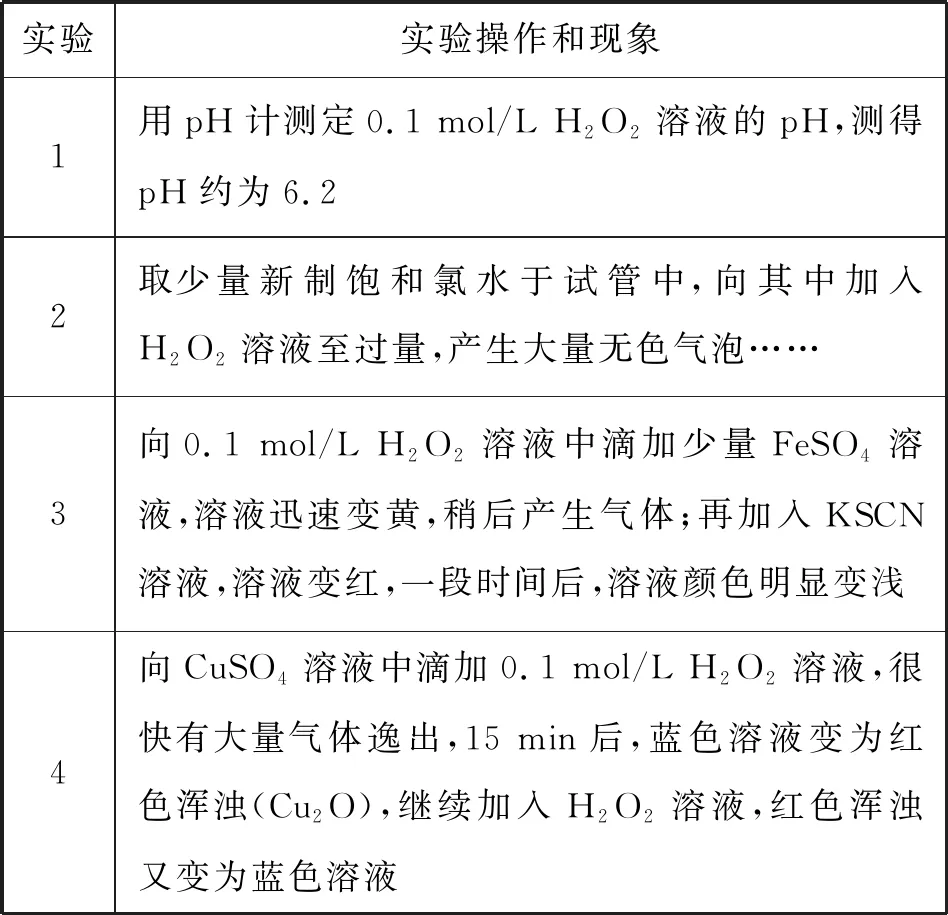
實驗實驗操作和現象1用pH計測定0.1 mol/L H2O2溶液的pH,測得pH約為6.22取少量新制飽和氯水于試管中,向其中加入H2O2溶液至過量,產生大量無色氣泡……3向0.1 mol/L H2O2溶液中滴加少量FeSO4溶液,溶液迅速變黃,稍后產生氣體;再加入KSCN溶液,溶液變紅,一段時間后,溶液顏色明顯變淺4向CuSO4溶液中滴加0.1 mol/L H2O2溶液,很快有大量氣體逸出,15 min后,藍色溶液變為紅色渾濁(Cu2O),繼續加入H2O2溶液,紅色渾濁又變為藍色溶液
下列有關說法錯誤的是
( )
A.由實驗1可知,室溫下,H2O2的第一步電離常數大于10-14
B.實驗2中還可觀察到溶液的顏色逐漸變淺,最后消失
C.實驗3中一段時間后,溶液顏色明顯變淺,可能是因為過量的H2O2有氧化、漂白作用
D.實驗3、4表明FeSO4溶液、CuSO4溶液對H2O2溶液的分解均有一定的催化作用
【參考答案】D
湖南省郴州市湘南中學 戴儒儉
題組三:化學反應原理—圖像分析
5.向500 mL 2 mol·L-1的NaOH溶液中通入一定體積的CO2使其充分反應,再向所得溶液中逐滴滴加1 mol·L-1的稀鹽酸。測得產生CO2的物質的量隨加入鹽酸的體積變化如圖所示。則下列說法錯誤的是
( )
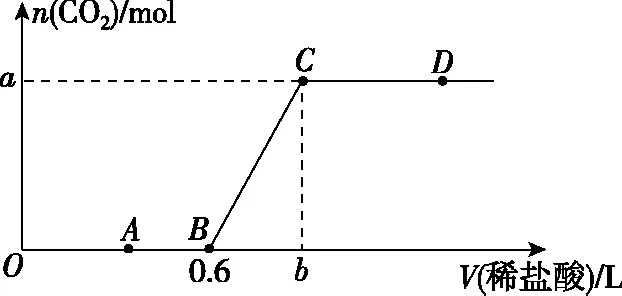
A.稀鹽酸滴加在0→0.6 L過程中,發生了兩個離子反應
B.所有過程中,Na+沒有參與化學反應,故c(Na+)一直保持不變
C.圖中的a=0.4,b=1.0
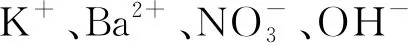
【參考答案】B
湖北省恩施市第三高級中學 陳洪義
6.HA和HB是兩種一元弱酸,在難溶鹽RA和RB的飽和溶液中,溶度積Ksp(RA)>Ksp(RB),R+不發生水解,實驗測得25℃時c2(R+)隨c(H+)的變化為線性關系,如圖中實線甲和實線乙所示。

下列說法中不正確的是
( )
A.實線甲表示難溶鹽RB中c2(R+)隨c(H+)的變化
B.溶液pH=4時,RA和RB的飽和溶液中c(R+)相等
C.電離常數Ka(HA)∶Ka(HB)=12∶5
D.溶液pH=7時,RA和RB的飽和溶液中c(A-)=c(B-)
【參考答案】D
黑龍江省綏化市慶安縣第一中學 孫秀民
題組四:化學反應原理—反應機理分析
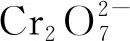

關于以下說法不正確的是
( )
A.該技術可以直接將光能轉化為化學能,而MIL-68(Fe)作光催化劑
B.光生空穴具有強氧化性,能將有機物(MG)氧化成無毒的CO2和H2O
C.在該過程中,每生成0.1 mol的Cr3+,理論上需要提供0.6 mol電子
D.MIL-68(Fe)處理污水中的有毒物質,是一種溫和、綠色的方法
【參考答案】C
江西省上饒市橫峰中學 景芬芬
8.以釕催化劑RuHCl(CO)(PPh3)2可以實現馬來酸二烷基酯順式和反式之間的轉化,如圖所示:
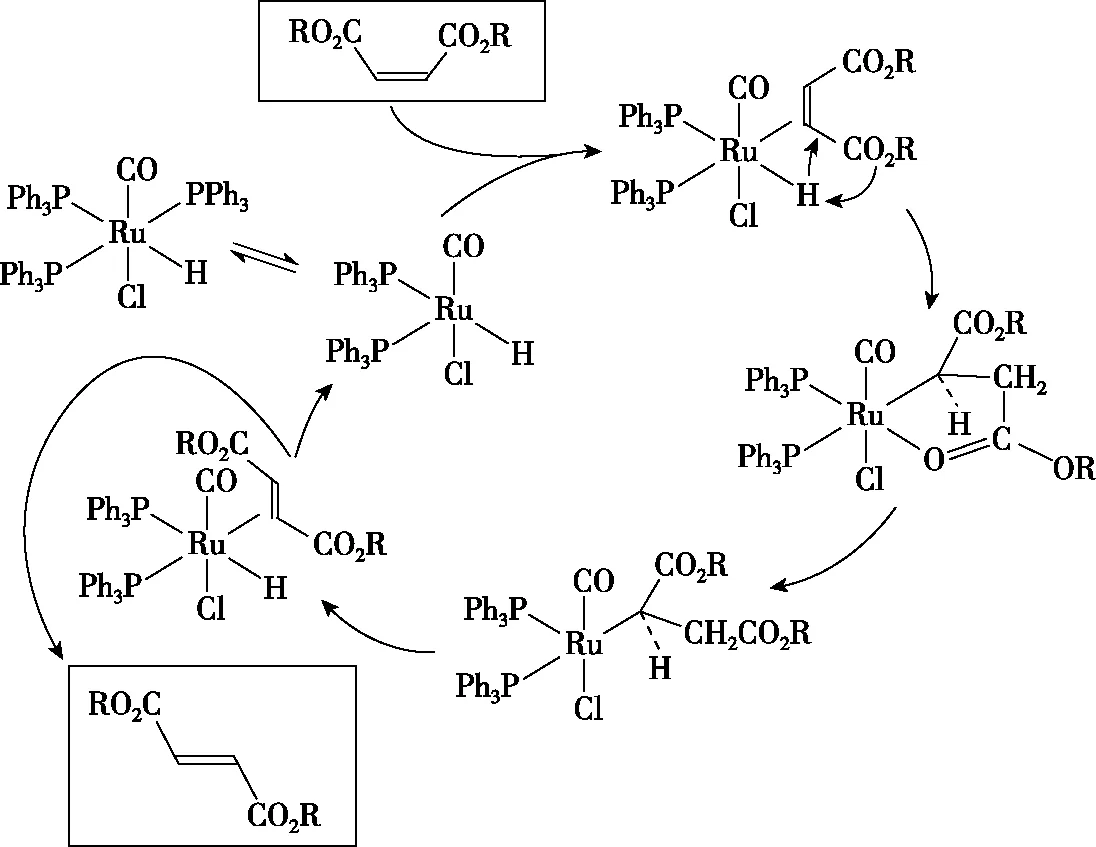
以下說法正確的是
( )
B.該過程僅有C—H和Ru—H鍵斷裂與形成
C.該過程Ru的成鍵數目發生了變化
D.與馬來酸二乙酯互為同分異構體的六元環二羧酸有3種
【參考答案】C
江西省上饒市橫峰中學 錢達康
題組五:工藝流程分析
9.錸(Re)是一種極其稀少的貴金屬,在航空航天、石油催化等領域有十分重要的作用。目前,從鉬(Mo)精礦(含極少量錸的化合物)中采用火法焙燒提錸是最常見的方法之一。

已知:含錸煙塵主要成分為:SiO2、Re2O7、MoO3、CuO、Fe3O4,其中Re2O7、MoO3易與氨水反應生成對應的鹽。
(1)金屬錸是第六周期75號元素,與Mn元素位于同一副族,其價電子排布式為________。
(2)“浸出”后的濾渣為____________,若改用NaOH溶液浸出,則濾渣少一成分,原因是
(用離子方程式表示)。
(3)氧化焙燒過程中,Re2S7焙燒生成Re2O7和一種污染性的氣體,其氧化劑與還原劑的比例為________;若用(熟)石灰焙燒法,產物以鈣鹽[CaMoO4、Ca(ReO4)2、CaSO4]的形式生成,試寫出Re2S7在此過程中發生的化學方程式:
________________________。對比氧化焙燒,其優點是
。
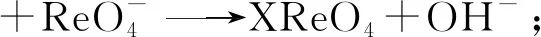
(5)工業上可用電化學還原沉積的方法從高錸酸銨中提取金屬錸。試補充完整電沉積過程中第二步b的電化學方程式。
b.____________________________,φ0=0.4 V


pH電解時間/s電解沉積產物(錸)質量/g電解效率/%65 0000035 0006.81.0315 00096.65.62
根據上述信息,請你寫出對工廠的建議,以及分析一段時間后電解效率下降的原因:
。
【參考答案】
(1)5d56s2


適當提高酸的濃度,可以提高錸的電解產量 金屬錸的電解需要消耗H+,一段時間后H+濃度下降,故電解效率下降
廣東省佛山市順德區樂從中學 胡凱威
題組六:有機推斷與合成
10.熒光探針可運用于Zn2+的定性檢測和定量分析,如圖是合成席夫堿結構的新型Zn2+熒光探針P1(化合物I)的流程圖:
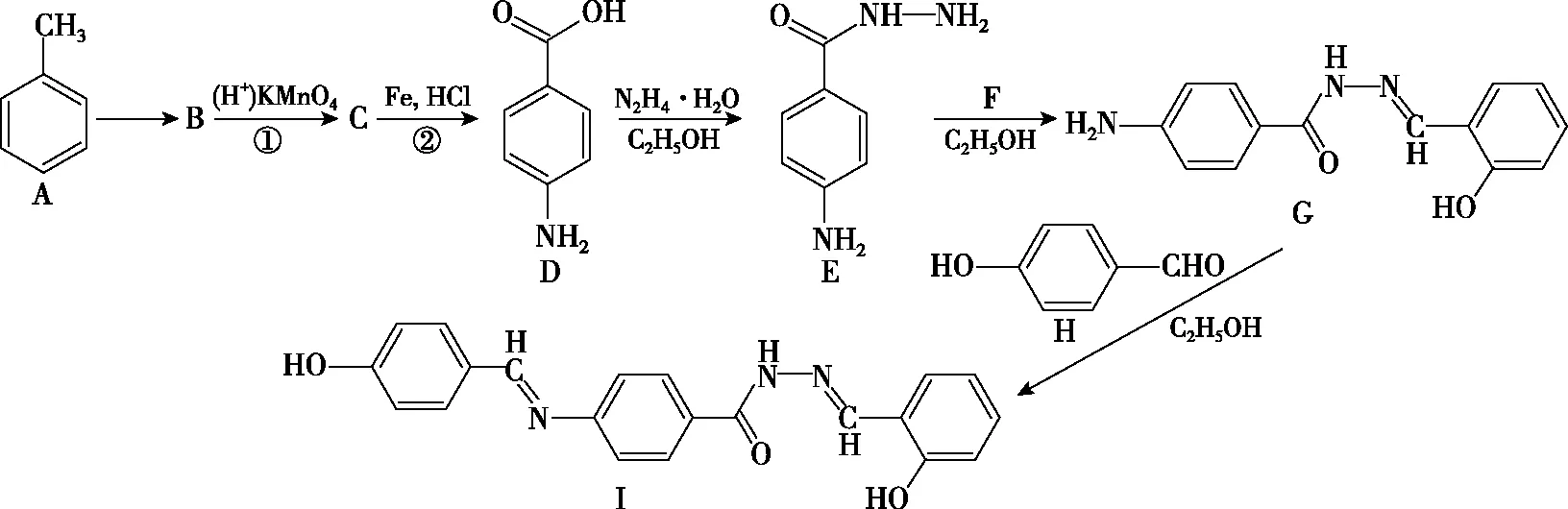

(1)D的化學名稱為________。
(2)反應①和反應②的順序能否調換,請說明其原因
。
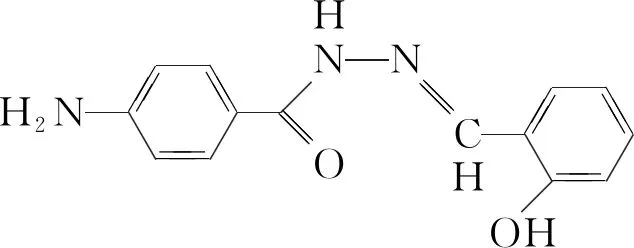
(3)F的結構簡式為________,其所含官能團的名稱為________。
(4)由G生成I的化學方程式為
____________________。
(5)化合物J是H的同系物,J的相對分子質量比H的大28,則滿足下列條件的J的同分異構體有________種,其中,核磁共振氫譜有四組峰,且峰面積之比為6∶2∶1∶1的結構簡式為________(寫出其中一種即可)。
①能夠發生銀鏡反應 ②能夠發生水解反應
線
(無機試劑任選)。
【參考答案】
(1)對氨基苯甲酸
(2)不能,若調換則生成的氨基又會被酸性高錳酸鉀氧化


廣東省佛山市順德區樂從中學 胡凱威
11.中藥葛根的有效成分為葛根大豆甙元(F),可以有效緩解高血壓引起的頭疼、頭暈、突發耳聾等癥。以下是以有機物A為起始原料合成F的一種方法:
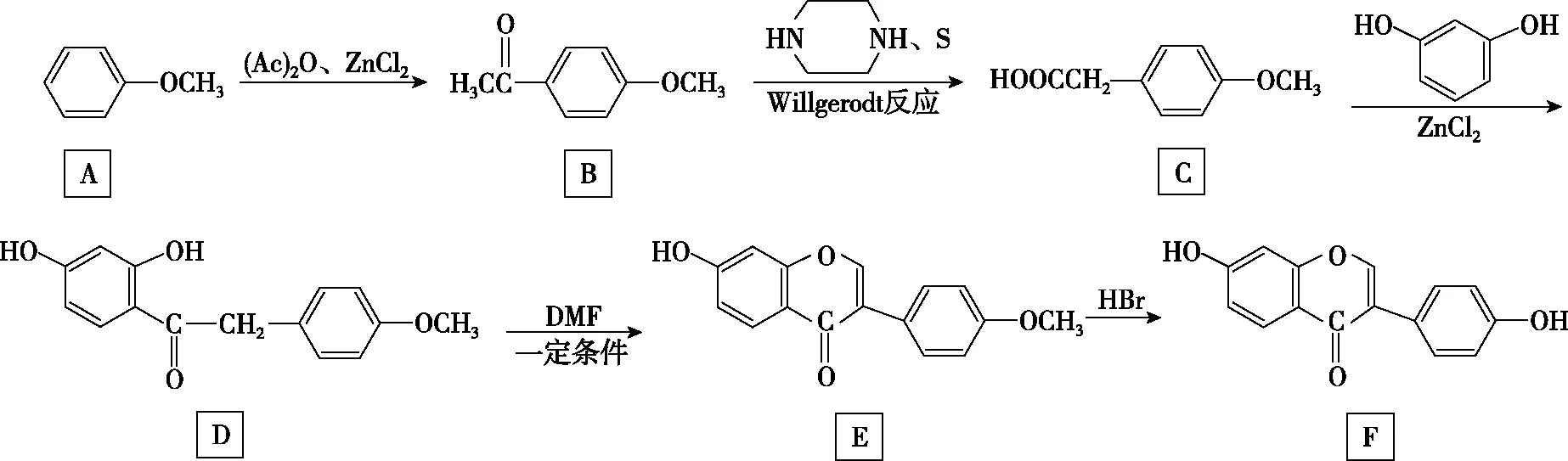
(1)A的化學名稱為________,C的分子式為________。
(3)1 mol D最多可與________mol H2發生加成反應。
(4)F與Na2CO3溶液反應的化學方程式為
。
(5)B有多種同分異構體,同時滿足下列條件的共有________種。其中,能發生銀鏡反應的結構簡式為________(寫出一種即可)。
①屬于芳香族化合物 ②能夠發生水解反應
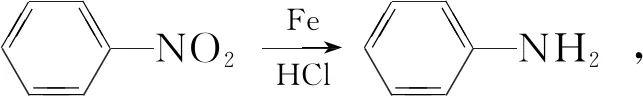
(無機試劑任選)。
【答案】(1)苯甲醚 C9H10O3
(2)醚鍵、羰基 取代反應
(3)7

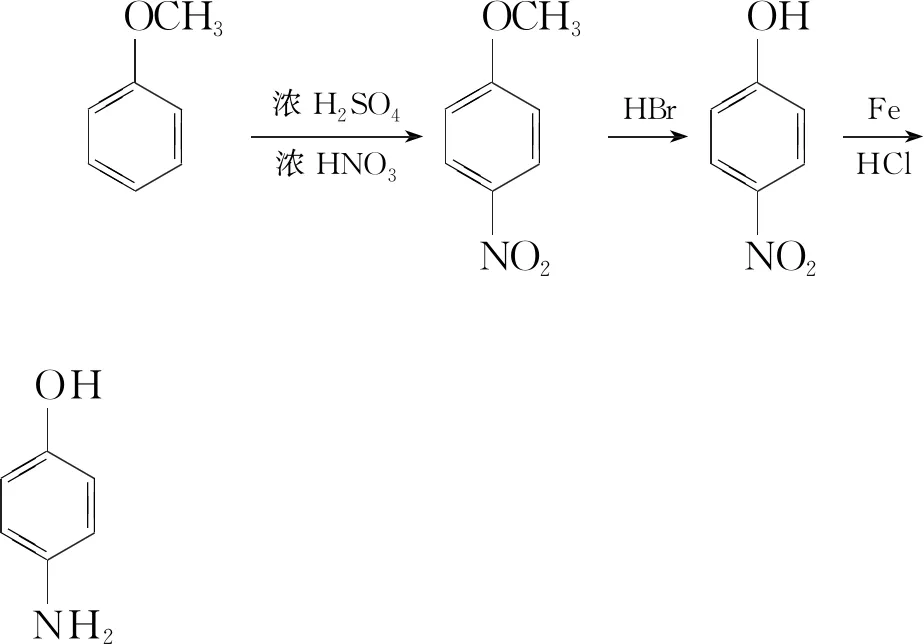
西安交通大學附屬中學 卓穎 張瑞超

