莫匹羅星劑型改造研究進展
李子烜 黃吉 孫震曉

摘要:莫匹羅星(Mupirocin,MPC)是一種廣泛使用的外用抗生素,其抑制細菌異亮氨酰-tRNA的形成使其抑菌效果獨特,但常規使用的MPC軟膏有一定毒副作用,如其對創傷部位正常成纖維細胞的毒性作用及軟膏基質的毒副作用等。同時,隨著細菌對MPC的耐藥性逐漸提高,MPC的抑菌效果也受到影響。近年來針對MPC的特點,已經發展出多種更加方便患者使用的新劑型。更重要的是,新劑型可以減少MPC的毒副作用、控制藥物釋放速度、延長血清半衰期等,在增進療效的同時,一定程度上減少了耐藥菌的篩選。本文主要綜述莫匹羅星噴霧劑、貼劑、水凝膠和納米等新制劑的研究進展。
關鍵詞:莫匹羅星;劑型改造;貼劑;水凝膠;納米制劑;進展
中圖分類號:R978.1? ? ? ? ?文獻標志碼:A? ? ? ? ?文章編號:1001-8751(2023)01-0013-06
Progress on Formulation Modification of Mupirocin
Li Zi-xuan,? ?Huang Ji,? ?Sun Zhen-xiao
(School of Life Sciences, Beijing University of Chinese Medicine,? ? Beijing 102488)
Abstract: Mupirocin (MPC) is a widely used topical antibiotic, its mechanism of inhibiting the formation of bacterial isoleucyl-tRNA makes its antibacterial effect unique and safe to use. The conventionally used MPC ointment has certain toxic and side effects, such as its toxic effect on normal fibroblasts at the wound site and the toxic and side effects of the ointment matrix. In addition, as the tolerance of bacteria to MPC gradually increased, the bacteriostatic effect of MPC was also affected. In recent years, according to the characteristics of MPC, a variety of new formulation that are more convenient for patients have been developed. More importantly, the new formulation can reduce the toxic and side effects of MPC, control the drug release rate, prolong the serum half-life, etc., while improving the curative effect and reducing the screening of drug-resistant bacteria to a certain extent. This paper mainly reviews the research progress of mupirocin sprays, patches, hydrogels and nano-formulations.
Key words: mupirocin; formulation modification; patch; hydrogels; nano formulation; progress
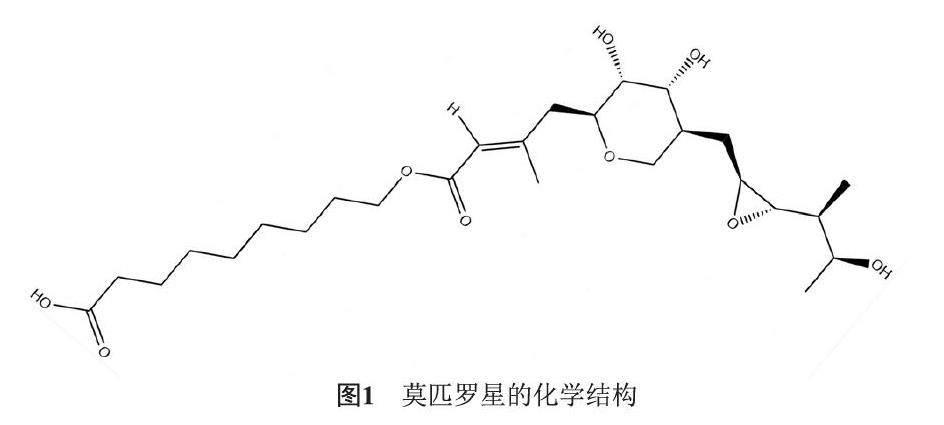
莫匹羅星(Mupirocin,MPC),即假單胞菌酸 A,是一種外用抗生素,對葡萄球菌和大多數鏈球菌具有較強的體外抑菌活性,對其他革蘭陽性菌和大多數革蘭陰性菌的活性較低[1]。MPC具有獨特的化學結構,由一個短脂肪酸側鏈與一個單胞菌酸連接而成[2](圖1)。MPC可以選擇性結合細菌異亮氨酰tRNA 合成酶,阻止異亮氨酰-tRNA 的形成,進而阻止異亮氨酸摻入新生多肽鏈[3]。這種特殊的結構與其獨有的作用機制,使得MPC與其他抗生素之間產生交叉耐藥性可能性很低[4]。當MPC被人體吸收后,可以由腎臟迅速代謝,并從尿液或糞便等途徑排出,其血清半衰期僅有30 min,這意味著它只能局部外用[5]。
金黃色葡萄球菌(Staphylococcus aureus)在全球廣泛分布,感染了數以億計的人畜,是人類感染的最常見病原菌之一,同時也是世界公認的公共衛生問題。金黃色葡萄球菌感染可導致皮膚炎癥、膿瘡等,甚至可以影響血液、軟組織以及下呼吸道,并可能造成一些嚴重的感染,如心內膜炎、骨髓炎等[6-7]。自60年代發現耐甲氧西林金黃色葡萄球菌(MRSA)后[8],MRSA對抗生素的耐藥性已經顯著增強[9],這也是臨床上治療MRSA感染所面臨的主要問題。目前用于抗MRSA的抗生素多為已上市藥物的新衍生物,細菌一旦對一種抗生素耐藥,將會對該抗生素的其他衍生物也產生耐藥 [10]。MPC具有良好的抗MRSA能力,又不易與其他抗生素產生交叉耐藥,廉價易得、使用方便,因而被廣泛用于治療MRSA引起的皮膚感染。
目前MPC在臨床應用中仍以軟膏為主,其表現出了較好的治療效果,具有藥效好、使用方便等優點。但MPC軟膏也有一些局限性:MPC軟膏主要用于治療皮膚感染、毛囊炎、膿包、創傷感染等,這些疾病大都伴隨有皮膚創傷,研究發現,MPC濃度高于700 μg/mL時會抑制成纖維細胞的生長,而MPC軟膏的臨床使用濃度一般在2%(20 000 μg/mL),遠高于700 μg /mL,這顯然不利于傷口愈合[11];MPC軟膏基質聚乙二醇可能通過破損的皮膚而被人體吸收,從而導致腎毒性[12-13]。另外,因極易獲取和使用方便,造成了濫用MPC現象,導致MRSA耐藥性持續增強,2022年的一項研究首次報道了同時耐甲氧西林和莫匹羅星的金黃色葡萄球菌的存在[14]。但MPC在臨床上仍然是廣泛使用的抑菌藥物,通過劑型改造可以增進療效或減低毒副作用,目前MPC的一些改造劑型,如噴霧劑、貼劑、水凝膠和納米等新制劑的研究均取得一定進展。
1 MPC噴霧劑
理想的創口敷料應該具有良好的生物相容性,可以最大程度降低患者疼痛和不適,而患者在使用MPC軟膏時,由于使用不當,可能對傷口再次造成傷害,引起患者不適并延長恢復時間。噴霧劑的使用,可以減少因物理接觸造成的疼痛感,能更好地保持藥物清潔和無菌狀態,保證了患者使用感受。在一項涉及52名I期壓力性損傷患者的研究中,將患者均分為各26名的兩組,使用以苯扎溴銨作為陽離子表面活性劑的MPC創面消毒噴霧劑治療,用藥組病情好轉或痊愈人數達25名,對照組僅15人。實驗結果表明,MPC噴霧劑在保持良好抑菌效果的同時,還能有效促進創面恢復,緩解患者痛苦[15]。在另一項Bakkiyaraj等[16]的研究中發現,MPC軟膏和噴霧劑表現出幾乎相同的對細菌和生物膜的抑制作用,但在清潔后的穩定性測驗中,發現約85%的MPC軟膏僅在一次沖洗(每次使用自來水沖洗15 s)后便被去除,在第二次洗滌后可被完全去除;而噴霧劑即使在沖洗三次后,仍然可以保持有效的抑菌作用。此外,該研究還發現,使用不同濃度MPC噴霧劑處理人成纖維細胞24 h后,在所有測試濃度中,細胞存活率均大于80%,達到了接近于無毒的效果。同樣,在一項同年的研究中,Sritharadol等[17]使用Eudragit E100作為成膜劑開發MPC噴霧劑,不僅具有良好的抗菌作用、穩定性和力學性能,而且沒有表現出對成纖維細胞、角質形成細胞和單核細胞的毒性。綜上所述,MPC噴霧劑用藥感受更好,并且在一定程度上可以解決MPC制劑的細胞毒性問題,尤其是對成纖維細胞的毒性,這使得MPC能被更加安全、廣泛地使用。
2 MPC貼劑
腹膜炎是腹膜透析的一種嚴重并發癥,可能導致超濾減少、腹膜衰竭、硬化等不良后果,其常為金黃色葡萄球菌感染引起[18-19]。使用MPC治療腹膜炎時,由于腹膜透析治療而引入的永久性導管,可能會受MPC軟膏中作為輔料的酒精影響而出現孔洞,導致導管內容物泄漏,進而需要更換導管,增加患者就診次數,此外,MPC在血清中的半衰期低,不能以靜脈注射的方式使用,因此,David的研究團隊[20]試圖研發基于有機硅黏合劑的控釋莫匹羅星貼劑。在該研究中,使用了Eudragit RS 100(丙烯酸乙酯、甲基丙烯酸甲酯與甲基丙烯酸三甲胺乙酯的共聚物)和乙基纖維素(Ethyl cellulose ether,EC)作為基質制作了MPC貼劑。實驗結果表明,Eudragit RS 100表現出了更好的擴散性和表面張力,即使在貼劑外3 cm處,仍能發揮抑菌作用。貼劑抗MRSA效果與2%軟膏無明顯差別,持續釋放藥物8 h后,也僅釋放了不到50%的藥物,并且未表現出皮膚刺激性。因此,貼劑或許比軟膏更加適用于需要長期用藥的情況,但其更長持續時間的高載藥量貼片仍然需要進一步研究。
3 MPC水凝膠
水凝膠作為一種新型的藥物釋放遞送系統,其本身有一定的抗菌作用,可以持續釋放藥物,延長藥物作用時間以避免耐藥株篩選,這在一定程度上應對了如今的細菌耐藥性增強的問題。并且水凝膠作為載體可以很好地搭載各類物質,進而發揮藥物之間的協同作用,提高抑菌效果[21]。嚴熒燕等[22]使用改性后的明膠與熱敏材料N-異丙基丙烯酰胺(N-isopropyl acrylamide,NIPAM)制備水凝膠裝載MPC,獲得的MPC水凝膠保留了NIPAM的溫敏性能,使得水凝膠在釋放MPC時,能在短時間達到平衡濃度從而殺滅細菌,減少耐藥菌的篩選。
活性氧(ROS)在傷口愈合中發揮重要作用,盡管ROS具有一定的殺菌活性,但過量的ROS也會阻礙傷口的恢復,這增加了患者被細菌感染的風險[23]。在2020年的一項研究中[24],研究人員使用ROS響應交聯劑N1-(4-硼芐基)-N3-(4-硼苯基)-N1,N1,N3,N3-四甲基丙烷-1,3-二胺(TPA)和聚乙烯醇(PVA)混合制成水凝膠,用該水凝膠封裝MPC和粒細胞—巨噬細胞集落刺激因子(GM-CSF)制成MPC水凝膠。當水凝膠與H2O2(1mmol/L,2mL)反應時,H2O2在24 h后被水凝膠完全清除,然后MPC被釋放出來發揮其抑菌活性。糖尿病患者的傷口通常較難愈合,這是由于其高血糖水平和傷口周圍的高氧化應激水平導致的。在該研究中[24],構建了糖尿病模型小鼠,使用具有ROS清除作用的水凝膠治療7 d后,傷口愈合43%,使用PBS、PVA、TPA普通基質組僅愈合18%~20%。在隨后的正常小鼠傷口愈合實驗中,MPC水凝膠(MPC+GM-CSF+水凝膠)治療8 d傷口愈合46%,而水凝膠、MPC+水凝膠、GM-CSF+水凝膠與PBS組傷口愈合僅為10%、17%、16%、7%。
4 MPC納米制劑
4.1MPC納米晶體
在最新的一項研究中,基于納米制劑可改善藥物水溶性差、感染區域可及性差的潛力,開發了MPC納米晶體(Mupirocin nanocrystal,MPC-NC),其為平均直徑70 nm和多分散指數為0.2的超小單分散球形顆粒,并將其制成了多種乳膏制劑。在微生物學研究中,PVA為穩定劑的MPC-NC-PVA乳膏比已經上市的配方表現出了更大的抑菌圈,可以增加MPC的飽和溶解度、溶出速率等。在治愈燒傷傷口感染的大鼠實驗中,使用MPC-NC-PVA治療的大鼠傷口收縮百分比的平均值顯著高于已上市MPC乳膏(P < 0.05),這可能是其通過防止炎癥期延長、提高成纖維細胞增殖率、促進上皮再生和增加膠原蛋白合成,加快了感染燒傷傷口的愈合[25]。然而,該研究中所描述的納米晶體在穩定性和皮膚滲透率方面卻值得擔憂:在該研究中,測量了MPC納米混懸劑在4 ℃下儲存的穩定性,在儲存一個月后,平均粒徑(PS)和多分散指數(PDI)變化不大,但在三個月后觀察到明顯的PDI變化,因此,穩定性只有三個月的藥物在實際應用中勢必存在局限性;其次是該納米晶體在皮膚滲透速率測試中,擁有較高的皮膚滲透能力,MPC一旦進入體內,會以極快的速度代謝,無法有效發揮其作用,如何保證MPC不被過多地吸收也是一個較為關鍵的問題。
4.2納米殼聚糖包裹MPC
殼聚糖作為一種天然聚合物,多項研究指出,其具有良好的生物相容性、生物降解性和抗菌性能,具有制成多種衍生物的潛力,可以成為多種化合物的載體,為藥物加以多種輔料成為可能[26-27]。Golmohammadi等[28]使用包埋了MPC和硒納米粒子(SeNPs)的殼聚糖-十六烷基三甲基溴化銨(CTAB)基水凝膠(CCH)制備了硒-殼聚糖-莫匹羅星(MPC-SeNPs-CCH)納米雜化系統,在糖尿病小鼠模型中測驗了該納米系統對大鼠傷口恢復的影響,結果顯示,該系統將MPC的最低抑菌濃度(Minimum Inhibitory Concentration,MIC)顯著降低為原來的三分之一左右,擁有較好的抗菌活性,額外的抗菌作用可能得益于制劑中使用了具有抗菌活性的硒和殼聚糖成分,該團隊首次將三者聯合使用研究他們之間的協同作用。不僅如此,該系統還在傷口收縮、血管生成、成纖維細胞增生、膠原增生、毛囊和表皮增殖等方面也發揮了重要作用,這對于實際應用十分有利。在一些其他關于MPC與納米殼聚糖的研究中,如Li等[29]學者的研究中,將莫匹羅星和鹽酸利多卡因通過靜電紡絲均勻摻入作為第一層支架的聚己內酯和作為第二層支架的納米纖維從而形成納米殼聚糖,不僅表現出了高效的抗菌活性,還顯示出了極佳的孔隙率和溶脹行為。Ay ?enyi?it等[30]在2021年發表的研究中,在納米凝膠殼聚糖中使用離子凝膠法合并添加了牛血清白蛋白和Carbopol 940以改善其黏合性,這使得莫匹羅星的體外滲透率非常低(1.172±0.202%和0.161±0.136%),并沒有表現明顯細胞毒性,這表明MPC納米凝膠殼聚糖可被視為細菌性皮膚感染的潛在且安全的局部治療選擇。此外,還有研究也表明了納米殼聚糖作為抑菌藥物載體的潛力:成功利用納米殼聚糖增強了β-內酰胺類抗生素對MRSA的活性,還證明了通過離子凝膠法制備的豆蔻油—殼聚糖納米粒子包封率大于90%,并且具有生物相容性和對MRSA的抗菌活性[31-33]。綜上所述,殼聚糖本身的低毒性、抗菌作用和好的生物相容性使其可以成為多種物質很好的載體以彌補MPC實際應用中的不足,從而滿足多樣化的臨床應用需求。
4.3 納米脂質體MPC
研究表明[34-37],使用納米脂質體封裝藥物可以進一步提高其功效多達一個數量級,如在抗MRSA萬古霉素的多項研究中,均制成了可提高其抑菌作用的納米脂質體藥物,因此,納米脂質體在作為抗菌藥物載體方面具備一定的潛力。近年也發展出多種納米脂質體MPC。在Goldman等[38]2019的研究中,合成了聚乙二醇化的納米脂質體MPC,小鼠體內實驗表明,相較于游離MPC,納米脂質體MPC能更高效地被感染了金黃色葡萄球菌的巨噬細胞吞噬,增強其清除胞內細菌能力;在金黃色葡萄球菌血流感染的小鼠實驗中,測量了腎和脛骨中MPC和金黃色葡萄球菌含量,在實驗d8游離MPC組已檢測不到MPC,而納米脂質體MPC處理的小鼠,仍可檢測出MPC,并且細菌數量小于游離MPC處理組;在嗜中性粒細胞減少的肺部感染的小鼠實驗中,納米脂質體MPC較游離MPC同樣表現出更好的抑菌活性。2021年,Cern等[39]進一步確認了聚乙二醇化納米脂質體MPC對多種突變型金黃色葡萄球菌均有抑菌活性;在測定細菌突變頻率和15 d的傳代研究中發現,納米脂質體MPC對MRSA幾乎沒有耐藥菌篩選壓力;小鼠靜脈注射納米脂質體MPC后,可以保持對MRSA的抑菌活性超24 h。Singh等[40]使用熔體乳液超濾技術配制出可在體外持續釋放24 h的納米脂質體MPC,配制時無需有機溶劑,因而避免了殘留溶劑的毒性風險,但尚缺乏相關動物實驗數據。綜上,納米脂質體MPC可減少耐藥菌篩選、降低藥物毒性風險,具備更長的血清半衰期,為MPC體內用藥提供了新方案。
5 總結和展望
現代制劑技術的發展使得多種MPC劑型改造成為可能,本文主要綜述了MPC噴霧劑、貼劑、水凝膠和納米制劑改造后的優勢(詳見表1),如減少MPC的毒副作用、控制藥物釋放速度、延長血清半衰期等,在增進療效的同時,一定程度上減少了耐藥菌篩選。
非納米殼聚糖在MPC劑型改造中也具有一定潛力。2022年的一項研究將裝載了MPC的殼聚糖微球嵌入到含有膠原蛋白支架的蔞葉提取物中,發現載于殼聚糖的MPC抗菌能力優于純MPC[41]。此外,Naseri等[42]提供了一種以N,O-羧甲基殼聚糖-淀粉生物材料作為3D打印傷口敷料的油墨,將MPC載于該油墨上時,MPC表現出了更大的抑菌圈,而通過調節該材料成分比例,還可以控制MPC的釋放速度和抑菌圈大小。
MPC作為目前廣泛使用的外用抗菌藥,主要用于抗金黃色葡萄球菌,其療效已經毋庸置疑。但金黃色葡萄球菌的高適應性已經使其發展出了抗MPC的MRSA菌株,其耐藥機制是產生了對MPC不敏感的由mupA基因編碼的異亮酰胺-tRNA合成酶,這從根本上逃離了MPC對其的抑制作用[43],MPC對MRSA的MIC也由512 μg/mL上升至>1 024 μg/mL[44-45]。如何增進MPC療效,快速高效地消滅細菌從而減少耐藥菌的篩選變得尤為重要。MPC劑型改造具有良好的潛力,在今后的研究中,應綜合考量多方面因素,不僅通過基質改造篩選出適用于患者的最佳MPC劑型,還可以考慮與其他新型抗菌藥物做成聯合制劑使用,以更好地為世界公共衛生問題提供方案。
參 考 文 獻
Ward A, Campoli-Richards D M. Mupirocin A review of its antibacterial activity, pharmacokinetic properties and therapeutic use[J]. Drugs, 1986, 32: 425-444.
Parenti M A, Hatfield S M, Leyden J J. Mupirocin: A promising new topical antimicrobial agent[J]. Antimicrob Chemother, 1987, 6: 761-770.
Hughes J, Mellows G. Inhibition of isoleucyl-transfer ribonucleic acid synthetase in Escherichia coli by pseudomonic acid[J]. Biochem, 1978, 176: 305-318.
Cookson B D. The emergence of mupirocin resistance: a challenge to infection control and antibiotic prescribing practice[J]. Antimicrob Chemother, 1998, 41: 11-8.
Solares C A, Batra P S, Hall G S, et al. Treatment of chronic rhinosinusitis exacerbations due to methicillin-resistant Staphylococcus aureus with mupirocin irrigations[J]. Am? J? Otolaryng, 2006, 27(3): 161-165.
Diekema D J, Pfaller M A, Schmitz F J, et al. Survey of infections due to Staphylococcus species: frequency of occurrence and antimicrobial susceptibility of isolates collected in the United States, Canada, Latin America, Europe, and the Western Pacific region for the SENTRY Antimicrobial Surveillance Program, 1997-1999[J]. Clin Infect Dis, 2001, 32(Suppl 2): S114-32.
Lowy F D. Staphylococcus aureus infections[J]. N Engl Med, 1988, 339: 520-532.
Eriksen K R. “Celbenin”-resistant staphylococci[J]. Ugeskr Laeger, 1961, 123: 384-386.
賴崇發,嚴華成,石磊. 抗MRSA感染新藥的應用與研究進展[J]. 國外醫藥抗生素分冊, 2017, 38(04):166-172,178
梁樹梅, 沈昊天. 某醫院2018年耐甲氧西林金黃色葡萄球菌的耐藥性及臨床分布[J]. 世界最新醫學信息文摘, 2019, 19(92):244-246.
Balin A K, Leong I, Carter D M. Effect of mupirocin on the growth and lifespan of human fibroblasts[J]. Invest Dermatol, 1987, 88(6): 736-740.
Herold D A, Rodeheaver G T, Bellamy W T, et al. Toxicity of topical polyethylene glycol[J]. Toxicol Appl Pharmacol, 1982, 65(2): 329-335.
Mueller R S. Chapter 24 - Topical dermatological therapy[C].Maddison J E, Page SW, Church DB. Small Animal Clinical Pharmacology (Second Edition). Edinburgh:W.B. Saunders, 2008:546-556.
Shittu A O, Layer-Nicolaou F, Strommenger B, et al. First report of a methicillin-resistant, high-level mupirocin-resistant Staphylococcus argenteus[J]. Front Cell Infect Microbiol, 2022, 12: 860163.
池智利, 孫麗琴, 王慧晶, 等. 莫匹羅星創面噴霧劑治療1期壓力性損傷的研究[J]. 循證護理, 2022, 8(04): 562-564.
Bakkiyaraj D, Sritharadol R, Padmavathi A R, et al. Anti-biofilm properties of a mupirocin spray formulation against Escherichia coli wound infections[J]. Biofouling, 2017, 33(7): 591-600.
Sritharadol R, Nakpheng T, Wan Sia Heng P, et al. Development of a topical mupirocin spray for antibacterial and wound-healing applications[J]. Drug Dev Ind Pharm, 2017, 43(10): 1715-1728.
Odudu A, Wilkie M. Controversies in the management of infective complications of peritoneal dialysis[J]. Nephron Clin Pract, 2011, 118(3): C301-C308.
Akoh J A. Peritoneal dialysis associated infections: an update on diagnosis and management[J]. World J Nephrol, 2012, 1(4): 106-122.
David S R, Malek N, Mahadi A H, et al. Development of controlled release silicone adhesive-based mupirocin patch demonstrates antibacterial activity on live rat skin against Staphylococcus aureus[J]. Drug Des Devel Ther, 2018, 12: 481-494.
Yang K, Han Q, Chen B, et al. Antimicrobial hydrogels: promising materials for medical application[J]. Nanomedicine, 2018, 13: 2217-2263.
嚴熒燕, 盧韻碧, 王炳濤, 等. 莫匹羅星溫敏水凝膠的制備和性能研究[J]. 中國現代應用藥學, 2021, 38(19): 2381-2388.
Gao D, Zhang Y, Bowers D T, et al. Functional hydrogels for diabetic wound management[J]. APL Bioeng, 2021, 5(3): 031503.
Zhao H, Huang J, Li Y, et al. ROS-scavenging hydrogel to promote healing of bacteria infected diabetic wounds[J]. Biomaterials, 2020, 258: 120286.
Najm M B, Rawas-Qalaji M, Assar N H, et al. Optimization, characterization and in vivo evaluation of mupirocin nanocrystals for topical administration[J]. Eur J Pharm Sci, 2022, 176: 106251.
Ahmadi F, Oveisi Z, Samani S M, et al. Chitosan based hydrogels: characteristics and pharmaceutical applications[J]. Res Pharm Sci, 2015, 10(1): 1-16.
De Oliveira Pedro R, Takaki M, Gorayeb T C, et al. Synthesis, characterization and antifungal activity of quaternary derivatives of chitosan on Aspergillus flavus[J]. Microbiol Res, 2013, 168(1): 50-55.
Golmohammadi R, Najar-Peerayeh S, Tohidi Moghadam T, et al. Synergistic antibacterial activity and wound healing properties of selenium-chitosan-mupirocin nanohybrid system: an in vivo study on rat diabetic Staphylococcus aureus wound infection model[J]. Sci Rep, 2020, 10(1): 2854.
Li X, Wang C, Yang S, et al. Electrospun PCL/mupirocin and chitosan/lidocaine hydrochloride multifunctional double layer nanofibrous scaffolds for wound dressing applications[J]. Nanomedicine, 2018, 13: 5287-5299.
Ay ?enyi?it Z, Co?kunmeri? N, ?a?lar E ?, et al. Chitosan-bovine serum albumin-Carbopol 940 nanogels for mupirocin dermal delivery: ex-vivo permeation and evaluation of cellular binding capacity via radiolabeling[J]. Pharm Dev Technol, 2021, 26(8): 852-866.
Garg U, Chauhan S, Nagaich U, et al. Current advances in chitosan nanoparticles based drug delivery and targeting[J].? Adv Pharm Bull, 2019, 9(2): 195-204.
Jamil B, Habib H, Abbasi S A, et al. Development of cefotaxime impregnated chitosan as nano-antibiotics: de novo strategy to combat biofilm forming multi-drug resistant pathogens[J]. Front Microbiol, 2016, 7: 330.
Jamil B, Abbasi R, Abbasi S, et al. Encapsulation of cardamom essential oil in chitosan nano-composites: in-vitro efficacy on antibiotic-resistant bacterial pathogens and cytotoxicity studies[J]. Front Microbiol, 2016, 7: 1580.
Hulme J. Application of nanomaterials in the prevention, detection, and treatment of methicillin-resistant Staphylococcus aureus (MRSA)[J]. Pharmaceutics, 2022, 14(4): 805.
Sande L, Sanchez M, Montes J, et al. Liposomal encapsulation of vancomycin improves killing of methicillin-resistant Staphylococcus aureus in a murine infection model[J]. Antimicrob Chemother, 2012, 67: 2191-2194.
Abrishami M, Motamed Shariati M, Malaekeh-Nikouei B, et al. Preparation and in vivo evaluation of nanoliposomes containing vancomycin after intravitreal injection in albino rabbits[J]. Basic Med Sci, 2020, 23: 551-555.
Serri A, Mahboubi A, Zarghi A, et al. Investigating the antimicrobial efficacy of liposomal vancomycin in gram-positive and gram-negative bacteria- a preliminary mechanistic study[J]. Pharm Sci, 2018, 14: 13-24.
Goldmann O, Cern A, Müsken M, et al. Liposomal mupirocin holds promise for systemic treatment of invasive Staphylococcus aureus infections[J]. J Control Release, 2019, 28 (316): 292-301.
Cern A, Bavli Y, Hod A, et al. Therapeutic potential of injectable nano-mupirocin liposomes for infections involving multidrug-resistant bacteria[J]. Pharmaceutics, 2021, 13(12): 2186.
Singh A P, Sharma S K, Gaur P K, et al. Fabrication of mupirocin-loaded nanostructured lipid carrier and its in vitro characterization[J]. Assay Drug Dev Technol, 2021, 19(4): 216-225.
Budhiraja M, Zafar S, Akhter S, et al. Mupirocin-loaded chitosan microspheres embedded in piper betle extract containing collagen scaffold accelerate wound healing activity[J]. AAPS Pharm Sci Tech, 2022, 23: 77.
Naseri E, Cartmell C, Saab M, et al. Development of N,O-carboxymethyl chitosan-starch biomaterial inks for 3D printed wound dressing applications[J]. Macromol Biosci, 2021, 21(12): e2100368.
Mlynarczyk-Bonikowska B, Kowalewski C, Krolak-Ulinska A, et al. Molecular mechanisms of drug resistance in Staphylococcus aureus[J]. Mol Sci, 2022, 23(15): 8088.
Cadilla A, David M Z, Daum R S, et al. Association of high-level mupirocin resistance and multi-drug resistant methicillin-resistant Staphylococcus aureus at an academic center in the midwestern United States[J]. Clin Microbiol, 2011, 49: 95-100.
Rasmussen A K, Skov R L, Venezia R A, et al. Evaluation of mupA EVIGENE assay for determination of high-level mupirocin resistance in Staphylococcus aureus[J]. Clin Microbiol, 2010, 48: 4253-4255.

