基于RPA技術對轉CP4-EPSPS基因產品的快速檢測
胡秀文, 鄧波, 王金斌, 劉華*, 唐雪明, 王宇,曾海娟, 蔣瑋, 李紅
(1.上海海洋大學食品學院,上海 201306; 2.上海市農產品質量安全中心,上海 201708; 3.上海農業科學院生物技術研究所,上海 201106; 4.上海交通大學農業與生物學院,上海 200240; 5.蘭州理工大學生命科學與工程學院,蘭州 730050; 6.上海市農業科學院畜牧獸醫研究所,上海 201106)
2019 年,全世界轉基因作物(genetically modified crops,GMC)的種植面積約27 億 hm2,比1996 年增加了約112 倍[1-2]。據統計,全球五大種植國的轉基因作物應用率已經接近飽和,如美國(大豆、玉米和油菜的平均應用率95%)、巴西(94%)、阿根廷(約100%)、加拿大(90%)和印度(94%)。目前,抗蟲和抗除草劑作物是最重要的2 種轉基因作物[3]。其中,轉基因抗草甘膦除草劑作物是將CP4-5-烯醇丙酮酸酯-3-磷酸合酶基因(CP4-5-enol acetate-3-phosphate synthase gene,CP4-EPSPS)[4]轉入作物基因組中[5-6],該基因表達的CP4-EPSPS 蛋白表現出對草甘膦較強的耐受性[7]。抗除草劑轉基因作物的種植面積約占43%,而具有抗除草劑和其他性狀的復合性狀占比約為45%。轉基因作物廣泛種植對環境的風險引起了公眾的極大關注,因此,研究轉入CP4-EPSPS基因的轉基因產品及其制品對于食品安全和預防生態潛在風險具有重要意義。全球用于食品、飼料、加工和種植用途的轉基因作物轉化體的批準數目越來越多,其中占比最高的是大豆、玉米、棉花和油菜。由于轉基因作物的迅速推廣,一些非法轉基因作物逐漸顯現。2020年12月歐盟食品和飼料類快速預警系統(Rapid Alert System for Food and Feed,RASFF)對華食品通報中指出,非法轉基因問題是我國食品出口貿易的主要問題[8]。盡管許多國家已經實施了嚴格的轉基因標簽規定,但未經授權和不受控制的轉基因作物種植依然被發現。因此,對轉基因作物的檢測在農產品安全監管中至關重要,迫切需要一種快速、靈敏、便攜、低成本和易操作的檢測技術對轉基因作物進行檢測。
目前,聚合酶鏈式反應(polymerase chain reaction,PCR)、酶聯免疫吸附試驗(enzyme linked immunosorbent assay,ELISA)和蛋白質測試條是檢測轉基因作物最常用的方法[9]。基于蛋白質水平的檢測方法,如ELISA或膠體金試紙條,獲得轉基因抗原的抗體較難,且制備過程耗時又昂貴,故基于蛋白質水平的檢測方法適用的轉基因作物靶標蛋白有限。PCR技術是核酸檢測水平上最常用的方法,然而,由于檢測時間長和需要熱循環儀等限制因素,無法做到現場速測。近年來出現的等溫擴增方法[10-11],如 環 介 導 等 溫 擴 增[12](loop-mediated isothermal amplification,LAMP)、交叉引物擴增[13](cross-priming amplification,CPA)和 滾 環 擴 增[14](rolling circle amplification,RCA),雖已克服熱循環儀的限制,但多數仍需要長達1 h才能完成DNA擴增。
自2006 年以來,省時和方便的重組酶聚合酶擴 增(recombinase polymerase amplification,RPA)[15-16]技術成為廣泛應用于病毒檢測的等溫核酸檢測技術之一,該系統識別度高且速度快,能夠將靶標片段快速擴增至可檢測水平[17-18],主要由3種核心酶組成,包括重組酶、單鏈DNA結合蛋白(single-stranded DNA-binding protein,SSB)和鏈狀聚合酶。在反應開始時,引物定位于同源序列,進行鏈交換反應以形成和啟動DNA 合成,并以指數擴增模板上的靶標區域,其擴增產物在10 min 內便可達到檢測水平;反應結束后,采用瓊脂糖凝膠電泳檢測擴增產物。與傳統PCR 相比,RPA 因其所需時間短、且實現等溫(37~42 ℃)擴增而廣受歡迎[19],已廣泛應用于病毒或細菌的檢測[20-22]。食品安全問題與民生息息相關,為有效防控食品安全風險,開展特異、靈敏、快速的食源性致病菌及轉基因作物核酸檢測是關鍵。為實現轉CP4-EPSPS基因作物的快速檢測,本研究采用RPA 技術建立了一種快速、靈敏度高、特異強的轉基因產品及其制品的檢測方法,該方法利用一對特異性引物,在恒溫條件下,可快速擴增出特異性DNA片段,并對該反應體系進行優化,選取最佳反應溫度。該方法符合轉基因作物的快速檢測要求,縮短了擴增時間,為大規模篩查CP4-EPSPS基因提供了一種新的途徑。
1 材料與方法
1.1 試驗材料
以轉基因玉米(NK603)、轉基因苜蓿(J101)、轉基因油菜(GT73)、轉基因甜菜(H7-1)、轉基因大 豆(MON89788)、轉 基 因 棉 花(Mon1445 和Mon88913)和非轉基因玉米為試驗材料。其中,轉基因玉米、轉基因苜蓿、轉基因油菜和轉基因甜菜購買于美國石油化學學會(American Oil Chemists' Society,AOCS)及標準物質與測量研究所(Institute of Reference Materialsand Metrology,IRMM);轉基因棉花、大豆和非轉基因玉米由農業部作物生態與環境安全監測中心提供;轉基因大豆MON89788 由本實驗室提供。材料列表如表1所示。選取轉基因棉花MON88913 作為CP4-EPSPS特異性、靈敏度及條件優化的研究對象。
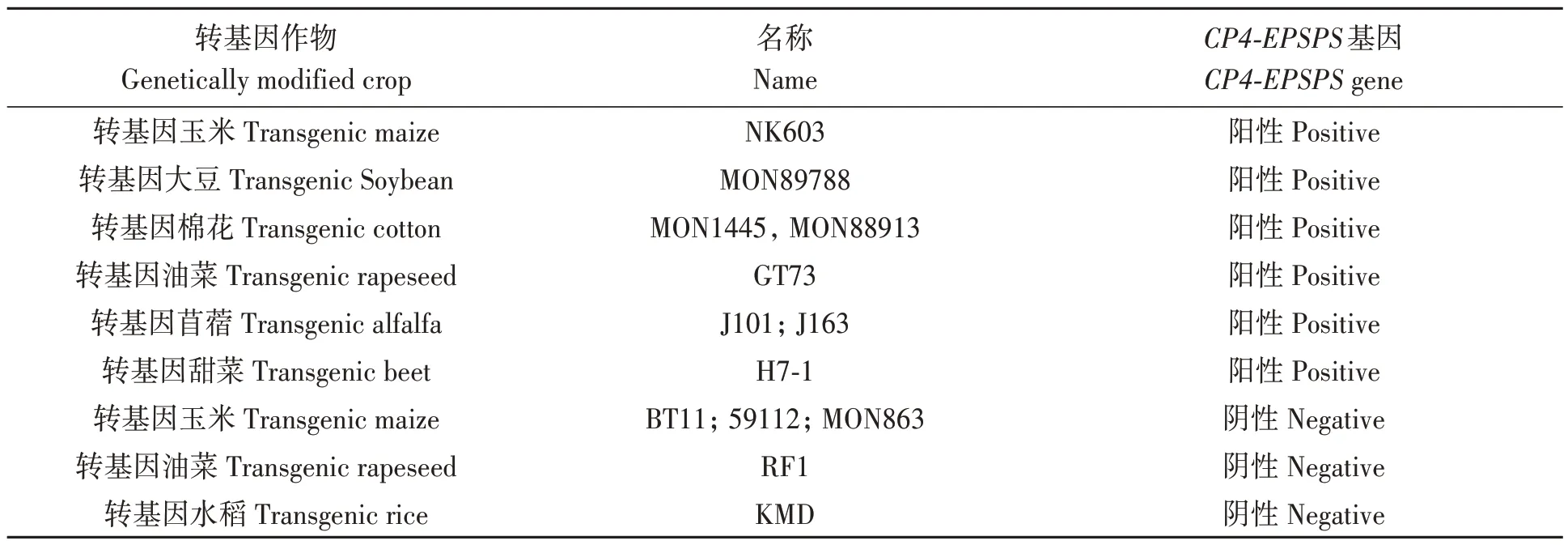
表1 試驗材料Table 1 Experimental materials
1.2 試驗試劑
RPA 引物、ssDNA 和CrRNA 由生物工程有限公司(中國上海)合成;RNase抑制劑購自生物工程有限公司;RPA檢測試劑盒購自TwistDx有限公司;植物基因組提取試劑盒購自天根生化科技(北京)有限公司。
1.3 DNA提取
將轉基因材料種子用研磨機粉碎,稱取0.1 g,利用基因組提取試劑盒提取并純化植物基因組DNA,使用NanoDrop 1000 UV/Vis 分光光度計(Thermo Scientific)和1%瓊脂糖凝膠電泳測定DNA樣品的質量和濃度,備用。
1.4 RPA引物設計
依據RPA引物設計原則,包括長度30~35個堿基,最好不要超過45 個堿基,以形成最佳的重組酶-引物聚合體;適宜的GC 含量(30%~70%),避免過低或過高;擴增產物大小為80~400 bp(最佳為150~350 bp)。因此,根據設計原則采用Primer Premier 5.0 軟件對抗草甘膦基因CP4-EPSPS設計引物,序列詳見表2。

表2 RPA引物Table 2 RPA primers
1.5 RPA擴增及條件優化
為了選擇最佳的反應溫度,根據試劑盒的建議,RPA 反應溫度分別設置為35、36、37、38、39、40、41 和42 ℃。除反應溫度外,還對RPA 體系進行優化,總反應體系分別設置為50、25、20 和15 μL,具體各成分加入量如表3所示。
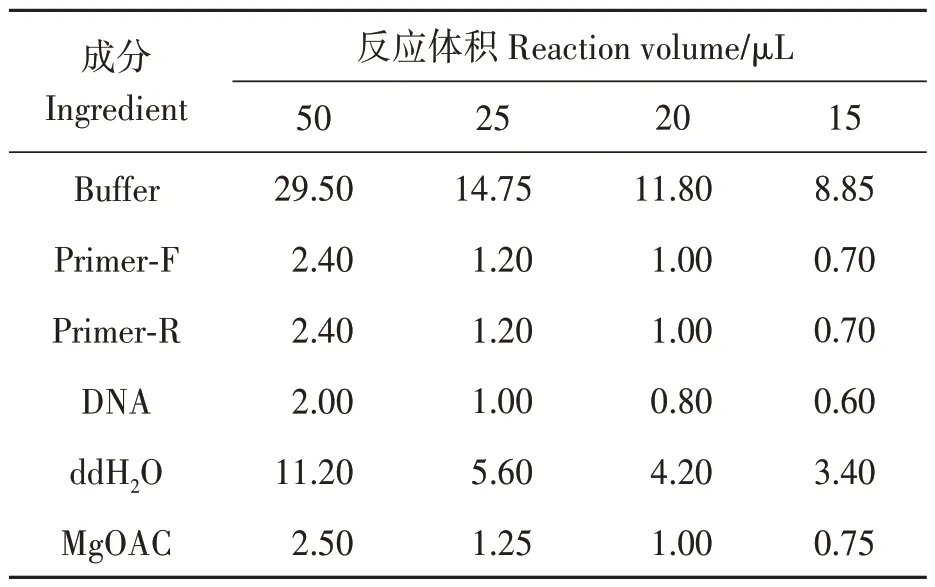
表3 RPA體系優化Table 3 RPA system optimization
RPA 擴增使用TwistAmp basic 試劑盒(TwistDX,Cambridge,UK)進行。選取轉基因棉花MON88913 基因組進行擴增,首先,反應物平均分配到每個含有凍干顆粒的反應管中,并充分混合;其次,將相應的MgOAc 放在試管的蓋子上,將反應混合物管倒置10 次以確保混合良好后,短暫離心后在恒溫擴增儀上進行反應;15 min后取出,短暫離心,然后加入50 μL 苯酚-氯仿,充分混勻后以12 000 r·min-1離心10 min,留上清(有RPA 擴增產物);最后用3%瓊脂糖凝膠電泳進行檢測。
1.6 RPA反應的特異性與靈敏性
將擴增產物片段進行克隆,獲得質粒,測定質粒濃度并計算拷貝數。將獲得的MON88913棉花質粒進行連續稀釋,稀釋濃度至每微升為10~100個拷貝(108~100),以10倍稀釋梯度進行靈敏度檢測試驗。
2 結果分析
2.1 RPA引物篩選
由圖1 可知,RPA 獲得了長度為140~204 bp的特異性條帶,5 對引物均能成功擴增得到目標條帶,而陰性對照無可見條帶。引物RPA-CP4-3、RPA-CP4-4和RPA-CP4-5出現擴增條帶,其中引物RPA-CP4-4的擴增效果最優。因此引物RPACP4-4的特異性強,擴增產物片段為167 bp,適合于RPA擴增。
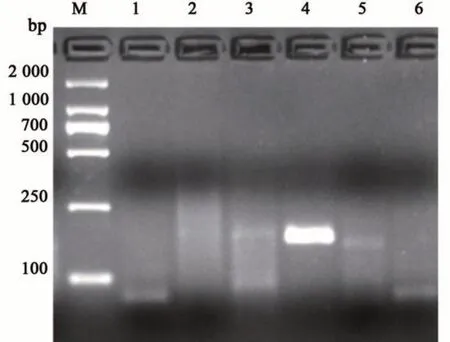
圖1 RPA-CP4-1~RPA-CP4-5的擴增產物Fig. 1 Amplification products of RPA-CP4-1~RPA-CP4-5
2.2 RPA體系優化
為降低試驗成本,對RPA 反應體系進行優化,結果(圖2)表明,隨著整個反應體系不斷縮小,反應穩定性逐漸降低。當反應體系為50、25和20 μL,瓊脂糖凝膠電泳檢測結果間無顯著差異;當反應體系為15 μL時,條帶模糊。因此,20 μL的RPA 反應體系為最佳反應體系,在保證體系擴增穩定性的基礎上,降低了每份樣品的檢測成本,可用于后續試驗。
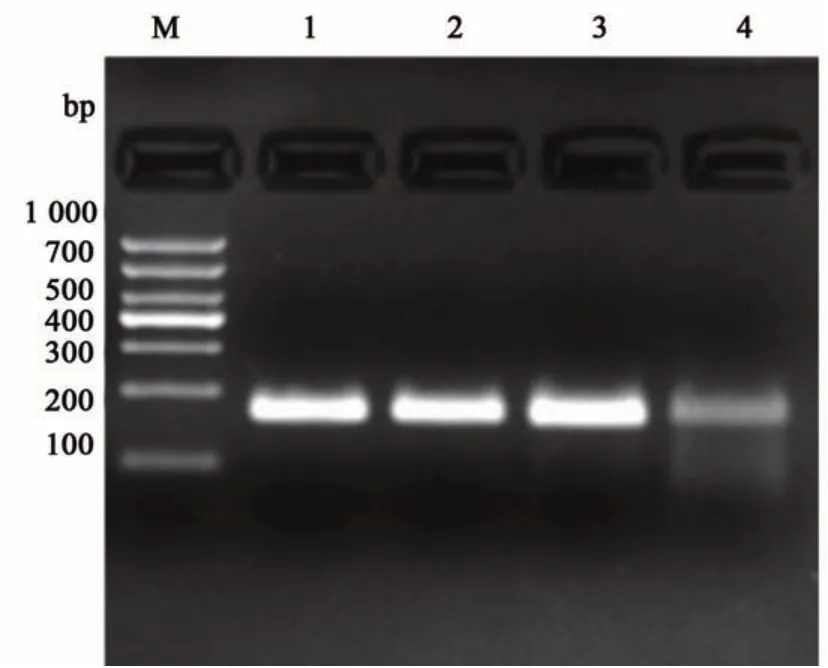
圖2 不同體積反應體系的擴增產物Fig. 2 Amplification products of different reaction system
溫度對RPA 起著關鍵的作用。由圖3 可知,隨著溫度的增加(36~39 ℃),條帶逐漸變亮且更加清晰;當溫度達到40 ℃后,隨著溫度的增加條帶又開始變淡,且出現雜帶。由此表明,RPA 對溫度要求較低,35~41 ℃范圍內均有擴增條帶,且特異性較強;當溫度為37 ℃時,條帶較清晰且無雜帶,為最佳反應溫度,可用于后續試驗。
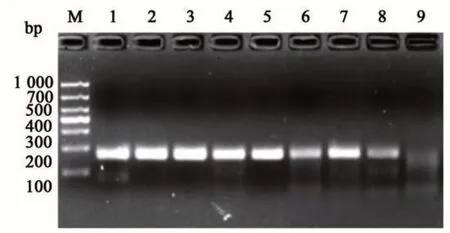
圖3 不同反應溫度的擴增產物Fig. 3 Amplification products of different reaction temperatures
2.3 RPA特異性檢測
為評估引物的特異性,將引物RPA-CP4-4用于檢測多種轉基因作物,包括含有Cry基因的轉基因玉米BT-11、轉基因水稻克螟稻(KMD),含有PAT基因的轉基因玉米59112、MON863、轉基因油菜RF1 及非轉基因大豆、玉米等。在37 ℃反應15 min,結果(圖4)表明,僅含有CP4-EPSPS基因的轉基因棉花MON88913 為陽性,其余不含CP4-EPSPS基因的材料均為陰性。此外,將上述轉基因作物進行混樣(同等質量1∶1∶1進行混合)后提取DNA 進行檢測,結果為陽性。由此可見,引物RPA-CP4-4具有較好的特異性,且條帶單一,適宜用于轉CP4-EPSPS基因作物的檢測。
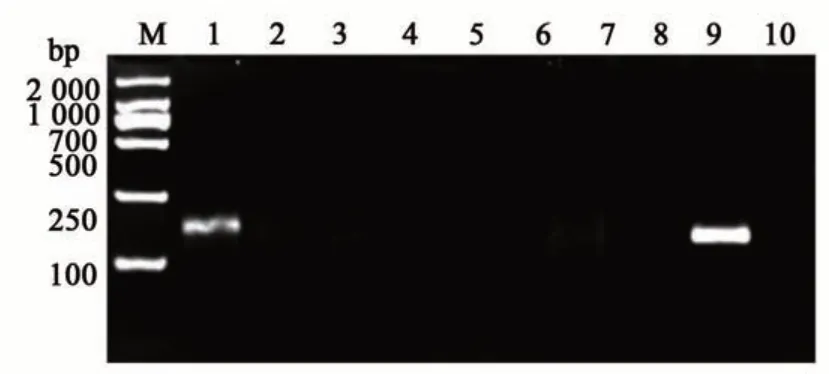
圖4 RPA特異性檢測Fig. 4 RPA specificity detection
2.4 RPA靈敏度檢測
靈敏度檢測結果如圖5 所示,從4.5×107~4.5×105,其擴增條帶均清晰、單一,且亮度基本一致;從104開始逐級遞減,條帶逐漸變暗;100時未觀察到條帶。由此可見,RPA 表現出較高的靈敏性,最低檢出限為45 拷貝,和熒光定量PCR 的檢出限一致。
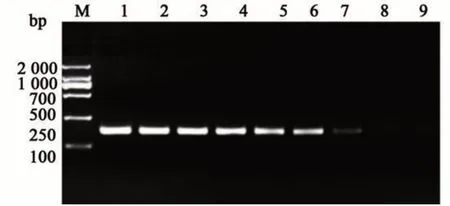
圖5 RPA靈敏度檢測Fig. 5 RPA sensitivity detection
2.5 轉基因產品及其制品檢測
為了驗證RPA 擴增體系在實際樣品檢測中的穩定性,對含有CP4-EPSPS的轉基因農作物進行檢測,選取10份含有CP4-EPSPS的不同種類的轉基因農作物,包括苜蓿、大豆、玉米、棉花、甜菜等,用優化后的重組酶聚合酶擴增技術法進行檢測,結果(圖6)表明,所有樣品均能擴增出目的片段,且條帶清晰,說明該反應具有良好的穩定性。
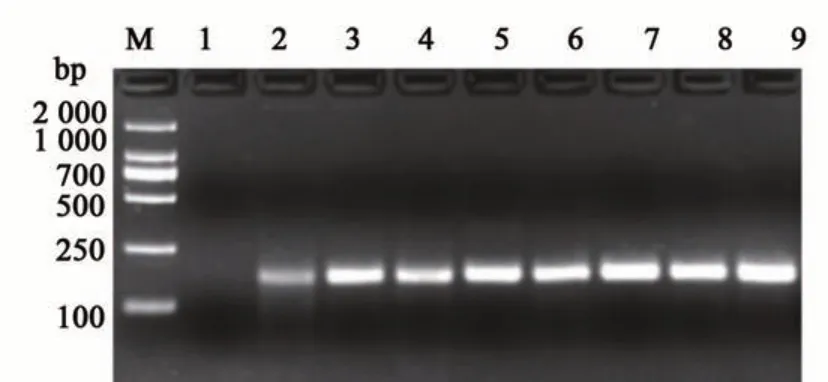
圖6 轉基因制品檢測Fig. 6 Detection of genetically modified products
3 討論
近年來,越來越多的轉基因產品應用于生產實踐,因此,各種檢測方法也應運而生(表4)。多數轉基因產品的檢測方法基于PCR 等試驗技術,如PCR、實時PCR 或數字PCR 等,這些技術需要特殊的試驗條件;而基于蛋白質分析的酶聯免疫反應、免疫傳感器等需要較長的時間。與上述方法相比,RPA 具有步驟簡單、操作方便、結果直觀等優點,且不需要昂貴的儀器和復雜的預處理程序。此外,該方法特異性和靈敏度高、穩定性好,有利于轉基因作物的檢測。RPA 的低溫操作(近體溫)及其較小的樣品制備要求,使得該體系可檢測各種生物樣品,例如血清、糞便、尿液、牛奶、鼻腔、陰道、血漿、食品、植物和動物組織等。
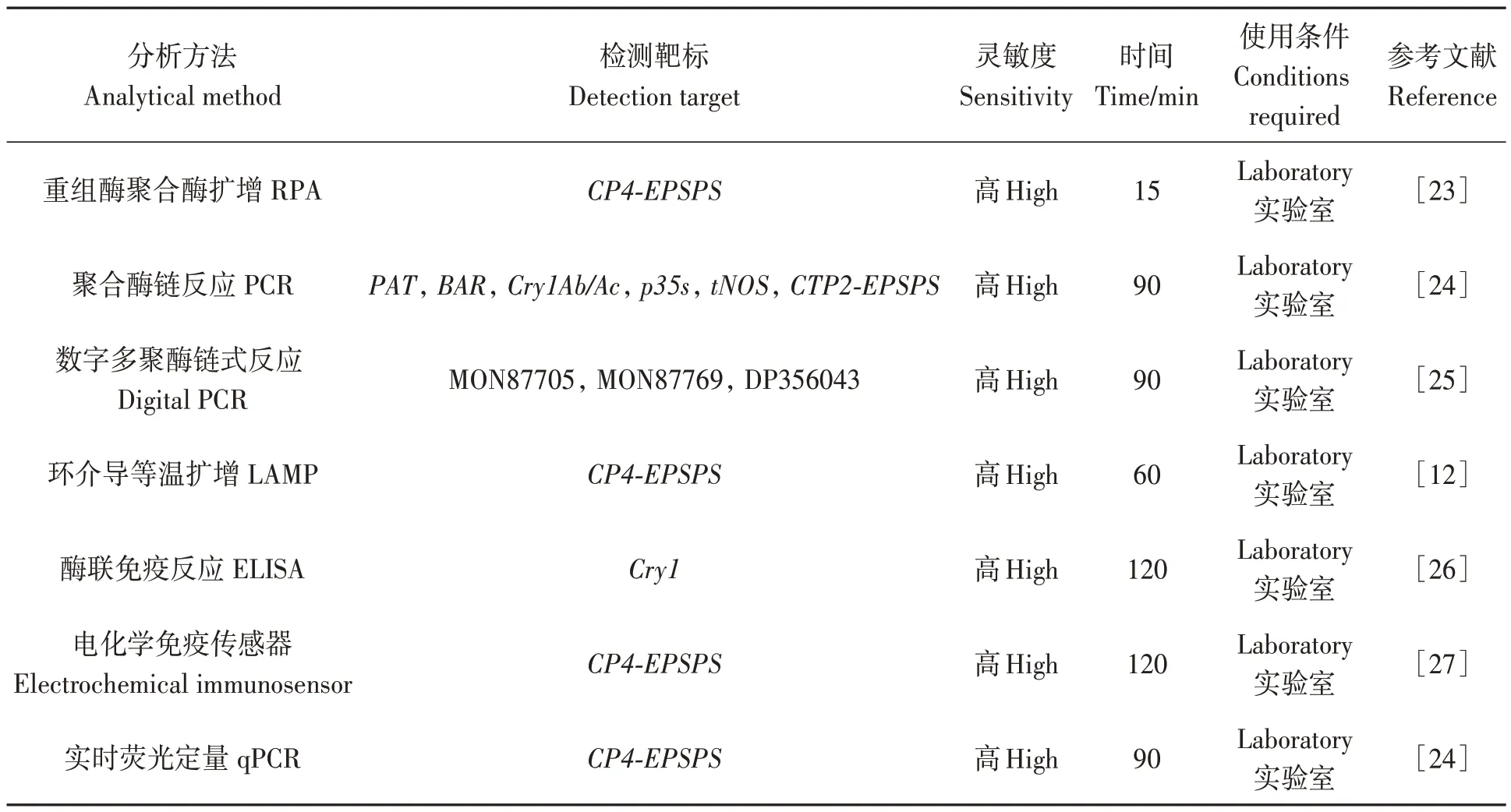
表4 核酸檢測方法比較Table 4 Comparison of nucleic acid detection methods
本研究將RPA 應用于轉基因生物的快速檢測,該方法不僅提高了檢測效率(15 min內完成),對CP4-EPSPS的檢出限為45個拷貝,具有較高的特異性、準確性和靈敏度。采用LAMP 進行核酸檢測時,擴增溫度需65 ℃[28],而RPA 只需室溫左右即可進行反應,因此更適合用來快速篩選。此外在RPA 檢測過程中,其引物對于該反應系統至關重要,本研究發現擴增片段越大,越不易出現DNA 污染現象;且引物設計時,應盡量避免產生二聚體。近年來,CRISPR-Cas(clustered regularly interspaced short palindromic repeats)系統展示了其強大的分子檢測潛在能力,未來將RPA 技術與其結合可能會成為新的檢測平臺,為轉基因產業的快速發展保駕護航。

