在真實世界中驗證冠心病抗血小板治療優選方案評分對高出血風險急性冠狀動脈綜合征患者介入術后缺血事件預測價值
李鵬霄, 裘淼涵, 曹 楊, 嚴育東, 曹伊楠, 李 毅, 韓雅玲
1.空軍軍醫大學,陜西 西安 710032;2.北部戰區總醫院 心血管內科,遼寧 沈陽 110016
急性冠狀動脈綜合征(acute coronary syndrome,ACS)是冠狀動脈粥樣硬化性心臟病(coronary artery disease,CAD)中的急危重癥,常伴隨高死亡風險[1]。基于上述特點,ACS患者的處理流程遵循了快速診斷、風險評估、動態監測、早期血運重建和全程抗栓的原則[2-3]。目前,隨著經皮冠狀動脈介入治療(percutaneous coronary intervention,PCI)的不斷完善與抗栓策略的持續優化,加之我國經濟的發展和醫療條件的改善,ACS患者的生存預后和生活質量得到一定程度的改善。然而,合并高出血風險(high-bleeding risk,HBR)的ACS患者作為其中的一類高危人群,出血和缺血風險均較高[4]。2019年,高出血學術研究聯合會(academic research consortium for high bleeding risk,ARC-HBR)基于專家共識提出了行PCI的患者中HBR人群的識別定義,包括了14條主要標準和6條次要標準,為更加全面客觀地識別HBR人群提供了理論依據[5]。合并HBR的ACS患者臨床表現多樣,各種危險因素組成復雜,臨床醫師往往難以準確衡量其出血和缺血風險。國內外指南均推薦使用風險評估工具準確衡量其缺血風險,以輔助臨床決策,改善患者預后[6-8]。冠心病抗血小板治療優選方案(optimal anti platelet therapy for Chinese patients with coronary artery disease score,OPT-CAD)評分是基于一項覆蓋我國31個省市自治區、107家中心的前瞻性觀察性研究(NCT01735305)建立的缺血事件風險評估與分層工具[9]。既往有研究報道,該評分能夠穩定且準確地預測ACS患者的缺血事件風險與死亡風險[10-11]。但是,對于合并HBR的ACS患者接受PCI治療后缺血風險的評估,目前尚無統一標準,且OPT-CAD評分對于此類高危患者的風險預測能力及臨床決策支持能力也尚未得到驗證。本研究旨在評估OPT-CAD評分對于合并HBR的ACS患者接受PCI治療后12個月內的缺血事件和死亡風險的預測價值及臨床決策支持效用。現報道如下。
1 對象與方法
1.1 研究對象 回顧性分析自2016年3月至2019年3月于北部戰區總醫院心血管內科行PCI的21 531例ACS患者為研究對象,根據以下納入與排除標準,最終篩選出4 265例接受PCI的合并HBR的ACS患者。納入標準:(1)年齡≥18歲;(2)入院明確診斷為ACS;(3)院內接受PCI;(4)符合ARC-HBR定義的HBR患者。排除標準:(1)院內發生死亡、冠狀動脈支架內血栓、心肌梗死、卒中等不良事件;(2)與ARC-HBR評估標準相關的重要信息缺失;(3)與OPT-CAD評分計算相關變量缺失;(4)無出院后隨訪資料。本研究經醫院倫理委員會批準。所有研究對象均簽署知情同意書。
1.2 研究方法 本研究基于北部戰區總醫院心血管介入平臺系統(CV-NET,思創貫宇科技開發有限公司,北京,中國)收集患者的人口學信息、一般臨床資料、手術相關特征及出院用藥情況。由專門的臨床研究隨訪小組完成電話或門診隨訪。研究的主要結局為患者出院后12個月內發生的缺血事件,包括心源性死亡、心肌梗死和卒中事件。隨訪的其他結局包括全因死亡和缺血事件的各組分事件。依據OPT-CAD評分將患者分為低缺血風險組(OPT-CAD評分<90分,n=1 546)與中高缺血風險組(OPT-CAD評分≥90分,n=2 719),分別比較兩組不同缺血風險的高出血風險患者的基線資料、手術及用藥相關特征,并比較組間缺血事件等結局的發生率。同時,驗證OPT-CAD評分工具在合并HBR的ACS患者中的區分度和臨床決策支持能力。
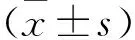
2 結果
2.1 兩組患者人口學及一般臨床資料比較 中高缺血風險組中不穩定性心絞痛(unstable angina,UA)患者比例低于低缺血風險組,ST段抬高型心肌梗死(st-segment elevation myocardial infarction,STEMI)及非ST段抬高型心肌梗死(non-st elevation myocardial infarction,NSTEMI)的比例高于低缺血風險組,差異均有統計學意義(P<0.05)。中高缺血風險組患者的年齡、OPT-CAD評分,以及高血壓、既往心肌梗死、既往缺血性卒中比例均高于低缺血風險組,差異均有統計學意義(P<0.05);而血小板計數、血紅蛋白水平、左室射血分數及估計腎小球濾過率(estimate glomerular filtration rate,eGFR)均低于低缺血風險組,差異均有統計學意義(P<0.05)。見表1。
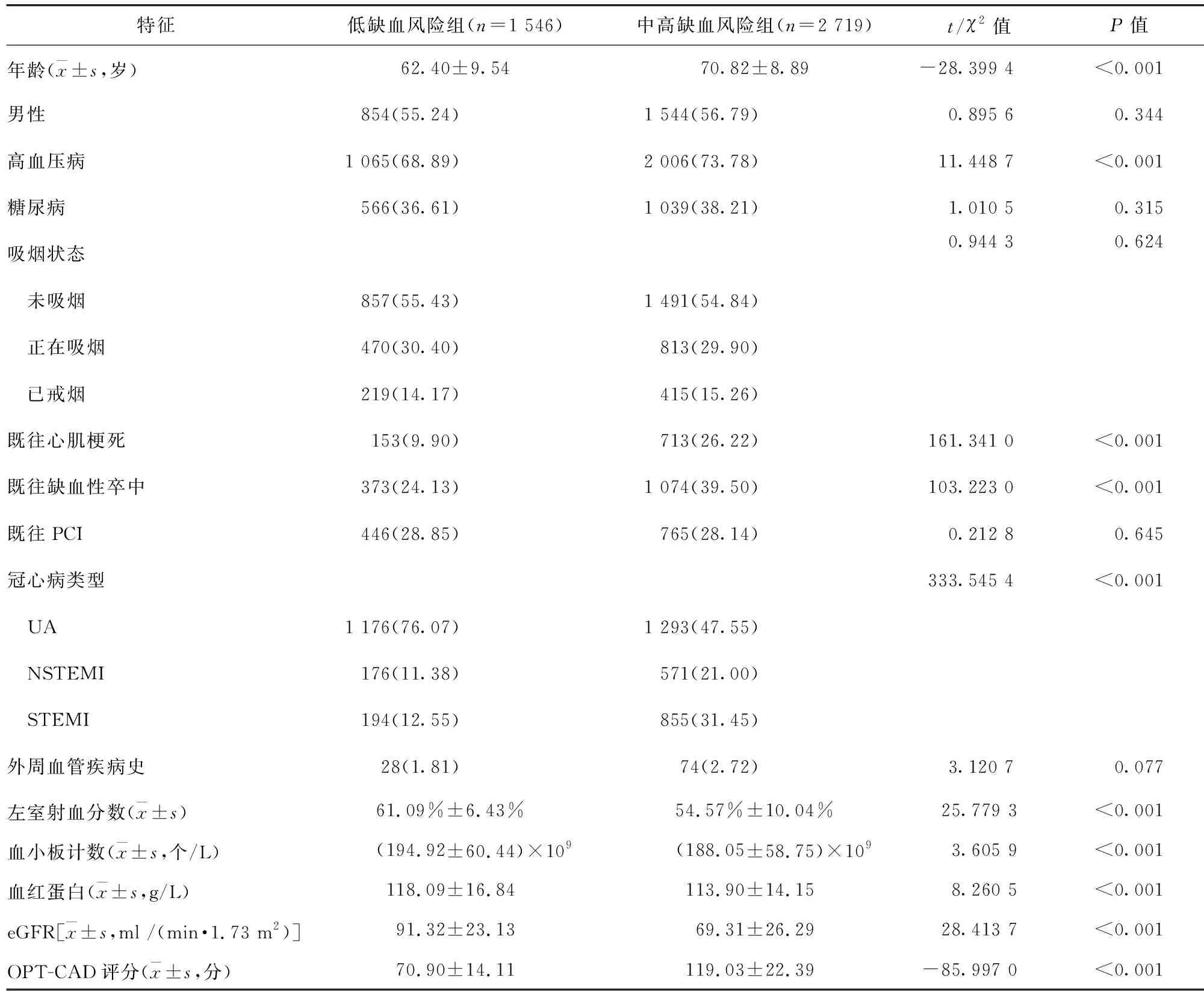
表1 兩組患者一般資料比較/例(百分率/%)
2.2 兩組患者手術資料比較 中高缺血風險組患者采用橈動脈入路的比例及左前降支病變的比例均低于低缺血風險組,且其SYNTAX評分高于低缺血風險組,差異均有統計學意義(P<0.05)。見表2。
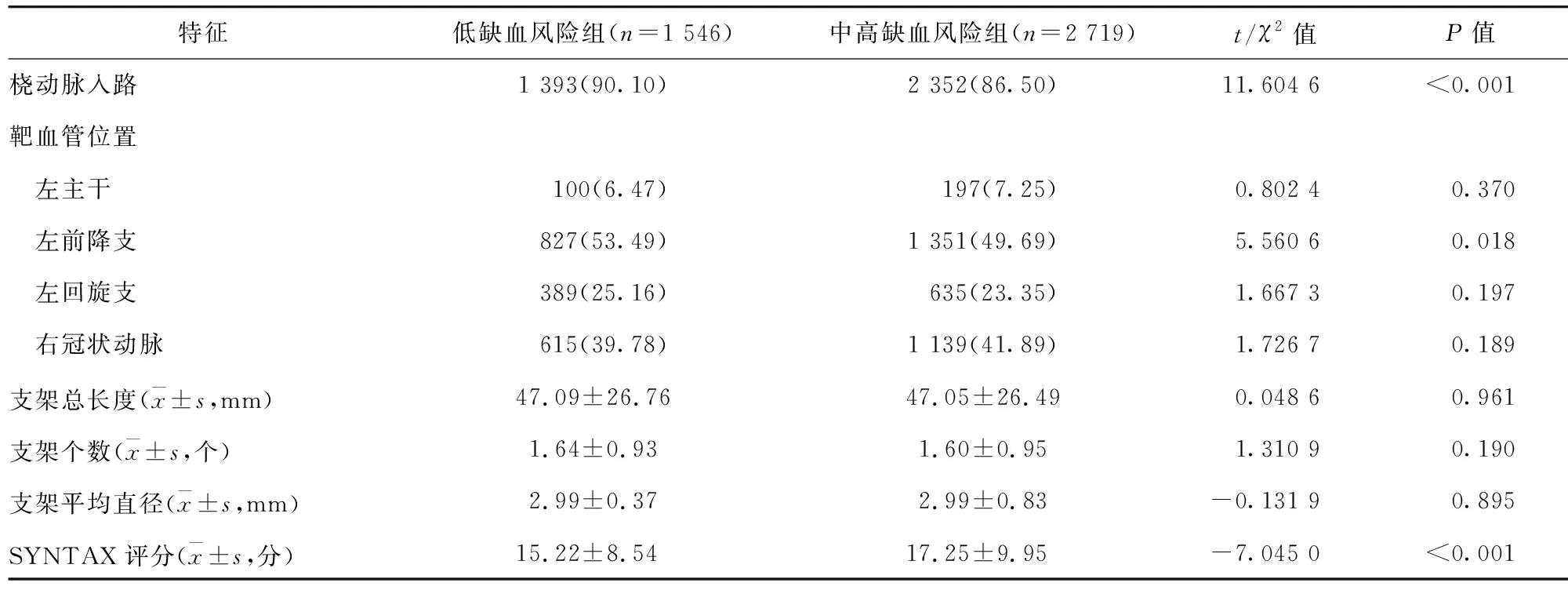
表2 兩組患者手術資料比較/例(百分率/%)
2.3 兩組患者出院用藥情況比較 兩組患者阿司匹林的使用率均較高,但中高缺血風險組患者阿司匹林使用率低于低缺血風險組,差異有統計學意義(P<0.05)。在P2Y12抑制劑的選擇上,中高缺血風險組患者氯吡格雷使用率高于低缺血風險組,且替格瑞洛使用率低于低缺血風險組,差異有統計學意義(P<0.05)。兩組他汀類藥物、血管緊張素轉化酶抑制劑、血管緊張素Ⅱ受體拮抗劑、β受體阻滯劑及質子泵抑制劑的使用率比較,差異均無統計學意義(P>0.05)。見表3。
表3 兩組患者出院后用藥情況比較/例(百分率/%)
2.4 兩組患者12個月隨訪結局比較 對4 265例HBR的ACS患者隨訪12個月后,共發生缺血事件177例(4.15%),全因死亡152例(3.56%)。其中,中高缺血風險組缺血事件、全因死亡、心源性死亡和心肌梗死事件發生率均高于低缺血風險組,差異均有統計學意義(P<0.05)。兩組卒中事件發生率比較,差異無統計學意義(P>0.05)。見表4。

表4 兩組患者結局事件比較/例(百分率/%)
2.5 OPT-CAD評分的缺血風險預測價值 OPT-CAD評分對HBR的ACS患者出院12個月內的缺血事件具有中等預測能力,3、6、12個月的AUC分別為0.76、0.74、0.72(圖1a)。另外,OPT-CAD評分對于HBR患者的全因死亡風險也具有良好的預測能力,3、6、12個月的AUC分別為0.78、0.75、0.73(圖1b)。
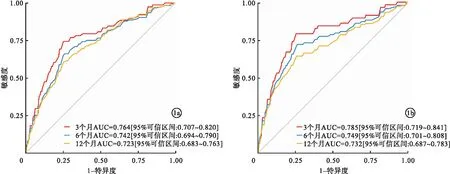
圖1 OPT-CAD評分預測缺血事件及全因死亡的時間依賴ROC曲線(a.預測缺血事件的時間依賴ROC曲線;b.預測全因死亡的時間依賴ROC曲線)
2.6 OPT-CAD評分的臨床決策支持能力 分別使用OPT-CAD評分評估HBR的ACS患者12個月內缺血事件風險和全因死亡風險,進而通過此風險提示輔助臨床決策,結果發現,相較于無干預和全干預策略,OPT-CAD評分可以使患者獲得更多的缺血事件或全因死亡方面的凈收益。見圖2。
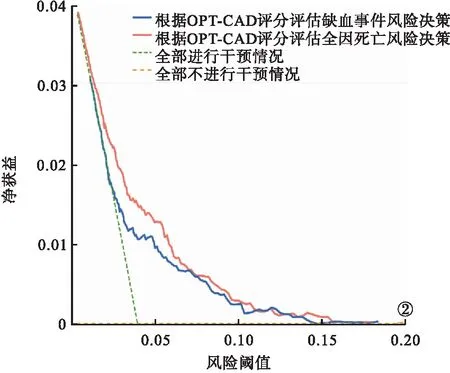
圖2 根據OPT-CAD評估患者缺血事件及全因死亡風險的臨床決策曲線
3 討論
合并HBR的ACS約占所有ACS患者的15%~55%[12-14],是臨床工作中不容忽視的一類特殊人群。而且,相比于一般ACS患者,合并HBR的ACS患者PCI術后在具有較高出血風險的同時,缺血風險同樣較高,其缺血風險與出血風險的平衡極為脆弱[15]。因此,在識別ACS患者HBR狀態的同時,評估其缺血和死亡風險對于輔助臨床決策和改善患者預后具有重要的現實意義。
合并HBR的ACS患者具有較高的缺血風險和死亡風險。大量研究報道,合并HBR的ACS患者缺血發生率和病死率遠高于非HBR的ACS患者[16-17]。因此,對合并HBR的ACS患者進行更加個性化的風險分層對于其介入術后的臨床決策支持與并發癥預防均具有重要現實意義。本研究進一步通過OPT-CAD評分進行缺血風險分層后發現,缺血與出血雙高危患者的缺血事件發生率更高,這凸顯了應用OPT-CAD評分進行缺血風險分層的重要臨床應用價值。其次,相比于目前廣泛應用的GRACE評分系統,OPT-CAD評分雖然納入變量更多,但是其評估程序所需要的變量并未進一步增加醫師的工作量。而且,既往研究證實了OPT-CAD評分在我國ACS患者中具有更高的穩定性和準確性[18]。本研究通過時間依賴性ROC曲線分析發現,OPT-CAD評分對于合并HBR的ACS患者PCI術后3、6和12個月的缺血事件和死亡風險預測達到了中等的區分度(AUC缺血事件=0.76、0.74、0.72,AUC全因死亡=0.79、0.75、0.73),顯示出OPT-CAD評分在預測合并HBR的ACS患者12個月內缺血和死亡風險的良好預測能力,為此類高危患者臨床決策提供了科學實用的量化工具。另外,Li等[19]發現,使用OPT-CAD評分對抗栓策略的選擇具有良好的決策支持作用。同樣,本研究通過決策曲線分析發現,根據OPT-CAD評分對行PCI且合并HBR的ACS患者進行缺血事件和全因死亡風險評估后進行臨床決策,可以使患者獲益。因此,使用OPT-CAD評分在合并HBR的ACS患者中具有良好的風險評估與分層能力,以及臨床決策支持效用。
本研究仍然存在一定局限性。首先,本研究屬于單中心真實世界研究,難以避免地存在選擇性偏倚和信息偏倚,將本研究結論推廣至其他地區時應該慎重。其次,本研究回顧性地收集患者數據,ARC-HBR標準相關的信息采集可能并不完善,對于HBR人群的分布情況與特征描述的報告仍需更大規模的研究支持。第三,本研究僅驗證了OPT-CAD評分對于合并HBR的ACS患者介入術后12個月內的預測價值,其遠期風險評估能力仍需要長期的隨訪支持。
綜上所述,在真實臨床實踐中,OPT-CAD評分對于評估合并HBR的ACS患者接受PCI術后12個月內的缺血事件風險和死亡風險具有良好的預測能力。對于已經識別為HBR的ACS患者,OPT-CAD評分可以輔助臨床工作者快速便捷地評估其缺血和死亡風險,并根據評估情況更加合理地進行臨床決策,使患者獲益。

