姜黃素治療潰瘍性結腸炎及其微納米粒傳遞系統研究進展
楊 慧,童 雨,廖正根
江西中醫藥大學 現代中藥制劑教育部重點實驗室,江西 南昌 330004
炎癥性腸病(inflammatory bowel disease,IBD)已成為世界上第3 大常見疾病[1],潰瘍性結腸炎(ulcerative colitis,UC)是IBD 主要形式之一,也是誘發結腸癌的主要因素之一。UC 可使結腸腸道菌群紊亂和腸道屏障功能嚴重破壞,雖然已有研究對其病理生理機制進行闡述,但確切的發病原因尚不清楚,且無完全治愈的方法[2]。氨基水楊酸鹽、皮質類固醇、免疫抑制劑和抗生素等藥物已被廣泛用于治療UC,然而,長期攝入這些藥物會對患者產生嚴重的不良反應[3-4],如急性胰腺炎、腸道菌群失衡和骨質疏松癥等[5-6]。因此,迫切需要開發有較高療效且不良反應較小的靶向治療藥物和方法。
姜黃素(curcumin)是一種提取于姜科植物姜黃CurcumalongaL.干燥根莖的多酚類脂溶性化合物,其化學結構如圖1 所示。大量研究證明,姜黃素具有抗炎、抗腫瘤、抗纖維化、抗氧化應激等多種生物活性,然而在臨床應用中,姜黃素的抗炎作用并不理想,由于其疏水性強,腸道代謝率高,胃腸道不穩定及從體內快速排泄,導致其在UC 治療中的應用受到嚴重限制,尚未作為治療藥物上市[7]。
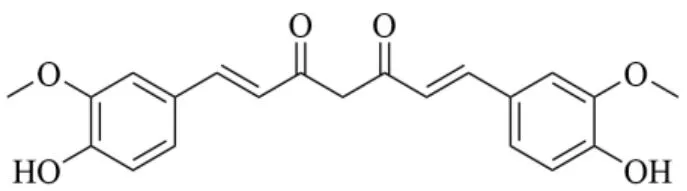
圖1 姜黃素的化學結構式Fig. 1 Chemical structural formula of curcumin
近年來,姜黃素及其制劑關于治療UC 的研究蓬勃發展,大量研究表明,其對UC 治療具有一定的優勢,有望將其開發為抗UC 制劑藥物。本文通過對姜黃素治療UC 的機制、姜黃素微納米遞藥系統抗UC 制劑研究進行綜述,為姜黃素制劑抗UC研究提供理論依據。
1 姜黃素治療UC 的機制
1.1 對信號通路的影響
IBD 的治療重點是控制炎癥,從而改善癥狀,目前抗炎或免疫抑制藥物的臨床效果并不理想,姜黃素被認為是治療IBD 的潛在藥物之一。UC 特點之一是腸道屏障的破壞,腸屏障的破壞通常歸因于核因子-κB(nuclear factor-κB,NF-κB)、激活蛋白-1(activater protein-1,AP-1)和絲裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)途徑激活腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α)、白細胞介素-1β(interleukin-1β,IL-1β)和γ-干擾素等促炎因子的過度表達[8]。姜黃素通過抑制NF-κB活化、細胞核形成,起到治療腸道炎癥性疾病的作用[9]。此外,姜黃素可抑制Toll 樣受體(Toll-like receptors-4,TLR4),并增強轉化生長因子-β(transforming growth factor-β,TGF-β)的生成,尤其是在腸屏障破壞的炎癥區域[10-11]。環氧化酶-2(cyclooxygenase-2,COX-2)是一種由NF-κB 和AP-1 信號誘導的炎癥酶,在腸道炎癥性疾病中其表達上調[12-13]。Kang 等[14]研究表明姜黃素可通過減少AP-1和NF-κB信號傳導消除COX-2基因的表達。此外,姜黃素還可通過下調磷酸肌醇 3-激酶(phosphoinositide 3-kinase,PI3K)/蛋白激酶B(protein kinase B,Akt)誘導的趨化作用[15]、JNK途徑[16]及抑制JAK 途徑[17]實現抗UC 作用。
1.2 對炎癥因子的影響
UC 具有復發性,如果治療不充分,可導致腸道的持續損傷,增加患結直腸癌的風險。在UC 中,上皮組織的損傷導致黏膜對腔內病原體的通透性增加,腸道免疫系統的潛在刺激增加,進而導致TNF-α、IL-12 和IL-13 等促炎因子的產生[18]。這些促炎因子通過Janus 激酶(Janus kinase,JAK)轉導信息,進一步增強淋巴細胞的活化和增殖[19-20]。在AP-1信號傳導中,姜黃素可以直接或間接抑制MAPK,從而限制炎癥靶基因的轉錄[21-22]。姜黃素通過信號通路及炎癥因子介導抗炎作用見表1。
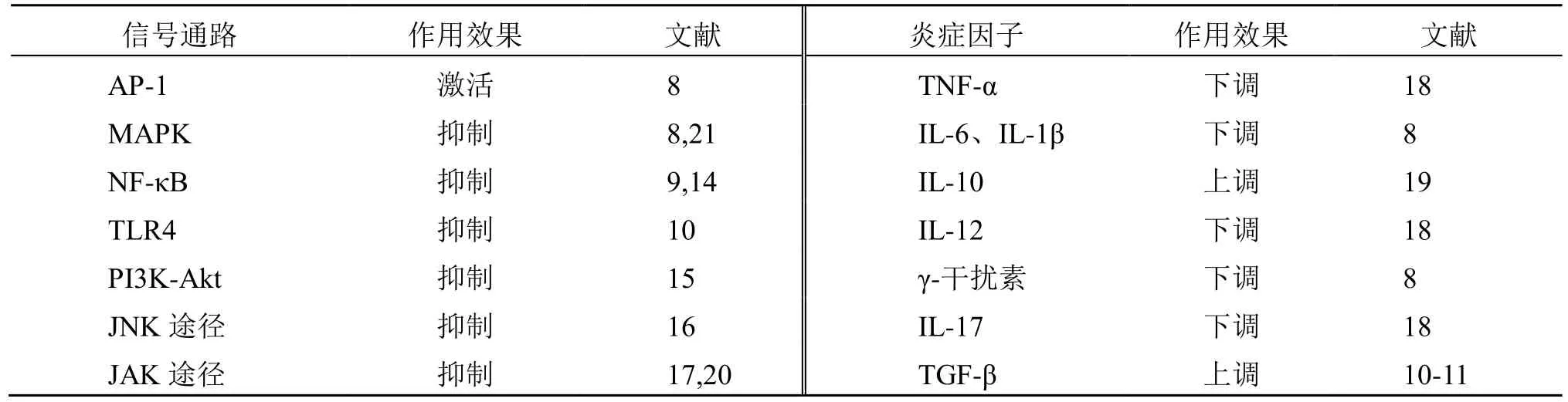
表1 姜黃素抗UC 信號通路及炎癥因子機制Table 1 Curcumin anti-UC signaling pathway and inflammatory factor mechanism
1.3 對免疫細胞的影響
UC 的發病機制往往與結腸上皮細胞和腸道免疫細胞密切相關。在UC 的發病過程中,T 細胞被炎癥因子激活,成熟樹突狀細胞的活化和敏感性也增加,發生炎癥級聯反應,表明這些細胞在產生炎癥中具有重要作用[22]。
1.3.1 樹突狀細胞 樹突狀細胞可表達大量的TLR,通過病原體的識別模式激活多種轉錄因子,從而引發炎癥級聯反應[23]。姜黃素通過抑制吲哚胺2,3-雙加氧酶,進而抑制樹突狀細胞分化與成熟,其抗炎作用類似于皮質類固醇[24]。
1.3.2 T 細胞 姜黃素已被證明可抑制T 細胞介導的免疫功能,在治療慢性腸道炎癥疾病中發揮重要作用[25],Chamani 等[26]研究表明姜黃素可降低淋巴細胞的增殖反應,其機制可能是由于姜黃素的抗氧化特性,抑制與活性氧相關的淋巴細胞增殖,及抑制在細胞的合成與分化的周期中至關重要的核糖核苷酸還原酶和DNA 聚合酶的激活。
1.3.3 巨噬細胞 研究表明,姜黃素治療可增強巨噬細胞的吞噬活性[27]。姜黃素可以通過抑制巨噬細胞產生IL-12 來阻斷Th1 細胞亞類的產生,同時也可以增強Th2 細胞亞類的增殖[28]。Zhang 等[27]在三硝基苯磺酸誘導的結腸炎大鼠模型中,姜黃素30 mg/kg 可增強Th2 細胞的合成并抑制Th1 細胞的增殖,從而減少炎癥反應。
1.4 抗氧化應激反應
過度氧化應激在腸道炎癥性疾病中起著致病作用[29],主要破壞結腸部位細胞組織的緊密連接[30]。腸道炎癥性疾病的特征是中性粒細胞募集和激活到達損傷部位,這一過程為黏膜和上皮細胞的損傷提供了活性氧的主要來源[31]。Larmonier 等[32-33]通過炎癥小鼠模型和細胞實驗研究表明姜黃素通過下調NF-κB 和PI3K/Akt 的作用及減少超氧化物釋放,防止中性粒細胞募集。 髓過氧化物酶(myeloperoxidase,MPO)是單核細胞和中性粒細胞的一種成分,可產生高水平的活性氧。MPO 在臨床上常被用作中性粒細胞浸潤到腸黏膜的標志物[34]。Jiang 等[13]在三硝基苯磺酸誘導的大鼠結腸炎模型中,發現姜黃素可降低與腸道炎癥相關的MPO 活性,從而限制氧化組織損傷。生理水平的一氧化氮可保護腸黏膜[35],但在腸道炎癥疾病進展過程中,通過一氧化氮合酶(inducible nitric oxide synthase,iNOS)釋放的大量一氧化氮可導致組織損傷和壞死[36]。Mouzaoui 等[37]證明了姜黃素能夠減少中性粒細胞腸道浸潤,從而降低MPO 活性,并通過抑制一氧化氮合酶和減少炎癥細胞浸潤將一氧化氮水平恢復到基線水平。此外,在大鼠甲氨蝶呤結腸炎模型中,姜黃素可通過降低腸道MPO 活性、清除自由基、增加超氧化物歧化酶(superoxide dismutase,SOD)的水平[38],達到治療UC 的作用。
1.5 對腸道微生物菌群的影響
人類腸道微生物群構成了體內最大的微生物集合,含有超過35 000 種細菌[39-40]。Frank 等[41]通過16S rRNA 測序發現UC 患者腸道微生物組成與健康人群截然不同。腸道微生物菌群是免疫系統和腸道穩態發育不可或缺的一部分,在防御和耐受機制間存在協同關系[42]。微生物群組成與宿主健康的各個方面存在關聯,包括生理發育、新陳代謝和免疫反應,為促進自身的健康,機體需要在致病菌群和共生菌群間取得平衡。然而,UC 患者腸道微生物群發生紊亂,具體表現為:細菌多樣性減少,厚壁菌門的比例降低,促炎腸桿菌科的比例升高[43]。厚壁菌是腸道微生物群中主要菌種之一,是具有抗炎特性的短鏈脂肪酸代謝物的生產者,而短鏈脂肪酸是結腸細胞的唯一能量來源,表明腸道微生物群在脂質代謝中具有重要作用。De Filippo 等[44]研究表明姜黃素可以調節產生短鏈脂肪酸的細菌數量,這些細菌可以提供腸黏膜保護并抑制腸道炎癥。此外姜黃素通過減少細菌移位和炎癥加強腸道屏障,進而對腸道上皮細胞和免疫系統發揮作用[45]。Ungaro等[46]研究表明腸道微生物群可通過TLR 信號通路在UC 的發展中發揮作用,而姜黃素已被證明可抑制TLR 的激活。
UC 的發病機制如圖2 所示。
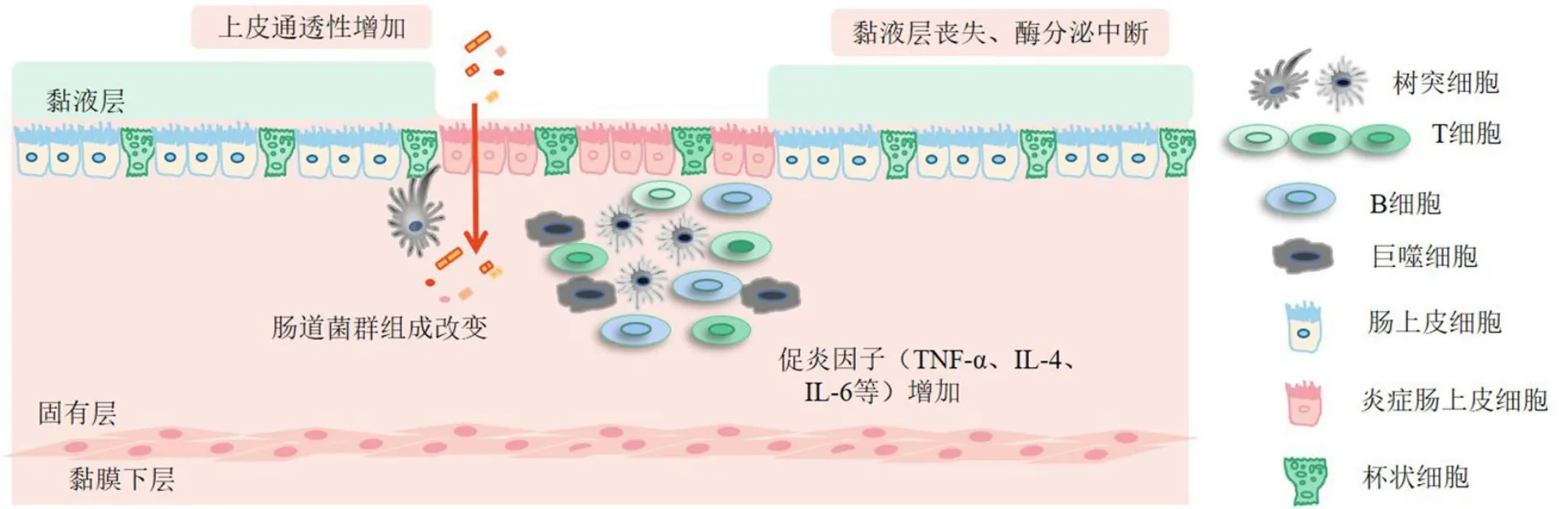
圖2 UC 的發病機制Fig. 2 Pathogenesis of UC
2 姜黃素抗UC 微納米遞藥系統
姜黃素具有顯著的抗炎作用,在治療UC 方面具有廣闊的應用前景,并且美國食品藥物管理局將姜黃素視為“公認安全”的化合物[47]。但姜黃素是一種強疏水性化合物,溶解度約為11 ng/mL[48],限制了其在結腸組織的吸收與分布。Chen 等[49]研究表明姜黃素12 g/d 被認為是其最大的安全劑量,由于肝臟的首過效應導致一些姜黃素在腸黏膜和肝臟中代謝,使其在結腸病變部位的吸收減少[50-51]。溶解度低、快速代謝及缺乏靶向傳遞是姜黃素在結腸病變部位藥效作用低的主要原因,基于此,通過結腸靶向藥物劑型設計策略改善藥物的吸收、分布、代謝和排泄是其開發的重要途徑。
2.1 納米粒
隨著納米技術的進步,納米粒由于其獨特的優點而成為藥物遞送的潛在載體,包括:增加藥物溶解度、延長結腸滯留時間、促進炎癥部位的藥物積累、藥物動力學特性的調節、將藥物遞送至所需細胞或細胞器的能力[52]。納米粒因其尺寸小使其滲透性增加,有利于穿過腸上皮細胞膜。因此,口服納米藥物遞送系統(oral nanomedicine delivery system,ODS)可最大限度地提高藥物的治療效率,同時減輕其不良反應,已被認為在炎癥性腸病治療中有前途的藥物載體[53]。
Luo 等[54]合成了一種以鞣酸包載的京尼平交聯人血清白蛋白包衣來封裝姜黃素的納米顆粒(TA/CURNPs)。該納米顆粒可增強姜黃素的結腸黏附,并提高了其在人結直腸腺癌Caco-2 細胞中的攝取。此外,TA/CURNPs 可阻斷與TLR4 相關的NF-κB信號傳導,有效改善葡聚糖硫酸鈉(dextran sulfate sodium,DSS)誘導的小鼠結腸炎癥狀。Sharma 等[55]采用固體二元脂質納米粒(solid binary lipid nanoparticles,SBLN)封裝姜黃素,提高制劑的穩定性、負載效率、細胞攝取及姜黃素的治療特性。對此,以二元脂質為載體,采用溶劑乳化蒸發法合成了負載姜黃素的SBLN。由此產生的姜黃素-SBLNs 顯著增強炎癥組織中細胞的攝取和定位。結果表明,在DSS 誘導的結腸炎模型中,口服姜黃素-SBLNs 可減少TNF-α 的浸潤、氧化應激和分泌。Kesharwani 等[7]使用納米共沉淀法通過親水性聚合物Eudragit?S100 開發Ora-姜黃素-S 納米粒(Ora-curcumin-S,Ora-CUR-S)。然后對制劑進行藥動學特性研究。結果表明,Ora-CUR-S 可增加姜黃素的溶解度和穩定性。同時在腸腔結腸組織中顯示出精確靶向的潛力。Ora-CUR-S 通過下調TLR-4 的表達,有效阻斷了細胞炎癥活性的發展,對UC 小鼠模型的體內研究進一步證實Ora-CUR-S 對結腸炎和相關損傷的顯著治療作用。Qiao 等[56]制備并表征了親水性聚乙二醇和通過二硫鍵連接的姜黃素納米粒。所得聚乙二醇-姜黃素(polyethylene glycol-curcumin,PCUR)顆粒在腸道炎癥病變部位具有更好的溶解性、聚集性及緩釋特性。Mutalik等[57]詳細介紹了適用于靶向結腸的藥物(負載姜黃素的接枝共聚物納米顆粒)的開發,合成了一種新型pH 敏感的聚丙烯酰胺接枝黃原膠(PAAm-g-XG)負載姜黃素納米顆粒(CURNPs),在大鼠乙酸誘導的結腸炎癥模型中,CURNPs 的吸收效果比姜黃素單體更好,同時,CURNPs 降低了骨髓過氧化物酶和亞硝酸鹽水平,使結腸部位炎癥損傷減弱。Beloqui 等[58]采用自發乳化溶劑擴散法,將聚乳酸-羥基乙酸和聚甲基丙烯酸聚合物結合起來開發姜黃素納米顆粒,結果表明,與姜黃素單體相比,姜黃素納米顆粒可導致其在細胞膜中的滲透性增加,體內實驗表明,姜黃素納米粒可減少中性粒細胞浸潤和TNF-α 分泌。Huang 等[59]采用雙乳液溶劑蒸發法將泊洛沙姆 407(pluronic F127,PF127)聚合物和過氧化氫酶(catalase,CAT)封裝姜黃素,制備用于治療UC 的多功能P-CAT/姜黃素納米顆粒,結果表明在NPs 中引入PF127 和CAT 可以提高其黏液穿透能力,并顯著緩解DSS 誘導的小鼠模型中UC的癥狀。為了提高抗炎藥在結腸炎組織中的滲透性、聚集性和靶向性,Chen 等[60]使用改進的雙乳液溶劑蒸發技術制備納米粒,將PF127 和PLGA 對納米顆粒的表面進行多孔功能化研究,以得到多孔PF127-CURNPs,研究結果表明,經PF127 修飾的多孔姜黃素納米顆粒在小鼠潰瘍性結腸炎組織部位具有更高的滲透性和靶向性。這些研究均揭示姜黃素納米粒在UC 臨床治療中有較大的運用前景。
2.2 微粒
微粒遞藥系統1~1000 μm 具有避免藥物過早降解、控制釋放等優勢,研究表明,微粒系統可減少藥物在小腸上的吸收,并延長其通過結腸區域的時間,因此,此類系統也可特異性靶向遞送藥物來增強其在腸道組織的治療效果,減少全身副作用[61]。
Xiao 等[62]使用乳液溶劑蒸發方法來制備具有pH 敏感的Eudragit S-100(ERS100)和PLGA 的微粒包載姜黃素,制備了一種pH 敏感的Eudragit S100(ERS100)/PLGA 微粒,用于結腸炎特異性藥物的輸送。體內實驗表明,與姜黃素單體相比,口服姜黃素微粒(curcumin-microparticles,CUR-MPs)在緩解UC 小鼠模型結腸炎方面具有更高的治療效率。Zhang 等[63]通過同軸電噴霧制備具有核殼結構的玉米蛋白微粒, 其中含有蟲膠涂層(shellac@CUR/MPs),制備的CUR-MPs 具有較高的包封率和載藥量,使用蟲膠作為外殼材料不僅可以用作pH 敏感材料,保護藥物的胃腸道輸送,還可以用作防分解劑,避免姜黃素氧化分解,有利于制劑的保存,且結果表明CUR-MPs 的抗UC 能力顯著增強。Sareen 等[64]采用乳液交聯法制備了Eudragit S-100 包覆的殼聚糖姜黃素微粒,可防止姜黃素的早期釋放,并在Higuchi 模型中表現出長達12 h 的緩釋。相比之下,未包被的姜黃素-殼聚糖微粒在4 h 后出現突然釋放。此外,在乙酸誘導的小鼠結腸炎模型中進行的體內研究證實,與游離姜黃素相比,載姜黃素微粒的結腸損傷程度和數量顯著降低,組織病理學分析進一步證明了這一點。Blanco-García 等[65]通過噴霧干燥法使用玉米蛋白、pH 敏感的聚丙烯酸樹脂、GantrezTMAN 聚合物制備載有姜黃素的微粒。結果表明載姜黃素的微粒對脂多糖誘導的巨噬細胞中的細胞因子(即TNF-α 和COX-2)活性產生了抑制作用,有較強的抗炎特性,是腸道輸送抗炎劑的有利候選物。Chen 等[66]使用乳液溶劑蒸發法構建載有姜黃素的碗狀微粒(bowl-shaped MPs,BMP),口服負載姜黃素的BMP顯示出良好的治療效果,并改善DSS 誘導的小鼠模型中UC 的癥狀。
2.3 微粒包載納米粒
將納米粒子封裝于微粒中作為結腸藥物口服遞送系統備受關注,避免納米粒子在胃和小腸中的過早降解或吸收,這種新的遞送方法相較于納米粒和微粒遞藥系統具有更強的結腸靶向特異性與藥物聚集性[67-68]。在單個藥物遞送系統中可同時結合納米和微粒系統固有的優點,聚合多種功能,更好地控制藥物釋放速率,減少爆裂效應,增強對藥物的保護和穩定性,及增強靶向定位組織細胞的能力。
Xu 等[69]使用己烷-1,6-二丙烯酸酯和4-氨基1-丁醇單體通過邁克爾加成實驗聚合合成pH 敏感的線性骨架聚(β-氨基酯) [poly(β-amino esters),PBAE],并通過琥珀酸酐連接劑在PBAE 側鏈上接枝活性氧響應PAPE,以獲得新型pH/活性氧雙敏感/響應納米載體(PBAE-SA-PAPE),同時,硫酸軟骨素(chondroitin sulfate,CS)修飾PBAE-SA-PAPE,再通過納米沉淀法制備具有pH/ROS 雙重敏感能力CS-CUR-NPs-Gel,結果表明CS-CUR-NPs-Gel 可以靶向巨噬細胞并在結腸周圍滯留更長時間,是針對UC 的靶向巨噬細胞藥物遞送的潛在方向。Oshi 等[70]使用超聲波輔助抗溶劑結晶和逐層靜電自組裝(layer by layer electrostatic self-assembly,LBL)涂層技術,以殼聚糖包載的姜黃素納米晶體(CUNCs)為核,以殼聚糖/海藻酸鈉/醋酸纖維素鄰苯二甲酸酯的pH 響應聚電解質多層為殼,開發了結腸靶向核殼結構姜黃素納米粒子(CAP1AG4CH5@CUNCs),成功制備了結腸靶向核殼納米粒子,可以特異性的將藥物遞送至結腸炎組織。其原理是通過利用納米顆粒周圍多層膜的表面電荷反轉特性來增強姜黃素在炎癥結腸組織中的積聚。結果表明該聚電解質能夠根據pH 的變化將殼的表面電荷從胃腸道中的負電荷改變為結腸中的正電荷,這種表面電荷反轉作用使得粒子能在結腸組織炎癥部位發生黏附和聚集,可與黏膜中帶負電的蛋白相互作用達到治療UC 效果。
2.4 膠束
膠束是大量表面活性劑在溶液中“自組裝”自由結合形成的膠體溶液。納米膠束是由一個親水基團和一個疏水基團在溶液中形成的共聚物自由結合而形成的納米級核-殼樣膠束。Wang 等[71]通過酯化反應成功制備海藻酸鹽-姜黃素(Alg-CUR)膠束,其在RAW264.7 細胞中發揮有效的抗炎作用。DSS誘導的結腸炎小鼠模型結果表明,92.32%的Alg-CUR 到達結腸部位,酯鍵被共生厭氧菌群產生的酯酶迅速剪切,釋放出姜黃素小分子被迅速吸收,從而減少促炎因子的表達和釋放,有效緩解UC 的癥狀。
2.5 脂質體
脂質體系指將藥物包封于類脂質雙分子層內而形成的超微球形載體制劑[72],具有改善藥物溶解性、提高藥物穩定性、增強體內靶向性等優點。Wang等[73]采用乙醇注射法成功制備姜黃素脂質體(curcumin-liposomes,CUR-LPs)。在DSS 誘導結腸炎動物模型實驗中,CUR-LPs 可防止結腸縮短、炎癥細胞浸潤和黏膜損傷,特別是顯著抑制淋巴細胞浸潤,從而減少組織病理學損傷。
2.6 小結
姜黃素微納米遞藥系統制劑抗UC 研究見表2。
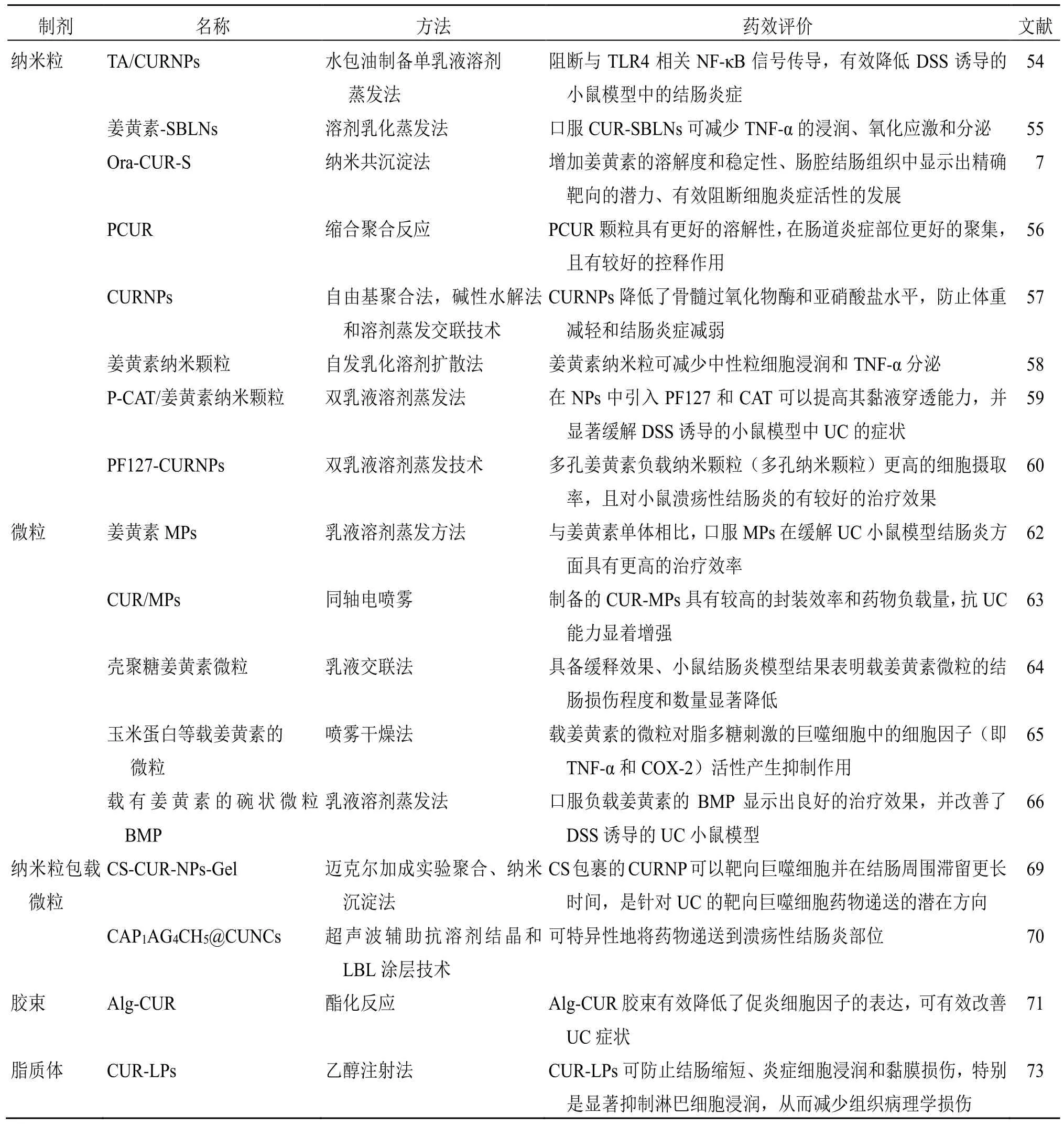
表2 姜黃素制劑微納米遞藥系統抗潰瘍性結腸炎研究Table 2 Anti-ulcerative colitis studies with curcumin formulation micro-nano drug delivery system
目前,治療潰瘍性結腸炎存在幾個關鍵挑戰,主要與結腸定位困難以及藥物向疾病部位的無效遞送有關,因此,需要尋找靶向遞送藥物的方法,同時降低靶外毒性、增加藥物療效。微納米遞藥系統的開發提供了一種可能性,其選擇性地針對結腸的炎癥區域,并保護藥物在胃腸道內的運轉過程中不被降解,具有緩釋、控釋等方面的作用,目前結腸靶向藥物遞送系統已被確定為最有前景的藥物遞送策略。但是,研究者還應考慮潰瘍性結腸炎生理和病理條件,其主要與屏障功能喪失、黏膜損傷、細胞/組織損傷和微生物菌群變化有關,表明需要設計更科學的藥物傳遞系統,以達到靶向、高效、特異性遞送藥物的目的。
3 結語與展望
UC 屬于炎癥性腸病,是一種以黏液膿血便、腹痛、里急后重為主要臨床表現,以結直腸黏膜連續性、彌漫性炎癥分布為特點的慢性非特異性腸道炎癥性疾病[74]。遺傳、免疫、腸道黏膜屏障功能、環境、心理等因素被認為是該病發病機制[75-76],但該疾病的確切機制仍不清楚,由于其發病率不斷增加,已成為沉重的社會負擔。慢性的腸道炎癥將導致免疫系統失調,免疫調節劑經常會在健康組織中產生嚴重的不良反應,如淋巴瘤的發展。如果沒有靶向傳遞,UC 治療藥物可能會經過體循環到健康組織,導致不良反應增加。目前,微納米藥物遞送系統已被廣泛應用于疏水藥物的裝載[77],具有改善藥物溶解性、提高藥物穩定性等優點,用于治療UC、結腸癌等疾病,這種新型的靶向給藥系統可以將藥物直接傳遞到結腸并釋放,具有炎癥靶向和提高藥效的作用,有望使全身不良反應最小化。
姜黃素是一種毒性較低、安全性較好的天然化合物,也是治療UC 的潛在候選藥物,姜黃素主要通過抑制NF-κB、AP-1、TLR 和MAPK 等信號通路發揮治療作用;對于UC 細胞因子譜的變化,姜黃素可抑制樹突狀細胞表達促炎因子、抑制T 細胞介導的免疫功能、增強巨噬細胞的吞噬活性;抑制TNF-α、IL-6 和IL-12 等促炎因子的表達;對于過度氧化應激,姜黃素可以有效清除過量的一氧化氮,防止中性粒細胞募集,從而降低MPO 活性;UC 的特點之一是腸道菌群失調,姜黃素還可以從整體上調節腸道微生物群,維持產生短鏈脂肪酸細菌的數量,減少細菌移位,從而達到抗UC 的作用。
大量體內外實驗研究均表明姜黃素在UC 治療中的有效性,但由于其溶解性差,結腸部位生物利用度低限制了其應用。對此,研究者可通過將姜黃素封裝到納米、微粒系統中改善其溶解性、生物利用度、穩定性和藥效作用。雖然姜黃素微納米制劑在治療UC 方面受到越來越多研究者的關注,但還需要進一步的對照臨床試驗,這些姜黃素制劑的實驗研究大多是在臨床前動物模型及細胞模型上進行的,并沒有在臨床中開展研究,由于UC 病理生理學的復雜性,動物模型遠不能模擬人類的疾病,比如小鼠和人類的腸道微生物群、pH 值、細胞中受體、黏液通過時間、黏液生長速度和厚度也有所不同,未來還需要開發出模擬人類腸道疾病的精確動物模型,如開發人源化小鼠模型或大型哺乳動物模型。
制備這些納米制劑所選用的材料與制備過程不盡相同,制備過程中選擇的輔料在臨床應用前必須對其潛在毒性進行嚴格評估,在人體中的適應性與安全性應該引起研究者的重視;同時,不同材料的組合可能影響彼此之間的穩定性,應科學的選擇輔料組合,以確定此組合材料能夠有效遞送藥物;另一方面盡管這些以UC 癥狀為靶點的納米給藥系統取得了很好的靶向和治療結果,但存在個體間和個體內差異,因此,在設計結腸靶向給藥系統時,研究人員應考慮個體炎癥狀態,以便更好地治療UC。
利益沖突所有作者均聲明不存在利益沖突

