葉面噴施2,3-二巰基丁二酸降低水稻幼苗莖葉鎘含量的機制
王曉麗,王常榮,劉仲齊,黃益宗,孔維勇,黃永春*,劉斌
(1.農業農村部環境保護科研監測所,天津 300191;2.廣西農業科學院農業資源與環境研究所,南寧 537000)
鎘(Cd)是一種有較強致癌風險[1]的高毒非必需重金屬元素。環境中的鎘主要來自于礦山開采[2]、污水灌溉[3]、施用有機肥[4]以及大氣沉降[5]等多種途徑。當前,鎘已經成為我國耕地中最主要的重金屬污染元素,其點位超標率高達7.0%[6]。在我國南方部分水稻主產區,土壤鎘污染問題尤為突出,這給水稻安全生產帶來潛在威脅。目前水稻已成為我國第一大糧食作物,同時水稻也是一種對鎘富集能力較強的大宗農作物[7],即使土壤鎘濃度在較低水平下也可能會出現稻米鎘含量超標現象。我國大部分人口以稻米為主糧,有研究表明我國人口攝入的鎘約56.0%來源于食用鎘污染稻米[8]。由此可見,鎘被水稻吸收后不僅會影響水稻的生長發育[9],而且還會對人體健康造成潛在威脅。由稻田土壤鎘污染導致的稻米鎘超標問題已經引起全球環境科學家的廣泛關注。
為實現水稻的安全生產,農業生產中已研發出多種有效的降鎘措施,如土壤重金屬鈍化技術[10-11]、水份調控技術[12]、植物修復技術[13]、篩選種植低鎘累積品種[14]等。近年來,隨著我國無人機產業的快速發展,無人機噴施技術在農業生產上得到廣泛應用,這極大提高了田間生產效率,顯著降低了生產成本,同時也助推了重金屬葉面阻控技術的快速發展。有研究表明,水稻籽粒中的鎘主要來源于營養生長階段累積在莖葉中的鎘[15],以及灌漿期由根部吸收轉運的鎘[16]。在水稻灌漿期提高水稻營養器官對鎘的攔阻能力,大幅阻斷鎘從營養器官向籽粒中轉運可顯著降低稻米中鎘含量。已有研究表明,于水稻灌漿期噴施硅元素[17]、鋅元素[18-19]、硒元素[20]、小分子酸[21]等都具有顯著降低水稻籽粒中鎘含量的作用。這些技術主要通過增加莖稈細胞壁攔阻能力[22]或通過離子拮抗作用以及生理調控等機制達到降低水稻籽粒鎘含量的目的。目前開發出的重金屬葉面阻控劑產品大部分用于水稻開花灌漿期,但是在實際生產中發現適宜噴施時間窗口較短,因此存在在窗口期內較難完成大面積推廣應用的問題,而且在水稻開花期常遇到降雨等不適宜噴施的氣象條件,這就更加縮短了施工窗口期。因此生產上更希望開發出在苗期至抽穗期噴施也可降低水稻鎘含量的葉面阻控劑產品。
前期本課題組已研究發現,在田間條件下于水稻開花期噴施2,3-二巰基丁二酸(DMSA)可顯著降低水稻籽粒中的鎘含量[23]。水培試驗也表明,噴施DMSA 可顯著減少鎘由根部向莖葉轉運,降低水稻幼苗莖葉鎘含量[24]。DMSA 是一種含有雙巰基的重金屬螯合劑,在人和動物體內其可與重金屬形成螯合物,進而通過排泄系統排出體外實現解毒功能[25],醫療上可以作為人和動物的重金屬解毒劑。但是到目前為止,尚不清楚葉面噴施DMSA 降低水稻幼苗莖葉鎘含量的潛在機制。本研究擬借助水培試驗,系統研究葉面噴施DMSA 對鎘在水稻幼苗根、莖基、莖葉等不同器官中分布的影響以及對水稻幼苗營養器官鎘脅迫的緩解作用。利用分步提取技術研究噴施DMSA 對水稻幼苗不同營養器官中鎘化學形態的影響,采用差速離心技術研究鎘在幼苗莖基中的亞細胞分布情況,借助高效液相色譜分析莖基中總植物螯合素(PCs)和谷胱甘肽(GSH)含量。并在此基礎上,進一步探究鎘在水稻莖基細胞壁不同組分(包括果膠、半纖維素、纖維素)中的分布情況,以揭示噴施DMSA 降低水稻幼苗莖葉鎘含量的潛在機制。
1 材料與方法
1.1 供試材料與培養方法
以我國南方主栽水稻品種之一“中早35”作為試驗材料。將飽滿均一的種子在H2O2中浸泡消毒30 min 后用去離子水反復沖洗多次,然后均勻鋪在育苗盤上,在去離子水中進行第一階段培養。待種子發芽后移至人工氣候室內,直至水稻幼苗長至兩葉一心期,將其轉移至盛有1/10 Hoagland 營養液的水培箱中進行第二階段培養,隨時觀察水稻幼苗生長情況并補充營養液。水稻幼苗長至三葉一心期時,挑選長勢一致的幼苗在去離子水中饑餓處理1 d后轉移至含有2.7 μmol·L-1CdCl2的1/10 Hoagland 營養液中繼續培養3 d,待噴藥處理。水培試驗在人工氣候室內完成。人工氣候室條件參數為晝夜時間16 h/8 h,晝夜溫度28 ℃/20 ℃,相對濕度60%。
1.2 試驗處理及樣品采集
水稻幼苗在96孔水培箱中培養,每孔種植3株水稻幼苗,每箱共計288 株。水稻幼苗鎘脅迫濃度統一設定為2.7 μmol·L-1。將適量DMSA溶于pH=7.4的磷酸緩沖液中,用蒸餾水稀釋至300.0 mL,分別配制成濃度為0.2、0.4 mmol·L-1和1.0 mmol·L-1的DMSA 溶液,每個濃度噴施處理設定5 次重復,每個重復噴施288 株幼苗,5 次重復共計1 440 株幼苗,同時設置只噴施磷酸緩沖液的對照處理(CK)。待水稻幼苗轉移至水培箱并經Cd 脅迫處理3 d 后,立即進行第1 次DMSA 噴施處理,以后每隔3 d 噴施1 次,共噴施4 次。最后一次噴施處理3 d后采集樣品。采集的幼苗樣品用剪刀分為根、莖基及莖葉3 個部分后分別裝于信封中,于70 ℃烘箱中烘干后備用。
1.3 測定方法
1.3.1 鎘含量參照Gutsch 等[26]的方法測定水稻營養器官中的鎘含量。將烘干后的植株樣品取出并研磨成粉。準確稱取粉碎后的根部樣品0.15 g,莖基樣品0.10 g,莖葉樣品0.25 g。將稱取的樣品置于消煮管中,加入7.0 mLMOS 級的濃HNO3浸泡過夜。在電熱消解儀上于110 ℃下加熱消解2.5 h,待樣品冷卻至室溫后加入1.0 mL H2O2繼續消解1.5 h,將溫度升至170 ℃繼續消解至管內剩余硝酸體積小于0.5 mL 后停止加熱。待溫度降至室溫后用去離子水將樣品轉移定容至25.0 mL。用原子吸收光譜儀測定樣品中鎘含量。
1.3.2 鎘化學形態
采用分步提取法測定水稻樣品中鎘的化學形態,參照Guan 等[27]的方法進行試驗。提取劑依次為80.0%乙醇,去離子水,1.0 mol·L-1氯化鈉,2.0%醋酸,0.6 mol·L-1鹽酸。準確稱取3.0 g 新鮮的水稻幼苗樣品加入20.0 mL 提取劑于低溫下勻漿,在25 ℃下恒溫振蕩22 h 后以3 000g離心10 min,倒出上清液。再向離心管中加入同種20.0 mL 提取劑于25 ℃恒溫振蕩2 h重復提取一次,3 000g離心10 min,合并兩次上清液于聚四氟乙烯消煮管中。每一種提取液均重復上述操作,共分5 次進行提取。提取液經HNO3-H2O2消解后,用原子吸收光譜儀測定樣品鎘含量。將乙醇及去離子水提取組分合并在一起作為可溶性組分,其余組分作為難溶性組分。
1.3.3 鎘亞細胞分布
參照Xiao 等[28]的方法進行鎘亞細胞分布試驗。稱取新鮮的水稻幼苗樣品0.5 g,加入20.0 mL 經預冷的勻漿緩沖液(0.25 mol?L-1蔗糖、50.0 mmol?L-1Tris-HCl 緩沖液和1.0 mmol?L-1二硫赤鮮糖醇),低溫下勻漿。勻漿液過80 μm 尼龍網后再用提取液沖洗尼龍網2次,收集合并濾液,殘余在尼龍網上的部分為細胞壁和細胞壁殘基。濾液于4 ℃下以20 000g離心45 min,上清液即為可溶性組分,沉淀為細胞器組分。參照1.3.1中的方法采用HNO3-H2O2消解,原子吸收光譜儀測定鎘含量。
1.3.4 細胞壁組分
參照Zhong等[29]的方法測定細胞壁組分。稱取水稻幼苗組織0.5 g,經過液氮冷卻后研磨成粉末,用7 mL 75.0%的乙醇將粉末轉移至15.0 mL 離心管中,再在冰浴中靜置20 min。冷卻后的勻漿液于1 000g下離心10 min,沉淀依次用5.0 mL 冷凍丙酮、5.0 mL 甲醇-氯仿(1∶1)、5.0 mL 甲醇洗滌3 次。棄掉所有上清液,離心沉淀冷凍干燥過夜。經過干燥的沉淀即為粗細胞壁組分。①果膠組分提取:向細胞壁粗提物中加入5.0 mL 0.5%的草酸銨緩沖液(含有0.1%NaBH4),在沸水中提取1 h,離心收集上清液;②半纖維素Ⅰ提取:將步驟①中剩余沉淀用5.0 mL 含有0.1% NaBH4的4.0% KOH 水溶液常溫提取24 h,3 000g離心,上清液中即為半纖維素Ⅰ組分,離心收集沉淀用于下一步提取;③半纖維素Ⅱ提取:將步驟②中離心獲得的沉淀繼續用5.0 mL 含有0.1%NaBH4的24.0%KOH 溶液常溫提取24 h,3 000g離心,上清液中為半纖維素Ⅱ組分;④纖維素提取:將步驟③中剩余沉淀部分凍干作為纖維素組分。提取液經消解后用原子吸收光譜儀測定提取液中鎘含量。
1.3.5 植物螯合素(PCs)和谷胱甘肽(GSH)含量
參照周蓉等[30]的方法測定樣品中巰基化合物PCs和GSH 含量。稱取0.5 g新鮮的水稻樣品置于液氮中研磨成粉末,將粉末轉移至2.0 mL 的EP 管中,加入1.0 mL 含有0.1%三氟乙酸(TFA)和6.3 mmol?L-1DT?PA 的提取緩沖液振蕩混合均勻。于4 ℃下12 000g離心10 min,取250.0 μL 上清液分別加入650.0 μL 的HEPES 緩沖液和25.0 μL 的TCEP 溶液,混合均勻后于25 ℃下孵育5 min。再加入20.0 μL mbbr 溶液,于25 ℃避光條件下衍生化30 min。衍生化結束后向混合液中加入100.0 μL 1.0 mmol?L-1的MSA終止衍生化反應,經0.22 μm 濾膜過濾后用HPLC 測定巰基化合物含量,采用外標法定性和定量。將PCs2、PCs3、PCs4含量相加,作為總PCs含量。
1.3.6 過氧化氫(H2O2)含量
參照Tyburski 等[31]的方法,采用2',7'-二氯二氫熒光素二乙酯(DCFHA)標記法測定水稻根系與莖葉中的H2O2含量。準確稱取50.0 μmol·L-1的DCFHA于容量瓶中,加入pH為7.5的50.0 mmol·L-1磷酸緩沖液充分溶解并定容至1 000.0 mL。將水稻幼苗根系或葉片在配制好的DCFHA 樣品中浸泡2 h 后取出,經50.0 mmol·L-1磷酸緩沖液反復沖洗3 次后在熒光顯微鏡下觀察熒光強度。激發波長488 nm,發射波長525 nm。
1.3.7 過氧化氫酶(CAT)與超氧化物歧化酶(SOD)活性
CAT 與SOD 活性均使用試劑盒測定,試劑盒購買于索萊寶公司。
1.4 數據分析與處理
采用Excel進行相關數據的計算處理和制圖。利用SPSS 17.0 軟件進行統計分析和差異顯著性檢驗。方差分析和多重比較采用單因素(ANOVA)和Dun?can 檢驗。
轉移效率為相鄰器官之間Cd含量的比值。
2 結果與分析
2.1 噴施DMSA對水稻幼苗莖葉和根部鎘含量的影響
由圖1 可見,噴施DMSA 后水稻莖葉鎘含量隨著DMSA噴施濃度的增加出現顯著降低趨勢。當DMSA噴施濃度達到0.4 mmol·L-1時,水稻幼苗莖葉中鎘含量降低27.8%,增加DMSA 噴施濃度至1.0 mmol·L-1時,水稻幼苗莖葉鎘含量繼續出現降低趨勢,但與噴施0.4 mmol·L-1的DMSA 處理相比未達顯著水平,表明0.4 mmol·L-1的DMSA為最佳降鎘噴施濃度。
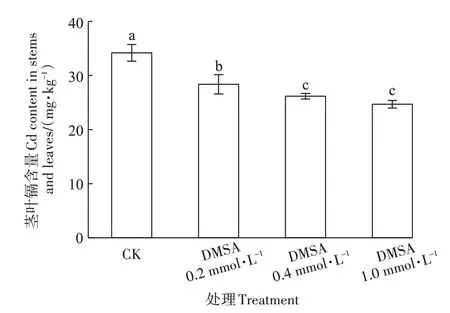
圖1 噴施DMSA對水稻幼苗莖葉鎘含量的影響Figure 1 Effects of foliar application DMSA on Cd content in rice seedling stems and leaves
水稻幼苗根系中富集的鎘濃度較高(圖2),可以達到1 200.0 mg·kg-1以上。隨著DMSA 噴施濃度增加,水稻幼苗根部鎘含量未出現顯著降低或升高趨勢,表明噴施DMSA 對水稻幼苗根部鎘含量無顯著影響。
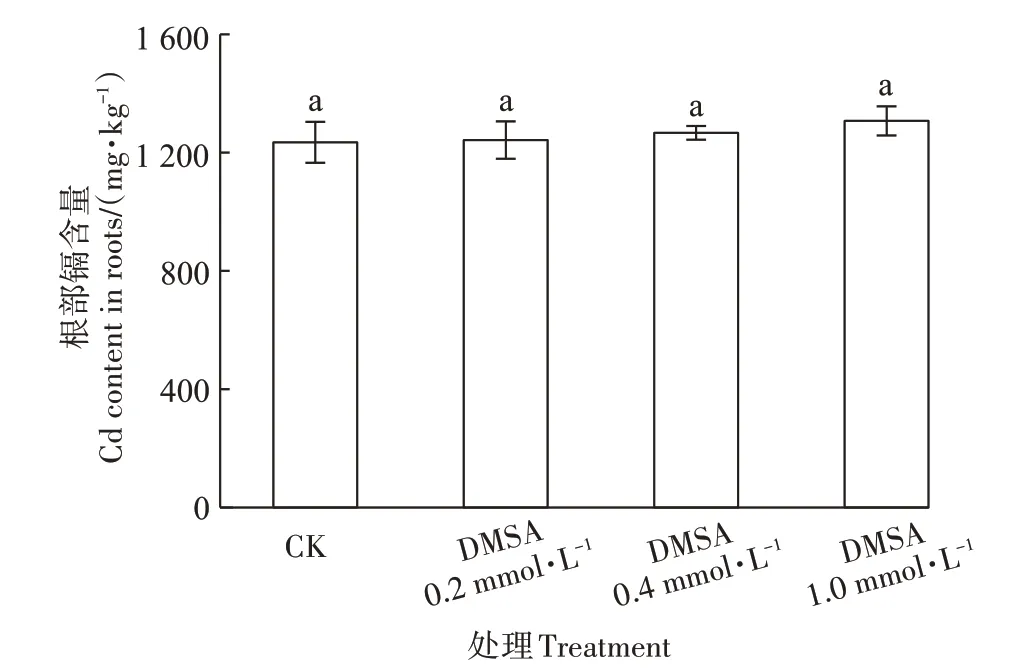
圖2 噴施DMSA對水稻幼苗根部鎘含量的影響Figure 2 Effects of foliar application DMSA on Cd content in rice seedling roots
2.2 噴施DMSA 對水稻幼苗莖基鎘含量和鎘轉移效率的影響
水稻幼苗莖基中富集了較高濃度的鎘(圖3),CK處理的幼苗莖基鎘含量達到275.0 mg·kg-1。隨著DMSA 噴施濃度增加,水稻幼苗莖基中鎘含量呈現顯著增加趨勢。當DMSA 噴施濃度達到1.0 mmol·L-1時莖基鎘含量達到433.0 mg·kg-1,與CK 處理相比增加了57.3%。結果表明噴施DMSA 顯著增加了水稻莖基對鎘的富集能力。
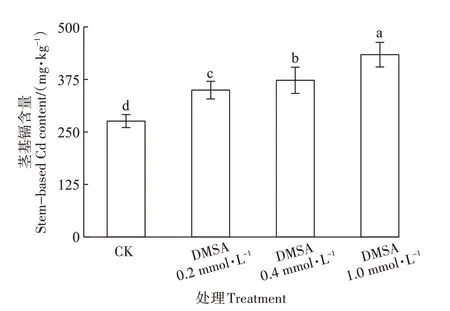
圖3 噴施DMSA對幼苗莖基鎘含量的影響Figure 3 Effects of foliar application DMSA on Cd content in stem base
由圖4 可知,隨著DMSA 噴施濃度的增加,鎘由水稻幼苗根部向莖基的轉移效率出現顯著增加趨勢。當噴施濃度達到1.0 mmol·L-1時根到莖基的轉移效率增加了45.5%。然而,鎘由水稻幼苗莖基向莖葉的轉移效率則出現顯著降低趨勢,當噴施濃度達到1.0 mmol·L-1時莖基到莖葉的轉移效率顯著降低了52.7%。以上數據表明,水稻莖基中累積了大量鎘,噴施DMSA 改變了鎘由根到莖基以及由莖基到莖葉的轉移效率,降低了鎘由莖基向莖葉轉運。

圖4 噴施DMSA對幼苗鎘轉移效率的影響Figure 4 Effects of foliar application DMSA on Cd transfer factors
2.3 噴施DMSA對水稻幼苗根部和莖基鎘形態的影響
水稻幼苗根部鎘主要以難溶態鎘形式存在(圖5),其占據根部總鎘含量的75.0%以上。隨著DMSA噴施濃度的增加,各試驗處理間根部難溶態鎘含量出現顯著增加趨勢,而可溶態鎘含量未出現顯著變化。當DMSA 噴施濃度達到1.0 mmol·L-1時,根部難溶態鎘含量與CK相比顯著增加18.1%。
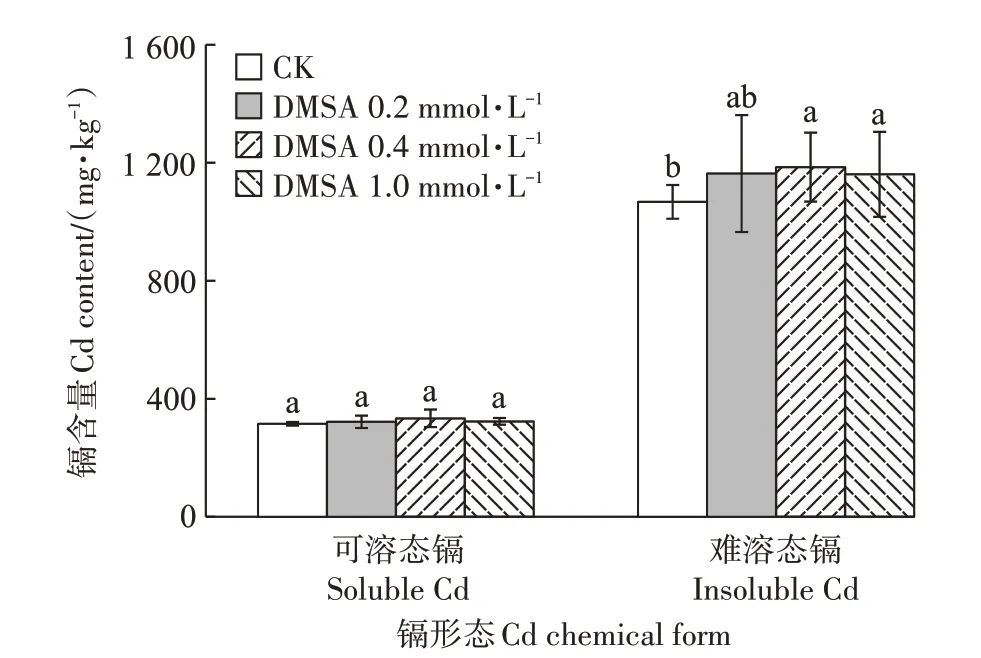
圖5 噴施DMSA對水稻幼苗根部鎘形態的影響Figure 5 Effects of foliar application DMSA on Cd chemical form in rice seedling roots
由圖6 可見,水稻幼苗莖基中鎘的化學形態與根部鎘賦存形態類似,大部分以難溶態鎘形式存在。隨著DMSA 噴施濃度的增加,水稻幼苗莖基部難溶態鎘含量出現顯著增加趨勢。當DMSA 噴施濃度達到1.0 mmol·L-1時,難溶態鎘含量與CK 相比顯著增加80.8%,但是噴施DMSA 對莖基可溶態鎘含量無顯著影響。
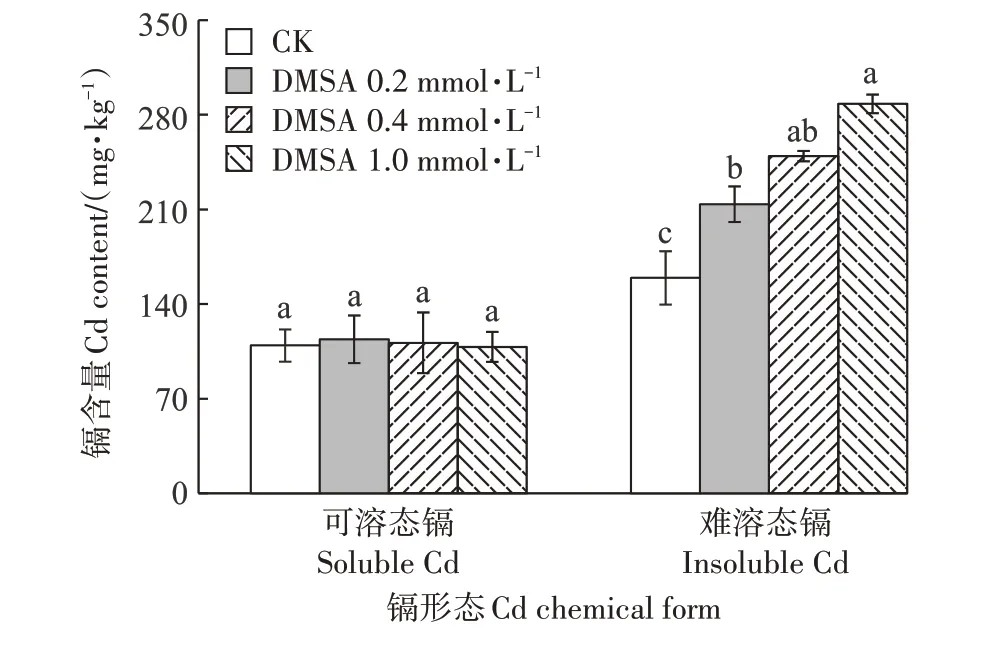
圖6 噴施DMSA對水稻幼苗莖基鎘形態的影響Figure 6 Effects of foliar application DMSA on Cd chemical form in rice seedling stem base
2.4 噴施DMSA對水稻幼苗莖基鎘亞細胞分布的影響
水稻幼苗莖基細胞壁中鎘含量最高(圖7)。噴施DMSA 后水稻幼苗莖基細胞壁中鎘含量隨著DMSA 噴施濃度的增加出現顯著增加趨勢。噴施濃度達到1.0 mmol·L-1時細胞壁中的鎘含量約是CK 組的2.1 倍。但是,噴施DMSA 對水稻莖基細胞器和可溶性組分中鎘含量無顯著影響。由以上結果可知,莖基中的鎘主要沉積在莖基細胞壁中。
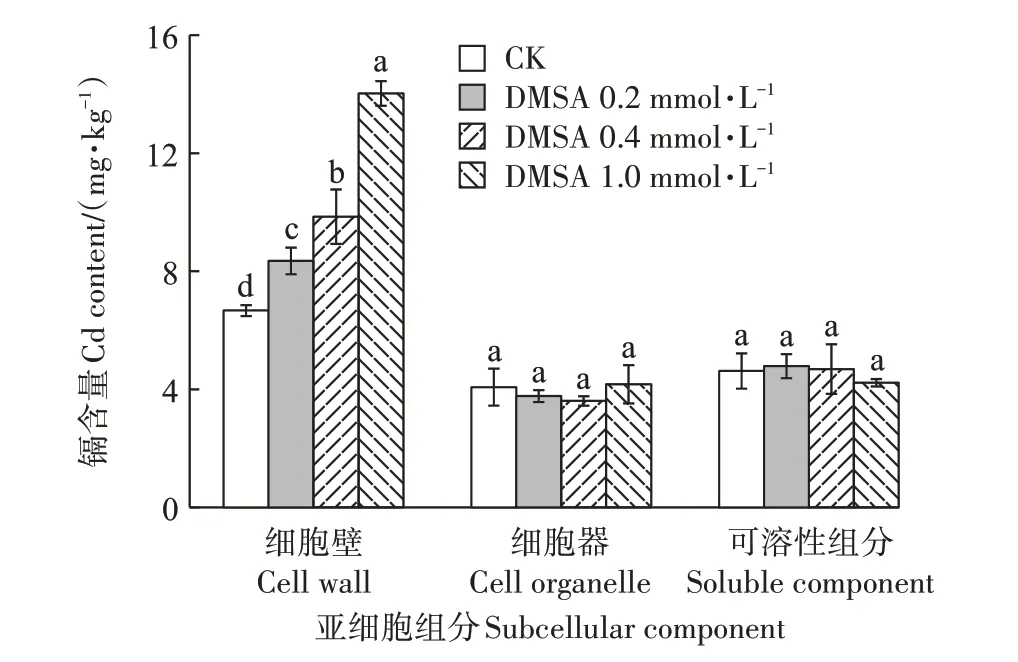
圖7 噴施DMSA對水稻莖基鎘亞細胞分布的影響Figure 7 Effects of foliar application DMSA on Cd subcellular distribution in rice seedling stem base
2.5 噴施DMSA對鎘在細胞壁組分中分布的影響
由圖8 可見,水稻莖基細胞壁的果膠組分中鎘含量最高。隨著DMSA噴施濃度的增加,果膠、半纖維素Ⅰ、半纖維素Ⅱ組分中鎘含量均出現顯著增加趨勢。當DMSA噴施濃度達到1.0 mmol·L-1時,果膠中鎘含量與CK處理相比顯著增加99.5%,半纖維素Ⅰ中的鎘含量顯著增加65.5%,半纖維素Ⅱ中鎘含量顯著增加31.6%,但是纖維素中鎘含量未出現顯著變化。
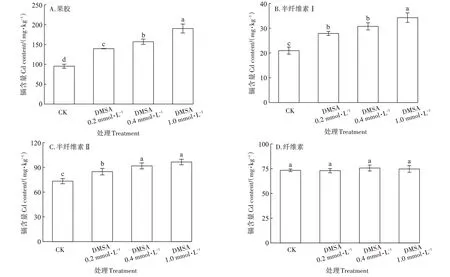
圖8 噴施DMSA對鎘在水稻幼苗莖基細胞壁組分中分布的影響Figure 8 Effects of foliar application of DMSA on Cd distribution rice stem base cell wall
2.6 噴施DMSA對莖基PCs和GSH含量的影響
隨著DMSA 噴施濃度的增加,水稻幼苗莖基中GSH含量出現顯著增加趨勢(圖9)。當DMSA噴施濃度達到1.0 mmol·L-1時莖基中GSH含量達到CK處理的3.1倍,表明噴施DMSA顯著增加了莖基GSH的含量。
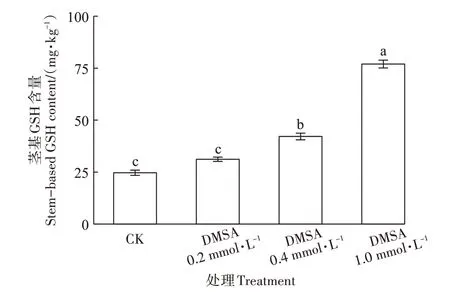
圖9 噴施DMSA對水稻幼苗莖基GSH含量的影響Figure 9 Effects of foliar application DMSA on GSH content in rice seedling stem base
由圖10 可見,隨著DMSA 噴施濃度的增加,水稻幼苗莖基中總PCs 含量也出現顯著增加趨勢。當DMSA 噴施濃度達到1.0 mmol·L-1時莖基中總PCs 含量達到CK 處理的2.2倍,表明噴施DMSA 顯著增加了莖基PCs的含量。
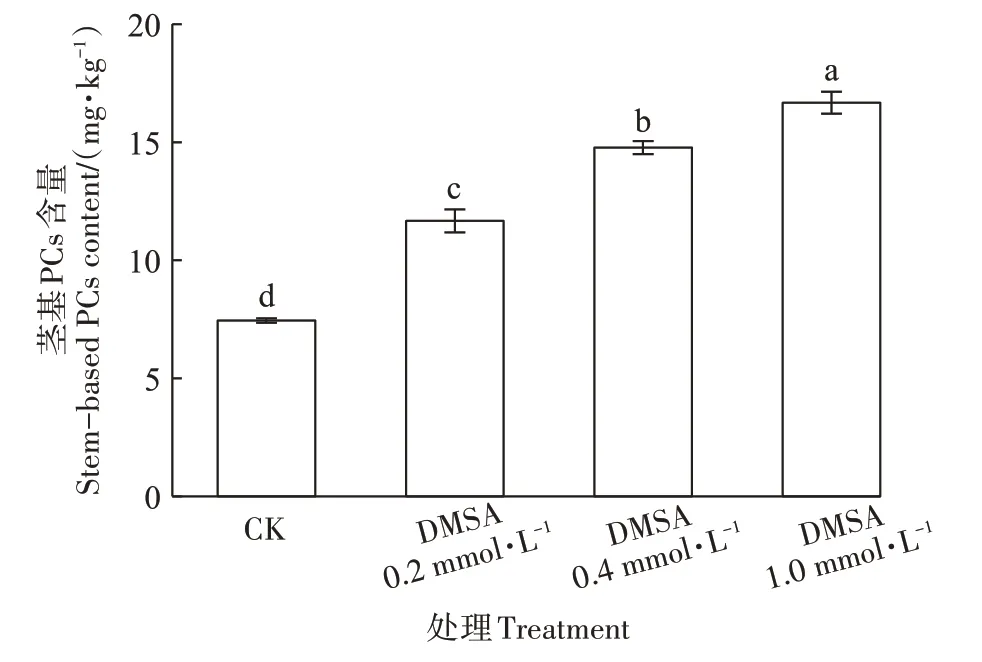
圖10 噴施DMSA對水稻幼苗莖基PCs含量的影響Figure 10 Effects of foliar application DMSA on PCs content in rice seedling stem base
2.7 噴施DMSA對水稻幼苗鎘脅迫的影響
由圖11可見,在激發波長為488 nm 條件下,H2O2分子經標記后在熒光顯微鏡下發出綠色熒光。CK處理幼苗葉片發出的綠色熒光強度最強,表明此時葉片中H2O2含量最高,葉片受到的鎘脅迫強度最大。隨著DMSA 噴施濃度增加,H2O2熒光強度出現顯著降低趨勢。當噴施濃度達到1.0 mmol·L-1時,葉片發出的綠色熒光強度最低,表明此時葉片在鎘脅迫下產生的H2O2量最少,鎘脅迫程度最低。
由圖12 可見,不同試驗處理的幼苗根部都發出較強的綠色熒光,水稻幼苗根部H2O2熒光強度未隨著DMSA 噴施濃度增加出現顯著降低趨勢,說明噴施DMSA對根部鎘脅迫未產生顯著緩解作用。
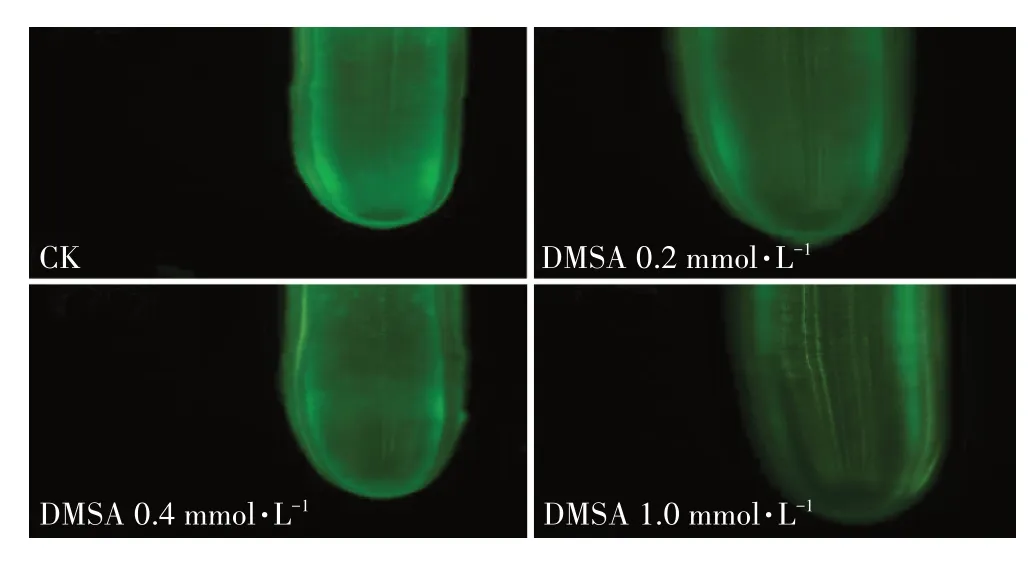
圖12 噴施DMSA對水稻幼苗根部鎘脅迫的影響Figure 12 Effects of foliar application DMSA on Cd stress in rice seedling roots
隨著DMSA 噴施濃度的增加,水稻幼苗莖葉中CAT 與SOD 的活性均呈現顯著增加趨勢(圖13),當DMSA 噴施濃度達到1.0 mmol·L-1時,莖葉中CAT 和SOD 活性分別達到CK 處理的2.7 倍和3.0 倍,但是對水稻幼苗根部CAT 與SOD 活性未造成顯著影響。以上結果表明,噴施DMSA 緩解了鎘對水稻幼苗莖葉的脅迫,但是對水稻幼苗根部的鎘脅迫未產生顯著緩解作用。

圖13 噴施DMSA對水稻幼苗CAT、SOD活性的影響Figure 13 Effects of foliar application DMSA on CAT and SOD activities of rice seedlings
3 討論
3.1 水稻幼苗莖基對鎘的攔阻作用
攔阻鎘由水稻根部向莖葉轉運對實現水稻安全生產、保障人體健康具有重要意義。水稻莖基部位是鎘由根向莖葉轉運的必經之路,增加水稻莖基對鎘的攔阻作用可有效降低水稻莖葉鎘含量。Wang 等[32]的研究表明,低鎘累積水稻品種與高鎘累積水稻品種間莖基鎘含量存在顯著差異,低鎘累積水稻品種D62B莖基鎘含量是高鎘累積水稻品種Wujin4B 的1.57 倍,低鎘累積品種的莖基累積了更高濃度的鎘,降低了鎘向水稻莖葉轉運,莖基對鎘的攔阻作用是影響水稻籽粒中鎘含量的重要原因。Li 等[33]對油菜鎘轉運的研究也表明,莖基是抑制鎘由根部向莖葉中轉運的重要攔阻器官。上述兩篇文獻對莖基含硫化合物濃度變化的研究發現,PCs和GSH 等顯著增加對鎘具有螯合功能的巰基化合物含量,而正是由于這些含硫螯合物含量的增加導致大量鎘被攔阻在莖基中。PCs 和GSH是植物體內重要的解毒物質,它們的分子結構中含有的活性巰基可以和多種重金屬元素如鎘、砷、鉛等形成螯合物[34]。在本研究中,噴施DMSA 顯著增加了水稻莖基鎘含量。當DMSA 噴施濃度達到1.0 mmol·L-1時,莖基鎘含量與CK 處理相比顯著增加了57.3%,鎘由莖基向莖葉中的轉移效率顯著降低了52.7%。與之相應,莖葉中鎘含量則顯著降低了27.8%。同時對莖基含巰基化合物PCs、GSH 的測定結果表明,隨著DMSA 噴施濃度增加,幼苗莖基中PCs 和GSH 的含量分別達到CK 處理的2.2 倍和3.1倍。據此推測,噴施DMSA 增加了莖基巰基化合物PCs和GSH的合成,進而導致大量鎘被PCs、GSH通過螯合作用固定在莖基部位,減少了向莖葉轉運。
水稻通過改變儲存在營養器官中鎘的化學形態從而起到自我解毒的作用[35],一方面通過增加難溶態鎘的含量而降低活性鎘對水稻自身的脅迫作用,另一方面大量研究表明難溶態鎘一般分布于細胞壁與液泡中,因此難溶態鎘含量的增加還可能影響到鎘的亞細胞分布[29]。本研究中隨著DMSA 噴施濃度的增加,莖基難溶態鎘含量與CK 處理相比顯著增加80.8%。由此可見,莖基中雖然儲存了大量的鎘,但是大部分以難溶態形式存在,因此未對水稻幼苗生長造成顯著影響。此外,莖基中鎘大部分以難溶態形式存在減少了儲存在莖基中鎘向幼苗莖葉轉運,本研究中鎘由莖基向莖葉的轉移效率與CK相比顯著降低了52.7%。
3.2 莖基細胞壁對鎘的攔阻作用
植物根部細胞壁是阻礙鎘進入植物細胞的第一道屏障[36]。植物細胞壁主要由果膠、半纖維素、纖維素等多糖構成。其中果膠是一種由ɑ-1,4-半乳糖醛酸聚合鏈構成的多糖,包含大量含有陰離子的羧基基團,因此對金屬陽離子表現出高度親和性,對鎘離子具有強鍵合能力。在所有的細胞壁多糖中果膠是固定鎘的最主要組分,尤其是當果膠脫甲基化以后對鎘的固持能力更加突出[37]。半纖維素包含多種功能基團(如羧基、羥基、醛基),因此也能夠與鎘鍵合阻止鎘向細胞質轉移。植物細胞壁中的半纖維素和果膠在與鎘鍵合過程中發揮最重要作用。鎘脅迫通常會誘導植物根細胞壁中合成更多的果膠和半纖維素,從而導致細胞壁對鎘的持留容量增加[38]。前人研究表明,細胞壁對鎘具有重要的攔截作用,而且大部分攔截的鎘分布在果膠和半纖維素組分中。截止到目前,大部分關于細胞壁攔阻鎘的報道都集中在對水稻根系的研究方面,對莖基和莖稈報道較少。本研究中噴施DMSA 顯著增加了水稻幼苗莖基鎘含量,對幼苗根部鎘含量無顯著影響。對幼苗莖基細胞壁鎘含量的測定結果表明,細胞壁鎘含量隨著DMSA 噴施濃度升高呈現顯著增加趨勢,細胞壁中鎘含量最高達到CK 處理的2.1倍。進一步對細胞壁果膠組分鎘含量的測定結果表明,細胞壁中大部分鎘存在于果膠組分中,其次是半纖維素組分,而且隨著DMSA 噴施濃度增加兩組分中的鎘含量也出現逐漸增加趨勢。以上結果進一步表明,噴施DMSA 增加了水稻幼苗莖基對鎘的攔阻作用,而且莖基中的鎘主要分布在細胞壁的果膠和半纖維素多糖組分中。
3.3 噴施DMSA對鎘脅迫的影響
重金屬脅迫對植物生長具有重要影響,可能導致農作物植株矮小、葉片失綠等,解除鎘脅迫恢復作物正常生長對提高作物產量和品質具有重要意義。噴施葉面阻控劑往往在一定程度上會同時降低營養器官中重金屬含量,因此大部分葉面阻控劑成分都具有一定的緩解重金屬脅迫的功能。Li 等[39]通過水培試驗和田間試驗發現,葉面噴施茉莉酸可以顯著降低水稻籽粒和莖葉中鎘含量,同時還可以顯著提高葉片中CAT、SOD 活性,顯著緩解水稻鎘脅迫。葉面噴施蘋果酸[21]、硅[17]、硒[20]等也可顯著降低鎘含量,緩解鎘脅迫導致的氧化損傷功能。重金屬脅迫引發的氧化損傷往往導致細胞膜損傷,進而產生大量丙二醛(MDA),該指標是表征植物氧化損傷程度的重要指標之一。楊曉榮等[24]的研究表明葉面噴施DMSA 可以顯著減少葉片組織中MDA 含量。本研究中,噴施DMSA 使水稻莖葉中具有抗氧化損傷功能的CAT 和SOD 活性升高,最高分別達到CK 處理的2.7 倍和3.0倍,同時熒光標記試驗結果表明H2O2熒光強度隨著DMSA 噴施濃度升高出現顯著降低,說明葉面噴施DMSA使水稻葉片受到的鎘脅迫得到有效緩解。但是本研究中水稻幼苗根部H2O2熒光強度隨著DMSA噴施濃度升高未出現顯著降低趨勢,同時噴施DMSA也未對根部鎘含量造成顯著影響,這些結果表明噴施DMSA對水稻幼苗根部鎘脅迫無顯著緩解作用。
4 結論
(1)噴施2,3-二巰基丁二酸通過顯著增加水稻幼苗莖基中植物螯合素和谷胱甘肽含量增加了莖基對鎘的攔阻作用,從而減少鎘向莖葉轉運,降低水稻幼苗莖葉中鎘含量。
(2)水稻幼苗莖基中持留的鎘主要被固定在細胞壁果膠組分和纖維素Ⅱ組分中。

