祛濕解毒方內外合治對宮頸人乳頭狀瘤病毒感染的治療效果觀察
王周鳳 周 薇 林 蓉
人乳頭狀瘤病毒(HPV)是一種具有傳染性的小型DNA病毒,無包膜,具有嗜上皮性;侵入機體上皮細胞后,于基底層細胞中復制,再移向表層包裝形成完整的病毒顆粒,通過修飾釋放于上皮表面[1]。當前已發現的HPV分型超過130多種,可依據宮頸癌發生危險性分為高危亞型、低危亞型,高危亞型能夠引起高度宮頸上皮瘤樣病變、宮頸癌及外生殖器癌性病變,其中通過HPV16、18型引發的宮頸癌病變在全部宮頸癌病例中高達70%[2]。臨床上對于高危型HPV持續感染合并低級上皮內瘤病變者,多囑定期觀察或給予局部用藥、物理治療等,無特效干預措施[3]。宮頸HPV感染屬于中醫學中“帶下病”范疇,為受到濕、熱、毒邪侵襲后引發脾腎虛、肝氣郁結,而致氣血瘀滯,濕熱毒侵犯沖任二脈引發帶下病[4]。雖然HPV感染病機以脾腎虛為主,但濕毒作用較強,故可通過補肝腎、清濕毒以改善宮頸糜爛狀態及陰道內局部免疫微環境,促進臨床癥狀緩解,提高HPV轉陰率[5]。本文采用祛濕解毒方內外合治用于宮頸HPV感染,觀察其療效,現報道如下。
1 資料與方法
1.1 對象與分組 選取浙江臨海市中醫院與浙江省臺州醫院2021年6月至2022年6月收治的高危型HPV感染患者168例。西醫診斷:依據宮頸HPV分型測定存在高危型HPV感染[HPV試劑盒(杭州迪安生物技術有限公司)測定],包含HPV16、18、31、33、35、39、45、51、52、56、58、59、66、68亞型,患者在3~6個月間隔隨訪期間,連續兩次及以上檢測出同種亞型的高危型HPV陽性。中醫診斷:依據《中醫婦科學》《中藥新藥臨床研究指導原則(試行)》中擬定氣陰兩虛兼濕熱下注證的中醫辨證標準。納入標準:有正常性生活史;年齡20~55歲;符合同種高危型HPV亞型感染病程超過1年;近3個月未接受宮頸相關治療;經陰道鏡組織活檢發現宮頸上皮內瘤變(CIN)≤Ⅱ級;服藥依從性好。排除標準:存在生殖道炎癥(如支原體、衣原體、滴蟲感染、念珠菌感染性陰道炎);生殖器官出現嚴重病變需手術治療;處于妊娠期或近期有妊娠意愿;存在心血管、糖尿病或其他重要臟器嚴重損害;近半年內服用短效避孕藥;不接受中醫治療。本方案遵循《赫爾辛基宣言》原則,患者均知情同意。按照治療方法不同,分為對照組(50例)、內服組(60例)與聯合組(58例)。
1.2 治療方法 對照組使用重組人干擾素α-2b陰道泡騰膠囊(上海華新生物高技術有限公司,80萬IU/粒),于陰道后穹隆處放置,每日睡前用藥1次。內服組在對照組基礎上服用“自擬祛濕解毒方”,基礎方劑組成:土茯苓18 g,鳳尾草15 g,敗醬草15 g,白花蛇舌草18 g,半枝蓮15 g;加減用藥,高危型HPV持續感染,加黃芪、白術、山藥、車前子、蒼術等;出現腎虛癥狀,可用生地黃、山茱萸、菟絲子;伴有燥熱加用祛濕清熱藥物,如牡丹皮、芒硝、黃柏等;畏寒加用活血化瘀、溫經止痛中藥,如薏苡仁、高良姜、小茴香等;伴血瘀,加活血藥物,如當歸、五靈脂、川芎、紅花等;伴陰部發癢,加用龍膽草、木通;伴有焦慮,加用甘麥大棗湯。溫水煎煮,每日1劑,早晚分服。聯合組在內服組基礎上加用自擬外用祛毒方。方劑組成:苦參50 g,廣藿香20 g,白蘚皮20 g,甘草10 g,蛇床子20 g,生大黃20 g,黃精20 g。溫水煎煮,取100 mL藥汁于睡前稀釋至1 000 mL,先用10 mL注射器抽吸待冷卻,其余藥物趁熱氣先熏蒸,降溫后再清洗會陰(注意使用無菌紗布),最后將冷卻的10 mL藥物噴注射于陰道,隔日用藥1次,經期停藥。三組均連續治療3個月。
1.3 觀察指標 ① 宮頸HPV感染臨床癥狀評分,依據《中藥新藥臨床研究指導原則(試行)》中相關標準判定,共計9項內容,每項3分,分數越高表示癥狀越嚴重。② 轉歸情況,依據《中醫病癥診斷療效標準》相關內容判定。轉陰:HPV檢測為陰性;顯效:高危HPV感染病毒載量降低;病情進展:陰道鏡及宮頸組織活檢為更高級別鱗狀上皮內病變,或病毒持續存在。轉陰與顯效合計為有效。③ 三組不良反應發生情況。
2 結果
2.1 三組一般資料比較 由表1可見,三組一般資料接近。
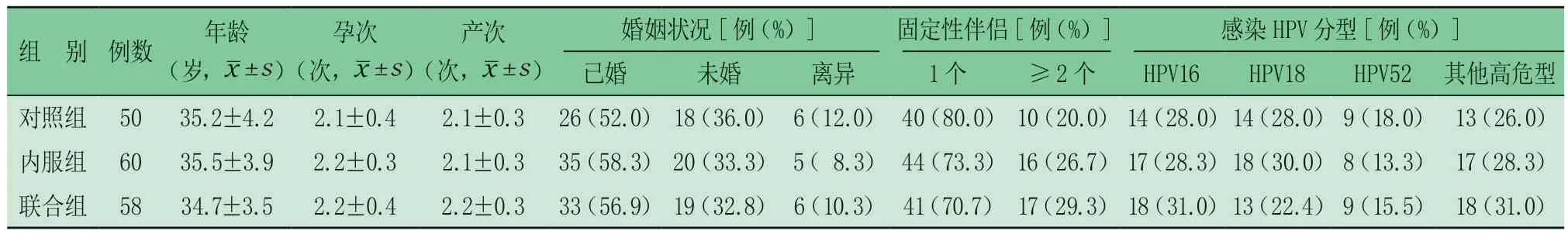
表1 三組一般資料比較
2.2 三組轉歸情況比較(表2) 三組治療期間均未發生明顯不良反應。治療3、6個月后,聯合組的有效率82.0%(41/58)、84.5%(49/58)高于內服組[63.3%(38/60)、68.3%(41/60)]、對照組[60.0%(30/50)、64.0%(32/50)]。
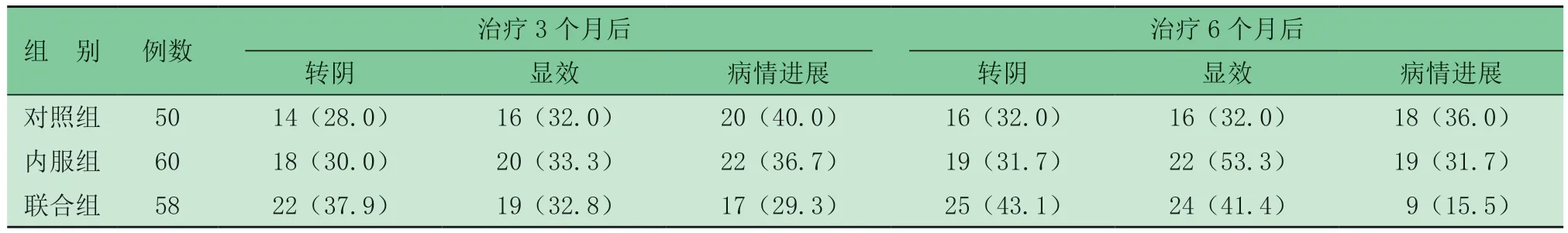
表2 三組轉歸情況比較 [例(%)]
2.3 三組治療前后宮頸HPV感染臨床癥狀評分變化 由表3可見,治療前三組各項宮頸HPV感染臨床癥狀評分及總分接近。治療6個月后,內服組的宮頸HPV感染臨床癥狀評分低于對照組,聯合組的宮頸HPV感染臨床癥狀評分低于內服組、聯合組。
表3 三組治療前后宮頸HPV感染臨床癥狀評分變化 (分,)
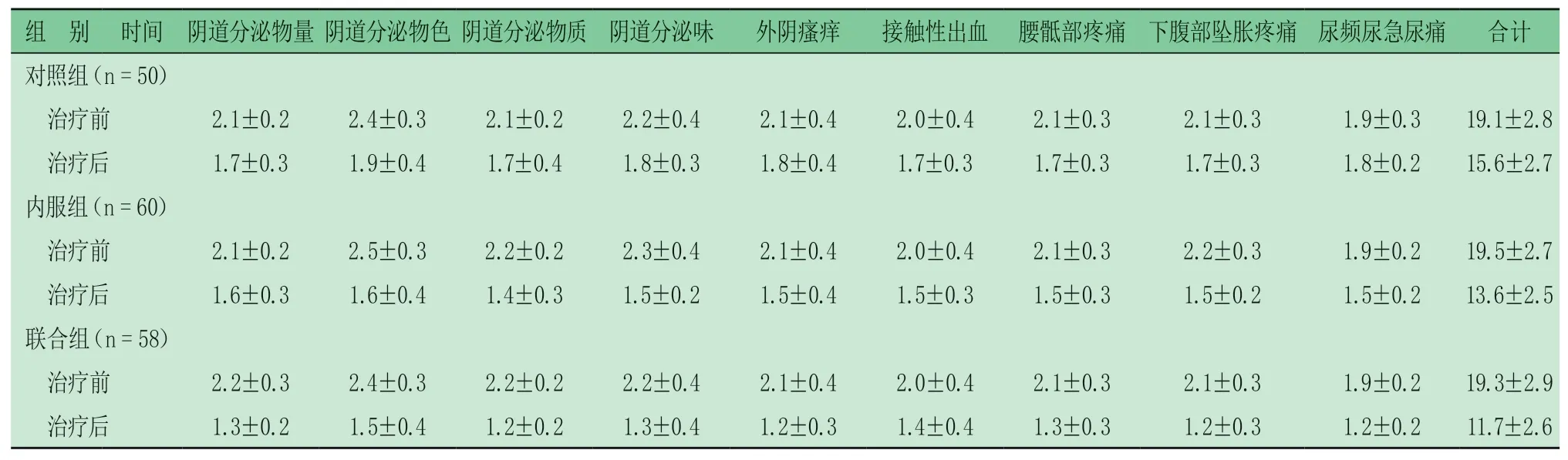
表3 三組治療前后宮頸HPV感染臨床癥狀評分變化 (分,)
組 別時間陰道分泌物量陰道分泌物色陰道分泌物質陰道分泌味外陰瘙癢接觸性出血腰骶部疼痛下腹部墜脹疼痛尿頻尿急尿痛合計對照組(n = 50)治療前2.1±0.22.4±0.32.1±0.22.2±0.42.1±0.42.0±0.42.1±0.32.1±0.31.9±0.319.1±2.8治療后1.7±0.31.9±0.41.7±0.41.8±0.31.8±0.41.7±0.31.7±0.31.7±0.31.8±0.215.6±2.7內服組(n = 60)治療前2.1±0.22.5±0.32.2±0.22.3±0.42.1±0.42.0±0.42.1±0.32.2±0.31.9±0.219.5±2.7治療后1.6±0.31.6±0.41.4±0.31.5±0.21.5±0.41.5±0.31.5±0.31.5±0.21.5±0.213.6±2.5聯合組(n = 58)治療前2.2±0.32.4±0.32.2±0.22.2±0.42.1±0.42.0±0.42.1±0.32.1±0.31.9±0.219.3±2.9治療后1.3±0.21.5±0.41.2±0.21.3±0.41.2±0.31.4±0.41.3±0.31.2±0.31.2±0.211.7±2.6
3 討論
HPV感染后累及CIN的病理機制,考慮原因為細胞增殖指標及Th1、Th2平衡紊亂引發,機體感染HPV病毒后,宮頸局部免疫環境中上述指標失衡,Th1細胞因子合成減少,使得T細胞活化的Th2細胞合成增加,并呈現出優勢表達,清除病毒的能力降低,參與并推進宮頸疾病病程[6]。重組人干擾素α-2b泡騰膠囊經陰道給藥后,能夠通過與病變部位的干擾素相結合,阻斷HPV外殼上的α受體,減少其活性釋放,進而減輕病毒侵襲對宮頸的損傷,但該藥物對病毒的作用靶點尚不明確,療效不理想[7]。
《黃帝內經》中最早出現“帶下病”的概念,提出病在子門,損及脾、腎等臟腑,帶下病的發生與各種因素致使濕邪侵襲機體有關[8]。故筆者認為,從“濕毒瘀結”病機作為基礎擬定“祛濕解毒方”具有可行性。本文所用的解毒方劑經由具有多年臨床經驗的教授擬定,其認為HPV持續感染雖然由“濕毒”引起,但患者的臨床表現以濕邪侵襲為主,故在治療方式上以解毒藥物為基礎進行加減,可發揮較好的作用。方劑中土茯苓、敗醬草、半枝蓮等藥物,具有解毒、除濕、治療濕熱淋濁、帶下等效果較好的特點。土茯苓常用以治療梅毒、淋病、滴蟲性陰道炎,能夠有效抑制體外實驗對子宮癌培養株系JTC226[9];白花蛇舌草的抗菌消炎作用較好,常與半枝蓮以藥對方式出現,在誘導腫瘤細胞凋亡及增強免疫力方面效果明顯;鳳尾草的抗病毒、抗腫瘤效果較好;敗醬草能夠抑制革蘭陽性/陰性桿菌及部分鏈球菌發揮抗菌作用,并可增強人體免疫力。本文結果表示,在干擾素α-2b陰道泡騰膠囊基礎上加用祛濕解毒方劑能夠強化治療效果,調整機體狀態,而改善患者臨床癥狀,但仍不能達到理想效果。
外治法屬于中醫治療學的組成部分,早在《素問·至真要大論》中提出“內者內治、外者外治”理論,尤其用于婦科某些局限于陰道、宮頸、外陰的疾病,藥物可直達病灶進而發揮祛除病邪作用。本文所用自擬外用祛毒方劑中,白蘚皮具有祛風止癢、清熱燥濕功效,可抗菌及抗非特異性炎癥;藿香具有清熱、化濕功效,可抑制革蘭陽性菌、大腸桿菌、金黃色葡萄球菌;甘草的止痛、清熱解毒及抗病毒效果良好,苦參在治療宮頸癌方面療效確切,蛇床子能夠抑制宮頸癌Hele細胞增殖而誘導細胞凋亡[10]。方藥按照內服方法煎煮后外用熏洗,可讓其被局部黏膜吸收,從而提升其生物利用度,更好地調節宮頸部糜爛狀況及陰道內區域的免疫微環境,使局部免疫細胞功能有效發揮,則病毒可被抑制。本文結果顯示,聯合組的臨床癥狀緩解程度、HPV轉歸率優于內服組與對照組。冷靜等[11]研究得出結論,中藥內服結合外用法可有效提高HPV轉歸率,與本文結果相符。
綜上所述,從“濕毒”角度提出中藥內外合治用于高危型HPV感染患者,可有效緩解臨床癥狀,提升轉陰率,且聯合用藥安全性良好。

