胃癌合并腦梗死的臨床特點及危險因素分析
王英南,趙 琦,白海威,武丹娜,魏金梅,李省江,李銳凌,張瑞星
(1.河北醫科大學第四醫院 消化內科,河北 石家莊 050000; 2.清河縣中心醫院 消化內科,河北 邢臺 054800; 3.河北醫科大學第四醫院 神經內科,河北 石家莊 050000; 4.平鄉縣人民醫院 內分泌科,河北 邢臺 054500; 5.平鄉縣人民醫院 神經內科,河北 邢臺 054500)
胃癌(gastric cancer, GC)是世界范圍內最常見的惡性腫瘤之一,發病率居所有惡性腫瘤的第5位,病死率居第4位,嚴重威脅著人們的生命健康[1]。中國更是GC大國,據2020年研究數據表明,中國每年新發病例45.7萬,死亡病例30.0萬,無論發病人數還是死亡人數,均居全球第一,防控形勢嚴峻[2]。GC所伴隨的并發癥多種多樣,常見的并發癥包括消化道出血、賁門或幽門梗阻、穿孔等,而少見的并發癥包括腦梗死(cerebral infarct, CI)、非細菌性血栓性心內膜炎、乳糜胸等[3-4]。其中CI在GC患者中的發病率逐年升高,胃癌合并腦梗死(gastric cancer-related stroke,GCS)不僅嚴重降低患者的生活質量,也會影響GC的針對性治療,降低患者的生存率。
CI又稱缺血性腦卒中,是因腦部血液供應障礙,缺血、缺氧所導致的局限性腦組織的缺血性壞死或軟化,已成為現代社會致死和致殘的最重要中樞神經系統血管事件。目前,隨著癌癥發生率及生存率的不斷增加,血栓栓塞事件,包括CI的風險也不斷上升。有相關研究發現,高達15%的癌癥患者可能患有CI[5]。此外,CI患者惡性腫瘤的發生率也比正常人高[6]。有趣的是,在惡性腫瘤的早期,發生CI的風險更高[7]。本研究通過探究GCS患者的臨床特點,并進一步分析影響GC患者發生CI的危險因素,旨在針對特定人群進行早期預警及干預,預防及降低GCS的發生。
1 資料與方法
1.1病例選擇 納入2014年1月至2019年12月在河北醫科大學第四醫院確診并在診治過程中新發腦梗死的GC患者(GCS組)42例,并選取同期就診并在診治過程中未出現過新發腦梗死的GC患者(對照組)84例。GC患者全部經病理明確診斷為腺癌,其中GCS患者均為確診GC后在診治過程中突然出現肢體無力、麻木、言語不清等局灶性神經功能缺損的癥狀和體征,經頭顱電子計算機斷層掃描(computer tomography,CT)及磁共振成像(magnetic resonance imaging,MRI)證實顱內有可以解釋癥狀的新發病灶,CI的診斷符合2014年中國急性缺血性腦卒中診治指南。GC未合并CI患者均在河北醫科大學第四醫院確診GC,并可以追溯隨訪到完整的腫瘤診療史,確保在GC治療過程中無新發CI。排除標準:①顱內原發性惡性腫瘤及顱內繼發轉移惡性腫瘤患者;②合并其他部位腫瘤;③合并腦出血、腦膿腫、放射性腦病、腦炎等顱內有異常信號的疾病;④病情嚴重瀕亡;⑤GC確診并臨床治愈后,超過5年無復發轉移患者;⑥合并其他嚴重并發癥。本研究通過醫院倫理委員會批準,患者及其家屬知情同意。
1.2方法 收集所有患者確診GC時的一般人口學資料、實驗室常規檢查、腫瘤學資料。一般人口學資料包括性別、年齡、高血壓病史、糖尿病病史、高脂血癥史(既往空腹血清膽固醇水平≥200 mg/dl或低密度脂蛋白膽固醇水平≥140 mg/dl)、冠心病病史、吸煙史、飲酒史、既往CI病史等。實驗室常規檢查包括血常規、凝血功能及腫瘤標記物(包括CEA、AFP、CA-199及CA-724)等。腫瘤學資料包括腫瘤部位、分期,以及GC確診后至最后一次隨訪期間的GC治療史(包括手術史、放療史、介入史、化療史及靶向治療史)等。
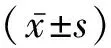
2 結 果
2.1GCS患者臨床特點 本研究共收集42例GCS患者,其中男性34例,女性8例,年齡47~86歲,平均年齡(67.14±8.15)歲,所有GC患者病理類型均為腺癌。CI發生在GC診斷后的0~985 d,中位發病時間為38 d,其中CI發生在GC診斷后的1個月內17例(40.5%),CI發生在GC診斷后6個月內27例(64.3%)。38例(90.5%)患者CI發生前存在1個或幾個CI危險因素,包括高血壓病史、糖尿病病史、冠心病史、高脂血癥史、既往CI病史、吸煙史及飲酒史等。所有患者均是在GC診治過程中突然起病,表現為單側或雙側肢體活動不利22例(52.4%),表現為言語不利11例(26.2%),出現麻木等感覺障礙7例(16.7%),出現嗜睡、譫妄等意識障礙3例(7.1%)。起病時美國國立衛生研究院卒中量表(nationalinstitution health stroke scale,NIHSS)評分為1~25分。頭顱MRI提示顱內多個病灶、多部位受累22例(52.4%)。因CI后續未再進行GC的針對性治療25例(59.5%)。
2.2影響GC患者發生CI的危險因素
2.2.1 一般人口學資料 GCS組高血壓病史、糖尿病病史、高脂血癥史及既往CI病史比例高于對照組(P<0.05),而性別、年齡、冠心病病史、吸煙史、飲酒史等差異均無統計學意義(P>0.05),見表1。

表1 兩組一般人口學資料比較[例(%)]
2.2.2實驗室指標 GCS組血漿凝血酶原時間(plasma thrombin time,PT)、D-二聚體(D dimer,D-D)及糖類抗原199(carbohydrate antigen199,CA-199)高于對照組,而血紅蛋白(hemoglobin,HGB)低于對照組,差異均有統計學意義(P<0.05)。兩組白細胞(white blood cell,WBC)計數、中性粒細胞計數(neutrophil count,NEUT)、血小板計數(platelet count, PLT)、紅細胞(red blood cell,RBC)計數、平均血小板體積(MPV)、部分凝血活酶時間(activated partial thromboplastin time,APTT)、纖維蛋白原(fibrinogen,FIB)、癌胚抗原(carcinoembryonic antigen,CEA)、甲胎蛋白(alpha fetoprotein,AFP)及糖類抗原724(carbohydrate antigen 724, CA724)差異均無統計學意義(P>0.05)。見表2~3。
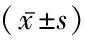
表2 兩組血常規、凝血功能比較
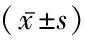
表3 兩組腫瘤標記物比較
2.2.3腫瘤學資料 GCS組手術史及化療史比例低于對照組,差異均有統計學意義(P<0.05),而兩組腫瘤部位、分期、放療史、介入史、化療周期以及是否聯合靶向藥物差異均無統計學意義(P>0.05)。見表4。

表4 兩組腫瘤學資料比較
2.2.4影響GC患者發生CI的危險因素 以GC患者發生CI為因變量,將兩組差異有統計學意義的因素(包括高血壓病史、糖尿病病史、高脂血癥史、既往CI病史、HGB、PT、D-D及CA-199)為自變量,引入多因素Logistic回歸分析,結果顯示:既往CI病史是GC患者發生CI的獨立危險因素,見表5。

表5 多因素分析影響胃癌患者發生腦梗死的危險因素
3 討 論
GC被認為是最易形成血栓的腫瘤類型之一,腫瘤細胞不僅可直接刺激血栓形成,還可通過促凝活性的增高及抗凝活性的降低導致血液凝固增強,從而引起癌癥相關血栓的形成[8-9]。有學者進行尸解研究發現,約14.6%的腫瘤患者存在腦卒中,其中7%為缺血性。近年來,GC患者CI的發病率逐年上升,迫切需要了解GCS患者的臨床特點以及影響GC患者CI的危險因素,以針對特定人群進行早期預警及干預,降低GCS的發生率。本研究發現GCS患者中位發病時間為38 d,其中40.5%的患者CI發生在GC診斷后的1個月內,64.3%的患者發生在GC診斷后6個月內。有研究表明,確診惡性腫瘤后發生CI的高峰在6個月以內[10]。與此相同的是,Saito等[11]研究發現,癌癥患者在確診癌癥后的1~3個月內患CI及腦中風的風險升高。Majmudar等[12]研究共納入612例GC和急性靜脈血栓栓塞患者,這些患者從癌癥診斷到靜脈血栓形成的中位時間為14周(3~44周),提示在惡性腫瘤活躍期CI風險增加。因此在確診GC后的6個月內,尤其是1個月內,應高度警惕CI的發生,積極采取相應的預防措施,如糾正貧血、改善營養狀況、治療傳統腦卒中相關疾病等,以避免GCS的發生[13]。
本研究中GCS組90.5%的患者CI發生前存在1個或幾個腦卒中危險因素,且與對照組相比,GCS組高血壓病史、糖尿病病史、高脂血癥史及既往CI病史比例高于對照組,表明傳統的腦卒中危險因素同樣是癌癥患者發生腦卒中的主要危險因素。多因素分析顯示,既往CI病史是GC患者發生CI的獨立危險因素之一,提示GC患者如果既往有CI病史,再次發生CI的風險明顯增加,臨床醫生應提高警惕,早期對患者進行篩查[14]。此外,本研究發現GCS組PT、D-D及CA-199水平較對照組高,而HGB水平較對照組低,這也與既往研究報道一致[15-16]。有研究發現血紅蛋白降低是急性卒中3個月和1年死亡率的預測因子[17]。貧血致CI的機制可能與充血性腦栓塞、炎癥介質增加、血液黏度改變和組織缺氧有關[18]。另外,D-D作為繼發性纖溶代謝產物,其水平升高提示機體處于高凝狀態,是惡性腫瘤患者發生缺血性腦卒中的獨立危險因素[19]。研究發現,癌癥合并腦梗死患者的D-二聚體水平明顯高于不伴有癌癥的腦梗死患者[20]。本研究還發現GCS組CA-199水平高于對照組,可能是因為本研究納入的GC患者病理類型全部為腺癌。有研究共納入31例癌癥合并CI的患者,31例癌癥患者均經病理活檢證實為腺癌,患者CEA、CA125和CA199水平較高,可能機制是腺癌產生的黏蛋白可導致血液高凝狀態,直接激活凝血酶原,并將其轉化為凝血酶,進一步激活凝血系統,然后與白細胞和血小板選擇素發生反應,形成富含血小板的微血栓,進而導致CI[21-22]。
與傳統動脈粥樣硬化性CI不同,腫瘤相關CI常表現為多發病灶、累及多支血管供血區[22],本研究52.4%的患者頭顱MRI提示急性CI病灶分布與前述類似,而且其中4例表現為多部位CI的患者無傳統CI危險因素。由此我們推測,合并惡性腫瘤發生急性CI的病理生理機制可能與惡性腫瘤導致的高凝狀態有關。此外,本研究中59.5%的患者因為CI的發生導致后續未再進行GC的針對性治療,且GCS組手術史及化療史比例低于對照組,提示惡性腫瘤合并CI患者預后不良,針對本病的治療水平尚有待提高。Davies等[23]研究發現,癌癥合并腦卒中患者的中位生存期為4.5個月,雖然42.5%的患者接受了靜脈溶栓治療和(或)血管內血栓取出術,但生存期仍較短。因此探索惡性腫瘤合并CI的發病機制及治療方法均有重要的意義。
綜上,CI在GC診斷后的1~6個月內高發,傳統的腦卒中危險因素同樣是GC患者發生CI的主要危險因素。多因素分析顯示,既往CI病史為GC患者發生CI的獨立危險因素。GCS患者由于喪失了針對GC治療的機會,多預后不良。因此探索GCS的臨床特點及危險因素,可指導臨床醫師對特定人群進行早期預警及干預,預防及降低GCS的發生。

