帶量采購前后左乙拉西坦片的應用及血藥濃度分析
余靜潔,史 蕾,柳思宇,劉 婷,沈 倩,張向輝,夏夢凡,張抗懷
0 引言
為深化醫藥衛生體制改革,完善藥品價格形成機制,2018年11月14日,在開展仿制藥一致性評價基礎上,中央全面深化改革委員會第五次會議審議通過《國家組織藥品集中采購試點方案》,明確了國家組織、聯盟采購、平臺操作的總體思路,以北京、上海、西安等11個城市為試點開展帶量采購工作。雖然中選品種均通過一致性評價,但二者能否互相替代、慢病患者能否安全轉換等問題仍存疑[1-2]。臨床藥師作為藥學與臨床的橋梁,能夠利用藥學相關技術開展多維度研究,利用真實世界研究多角度驗證中選與原研品種的臨床一致性,幫助醫生及患者合理轉換藥物。
原研藥左乙拉西坦片(開浦蘭)于1999年首次被FDA批準在美國上市,于2007年進入中國市場,自專利到期以來已有多個仿制藥品種上市。抗癲癇藥物屬于低治療指數/嚴格劑量藥物(NTI/CD Drugs),因血藥濃度出現微小變化即可導致藥代動力學出現顯著變化,因此在臨床使用過程中需進行治療藥物濃度監測(Therapeutic drug monitoring,TDM)。部分研究表明,相當比例的患者在更換為仿制藥后,癲癇發作控制不佳或不良反應增加,迫使其重新使用原研制劑[3-4],而血藥濃度是癲癇控制效果及不良反應發生的重要影響因素之一[5]。一致性評價工作開展以來已取得明顯進展,但目前主要集中在經濟性、臨床療效、安全性等方面,且對于左乙拉西坦的相關研究較少,尚無原研與中選品種血藥濃度對比的報道[6-7]。本研究對帶量采購政策實施前后左乙拉西坦用藥情況進行統計分析,采用傾向性評分匹配(Propensity score matching,PSM)矯正患者基線,探索在真實診療環境下原研與中選品種血藥濃度的一致性,為慢病藥物合理轉換、進一步推進帶量采購政策提供參考。
1 資料與方法
1.1 一般資料 通過西安交通大學第二附屬醫院HIS系統調取左乙拉西坦片進入帶量采購目錄前2年(即2017年3月25日-2019年3月24日)和進入目錄后3年(即2019年3月25日-2022年3月24日)門急診和住院部中選品種及原研藥品使用相關數據,包括藥品名稱、規格、數量、金額等。本次調查中原研藥品為左乙拉西坦片(UCB Pharma S.A.,國藥準字HJ20160253,開浦蘭,0.25 g×30片),帶量采購中選品種為左乙拉西坦片(浙江京新藥業股份有限公司,國藥準字H20143177,吉易克,0.25 g×30片)。
收集2019年4月-2021年1月西安交通大學第二附屬醫院小兒內科施行集采政策后使用中選及原研左乙拉西坦片患兒的性別、年齡、體重、日劑量、血藥濃度、聯合用藥等基本信息。納入標準:①診斷為癲癇;②4~17歲;③體重<50 kg;④服用左乙拉西坦達到穩態血藥濃度;⑤1個月內未更換過藥物廠家者。排除標準:①診斷為癲癇綜合征的患者;②血藥濃度超過監測下限;③非谷濃度;④聯合使用2種以上抗癲癇藥物;⑤聯合使用卡馬西平及苯巴比妥者。晨起給藥前采集血樣2~3 ml作為血藥濃度監測樣本,共收集中選品種血樣191份,原研組血樣226份。
1.2 方法 用藥頻度(DDDs)=藥品消耗量/限定日劑量(DDD),左乙拉西坦的DDD為1.5 g[7]。DDDs反映了藥品的使用頻率,DDDs越高,使用頻率越高,選擇的傾向性越大。將藥品價格轉換為日均費用(Daily drug cost,DDC),DDC=藥品的用藥金額/DDDs,DDC反映了藥品的平均日費用情況,DDC越高說明患者經濟負擔越重。
采用高效液相色譜方法,以甲硝唑為內標,對全血中左乙拉西坦濃度進行分析。通過方法學考察確立檢測條件,得到血藥濃度(C,μg/ml),根據體重計算每千克體重日劑量(D,mg/kg),對比兩組血藥濃度/劑量比[C/D,(μg/ml)/(mg/kg)]是否存在顯著差異。
為減少回顧性研究的偏差和混雜變量的影響,對原研組和中選組數據進行處理,通過入組篩選剔除合并癥及聯合用藥對左乙拉西坦濃度的影響,采用PSM法對使用原研與中選品種的患兒進行組間基線校正。PSM納入的協變量包括年齡、體重、左乙拉西坦給藥劑量(mg/kg)。按1∶1最鄰近匹配和匹配容差0.02進行匹配。

2 結果
2.1 左乙拉西坦消耗量和DDDs 2019年3月實施帶量采購政策前,國產左乙拉西坦片消耗量占總消耗量的17.88%,政策實施后占比為69.04%,與2017年未施行政策相比,2022年中選左乙拉西坦消耗量提高630.49%,DDDs增加6倍余,見表1。

表1 中選及原研左乙拉西坦消耗量和DDDs
2.2 左乙拉西坦用藥金額和DDC 2019年3月實施帶量采購政策前,國產左乙拉西坦片用藥金額占總金額的10.88%,政策實施后占比逐年提升,最高為57.59%,與2017年未施行政策相比,2022年左乙拉西坦用藥金額下降24.58%,DDC降至11.47元,降幅35.42%,見表2。
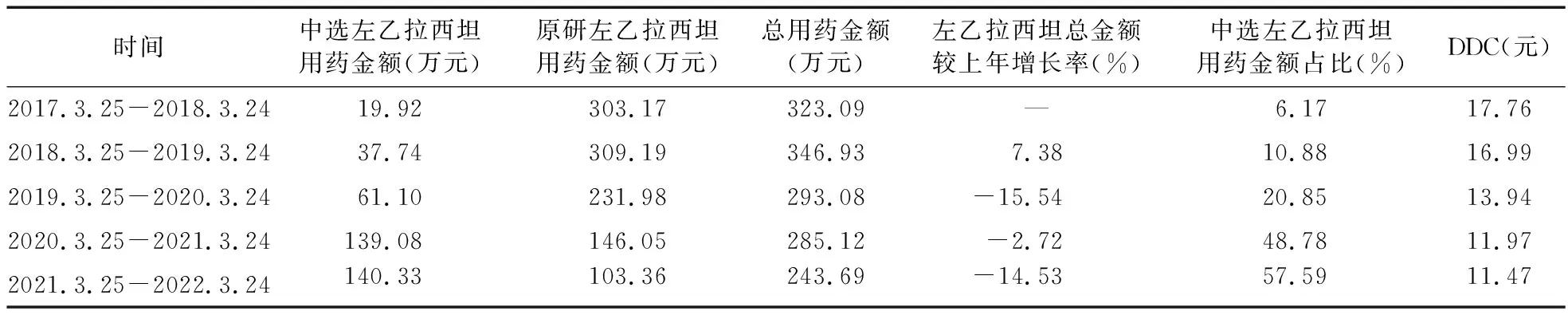
表2 中選及原研左乙拉西坦用藥金額和DDC
2.3 中選及原研左乙拉西坦片濃度劑量(C/D)比 本研究共納入中選左乙拉西坦片血藥濃度191人次,原研濃度226人次。采用PSM前患兒年齡及體重差異有統計學意義(P<0.05),導致兩組患兒左乙拉西坦平均日劑量有明顯區別,中選品種平均日劑量為(850.03±333.70)mg/d,進口品種平均日劑量為(707.67±267.27)mg/d。按照1∶1的比例成功匹配123例患者,匹配后兩組患者年齡、體重、平均日劑量比較,差異無統計學意義(P>0.05),具有可比性,匹配后的每日公斤體重劑量及兩組濃度劑量比差異均無統計學意義(P>0.05),見表3。
3 討論
藥物至今仍是癲癇的首選治療方式。最新數據顯示,全球約有7 000萬癲癇患者,我國已超過千萬人,且每年新增癲癇患者達65~70萬,癲癇在世界疾病負擔排名中位居第四[8-9]。Begley等[10]對全球約5 251萬癲癇患者人均費用回顧分析顯示,約80%的癲癇患者生活在低收入和中等收入國家,各國抗癲癇平均年花費從低收入國家的204美元到高收入國家的11 432美元不等。王冰玉等[11]對我國不同地區門診癲癇患者的經濟負擔現狀進行分析,收入最低的家庭中,癲癇患者年度門診診療費用已占其人均年收入的71.7%。多項研究顯示,我國帶量采購政策的實施切實降低了部分患者的經濟負擔,中選品種在治療過程中存在巨大的經濟優勢,在降低醫療成本的同時優化了醫保費用結構[12-14]。本研究通過對比實施帶量采購政策前后左乙拉西坦片數量、金額等數據,發現左乙拉西坦片作為國家首批及第一個抗癲癇帶量采購藥品,在政策實施后,患者及醫務人員接受度及執行率逐年升高,截至2022年3月,中選品種使用量提升至近70%,原研品種使用量逐漸下降。左乙拉西坦日均治療費用由2017年的17.76元降至11.47元,截至2022年3月政策實施3年后,其治療費用降幅達35.42%,與楊黎等[7]政策實施近1年后DDC降幅23.22%相比,經濟優勢更加明顯。中選左乙拉西坦片的推廣使得部分癲癇患者經濟負擔明顯下降,同時減少了醫保相關支付壓力。
抗癲癇藥物的仿制藥替換一直備受爭議,近年來國內外多項研究及報道均顯示,抗癲癇仿制藥替換可增加癲癇復發和發作的頻率,甚至有可能是癲癇復發的獨立危險因素[15-16],且我國目前尚無左乙拉西坦原研與仿制品種濃度對比的報道,考慮兒童患者劑量需根據體重進行計算,因此本研究針對中選與原研左乙拉西坦片濃度劑量比進行比較。采取PSM減少兩組患者年齡、體重、給藥劑量差異的影響,結果證實,在左乙拉西坦說明書推薦適應人群及用法用量下,無論癲癇患兒年齡與體重是否有統計學差異,濃度劑量比差異均無統計學意義,與Reimers等[5]和Contin等[17]研究結論一致。同時,本研究結果也與此前本院小兒內科一項前瞻性自身對照研究結果一致,50例癲癇患兒由左乙拉西坦原研轉換為中選品種,其臨床有效率、公斤體重劑量及濃度劑量比差異均無統計學意義,提示中選品種臨床療效并不劣于原研藥。
本研究基于真實世界臨床數據回顧性研究左乙拉西坦原研與中選品種濃度劑量比差異,同時采取PSM盡量減少組間基礎數據偏差,具有一定可信度。但也存在一些局限:研究樣本量較小,為單中心研究,數據代表性有限;僅就濃度劑量數據層面進行對比,未對患者進行有效性及安全性評價,無法從結論推斷二者具有臨床等效性,還需進一步擴大樣本深入研究。
基于本研究結果,對于兒童癲癇患者采用中選左乙拉西坦片替換原研品種,濃度劑量比無明顯差異,而在經濟性方面存在明顯優勢,初步證實了中選品種替換方案值得推廣,但仍需要更大規模的隨機、雙盲、對照、前瞻性研究,結合臨床療效、安全性及血藥濃度來進一步證實。

