以磷鐵為原料水熱法制備電池級磷酸鐵的研究
李珍珍
(龍佰集團股份有限公司,河南 焦作 454006)
0 引言
磷酸鐵鋰由于具有高理論容量、高工作電壓、循環性能好、無記憶效應等優良性能,且具有價廉、環境友好的優點,因此具有取代成本較高的LiCoO2而成為新一代鋰離子電池正極材料,而且有望成為電動汽車等所需大型儲能電池的重要材料。固相反應法是目前磷酸鐵鋰生產和研究過程中廣泛使用的方法,磷酸鐵逐漸成為碳熱還原法中制作磷酸鐵鋰的重要前驅體[1-2]。
磷鐵是電爐法黃磷生產中的一種副產物,是FeP、Fe2P、Fe3P 與FeP2的混合物,其中w(P)為20%~30%,w(Fe)為70%~80%。在化學工業上,磷鐵可以用于制備磷酸三鈉及鐵紅等產品。由于環保意識的加強,目前磷酸三鈉在洗滌劑中使用量大大降低,國內黃磷廠家生產的副產品磷鐵經過簡單加工后用于出口,出于對資源的保護,國內對于磷鐵的出口有所限制,因此,開發磷鐵資源,成為資源的再利用與磷化工可持續發展的研究課題[3]。鑒于磷鐵中磷與鐵的含量,結合磷酸鐵鋰制備中磷酸鐵的需求,因此,利用磷鐵制備電池級磷酸鐵即解決資源再生問題,又符合新能源材料發展需求。
1 實驗材料與方法
1.1 實驗原料
磷鐵,龍佰集團股份有限公司黃磷生產副產物磷鐵,Fe、P、Mn、Ti、Ni、Cr 的質量分數分別為63.74%、20.77%、0.98%、0.34%、0.02%、0.017%;貴州某企業黃磷生產副產物;磷酸-H3PO4(AR)、硝酸-(HNO3)(AR),國藥集團化學試劑上海有限公司。
1.2 實驗儀器
FCF 系列升降型高溫高壓反應釜,河南佰年儀器有限公司;EA3000 元素分析儀,意大利EURO 公司;D8ADVANCE 衍射儀,德國布魯克公司生產;Icp-ms等離子體質譜儀,德國SPECTRO。
1.3 實驗方法
1.3.1 電池級磷酸鐵的制備與表征
將磷鐵原料研磨至200~300 目(0.05~0.074 mm),稱取一定量磷鐵樣品、磷酸、硝酸于高壓反應釜的聚四氟內膽中。設定高壓反應釜電機轉速、反應溫度、反應時間,經冷卻、抽濾、洗滌、干燥后得到磷酸鐵樣品,對磷酸鐵樣品進行表征[4]。
1.3.2 磷酸鐵鋰的制備
以磷酸鐵樣品為原料,加入一定比例的Li2CO3和葡萄糖,采用無水乙醇為分散劑,采用高溫固相加熱法制備磷酸鐵鋰樣品,對磷酸鐵鋰樣品進行表征[5]。
2 結果與討論
2.1 反應條件對制備電池級磷酸鐵的影響
2.1.1 硝酸濃度
設定其他反應條件不變的情況下,研究加入不同的硝酸濃度(0、2.5、3.0、3.5、4.0 mol/L)對制備電池級磷酸鐵的影響,以鐵離子轉化率定義電池級磷酸鐵的產率,實驗結果如圖1 所示。

圖1 不同硝酸濃度對制備電池級磷酸鐵的影響
當反應中加入的硝酸濃度為0.00 mol/L 時,無電池級磷酸鐵生成,有70%左右的磷鐵未溶解,該反應條件中無硝酸時,磷鐵無法進行有效溶解,后期反應無法進行。當反應中加入的硝酸濃度從0 增加到4.0 mol/L 時,產品中w(Fe)和n(Fe)/n(P)均表現為先增加后下降趨勢,當加入的硝酸濃度為3.0 mol/L 時,產品中w(Fe)和n(Fe)/n(P)均達到最大值,分別為28.8%、1.02。加入的硝酸能分解生成氧氣,進而生成FePO4·2H2O,加入硝酸濃度增加,進而生產的FePO4·2H2O 也相應增加;當硝酸濃度超過3 mol/L 時,加入的硝酸能抑制三價鐵子的水解,導致生成FePO4·2H2O 量降低,此時隨著硝酸濃度的增加,w(Fe)和n(Fe)/n(P)表現出下降趨勢。確定加入最佳硝酸濃度為3.0 mol/L。
2.1.2 反應溫度
設定其他反應條件不變的情況下,研究不同的反應溫度(100、110、120、130 ℃)對制備電池級磷酸鐵的影響,以鐵離子轉化率定義電池級磷酸鐵的產率,實驗結果如圖2 所示。
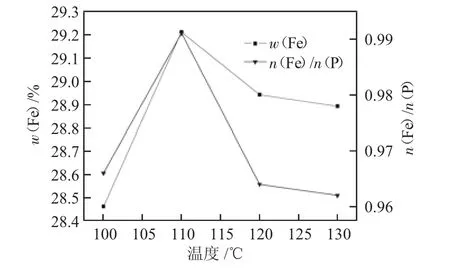
圖2 不同反應溫度對制備電池級磷酸鐵的影響
從圖2 數據可知,當反應溫度從100 ℃增加到130 ℃的過程中,產品w(Fe)和n(Fe)/n(P)表現為先增加后下降趨勢,當反應溫度為110 ℃時產品中w(Fe)和n(Fe)/n(P)均達到最大值,分別為29.24%、0.993;當反應溫度超過110 ℃,w(Fe)和n(Fe)/n(P)開始下降,這是因為溫度過高時三價鐵離子會發水反應生成Fe(OH)3。確定最佳反應溫度為110 ℃。
2.1.3 反應時間
設定其他反應條件不變的情況下,研究不同的反應時間(60、90、120、150 min)對制備電池級磷酸鐵的影響,以鐵離子轉化率定義電池級磷酸鐵的產率,實驗結果如圖3 所示。
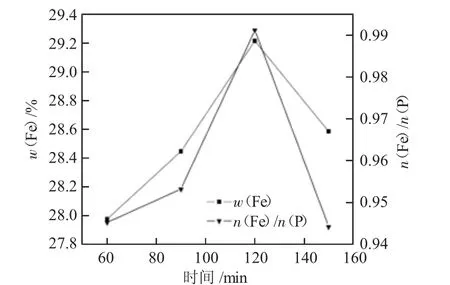
圖3 不同反應時間對制備電池級磷酸鐵的影響
從圖3 數據可知,當反應時間從60 min 增加到150 min 的過程中,產品w(Fe)和n(Fe)/n(P)表現為先增加后下降趨勢,當反應時間為120 min 時產品中w(Fe)和n(Fe)/n(P)均達到最大值,分別為29.28%、0.992;當反應時間超過120 min 后,w(Fe)和n(Fe)/n(P)開始下降,這是因為反應時間過長,樣品會異常長大,還會有副反應等發生[6]。確定最佳反應時間為120 min。
2.1.4 體系濃度
設定其他反應條件不變的情況下,研究不同的水熱反應體系(鐵質量濃度分別為22.0、20.0、18.0、16.0 g/L)對制備電池級磷酸鐵的影響,以鐵離子轉化率定義電池級磷酸鐵的產率,實驗結果如圖4 所示。
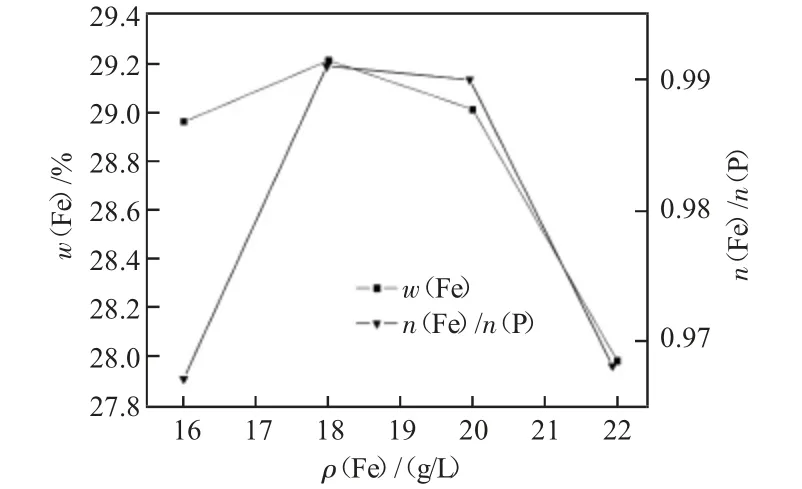
圖4 不同體系濃度對制備電池級磷酸鐵的影響
從圖4 數據可知,當反應體系中鐵質量濃度從16.0 g/L 增加到22.0 g/L 時,產品w(Fe)和n(Fe)/n(P)表現為先增加后下降趨勢,當鐵質量濃度為18.0g/L時產品中w(Fe)和n(Fe)/n(P)均達到最大值,分別為29.22%、0.991;當鐵質量濃度為18.0 g/L 后,w(Fe)和n(Fe)/n(P)開始下降,這是因為,當鐵質量濃度增大后反應釜中的酸度也會相應增加,影響磷酸的電離。確定最佳反應體系濃度鐵質量濃度為18.0 g/L。
2.2 水熱法生成磷酸鐵的制備與表征
采用水熱法電池級磷酸鐵,最佳工藝參數為:硝酸濃度為3.0 mol/L,最佳反應溫度為110 ℃,最佳反應時間為120min,反應體系濃度鐵質量濃度為18.0g/L,經冷卻、洗滌、抽濾、干燥后得到的FePO4·2H2O,樣品中鐵含量與鐵磷比接近理論值。
對樣品進行元素分析可得:樣品中鐵和磷質量分數為29.19%、16.36%,鐵磷物質的量的比為0.991,結合XRD 分析說明樣品為正磷酸鐵。采用電感耦合等離子體質譜進行微量金屬元素分析,金屬鈦的質量分數從磷鐵時的0.34%增加到0.831%,未超出電池級磷酸鐵的指標要求。樣品熱分析結果表明:在200 ℃左右出現有一個明顯的吸熱峰,質量損失為18.89%,結合XRD 分析可確定有2 個結晶水。從SEM 圖可知,樣品微觀形貌為均勻的片狀結構,樣品間孔隙較大,說有樣品表面積大,有利于提高后續固相加熱法制備LiFePO4的電化學性能。
2.3 磷酸鐵鋰的表征
用水熱法生成的電池級磷酸鐵制備磷酸鐵鋰(LiFePO4/C)。樣品XRD 分析可知,產物為有序的橄欖石結構,無碳衍射峰出現,碳的加入不影響到磷酸鐵鋰的橄欖石結構。SEM分析可知,合成的LiFePO4/C樣品表面形貌均勻規則,接近球形。LiFePO4/C 樣品首次充電容量、放電容量、放電的庫倫效率分別為158.8 mAh/g、147.8 Ah/g、93.1%,充分說明以該磷酸鐵為原料制備的磷酸鐵鋰電化學性能較好,能用于鋰電池的正極材料。
3 結論
以黃磷所得副產品磷鐵為原料,采用水熱法制備了磷酸鐵并確定了最佳工藝參數,然后利用制備出的磷酸鐵制備磷酸鐵鋰。LiFePO4/C 樣品首次充電容量、放電容量、放電的庫倫效率分別為158.8 mAh/g、147.8 Ah/g、93.1%,說明磷酸鐵鋰電化學性能較好,能用于鋰電池的正極材料。

