基于實(shí)驗(yàn)異常現(xiàn)象的生成性教學(xué)實(shí)踐研究
朱成東 孫永興 徐泓 孫影


摘要: 以海帶中碘含量測(cè)定過(guò)程中待測(cè)液反復(fù)變藍(lán)的實(shí)驗(yàn)異常現(xiàn)象作為課堂生成性資源,通過(guò)引導(dǎo)學(xué)生對(duì)其進(jìn)行猜想、假設(shè)和驗(yàn)證組織課堂教學(xué),從而在體驗(yàn)科學(xué)探究的一般過(guò)程中,發(fā)展證據(jù)推理與模型認(rèn)知、科學(xué)探究與創(chuàng)新意識(shí)等學(xué)科核心素養(yǎng)。
關(guān)鍵詞: 中學(xué)化學(xué); 生成性教學(xué); 異常現(xiàn)象; 碘含量的測(cè)定
文章編號(hào): 10056629(2023)07003708
中圖分類號(hào): G633.8
文獻(xiàn)標(biāo)識(shí)碼: B
1 問(wèn)題提出
生成性教學(xué)是指教師根據(jù)課堂中的互動(dòng)狀態(tài)及時(shí)地調(diào)整教學(xué)思路和教學(xué)行為的教學(xué)形態(tài)[1]。生成性教學(xué)有賴于課堂中師生互動(dòng)產(chǎn)生的生成性資源,而實(shí)驗(yàn)作為化學(xué)學(xué)科的基礎(chǔ),是化學(xué)課堂生成性資源的重要來(lái)源。“預(yù)設(shè)”與“生成”是一對(duì)矛盾統(tǒng)一體[2],教科書已經(jīng)闡明的實(shí)驗(yàn)結(jié)果,抑或是由學(xué)生通過(guò)已經(jīng)掌握的化學(xué)知識(shí)進(jìn)行證據(jù)推理與預(yù)測(cè)得到的實(shí)驗(yàn)現(xiàn)象等均可作為課堂“預(yù)設(shè)”,而在化學(xué)實(shí)驗(yàn)中出現(xiàn)一些與預(yù)期的實(shí)驗(yàn)現(xiàn)象不相符的異常現(xiàn)象,如顏色變化的異常等,則是課堂中的動(dòng)態(tài)“生成”。教師利用異常現(xiàn)象組織生成探究式課堂,對(duì)異常現(xiàn)象進(jìn)行猜想、假設(shè)、驗(yàn)證的過(guò)程中,既能體驗(yàn)科學(xué)探究的一般過(guò)程,又可發(fā)展證據(jù)推理與模型認(rèn)知、科學(xué)探究與創(chuàng)新意識(shí)等學(xué)科核心素養(yǎng)。
海帶中碘含量的測(cè)定方法眾多,如分光光度法[3]、氣相色譜法[4],這些方法雖精確易行,但所涉及的原理和設(shè)備均超出高中教學(xué)要求和條件;我國(guó)現(xiàn)行行業(yè)標(biāo)準(zhǔn)《海帶碘含量的測(cè)定》中所提及的碘量法雖原理簡(jiǎn)單,但過(guò)程復(fù)雜且需要用到溴水和甲酸鈉等對(duì)人體不友好的化學(xué)物質(zhì),因此也不適用于高中課堂教學(xué)[5]。筆者在實(shí)際教學(xué)時(shí)擬采用雙氧水做氧化劑氧化碘離子,再用硫代硫酸鈉標(biāo)準(zhǔn)液進(jìn)行滴定,從原理、安全等多個(gè)角度基本滿足課堂小組實(shí)驗(yàn)的需求。但在進(jìn)行預(yù)實(shí)驗(yàn)時(shí),意外發(fā)現(xiàn)變?yōu)闊o(wú)色后的待測(cè)液會(huì)反復(fù)變回藍(lán)色的異常現(xiàn)象(如圖1所示)。查閱文獻(xiàn)發(fā)現(xiàn),造成該異常現(xiàn)象的原因在于過(guò)氧化氫氧化碘離子的反應(yīng)慢于硫代硫酸鈉還原碘分子至碘離子的反應(yīng)[6]。
現(xiàn)有“海帶提碘”“碘含量的測(cè)定”等相關(guān)教學(xué)研究[7~9]和實(shí)驗(yàn)研究[10],主要側(cè)重于探究實(shí)驗(yàn)最佳條件以及以了解物質(zhì)的提取和分離方法為教學(xué)目標(biāo)的項(xiàng)目式教學(xué)或定量測(cè)定的STEM教學(xué),一般忽略了雙氧水氧化碘離子,再用硫代硫酸鈉標(biāo)準(zhǔn)液進(jìn)行滴定的實(shí)驗(yàn)中的“異常”現(xiàn)象。本研究運(yùn)用該異常現(xiàn)象的生成性教學(xué)模型(如圖2),立足于“提出猜想→設(shè)計(jì)方案→實(shí)驗(yàn)驗(yàn)證→收集證據(jù)→得出結(jié)論→交流討論”的科學(xué)探究一般步驟,讓學(xué)生經(jīng)歷真實(shí)的科學(xué)探究歷程,培養(yǎng)嚴(yán)謹(jǐn)求實(shí)的科學(xué)態(tài)度,以期達(dá)成對(duì)實(shí)驗(yàn)中的“異常”現(xiàn)象能提出質(zhì)疑或新的設(shè)想,并進(jìn)一步付諸探究實(shí)踐的素養(yǎng)水平[11]。
2 基于實(shí)驗(yàn)異常現(xiàn)象的生成性教學(xué)實(shí)踐
2.1 教學(xué)內(nèi)容分析
本課時(shí)選自魯科版高中化學(xué)必修第二冊(cè)第一章微項(xiàng)目“海帶提碘與海水提溴”,是基于該內(nèi)容設(shè)計(jì)的實(shí)驗(yàn)復(fù)習(xí)課[12]。“從海帶中提取碘”“含碘鹽的檢驗(yàn)”是高中階段兩個(gè)重要的化學(xué)實(shí)驗(yàn),多個(gè)版本的必修教材和實(shí)驗(yàn)選修教材均有涉及[13, 14]。此外,強(qiáng)酸與強(qiáng)堿的中和滴定是高中階段必做的定量實(shí)驗(yàn),對(duì)海帶中的碘進(jìn)行提取與含量測(cè)定不僅是對(duì)酸堿滴定的拓展和提升,更是需要綜合運(yùn)用氧化還原反應(yīng)、化學(xué)反應(yīng)速率與限度等核心知識(shí)。因此,從知識(shí)內(nèi)容上看,該課時(shí)具有鞏固化學(xué)反應(yīng)原理、強(qiáng)化酸堿中和滴定實(shí)驗(yàn)技能、進(jìn)一步發(fā)展學(xué)生解決問(wèn)題能力的功能;從學(xué)習(xí)方法上看,基于真實(shí)情境的科學(xué)探究過(guò)程可以有效地促進(jìn)知識(shí)與技能的遷移,為后續(xù)開(kāi)展復(fù)雜真實(shí)的實(shí)驗(yàn)探究活動(dòng)打下基礎(chǔ)。其教學(xué)功能歸納如圖3所示。
2.2 教學(xué)目標(biāo)
(1) 通過(guò)海帶中的碘含量的測(cè)定,鞏固滴定實(shí)驗(yàn)的操作技能,認(rèn)識(shí)滴定實(shí)驗(yàn)的重要價(jià)值。
(2) 通過(guò)實(shí)驗(yàn)中異常現(xiàn)象的發(fā)現(xiàn),樹(shù)立嚴(yán)謹(jǐn)求實(shí)的科學(xué)態(tài)度,形成敢于質(zhì)疑、探索未知、崇尚真理的意識(shí)。
(3) 通過(guò)對(duì)實(shí)驗(yàn)中異常現(xiàn)象原因的探究,形成提出假設(shè)、設(shè)計(jì)方案、實(shí)驗(yàn)驗(yàn)證的探究思路,并運(yùn)用氧化還原理論進(jìn)行分析、推理,用實(shí)驗(yàn)加以證實(shí)或證偽,建立觀點(diǎn)、結(jié)論和證據(jù)之間的邏輯關(guān)系。
(4) 通過(guò)對(duì)實(shí)驗(yàn)曲線的解釋和宏觀現(xiàn)象的分析,建立多反應(yīng)復(fù)雜體系的分析思路,初步形成從熱力學(xué)和動(dòng)力學(xué)等角度分析化學(xué)反應(yīng)的意識(shí)。
2.3 教學(xué)流程
具體教學(xué)流程如圖4所示。
2.4 教學(xué)實(shí)施
環(huán)節(jié)一:發(fā)現(xiàn)異常——待測(cè)液反復(fù)變藍(lán)
[提出問(wèn)題]碘元素是人體必需的微量元素之一,健康成人體內(nèi)的碘的總量約為30毫克,攝入過(guò)多或攝入不足均會(huì)對(duì)我們的健康造成危害,加碘鹽和海帶是我們?nèi)粘z入碘的主要來(lái)源。上節(jié)課我們將海帶通過(guò)灼燒、浸泡、過(guò)濾等實(shí)驗(yàn)操作,獲得了含碘離子的待測(cè)液,現(xiàn)在如何去測(cè)定海帶中的碘含量呢?
[生]聯(lián)系舊知,根據(jù)強(qiáng)酸與強(qiáng)堿的中和滴定,明確滴定法是實(shí)驗(yàn)室測(cè)定未知離子濃度的一般方法。
[追問(wèn)1]如何選取指示劑和標(biāo)準(zhǔn)液呢?
[思考討論]碘單質(zhì)遇淀粉溶液變藍(lán),可以先將碘離子氧化成碘單質(zhì),選取淀粉溶液做指示劑,再選取還原劑做標(biāo)準(zhǔn)液。
[歸納總結(jié)]含碘待測(cè)液的測(cè)定原理為:
H2O2+2I-+2H+I2+2H2O①
2Na2S2O3+I22NaI+Na2S4O6②
[小組實(shí)驗(yàn)]根據(jù)實(shí)驗(yàn)原理進(jìn)行小組實(shí)驗(yàn)(如圖5所示)。
[生1]發(fā)現(xiàn)問(wèn)題:達(dá)到滴定終點(diǎn)時(shí)的實(shí)驗(yàn)現(xiàn)象應(yīng)為藍(lán)色變?yōu)闊o(wú)色且半分鐘內(nèi)不變,但是在實(shí)驗(yàn)時(shí),待測(cè)液變?yōu)闊o(wú)色后會(huì)反復(fù)變回藍(lán)色,為什么一直達(dá)不到滴定終點(diǎn)?
[引導(dǎo)提問(wèn)]待測(cè)液變回藍(lán)色后你是如何操作的?
[生1]繼續(xù)滴加硫代硫酸鈉標(biāo)準(zhǔn)液,再次讓待測(cè)液變回?zé)o色,但是很快又變?yōu)樗{(lán)色。
[追問(wèn)]待測(cè)液反復(fù)變回藍(lán)色,實(shí)驗(yàn)出現(xiàn)了異常現(xiàn)象,同學(xué)們能結(jié)合所學(xué)的化學(xué)知識(shí),提出合理的猜想嗎?
環(huán)節(jié)二:初步猜想——應(yīng)用氧化還原反應(yīng)模型探究異常現(xiàn)象
出現(xiàn)異常現(xiàn)象后,教師應(yīng)充分利用該生成性資源進(jìn)行教學(xué),逐步引導(dǎo)學(xué)生自主討論探究。由于造成該異常現(xiàn)象的原因較為復(fù)雜,學(xué)生在未熟悉科學(xué)探究的一般步驟時(shí),很難主動(dòng)地提出合理猜想,這時(shí)就需要教師充分扮演好課堂引導(dǎo)者的角色,從學(xué)生熟悉的易想到的原因入手,在平等的對(duì)話中進(jìn)行持續(xù)探究。
[引導(dǎo)發(fā)問(wèn)]待測(cè)液藍(lán)色褪去,說(shuō)明碘單質(zhì)轉(zhuǎn)化為了碘離子,那藍(lán)色恢復(fù)呢?
[生]說(shuō)明碘離子又被氧化成了碘單質(zhì)。
[追問(wèn)1]氧化劑是誰(shuí)?
[生]錐形瓶為敞口容器,溶液接觸氧氣。提出猜想一:待測(cè)液反復(fù)變藍(lán)是因?yàn)榈怆x子被空氣中的氧氣氧化。
[追問(wèn)2]如何設(shè)計(jì)實(shí)驗(yàn)進(jìn)行驗(yàn)證呢?
[小組討論]可以向滴有淀粉溶液的含I-待測(cè)液中鼓入空氣,觀察溶液是否會(huì)變?yōu)樗{(lán)色。
[評(píng)價(jià)實(shí)驗(yàn)方案]方案巧妙可行,但是待測(cè)液中依然需要加入等量的酸進(jìn)行酸化。
[小組實(shí)驗(yàn)]實(shí)驗(yàn)現(xiàn)象:打開(kāi)充氣泵開(kāi)關(guān),待測(cè)液始終保持為無(wú)色(如圖6所示)。得出結(jié)論:空氣中的氧氣很難在短時(shí)間內(nèi)氧化碘離子,猜想一為錯(cuò)誤猜想。
[追問(wèn)3]反應(yīng)體系中是否還存在其他氧化劑呢?
[交流思考]滴定前,待測(cè)液中加入了過(guò)量的H2O2溶液,提出猜想二:待測(cè)液反復(fù)變藍(lán)是因?yàn)榈怆x子被過(guò)量的H2O2氧化了。
[追問(wèn)1]如何設(shè)計(jì)實(shí)驗(yàn)驗(yàn)證呢?
[交流討論]可以向滴有H2SO4溶液和淀粉溶液的待測(cè)液中加入少量H2O2溶液再滴定,進(jìn)行對(duì)比實(shí)驗(yàn)。
[評(píng)價(jià)實(shí)驗(yàn)方案]待測(cè)液中的碘離子含量未知,如何確保H2O2溶液為少量呢?
[定量實(shí)驗(yàn)]在試管中加入兩滴管0.1mol/L KI溶液,經(jīng)硫酸酸化,滴加淀粉溶液做指示劑后僅僅加入1滴0.2mol/L H2O2溶液進(jìn)行氧化,從而確保過(guò)氧化氫的量為少量(如圖7所示)。
[小組實(shí)驗(yàn)]實(shí)驗(yàn)現(xiàn)象:變?yōu)闊o(wú)色后的待測(cè)液會(huì)再次變藍(lán)。得出結(jié)論:過(guò)量的H2O2不是造成該異常現(xiàn)象發(fā)生的主要原因。
[得出結(jié)論]猜想二為錯(cuò)誤猜想。
環(huán)節(jié)三:深入探索——化學(xué)反應(yīng)的速率和限度對(duì)異常現(xiàn)象的影響
利用氧化還原反應(yīng)原理進(jìn)行了兩次猜想與假設(shè)后,學(xué)生已經(jīng)熟悉了科學(xué)探究的一般步驟,這時(shí)只需從化學(xué)反應(yīng)的限度入手稍加引導(dǎo),學(xué)生便可自主生成新的猜想,隨后再利用實(shí)驗(yàn)證據(jù)逐漸過(guò)渡到反應(yīng)的速率角度,讓探究活動(dòng)與學(xué)生的思維生成始終保持一致,課堂的生成性在該環(huán)節(jié)中也得到較大程度的體現(xiàn)。
[引導(dǎo)]大家能否再提出新的猜想與假設(shè),思考什么情況下溶液中會(huì)始終存在碘單質(zhì)?
[生1]提出猜想三:有沒(méi)有可能過(guò)氧化氫與碘離子的反應(yīng)是一個(gè)可逆反應(yīng),即:
H2O2+2I-+2H+I2+2H2O
[生2]若為可逆反應(yīng),溶液中始終存在I2,滴加Na2S2O3,溶液不會(huì)變?yōu)闊o(wú)色。
[追問(wèn)]如何判斷一個(gè)反應(yīng)進(jìn)行的程度?
[生3]可以利用平衡常數(shù)的數(shù)值來(lái)進(jìn)行判斷。
[提供資料]該反應(yīng)的平衡常數(shù)約為1×1042。
[得出結(jié)論]猜想三為錯(cuò)誤猜想。
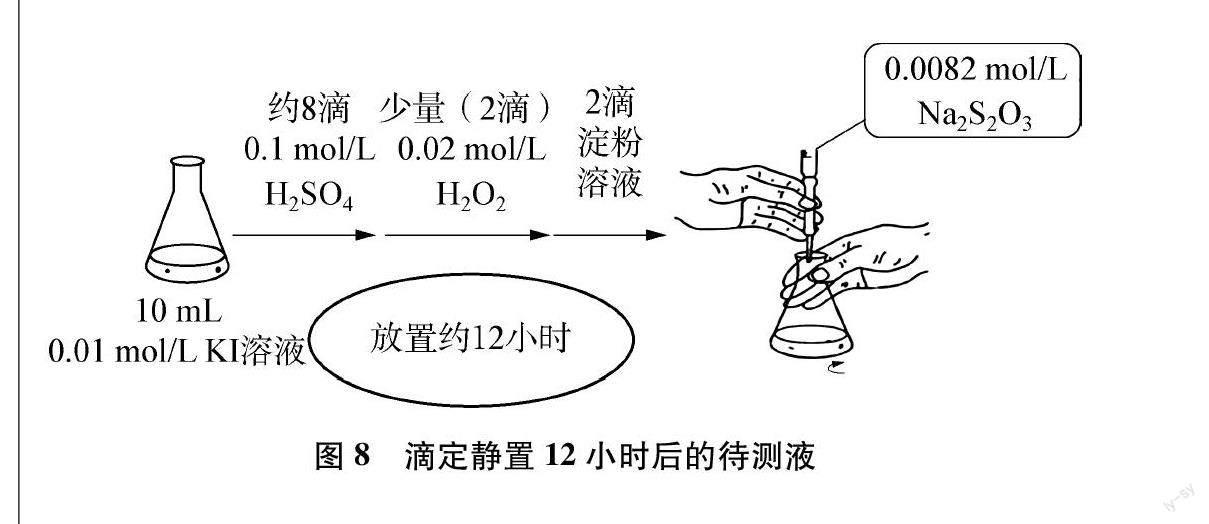
[啟發(fā)思考]課前,進(jìn)行了如圖8所示的實(shí)驗(yàn),待測(cè)液放置12小時(shí)后再進(jìn)行滴定,異常現(xiàn)象就消失了,這是為什么呢?
[生1]說(shuō)明反應(yīng)①的時(shí)間長(zhǎng)短對(duì)滴定過(guò)程有一定的影響。
[追問(wèn)1]反應(yīng)時(shí)間的長(zhǎng)短又取決于什么?
[生2]化學(xué)反應(yīng)速率。
[追問(wèn)2]化學(xué)反應(yīng)速率是否會(huì)對(duì)該異常現(xiàn)象造成影響呢?請(qǐng)大膽猜想。
[交流討論]從化學(xué)反應(yīng)速率的角度思考,提出猜想四:造成異常現(xiàn)象的可能原因是H2O2氧化I-的反應(yīng)比Na2S2O3還原I2的反應(yīng)慢,因此在滴定的過(guò)程中不斷產(chǎn)生新的I2,故溶液會(huì)再次變藍(lán)(如圖9所示)。
[提問(wèn)]如何驗(yàn)證反應(yīng)①在滴定的過(guò)程中是持續(xù)進(jìn)行的慢反應(yīng)呢?
[交流討論]很難根據(jù)宏觀實(shí)驗(yàn)現(xiàn)象進(jìn)行判斷。
[教師引導(dǎo)]我們可以引入氧化還原電勢(shì)傳感器(ORP),去測(cè)定滴定過(guò)程中的電勢(shì)變化,進(jìn)而通過(guò)曲線變化趨勢(shì)探尋反應(yīng)的微觀本質(zhì)(實(shí)驗(yàn)裝置如圖10所示)。
[預(yù)測(cè)]已知氧化性物質(zhì)的電勢(shì)值高于還原性物質(zhì)的電勢(shì)值,如果猜想四為正確猜想,請(qǐng)預(yù)測(cè)曲線變化趨勢(shì)。
[觀察]預(yù)測(cè)結(jié)束后,注意觀察燒杯內(nèi)溶液顏色變化和曲線變化(曲線變化如圖11所示)。
[解釋]構(gòu)建四重表征(如圖12所示)。滴定前,燒杯中溶液為藍(lán)色,打開(kāi)雙閥滴液管滴加硫代硫酸鈉,曲
線立刻呈現(xiàn)下降趨勢(shì),溶液也由藍(lán)色變?yōu)闊o(wú)色;恰好變?yōu)闊o(wú)色后,關(guān)閉雙閥滴液管,曲線又呈現(xiàn)上升趨勢(shì),溶液也恢復(fù)為藍(lán)色。重復(fù)實(shí)驗(yàn)操作可以觀察到相同的宏觀現(xiàn)象和曲線變化。
[提問(wèn)]曲線在下降和上升的過(guò)程中,溶液中的離子分別發(fā)生怎樣的化學(xué)變化?
[生1]碘單質(zhì)具有氧化性,其電勢(shì)值較高,曲線下降,說(shuō)明是碘單質(zhì)被還原為碘離子;相反,曲線上升則說(shuō)明是具有還原性的碘離子又被氧化成碘單質(zhì)。
[追問(wèn)1]關(guān)閉雙閥滴液管后曲線上升的趨勢(shì)重復(fù)出現(xiàn),說(shuō)明什么?
[生2]說(shuō)明H2O2與I-的反應(yīng)確實(shí)在滴定的過(guò)程中持續(xù)進(jìn)行著。
[追問(wèn)2]為什么a點(diǎn)的電勢(shì)值始終高于c點(diǎn)和之后的每一個(gè)曲線頂點(diǎn)呢?
[生3]因?yàn)榈渭恿肆虼蛩徕c,相當(dāng)于稀釋溶液,溶液中各溶質(zhì)的物質(zhì)的量濃度都會(huì)降低。
[生4]因?yàn)閍點(diǎn)為滴定起點(diǎn),滴定前溶液靜置的時(shí)間長(zhǎng),所以此時(shí)溶液中的碘單質(zhì)含量高,電勢(shì)值就高;而b與c之間的時(shí)間間隔短,H2O2與I-的反應(yīng)速率可能較慢,因此c點(diǎn)溶液中的碘單質(zhì)含量低,電勢(shì)值就低。
[評(píng)價(jià)升華]我們需要從多個(gè)角度認(rèn)識(shí)化學(xué)反應(yīng),特別是要從化學(xué)反應(yīng)速率的角度對(duì)實(shí)驗(yàn)現(xiàn)象進(jìn)行解釋。
宏觀現(xiàn)象曲線表征符號(hào)表征微觀表征
過(guò)氧化氫在不斷緩慢地氧化碘離子:H2O2+2I-+2H+I2+2H2O溶液中部分碘離子被氧化為碘單質(zhì),到達(dá)波谷前溶液中含有:I-、 I2
碘單質(zhì)被還原:2Na2S2O3+I22NaI+Na2S4O6
碘單質(zhì)被還原速率大于碘離子被氧化速率,所以波谷位置溶液中僅含有:I-
剩余碘離子繼續(xù)被氧化:
H2O2+2I-+2H+I2+2H2O碘離子被氧化為碘單質(zhì),波峰位置溶液中含有:I-、 I2
[設(shè)問(wèn)]那如何進(jìn)一步驗(yàn)證H2O2與I-的反應(yīng)速率就很慢呢?可以直接測(cè)定H2O2與I-反應(yīng)過(guò)程中的電勢(shì)變化,曲線如圖13所示。可以發(fā)現(xiàn)2小時(shí)后電勢(shì)還有上升的趨勢(shì),說(shuō)明該反應(yīng)確實(shí)很慢。
[提問(wèn)]那如何設(shè)計(jì)實(shí)驗(yàn)表征Na2S2O3與I2的反應(yīng)很快呢?
[生]依然可以測(cè)定反應(yīng)過(guò)程的電勢(shì)變化,觀察電勢(shì)曲線趨于平穩(wěn)所需的時(shí)間。
[引導(dǎo)]大家還可以將待測(cè)液直接倒入硫代硫酸鈉溶液中,觀察現(xiàn)象。
[小組實(shí)驗(yàn)]如圖14所示,實(shí)驗(yàn)現(xiàn)象:幾乎在倒入的瞬間,藍(lán)紫色就會(huì)消失。實(shí)驗(yàn)結(jié)論:說(shuō)明反應(yīng)②的速率遠(yuǎn)遠(yuǎn)大于反應(yīng)①。
[總結(jié)]通過(guò)宏觀現(xiàn)象和曲線斜率等多種途徑,讓化學(xué)反應(yīng)速率可視化,最終得出結(jié)論:碘含量測(cè)定中被測(cè)液反復(fù)變藍(lán)的異常現(xiàn)象是因?yàn)榉磻?yīng)①與反應(yīng)②速率相差過(guò)大導(dǎo)致的。同學(xué)們課下還可繼續(xù)探討造成該異常現(xiàn)象的其他可能原因。
環(huán)節(jié)四:拓展升華——如何精確地測(cè)定海帶中的碘含量
[提問(wèn)]既然H2O2做氧化劑有這么多的弊端,還是造成該異常現(xiàn)象的主要原因,我們能否更換氧化劑進(jìn)行實(shí)驗(yàn)?zāi)兀?/p>
[生]交流討論,選取其他常見(jiàn)的氧化劑,如KMnO4等。
[總結(jié)]如圖15所示。
[課后作業(yè)]請(qǐng)大家課后查閱文獻(xiàn),找到國(guó)家制定的海帶中碘含量測(cè)定的標(biāo)準(zhǔn),思考不同氧化劑對(duì)碘含量測(cè)定的影響。
3 教學(xué)反思
我們?cè)诮虒W(xué)中充分挖掘過(guò)氧化氫“碘鐘”實(shí)驗(yàn)的教學(xué)資源,以測(cè)定海帶中碘含量為情境,利用學(xué)生分析多反應(yīng)復(fù)雜體系的實(shí)驗(yàn)結(jié)果時(shí)習(xí)慣性地僅從熱力學(xué)視角進(jìn)行分析,使之實(shí)驗(yàn)現(xiàn)象與學(xué)生認(rèn)識(shí)產(chǎn)生沖突,順勢(shì)引導(dǎo)學(xué)生轉(zhuǎn)從動(dòng)力學(xué)視角進(jìn)行探究,并運(yùn)用其生成性特點(diǎn)來(lái)發(fā)展學(xué)生的科學(xué)探究與創(chuàng)新意識(shí)素養(yǎng)。對(duì)本節(jié)課的生成性教學(xué)實(shí)踐具體反思如下。
3.1 生成性教學(xué)需要合理的預(yù)設(shè)
精心預(yù)設(shè)可以為動(dòng)態(tài)生成“保駕護(hù)航”——保證生成性資源的合情、合理和有效[15]。如果把異常實(shí)驗(yàn)現(xiàn)象的產(chǎn)生看作為“合情”,那么對(duì)異常實(shí)驗(yàn)現(xiàn)象的持續(xù)探究過(guò)程則需“合理和有效”,這種“合理”是建立在教師前期的實(shí)驗(yàn)研究之上的。本文用過(guò)氧化氫氧化碘離子,再用硫代硫酸鈉標(biāo)準(zhǔn)液滴定碘,從而確定碘含量,是中學(xué)常見(jiàn)的碘含量測(cè)定的一種方法。在實(shí)驗(yàn)室重現(xiàn)該實(shí)驗(yàn)時(shí)發(fā)現(xiàn)該異常現(xiàn)象,對(duì)此進(jìn)行深入的探究;再將整個(gè)探究過(guò)程濃縮成一節(jié)基于實(shí)驗(yàn)現(xiàn)象異常的生成性探究課。因而異常實(shí)驗(yàn)現(xiàn)象的生成性教學(xué)需要教師經(jīng)常在實(shí)驗(yàn)中“備課”,才能把握住實(shí)驗(yàn)課中生成性教學(xué)的預(yù)設(shè)機(jī)會(huì)。
3.2 生成性教學(xué)更需關(guān)注學(xué)生的真實(shí)表現(xiàn)
生成性教學(xué)中學(xué)生的表現(xiàn)行為是個(gè)性的和未知的,學(xué)生的素養(yǎng)發(fā)展往往就體現(xiàn)在各種課堂表現(xiàn)之中,因此需要不斷地關(guān)注學(xué)生在復(fù)雜情境中的活動(dòng)表現(xiàn),注重“教學(xué)評(píng)”一體化理念的落實(shí)。如用硫代硫酸鈉滴定碘的實(shí)驗(yàn)中反復(fù)出現(xiàn)藍(lán)色的異常現(xiàn)象,對(duì)學(xué)生的認(rèn)知產(chǎn)生較大沖突,學(xué)生的驚訝、疑惑等真實(shí)表現(xiàn)都體現(xiàn)了學(xué)生對(duì)探索未知的渴望。對(duì)異常現(xiàn)象原因的探究中,教師關(guān)注學(xué)生提出的猜測(cè)、實(shí)驗(yàn)方案,以判斷學(xué)生的思維水平;用數(shù)字化實(shí)驗(yàn)做出曲線后,關(guān)注學(xué)生對(duì)曲線的解釋,以判斷學(xué)生對(duì)問(wèn)題本質(zhì)的理解能力和對(duì)異常化學(xué)現(xiàn)象的解釋能力。
3.3 生成性教學(xué)能夠有助于發(fā)展學(xué)生的科學(xué)探究能力與創(chuàng)新意識(shí)
課堂以師生之間的平等互動(dòng)為基礎(chǔ),生成性教學(xué)則更加關(guān)注師生在課堂中由高質(zhì)量互動(dòng)產(chǎn)生的一系列具有挑戰(zhàn)性的任務(wù),由師生對(duì)話引發(fā)的“設(shè)計(jì)—實(shí)驗(yàn)—再設(shè)計(jì)—再實(shí)驗(yàn)”的課堂經(jīng)歷使得學(xué)生的“生成”能力不斷提高。如此一來(lái),生成性教學(xué)對(duì)發(fā)展學(xué)生科學(xué)探究與創(chuàng)新意識(shí)等素養(yǎng)的價(jià)值不斷得到體現(xiàn)。如本節(jié)課對(duì)實(shí)驗(yàn)異常現(xiàn)象原因的探究是先通過(guò)對(duì)學(xué)生提出的“空氣中氧氣的氧化、過(guò)量過(guò)氧化氫氧化”等猜想進(jìn)行證偽探究,然后從化學(xué)反應(yīng)速率視角對(duì)其進(jìn)行證實(shí)探究,以此培養(yǎng)學(xué)生基于實(shí)驗(yàn)事實(shí)對(duì)猜想進(jìn)行論證,在證偽中勇于創(chuàng)新的精神。在證偽與證實(shí)過(guò)程中不斷地設(shè)計(jì)方案、運(yùn)用實(shí)驗(yàn)進(jìn)行探究,以此來(lái)培養(yǎng)學(xué)生堅(jiān)韌不拔、持之以恒的學(xué)科素養(yǎng)和能力。
參考文獻(xiàn):
[1]羅祖兵. 生成性教學(xué)及其基本理念[J]. 課程·教材·教法, 2006, (10): 28~33.
[2]李祎, 涂榮豹. 生成性教學(xué)的基本特征與設(shè)計(jì)[J]. 教育研究, 2007, (1): 41~44.
[3]張愛(ài)梅, 王術(shù)皓, 崔慧. 阻抑動(dòng)力學(xué)分光光度及熒光光度法測(cè)定微量碘[J]. 分析化學(xué), 2001, (10): 1160~1162.
[4]單守堯. 海帶碘含量的氣相色譜測(cè)定[J]. 食品科學(xué), 1991, (4): 46~48.
[5]國(guó)家水產(chǎn)品質(zhì)量監(jiān)督檢驗(yàn)中心. 海帶碘含量的測(cè)定:SC/T 3010—2001 [S]. 2001.
[6]陳肖虎, 薛安, 楊善志等. 過(guò)氧化氫硫酸氧化碘離子反應(yīng)動(dòng)力學(xué)研究[J]. 過(guò)程工程學(xué)報(bào), 2009, (S1): 181~184.
[7]張琦, 盧鳳琴, 陳雷等. 海產(chǎn)品中碘的提取與測(cè)定探究實(shí)驗(yàn)[J]. 化學(xué)教學(xué), 2021, (11): 80~84.
[8]喬琦. “海帶中碘的檢驗(yàn)和提取”的教學(xué)和反思[J]. 化學(xué)教學(xué), 2012, (2): 24~26.
[9]張金水. 淺談碘的提取[J]. 化學(xué)教學(xué), 2018, (10): 87~90.
[10]楊孝容, 熊俊如, 張?zhí)? 過(guò)氧化氫提取海帶中碘的實(shí)驗(yàn)條件優(yōu)化[J]. 化學(xué)教學(xué), 2015, (8): 48~51.
[11]中華人民共和國(guó)教育部制定. 普通高中化學(xué)課程標(biāo)準(zhǔn)(2017年版2020年修訂)[S]. 北京:人民教育出版社, 2020.
[12]王磊主編. 普通高中教科書·化學(xué)必修第二冊(cè)[M]. 濟(jì)南:山東科學(xué)技術(shù)出版社, 2019: 30~33.
[13]王祖浩主編. 普通高中教科書·化學(xué)必修第一冊(cè)[M]. 南京: 江蘇鳳凰教育出版社, 2020: 81~83.
[14]宋心琦主編. 普通高中課程標(biāo)準(zhǔn)實(shí)驗(yàn)教科書·實(shí)驗(yàn)化學(xué)[M]. 北京: 人民教育出版社, 2007: 20~22.
[15]吳玲, 郭孝文. 有效教學(xué): 讓課堂生成與課前預(yù)設(shè)互動(dòng)共生[J]. 中國(guó)教育學(xué)刊, 2007, (11): 52~54.

