基于HPLC指紋圖譜和網絡藥理學的加味四逆散(顆粒)質量標志物分析及含量測定方法的建立
陳靜梅,李澤宇,梁秋明,岳子俊,唐佐偉,郝二偉,杜正彩,侯小濤*,鄧家剛
基于HPLC指紋圖譜和網絡藥理學的加味四逆散(顆粒)質量標志物分析及含量測定方法的建立
陳靜梅1, 2, 3, 4,李澤宇2, 3, 4, 5,梁秋明6,岳子俊1,唐佐偉1,郝二偉2, 3, 4, 5,杜正彩2, 3, 4, 5,侯小濤1, 2, 3, 4*,鄧家剛2, 3, 4, 5
1. 廣西中醫藥大學藥學院,廣西 南寧 530200 2. 廣西中藥藥效研究重點實驗室,廣西 南寧 530200 3. 廣西農作物廢棄物功能成分研究協同創新中心,廣西 南寧 530200 4. 廣西中醫濕病方藥理論與轉化重點實驗室,廣西 南寧 530200 5. 廣西中醫藥大學廣西中醫藥科學實驗中心,廣西 南寧 530200 6. 廣西欽州市中醫醫院,廣西 欽州 535000
基于指紋圖譜和網絡藥理學方法,分析預測加味四逆散(Jiawei Sini Powder,JSP)(顆粒)潛在的質量標志物(quality markers,Q-Marker),并對Q-Marker成分進行含量測定,為其質量控制提供參考。采用HPLC指紋圖譜結合化學計量學分析JSP(顆粒)潛在Q-Marker。通過網絡藥理學構建物質-效應網絡,進一步分析預測JSP(顆粒)藥效關聯的Q-Marker,并建立對預測得到的標志性成分進行含量測定的HPLC方法。建立了JSP(顆粒)的HPLC指紋圖譜,標記28個共有峰,對其進行峰歸屬,其中1、9、11號峰來自白芍,26、27號峰來自枳實,13、28號峰來自炙甘草,2、4、10、12、16、24號峰來自代代花,15、17、22號峰來自半枝蓮,25號峰來自白芍和炙甘草共有,3、5~8、14、18~21、23號峰來自枳實和代代花共有,并指認了其中的9個共有峰,分別為芍藥內酯苷、芍藥苷、甘草苷、野黃芩苷、柚皮苷、橙皮苷、新橙皮苷、柚皮素、甘草酸銨。相似度評價顯示,10批JSP(顆粒)樣品的相似度為0.954~1.000。主成分分析(principal component analysis,PCA)顯示前4個主成分的累積方差貢獻率為95.003%,正交偏最小二乘-判別分析(orthogonal partial least squares-discriminant analysis,OPLS-DA)顯示有12個成分變量重要性投影(variable importance projection,VIP)值較大。采用網絡藥理學的方法分析得出芍藥內酯苷、芍藥苷、柚皮苷、橙皮苷、新橙皮苷5個成分可能為JSP(顆粒)潛在的Q-Marker。同時測定以上5個成分的含量,方法學考察結果良好,平均加樣回收率為92.52%~96.48%,RSD為1.3%~2.6%。10批樣品中芍藥內酯苷、芍藥苷、柚皮苷、橙皮苷、新橙皮苷的質量分數分別為0.107 6~0.203 6、0.475 9~1.204 6、2.310 9~5.223 8、0.410 3~0.796 8、4.311 9~8.343 3 mg/g。建立了JSP(顆粒)的HPLC指紋圖譜,并結合網絡藥理學預測出5個Q-Marker成分及建立其定量測定方法,為JSP(顆粒)研制成古代經典名方中藥復方制劑提供質量控制依據。
加味四逆散;質量標志物;HPLC;指紋圖譜;網絡藥理學;主成分分析;正交偏最小二乘-判別分析;芍藥內酯苷;芍藥苷;柚皮苷;橙皮苷;新橙皮苷
胃痛是以胃脘部近歧骨處疼痛為主要癥狀的一種病證[1]。胃脘部疼痛是其主要的臨床表現[2],多發病于青中年階段,占到總發病人群的65%左右,幼兒和老年人較少,且無顯著的性別差異[3]。近年來,中醫應用于此病的臨床效果卓見成效,利用中醫辨證論治的理念,并依據病情需要進行臨床加減,可減輕胃痛,改善患者生活質量,安全性高,值得推廣。加味四逆散(Jiawei Sini Powder,JSP)是在全國第6批老中醫藥專家學術思想傳承工作指導老師鄧家剛教授指導下,在漢代張仲景經典名方四逆散中柴胡、白芍[芍藥]、枳實、炙甘草的基礎上增加2味藥物,即代代花、半枝蓮而形成的,共6味藥材組成。代代花理氣寬胸、和胃止嘔,半枝蓮清熱解毒、活血化瘀、消腫止痛,整個方劑的功效概括為“疏肝解郁,理氣止痛”,主要用于中醫肝脾氣郁證之胃痛、脅痛等多種病癥[4-7]。該方長期在臨床應用,取得滿意效果。目前,尚未有對JSP整體性狀控制方面的研究,建立與完善其質量標準具有重要的意義。劉昌孝院士[8-11]提出的質量標志物(quality markers,Q-marker)的概念,旨在建立中藥全程質量控制及質量溯源體系。而中藥指紋圖譜結合化學計量學研究,可以在整體觀的基礎上篩選出最能反映中藥質量的標志性成分[12-13];網絡藥理學多基因、多靶點的特點與中醫藥多成分、多靶點的特點有異曲同工之妙,在中醫藥現代化研究中具有較高的應用價值[14-16]。因此,本研究以JSP顆粒劑為研究對象,將HPLC指紋圖譜與網絡藥理學相結合,并應用相似度評價軟件和化學計量學手段,預測其發揮藥效的潛在Q-Marker,進而采用HPLC技術對其進行含量測定,可以更加系統、全面地對其質量進行控制,以期為JSP研制成古代經典名方中藥復方制劑提供質量控制依據。
1 儀器與材料
1.1 儀器
Waters-HPLC型高效液相色譜儀,沃特世科技有限公司;SQP型十萬分之一電子分析天平,賽多利斯科學儀器有限公司;SB25-12D型超聲儀,寧波新芝生物科技股份有限公司;DZKW-D-6型電熱恒溫水浴鍋,北京市光明醫療儀器有限公司。
1.2 材料
1.2.1 試藥 色譜純乙腈、甲醇,賽默飛世爾科技(中國)有限公司;磷酸為色譜級,上海阿拉丁生化科技股份有限公司;其余均為分析純,水為超純水。
1.2.2 對照品 芍藥苷(批號110736-202145)、柚皮苷(批號110722-202116)、橙皮苷(批號110721- 202019)、新橙皮苷(批號111857-201804)、甘草苷(批號111610-201908)、野黃芩苷(批號110842- 202010)、甘草酸銨(批號110731-202122)對照品均購買于中國食品藥品檢定研究院,質量分數均≥98%;芍藥內酯苷(批號MUST-20131601)、柚皮素(批號MUST-20032406)對照品均購買于成都曼思特生物技術有限公司,質量分數均≥98%;JSP(顆粒),批號S211003、S211004、S211005、S211006、S211007、S211008、S211009、S221101、S221102、S221103,依次編號S1~S10,來自廣西大海陽光藥業有限公司,規格為15 g/袋。
2 方法與結果
2.1 JSP(顆粒)的HPLC指紋圖譜研究
2.1.1 供試品溶液的制備 取JSP(顆粒)2 g,精密稱定,置于錐形瓶中,精密加入70%甲醇20 mL,密塞,稱定質量,超聲提取1.5 h,放冷,再稱定質量,用70%甲醇補足減失的質量,搖勻,濾過,取續濾液,即得供試品溶液。
2.1.2 對照品溶液的制備 取各對照品適量,精密稱定,加70%甲醇分別制成含芍藥內酯苷1 mg/g、芍藥苷2 mg/g、甘草苷1 mg/g、野黃芩苷1 mg/g、柚皮苷3 mg/g、橙皮苷1 mg/g、新橙皮苷3 mg/g、柚皮素1 mg/g、甘草酸銨1 mg/g的單一對照品儲備液。分別吸取以上9種對照品儲備液適量,加70%甲醇制成不同質量濃度的混合對照品溶液。
2.1.3 單味藥材溶液的制備 按JSP(顆粒)處方比例分別稱取柴胡、白芍、枳實、炙甘草、代代花、半枝蓮藥材,按“2.1.1”項下方法分別制備單味藥材溶液。
2.1.4 色譜條件 色譜柱為X Select?HSS T3 C18柱(250 mm×4.6 mm,5 μm);流動相為乙腈-0.1%磷酸水溶液;梯度洗脫條件:0~10 min,5%~7%乙腈;10~15 min,7%~10%乙腈;15~30 min,10%~12.5%乙腈;30~40 min,12.5%~17%乙腈;40~45 min,17%~18%乙腈;45~50 min,18%乙腈;50~60 min,18%~20.5%乙腈;60~68 min,20.5%~21%乙腈;68~70 min,21%~24%乙腈;70~80 min,24%~28%乙腈;80~85 min,28%~35%乙腈;85~90 min,35%~40%乙腈;90~100 min,40%~55%乙腈;體積流量1.0 mL/min;柱溫25 ℃;進樣體積10 μL;紫外檢測波長為240 nm。
2.1.5 精密度試驗 取同一批次JSP(顆粒)樣品(S1),按“2.1.1”項下方法制備供試品溶液1份,按“2.1.4”項下色譜條件進行測定,連續進樣6次,記錄各共有峰的保留時間和峰面積,以柚皮苷為參照峰,計算各共有峰的相對保留時間和相對峰面積。28個共有峰的相對保留時間和相對峰面積的RSD分別小于0.30%和2.80%,表明儀器和實驗方法精密度良好。
2.1.6 穩定性試驗 取同一批次JSP(顆粒)樣品(S1),按“2.1.1”項下方法制備供試品溶液1份,分別于室溫放置2、4、8、12、16、24 h后,按“2.1.4”項下色譜條件進樣分析,記錄各共有峰的保留時間和峰面積,以柚皮苷為參照峰,計算各共有峰的相對保留時間和相對峰面積。28個共有峰的相對保留時間和相對峰面積的RSD分別小于0.53%和3.00%,表明供試品溶液在室溫條件下24 h內穩定性良好。
2.1.7 重復性試驗 取同一批次JSP(顆粒)樣品(S1),按“2.1.1”項下方法平行制備6份供試品溶液,按“2.1.4”項下色譜條件進樣分析,記錄各共有峰的保留時間和峰面積,以柚皮苷為參照峰,計算各共有峰的相對保留時間和相對峰面積。28個共有峰的相對保留時間和相對峰面積的RSD分別小于0.97%和2.90%,表明該提取方法的重復性良好。
2.1.8 指紋圖譜的建立及相似度分析 取10批JSP(顆粒)樣品(S1~S10),按“2.1.1”項下方法制備供試品溶液,按“2.1.4”項下測定方法分析供試品溶液,并記錄生成HPLC圖。采用“中藥色譜指紋譜圖相似度評價系統(2012版)”對上述譜圖進行處理分析,以色譜圖S1為參照圖譜,采用中位數法,時間窗為0.1 min,對10批JSP(顆粒)樣品(S1~S10)的指紋圖譜進行擬合生成對照指紋圖譜(R),根據峰面積的穩定性和分離度共標定了28個共有峰,以柚皮苷為參照峰,結果見圖1。10批JSP(顆粒)樣品(S1~S10)的指紋圖譜與對照指紋圖譜自動匹配,其相似度為0.954~1.000,結果見表1。
2.1.9 共有峰的歸屬與指認 取“2.1.1”“2.1.2”“2.1.3”項下供試品溶液、混合對照品溶液、單味藥材溶液,按“2.1.4”項下色譜條件進樣分析,通過比較各色譜峰的相對保留時間、紫外吸收光譜圖以及單味藥材色譜圖,確定了JSP(顆粒)中28個共有峰(1~28)在6味藥材中的歸屬,結果見圖2、3和表2。結果發現,1、9、11號峰來自白芍,26、27號峰來自枳實,13、28號峰來自炙甘草,2、4、10、12、16、24號峰來自代代花,15、17、22號峰來自半枝蓮,25號峰來自白芍和炙甘草共有,3、5~8、14、18~21、23號峰來自枳實和代代花共有。通過對照品比對保留時間和最大吸收波長,確定了其中的9個成分,即9(芍藥內酯苷)、11(芍藥苷)、13(甘草苷)、17(野黃芩苷)、19(柚皮苷)、20(橙皮苷)、21(新橙皮苷)、26(柚皮素)、28(甘草酸銨)號峰。

圖1 10批JSP (顆粒) 樣品(S1~S10)的HPLC指紋圖譜和對照指紋圖譜(R)
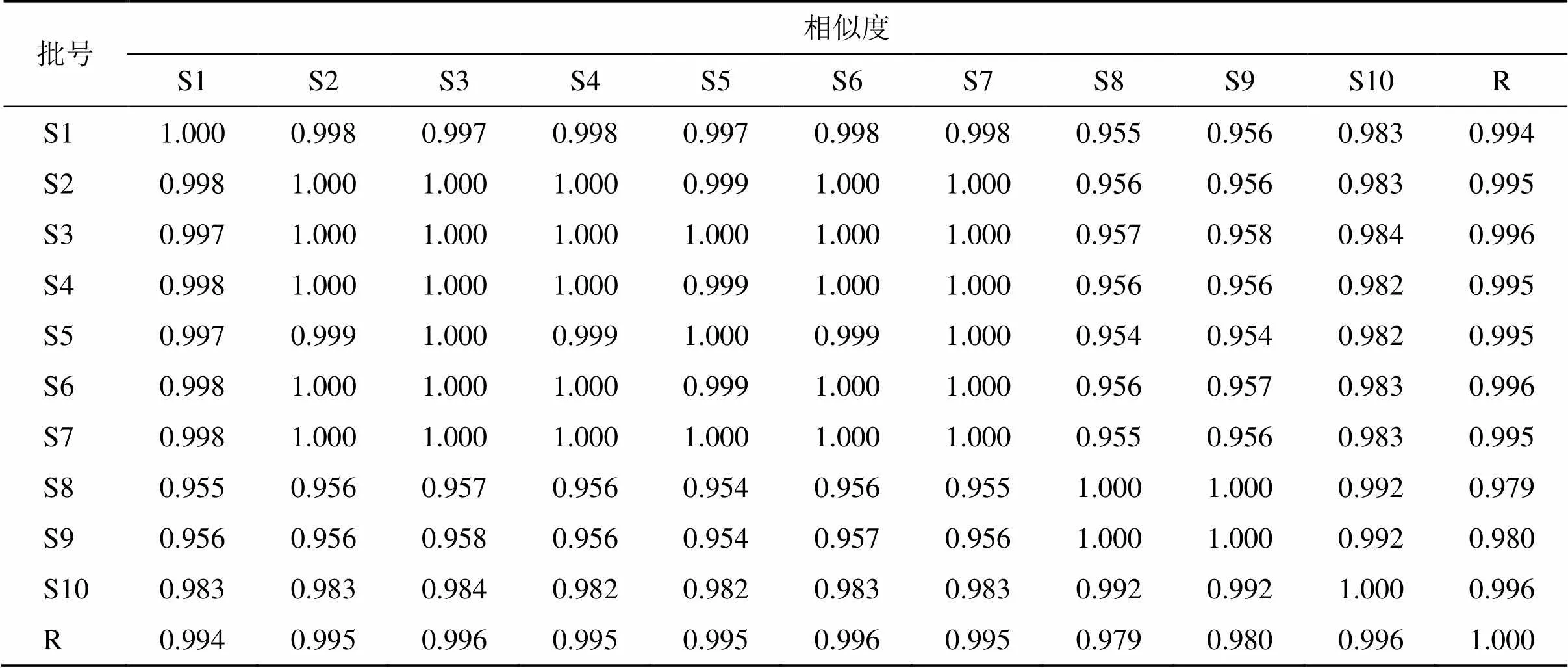
表1 10批JSP(顆粒)指紋圖譜相似度計算結果

圖2 共有峰的藥材歸屬HPLC圖
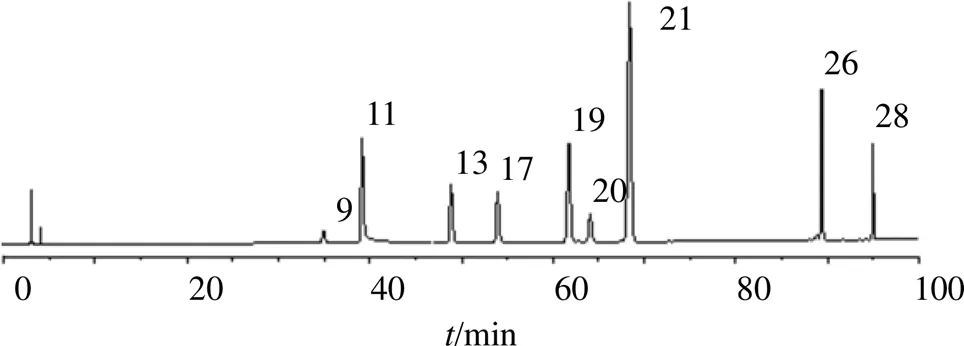
9-芍藥內酯苷 11-芍藥苷 13-甘草苷 17-野黃芩苷 19-柚皮苷 20-橙皮苷 21-新橙皮苷 26-柚皮素 28-甘草酸銨
2.2 主成分分析(principal component analysis,PCA)
將10批胃痛顆粒指紋圖譜共有峰的峰面積為變量,導入SPSS 26.0軟件,以特征值>1為提取標準,得到4個主成分,累積方差貢獻率為95.003%。說明前4個成分可以反映JSP指紋圖譜中的大部分化學信息。通過Kaiser標準化的正交旋轉法,處理得到旋轉后的成分得分系數矩陣。各色譜峰系數反映了成分貢獻率大小,排名前8的成分分別為峰24、23、22、28(甘草酸銨)、26(柚皮素)、27、13(甘草苷)。

表2 JSP (顆粒)共有峰歸屬
2.3 正交偏最小二乘-判別分析(orthogonal partial least squares-discriminant analysis,OPLS-DA)
在PCA分組的基礎上,以10批樣品中28個共有峰面積為原始數據,導入SIMCA-P13.0軟件,進行OPLS-DA建模分析,結果見圖4。從模型驗證的參數圖可知,模型的穩定性和交叉驗證的預測力都較高(2=0.852,R2=0.993,R2=0.986),說明所建立的OPLS-DA模型可以很好地用于不同批次間JSP的分析。

圖4 10批JSP(顆粒)的OPLS-DA得分散點圖
為了進一步確認對樣品分類貢獻度較大的成分,采用OPLS-DA中變量重要性投影值(variable importance projection,VIP)篩選差異性標志物,結果見圖5。按VIP值由大到小篩選出組間具有差異的標志性成分,VIP值越大,成分對樣品分類貢獻越大。由圖可知前15名VIP值較大,分別為峰18、27、13(甘草苷)、17(野黃芩苷)、20(橙皮苷)、11(芍藥苷)、10、14、21(新橙皮苷)、19(柚皮苷)、16、9(芍藥內酯苷)、1、7、4。

圖5 10批JSP(顆粒)中28個共有峰的VIP值
2.4 基于物質-效應關聯的JSP(顆粒)核心成分篩選分析
2.4.1 成分與疾病交集靶點的獲取 綜合考慮JSP的HPLC指紋圖譜結合化學計量學結果,以及基于可測性及可溯性的原則,共篩選出潛在芍藥內酯苷、芍藥苷、甘草苷、野黃芩苷、柚皮苷、橙皮苷、新橙皮苷、柚皮素、甘草酸銨9個指標性成分作為候選成分。在swiss target prediction數據庫獲取這9個指標性成分的作用靶點,并結合中藥系統藥理學數據庫與分析平臺(traditional Chinese medicine systems pharmacology database and analysis platform,TCMSP),確定特征圖譜鑒定出的有效作用靶點。除甘草酸銨無有效作用靶點外,經過Uniport數據庫統一校正去重后共得到成分靶點183個。以“stomachache”“hypochondriac pain”“gastritis”為關鍵詞檢索與胃痛疾病相關的基因,在GeneCards數據庫中獲取疾病作用靶點1581個。最終取藥物成分靶點與疾病靶點交集,得到55個JSP治療胃痛相關疾病的潛在作用靶點(圖6)。
2.4.2 蛋白與蛋白相互作用(protein protein interaction,PPI)網絡關系的構建與關鍵靶點分析 將成分與疾病的交集靶點導入STRING軟件中進行PPI分析,物種限定為“Homo sapiens”。以置信度>0.9作為篩選條件,隱藏無關聯性的點位,得到核心PPI網絡,將網絡圖導入Cytocape 3.8.2軟件中進行可視化分析,包括度值(degree)、介數中心性(betweenness centrality)、接近中心度(closeness centrality)的數值分析,詳細分析圖及拓撲異構參數如圖7和表3所示。篩選得到的核心互作蛋白包括血管內皮生長因子A(vascular endothelial growth factor A,VEGFA)、表皮生長因子受體(epidermal growth factor receptor,EGFR)、腫瘤壞死因子(tumor necrosis factor,TNF)等。

圖6 成分靶點與疾病靶點的韋恩圖

圖7 PPI核心網絡圖
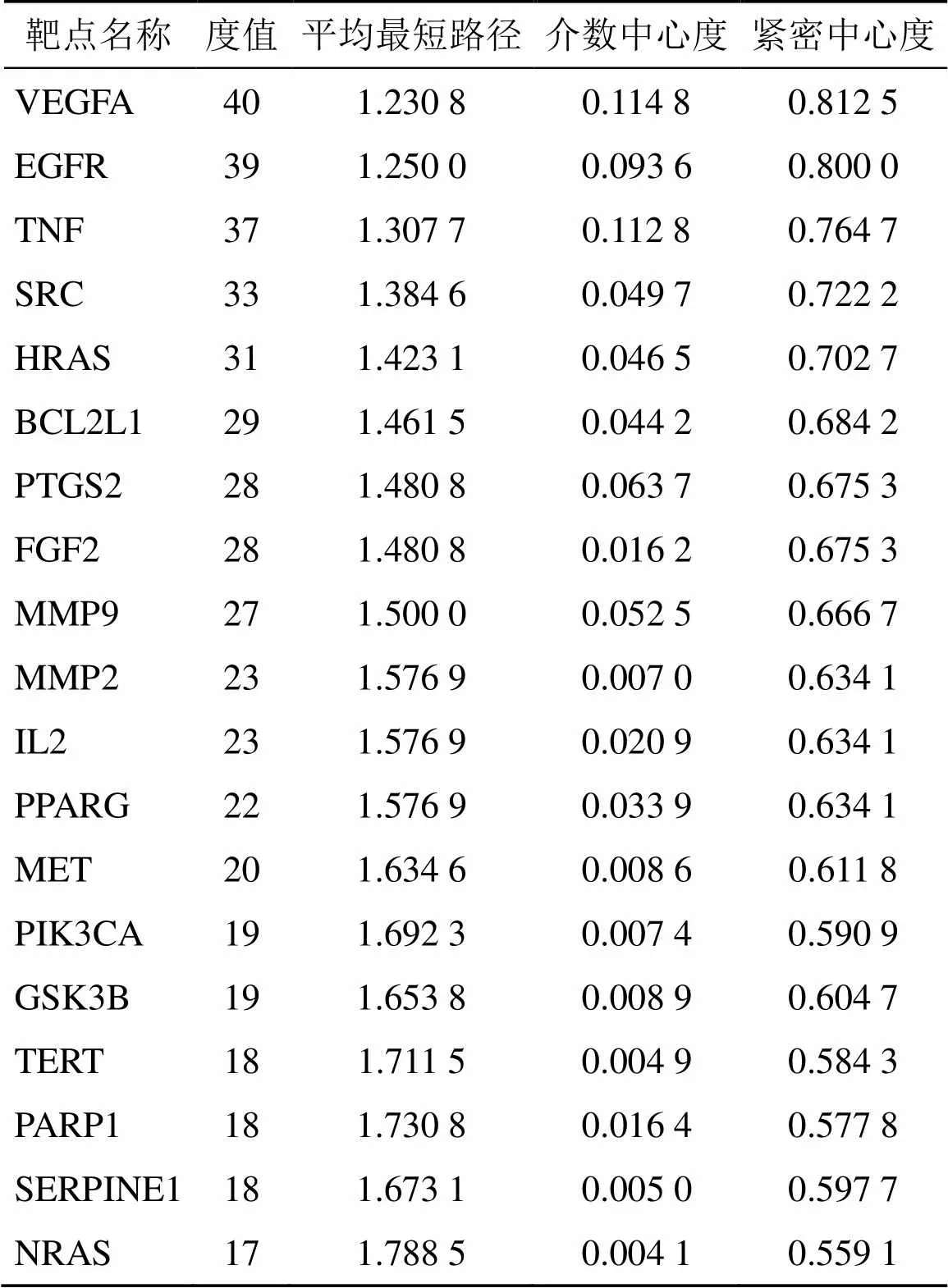
表3 PPI核心拓撲異構參數信息
2.4.3 基因本體論(gene ontology,GO)生物功能注釋與京都基因與基因組百科全書(Kyoto encyclopedia of genes and genomes,KEGG)通路富集 將JSP治療胃痛相關疾病的核心靶點信息導入Metascape平臺和David平臺進行功能和信號通路分析,依據<0.01,涉及靶點數量≥3,富集因子>1.5的條件篩選出關鍵作用通路,結合核心作用通路的有效作用靶點,得到KEGG富集分析-核心靶點-通路作用圖(圖8)。分析結果顯示,JSP治療胃痛相關疾病作用靶點主要富集在Ras信號通路(Ras signaling pathway)、磷脂酰肌醇-3-羥激酶(phosphatidylinositol-3-hydroxykinase,PI3K)-蛋白激酶B(protein kinase B,Akt)信號通路、松弛素信號通路(Relaxin signaling pathway)、Rap1信號通路(Rap1 signaling pathway)等,提示這些經典通路可能在JSP治療胃痛相關疾病作用中發揮著重要作用。
JSP治療胃痛相關疾病在體內的作用位置和生物過程見GO分析圖(圖9)。生物學過程(biological processes,BP)富集分析提示,細胞遷移的正向調節、細胞對氮化合物的反應、半胱氨酸型內肽酶活性的調控在JSP治療胃痛相關疾病中比較重要;細胞組分(cellular component,CC)富集分析表明,靶點的產物可能主要在細胞外基質、薄膜側面、血小板α顆粒部位;分子功能(molecular function,MF)富集分析表明,靶點可能是通過調節蛋白激酶活性、絲氨酸型內肽酶活性、蛋白酪氨酸激酶活性等發揮作用。
2.4.4 物質-效應網絡的構建 為了進一步確定JSP的關鍵效應物質,為后續成分定量及相關方法學檢測分析做鋪墊,擬通過構建物質-效應網絡確定最為核心的效應成分。篩選原則是基于以上的作用靶點及作用通路分析,選出作用最強的前10條作用通路,并與相匹配的作用靶點及成分一一對應,將數據導入Cytoscape軟件中,根據節點度值的連接強度確定核心效應物質(圖10)。研究發現芍藥內酯苷、芍藥苷、橙皮苷、新橙皮苷、柚皮苷的連接強度較大,表明這5種物質相對來說對應更強的效應。
2.4.5 Q-Marker的分析 通過建立JSP的HPLC指紋圖譜,共標定了28個共有峰,指認了9個化學成分,再根據PCA和OPLS-DA結果可知,PCA中對主成分貢獻較大的前8名色譜峰分別為峰24、23、22、28(甘草酸銨)、26(柚皮素)、27、13(甘草苷),OPLS-DA中VIP值前15名色譜峰分別為峰18、27、13(甘草苷)、17(野黃芩苷)、20(橙皮苷)、11(芍藥苷)、10、14、21(新橙皮苷)、19(柚皮苷)、16、9(芍藥內酯苷)、1、7、4。綜合考慮JSP的HPLC指紋圖譜結合化學計量學結果,以及基于可測性及可溯性的原則,剔除未知色譜峰,共篩選出芍藥內酯苷、芍藥苷、甘草苷、野黃芩苷、柚皮苷、橙皮苷、新橙皮苷、柚皮素、甘草酸銨9個指標性成分作為候選成分。將9個候選成分進行網絡藥理學分析,構建物質-效應的網絡,進一步分析JSP的潛在Q-Marker。在物質-效應網絡的構建中,其主要靶點為EGFR、轉化蛋白p21/H-Ras-1(transforming protein p21/H-Ras-1,HRAS)、人絲裂原激活蛋白激酶激酶1(recombinant mitogen activated protein kinase 1,MAP2K1)、血管內皮生長因子A(vascular endothelial growth factor A,VEGFA)等靶點;主要通路為癌癥相關通路、PI3K-Akt信號通路(PI3K-Akt signaling pathway)、Ras信號通路(Ras signaling pathway)等。主要的靶點和信號通路與治療胃痛相關疾病均有一定聯系,如PI3K/Akt信號通路參與胃黏膜上皮重建、促進胃部腫瘤的發生發展[17]。實驗研究表明,PI3K/Akt通路能夠調控萎縮性胃炎和胃癌胃黏膜的損傷程度,當PI3K激活后,在細胞質膜上產生磷脂酰肌醇三磷酸酯,該蛋白與信號蛋白Akt和磷酸肌醇依賴性激酶1結合,后者在細胞中含有PH結構域,導致Akt激活,從而調節胃黏膜細胞的增殖、分化和凋亡[18]。由網絡圖可知芍藥內酯苷、芍藥苷、橙皮苷、新橙皮苷、柚皮苷的連接強度較大,表明這5種物質相對來說對應更強的效應。

圖8 KEGG富集分析-核心靶點-通路作用圖

圖9 GO富集分析圖

圖10 物質-效應網絡圖
有文獻報道,以芍藥苷和芍藥內酯苷為代表的單萜及其苷類成分具有鎮痛、抗炎的作用,是白芍中公認的藥效物質,以前者含有量最高,為質量控制指標成分[19-20]。橙皮苷、新橙皮苷、柚皮苷等黃酮類成分具有胃排空、改善大鼠的胃潰瘍癥狀及抗炎鎮痛等作用[21-22];枳實中柚皮苷和新橙皮苷被預測為Q-Marker[23]。研究表明[6],代代花中含有豐富的揮發油、柚皮苷、橙皮苷、新橙皮苷等二氫黃酮類成分,具有抗炎、抗病毒、促進胃腸蠕動等藥理作用。
綜上所述,通過指紋圖譜和化學計量學分析所獲得的9個指標性成分可通過作用于多靶點、干預多條通路發揮藥效作用,說明指紋圖譜結合化學計量學所選的指標成分具有合理性。而從物質-效應網絡中可知,9個指標性成分中,芍藥內酯苷、芍藥苷、橙皮苷、新橙皮苷、柚皮苷的連接強度較大,表明這5種物質相對來說對應更強的效應。因此,綜合有效性、可測性和可溯源性原則,確定芍藥內酯苷、芍藥苷、橙皮苷、新橙皮苷、柚皮苷為JSP的潛在Q-Marker,可作為JSP的檢測成分。
2.5 JSP(顆粒)中5個成分含量測定
2.5.1 供試品溶液的制備 制備方法同“2.1.1”項。
2.5.2 對照品溶液的制備 取各對照品適量,精密稱定,加70%甲醇分別制成含芍藥內酯苷1 mg/mL、芍藥苷2 mg/mL、柚皮苷3 mg/mL、橙皮苷1 mg/mL、新橙皮苷3 mg/mL的單一對照品儲備液:分別吸取以上5種對照品儲備液適量,加70%甲醇制成不同質量濃度的混合對照品溶液。
2.5.3 陰性樣品溶液的制備 按JSP(顆粒)處方工藝分別制備缺白芍陰性、缺枳實、代代花的陰性樣品,按“2.1.1”項下方法制備陰性樣品溶液。
2.5.4 色譜條件 色譜柱為X Select?HSS T3 C18柱(250 mm×4.6 mm,5 μm);流動相為乙腈-0.1%磷酸水溶液;梯度洗脫條件:0~10 min,2%~3%乙腈;10~15 min,3%~14%乙腈;15~25 min,14%~19.5%乙腈;25~35 min,19.5%~21.5%乙腈;35~45 min,21.5%~22%乙腈;45~47 min,22%~42%乙腈;47~55 min,42%~50%乙腈;55~58 min,50%乙腈;體積流量1.0 mL/min;柱溫25 ℃;進樣體積10 μL;紫外檢測波長為230 nm。
2.5.5 系統適用性與專屬性試驗 取“2.5.1”~“2.5.3”項下的供試品溶液、混合對照品溶液和陰性樣品溶液,按“2.5.4”項下液相色譜條件進樣測定,結果如圖11所示,5種指標成分色譜峰于其相鄰色譜峰之間的分離度均>1.5,各陰性樣品溶液色譜圖在待測成分出峰位置無干擾,表明該方法下5種成分專屬性良好。

1-芍藥內酯苷 2-芍藥苷 3-柚皮苷 4-橙皮苷 5-新橙皮苷
2.5.6 線性關系考察 將“2.5.2”項下制成的5個質量濃度的混合對照品溶液,按“2.5.4”項下色譜條件進樣測定,并記錄5種成分的峰面積。以質量濃度為橫坐標(),以峰面積為縱坐標()進行線性回歸,分別繪制標準曲線并得到相關系數和線性范圍,結果分別為芍藥內酯苷=11 338 712.0+8 780.3,=1.000 0,線性范圍3.571~238.000 μg/mL;芍藥苷=13 110 958.8+59 875.4,=0.999 7,線性范圍12.60~492.00 μg/mL;柚皮苷=25 184 174.0+145 092.5,=1.000 0,線性范圍254.0~1 222.0 μg/mL;橙皮苷=23 394 991.5-108 034.5,=0.999 6,線性范圍6.144~400.000 μg/mL;新橙皮苷=24 395 012.9-122 447.7,=0.999 9,線性范圍56.83~1 820.00 μg/mL;結果表明5種成分在各自質量濃度范圍內線性關系均良好。
2.5.7 精密度試驗 取樣品(S1)約2 g,按“2.5.1”項下方法制備供試品溶液,按“2.5.4”項下色譜條件連續進樣6次,記錄峰面積,計算各成分RSD值。結果顯示,5種成分芍藥內酯苷、芍藥苷、柚皮苷、橙皮苷、新橙皮苷的峰面積RSD分別為0.9%、0.4%、0.6%、0.6%、0.5%,表明儀器精密度良好。
2.5.8 穩定性試驗 取樣品(S1)約2 g,按“2.5.1”項下方法制備供試品溶液,于室溫下放置0、2、4、8、12、24 h后,按“2.5.4”項下色譜條件進樣分析,記錄峰面積,計算各成分RSD值。結果顯示,5種成分芍藥內酯苷、芍藥苷、柚皮苷、橙皮苷、新橙皮苷的峰面積RSD分別為1.7%、0.7%、0.3%、0.5%、0.4%,表明供試品溶液在24 h內穩定性良好。
2.5.9 重復性試驗 取同一批次的樣品(S1),每份約2 g,按“2.5.1”項下方法平行制備6份供試品溶液,按“2.5.4”項下色譜條件分別進樣分析,記錄峰面積,計算各成分含量及其RSD值。結果顯示,5種成分芍藥內酯苷、芍藥苷、柚皮苷、橙皮苷、新橙皮苷質量分數的RSD分別為1.7%、0.7%、0.3%、0.5%、0.4%,表明提取方法的重復性良好。
2.5.10 加樣回收率試驗 取同一批次已測定5種成分含量的樣品(S1)6份,每份1.0 g,精密稱定,分別加入具塞錐形瓶中,精密加入1 mL混合對照品溶液(與樣品中5種待測成分相同含量的混合對照品溶液),按“2.5.1”項下方法制備供試品溶液,按“2.5.4”項下色譜條件進樣測定,記錄峰面積,計算6份供試品平均加樣回收率及RSD值。結果顯示,芍藥內酯苷、芍藥苷、柚皮苷、橙皮苷、新橙皮苷的平均加樣回收率分別為95.23%、96.48%、92.52%、94.26%、93.96%,RSD分別為2.6%、0.95%、2.0%、1.4%、1.3%,表明提取方法的準確度良好。
2.5.11 供試品含量測定 取10批JSP(顆粒)樣品(S1~S10)各2 g,按“2.5.1”項下方法分別制備供試品溶液,按“2.5.4”項下色譜條件進樣測定,記錄峰面積,計算樣品中5種成分平均含量,結果見表4。結果顯示10批JSP(顆粒)樣品(S1~S10)中成分芍藥內酯苷在0.107 6~0.203 6 mg/g、芍藥苷在0.475 9~1.204 6 mg/g、柚皮苷在2.310 9~5.223 8 mg/g、橙皮苷在0.410 3~0.796 8 mg/g、新橙皮苷在4.311 9~8.343 3 mg/g,10批樣品中5種成分平均含量波動范圍不大,制備工藝穩定。
3 討論
本實驗基于Q-Marker可測、特有、有效、傳遞及配伍“五原則”,首先采用HPLC建立JSP(顆粒)指紋圖譜,篩選出28個共有峰,確定了28個共有峰在6味藥材中的歸屬,并結合PCA及OPLS-DA和可測性,篩選出9個候選Q-Marker,分別為芍藥內酯苷、芍藥苷、甘草苷、野黃芩苷、柚皮苷、橙皮苷、新橙皮苷、柚皮素、甘草酸銨。隨后采用網絡藥理學方法從有效性方面對9個可能的標志物成分進行靶點預測及相關通路的富集,涉及的靶點和通路與治療胃痛相關癥狀有關,主要包括VEGFA、EGFR、TNF、SRC、HRAS、BCL2L1、PTGS2等核心靶點,富集的通路包括Ras signaling pathway、PI3K-Akt signaling pathway、Relaxin signaling pathway、Rap1 signaling pathway等,最終預測得到5個Q-Marker成分,建立其HPLC含量測定方法。

表4 10批JSP (顆粒) 中5個成分的含量測定結果(n = 3)
建立JSP(顆粒)的指紋圖譜,從整體上對其質量進行控制,本實驗分別考察了甲醇-水、乙腈-水、乙腈-0.1%磷酸水溶液、甲醇-0.1%硫酸水溶液5 種不同的流動相下色譜峰的分離情況,結果發現流動相為乙腈-水、甲醇-水時,峰較少,流動相為乙腈-0.1%磷酸水溶液、甲醇-0.1%磷酸水溶液溶液時,峰的數量接近,但乙腈-0.1%磷酸水溶液系統各峰分離效果好,故選擇乙腈-0.1%磷酸水溶液為流動相。同時,采用200~400 nm全波長掃描,發現在240 nm處色譜峰數目較多,各峰吸收較均勻,可體現指紋圖譜的整體性和模糊性。而在對芍藥內酯苷、芍藥苷、柚皮苷、橙皮苷、新橙皮苷5種成分進行含量測定時,發現檢測波長230 nm時的峰信號響應值較高,分離度良好,可同時測定5種成分含量。另外,考察了色譜柱溫度(25、30、35 ℃),體積流量(0.8、1.0、1.2 mL/min)及不同類型色譜柱,最終確定上述色譜條件。
綜上所述,本研究首次采用指紋圖譜結合化學計量學聯合網絡藥理學的方法,預測JSP(顆粒)的Q-Marker,然后測定其含量,為JSP研制成古代經典名方中藥復方制劑提供質量控制依據,同時也為中藥質量控制指標性成分的選擇提供了一種新的思路。
利益沖突 所有作者均聲明不存在利益沖突
[1] 楊麗華, 馬春. 中醫治療胃痛的研究進展 [J]. 世界中西醫結合雜志, 2007, 2(9): 553-555.
[2] 吳遷. 疏肝健脾和胃法治療消化科肝胃不和型胃脘痛的效果分析 [J]. 現代消化及介入診療, 2018, 23(S2): 111-112.
[3] 趙愛紅, 趙雪勤, 景忠良. 中西醫結合治療胃脘痛的臨床觀察與辨證施護 [J]. 中國民間療法, 2012, 20(3): 70.
[4] 徐凌志, 李樹波. 四逆散的神經系統藥理作用與臨床應用 [J]. 長春中醫藥大學學報, 2010, 26(1): 126-127.
[5] 吳紅偉, 李東輝, 張育貴, 等. 四逆散研究進展及質量標志物的預測分析 [J]. 中華中醫藥學刊, 2021, 39(12): 13-20.
[6] 王婷, 婁鑫, 苗明三. 代代花的現代研究與思考 [J]. 中醫學報, 2017, 32(2): 276-278.
[7] 中國藥典[S]. 一部. 2020: 122-123.
[8] 劉昌孝, 陳士林, 肖小河, 等. 中藥質量標志物(Q-Marker): 中藥產品質量控制的新概念 [J]. 中草藥, 2016, 47(9): 1443-1457.
[9] 劉昌孝. 中藥質量標志物 (Q-marker): 提高中藥質量標準及質量控制理論和促進中藥產業科學發展 [J]. 中草藥, 2019, 50(19): 4517-4518.
[10] Zhang L, Jia Y Z, Li B,. A review of lignans from genusand their spectrum characteristics [J]., 2021, 13(2): 157-166.
[11] 劉昌孝. 中藥質量標志物(Q-Marker)研究發展的5年回顧 [J]. 中草藥, 2021, 52(9): 2511-2518.
[12] 李佳涵, 王慧, 劉佳星, 等. 整合指紋圖譜與多成分含量測定的酸棗仁湯質量評價研究 [J]. 中草藥, 2022, 53(15): 4698-4708.
[13] 王堯, 張小飛, 鄒俊波, 等. 當歸揮發油治療高血壓藥理機制的網絡分析 [J]. 天然產物研究與開發, 2021, 33(4): 657-666.
[14] 王迎春, 馬永犇, 甄亞欽, 等. 基于指紋圖譜和網絡藥理學的芍藥甘草湯抗肝損傷活性成分及含量測定研究 [J]. 世界科學技術—中醫藥現代化, 2022, 24(8): 3030- 3042.
[15] 李海倫, 李恒, 孫飛, 等. 經典名方大秦艽湯HPLC指紋圖譜及含量測定方法研究 [J]. 中草藥, 2021, 52(1): 99-107.
[16] 牛明, 張斯琴, 張博, 等.《網絡藥理學評價方法指南》解讀 [J]. 中草藥, 2021, 52(14): 4119-4129.
[17] 孫兆瑞, 劉紅梅, 楊志洲, 等. 腸三葉因子介導PI3K/ Akt信號通路保護胃黏膜上皮細胞緊密連接 [J]. 臨床急診雜志, 2014, 15(7): 379-382.
[18] Rao V S, Srinivas K, Sujini G N,. Protein-protein interaction detection: Methods and analysis [J]., 2014, 2014: 147648.
[19] 吳麗, 王麗麗, 費文婷, 等. 芍藥苷和芍藥內酯苷對小鼠疼痛模型的鎮痛作用及對β-EP、PGE2的影響 [J]. 中華中醫藥雜志, 2018, 33(3): 915-918.
[20] 張燕麗, 田園, 付起鳳, 等. 白芍的化學成分和藥理作用研究進展 [J]. 中醫藥學報, 2021, 49(2): 104-109.
[21] Chen K H, Weng M S, Lin J K. Tangeretin suppresses IL-1beta-induced cyclooxygenase (COX)-2 expression through inhibition of p38 MAPK, JNK, and AKT activation in human lung carcinoma cells [J]., 2007, 73(2): 215-227.
[22] 謝仁峰, 文雙娥, 李洋, 等. 柚皮苷抗炎鎮痛作用的實驗研究 [J]. 湖南師范大學學報: 醫學版, 2011, 8(4): 5-8.
[23] 許姍姍, 許浚, 張笑敏, 等. 常用中藥陳皮、枳實和枳殼的研究進展及質量標志物的預測分析 [J]. 中草藥, 2018, 49(1): 35-44.
Analysis of quality markers of Jiawei Sini Powder (Granules) based on HPLC fingerprint and network pharmacology and establishment of content determination method
CHEN Jing-mei1, 2, 3, 4, LI Ze-yu2, 3, 4, 5, LIANG Qiu-ming6, YUE Zi-jun1, TANG Zuo-wei1, HAO Er-wei2, 3, 4, 5, DU Zheng-cai2, 3, 4, 5, HOU Xiao-tao1, 2, 3, 4, DENG Jia-gang2, 3, 4, 5
1. Faculty of Pharmacy, Guangxi University of Chinese Medicine, Nanning 530200, China 2. Guangxi Key Laboratory of Efficacy Study on Chinese Materia Medica, Nanning 530200, China 3. Guangxi Collaborative Innovation Center of Research on Functional Ingredients of Agricultural Residues, Nanning 530200, China 4. Guangxi Key Laboratory of Theory and Transformation of Damp Disease Prescriptions, Nanning 530200, China 5. Guangxi Scientific Experimental Center of Traditional Chinese Medicine, Guangxi University of Chinese Medicine, Nanning 530200, China 6. Guangxi Qinzhou Hospital of Traditional Chinese Medicine, Qinzhou 535000, China
To analyze and predict potential quality markers (Q-Marker) of Jiawei Sini Powder (JSP, 加味四逆散) (Granules), and determine the content of Q-Marker components based on fingerprint and network pharmacology methods, providing reference for quality control.Firstly, the potential Q-Marker of JSP (Granules) were analyzed by fingerprint and chemometrics. On this basis, a substance effect network was constructed through network pharmacology to further analyze and predict the Q-Marker associated with the efficacy of JSP (Granules), and an HPLC method was established to determine the content of the predicted landmark components.An HPLC fingerprint of JSP (Granules) was established, identifying 28 common peaks, and assigning them to different peaks. Among them, peaks 1, 9, and 11 come from Baishao (, PRA), peaks 26, and 27 come from Zhishi (, AFI), peaks 13, and 28 come from Zhigancao (etcum, GRRPM), peaks 2, 4, 10, 12, 16, and 24 come from Daidaihua (var.), peaks 15, 17, and 22 come from Banzhilian (), peaks 25 come from both PRA and GRRPM, peaks 3, 5—8, 14, 18—21, and 23 come from both AFI andvar.. Nine common peaks were identified, including albiflorin, paeoniflorin, glycyrrhizin, scutellarin, naringin, and hesperidin, neohesperidin, naringin, ammonium glycyrrhetate. The similarity evaluation showed that the similarity of 10 batches of JSP (Granules) samples ranges from 0.954—1.000. Principal component analysis (PCA) showed that the cumulative variance contribution rate of the first four principal components was 95.003%, while orthogonal partial least squares-discriminant analysis (OPLS-DA) showed that 12 components had higher variable importance projection values. On this basis, the network pharmacology method was used to analyze and conclude that albiflorin, paeoniflorin, naringin, hesperidin and neohesperidin may be the potential Q-Marker of JSP (Granules). The content of the above five components was determined simultaneously, and the methodological investigation results were good. The average sample recovery rate was 92.52%—96.48%, and the RSD was 1.3%—2.6%. The mass fractions of albiflorin, paeoniflorin, naringin, hesperidin, and neohesperidin in 10 batches of samples were 0.107 6—0.203 6, 0.475 9—1.204 6, 2.310 9—5.223 8, 0.410 3—0.796 8, 4.311 9—8.343 3 mg/g.This study established an HPLC fingerprint of JSP (Granules) and combined it with network pharmacology to predict five Q-marker components and establish a quantitative determination method, providing a quality control basis for the development of JSP (Granules) into ancient classic Chinese medicine compound formulations.
Jiawei Sini San; quality markers; HPLC; fingerprint; network pharmacology; principal component analysis; orthogonal partial least squares-discriminant analysis; albiflorin; paeoniflorin; naringin; hesperidin; neohesperidin
R283.6
A
0253 - 2670(2023)20 - 6682 - 12
10.7501/j.issn.0253-2670.2023.20.012
2023-05-26
中國東盟傳統藥物研究國際合作聯合實驗室建設(二期)資助項目(AD19110165);廣西中醫藥大學2022年研究生教育創新計劃項目(YCSZ2022004);2020年度廣西中藥藥效研究重點實驗室運行補助項目(20-065-38)
陳靜梅(1996—),女,廣西梧州人,碩士研究生,從事中藥分析學研究。Tel: 13257715817 E-mail: 2369375473@qq.com
通信作者:侯小濤(1969—),女,博士生導師,教授,從事中藥活性成分與質量控制研究。E-mail: xthou@126.com
[責任編輯 鄭禮勝]

