不同踝下流出道病變程度糖尿病足患者接受膝下動脈球囊擴張的療效及其影響因素
林 峰,陳鈴雄,劉 羽,張旭明,尹志達
糖尿病足是糖尿病常見并發癥,近年來隨著人們生活水平的不斷提高和飲食結構的改變,糖尿病足的發病率逐年增加,全世界約15%的糖尿病患者患有足潰瘍和壞疽,每年截肢患者中有50%是糖尿病患者,其中85%以上的患者因足潰瘍惡化導致深度感染或壞疽而截肢[1]。糖尿病代謝異常可導致動脈結構和功能的改變,表現為外周動脈硬化和閉塞,好發于膝以下的腘動脈、脛動脈及其分支,下肢動脈粥樣硬化閉塞癥(arteriosclerosis occlusion,ASO)可導致嚴重的肢體缺血,是糖尿病足發病和截肢的主要原因[2]。動脈球囊擴張術是治療外周動脈病變的主要方法,治療癥狀性股淺動脈和腘動脈疾病具有較高的初始成功率和安全性[3]。糖尿病足合并ASO患者接受膝下動脈球囊擴張術治療可降低動脈狹窄率,減輕足部潰瘍,促使潰瘍愈合,但是動脈球囊擴張術后血管再狹窄率也較高[3-4],影響手術治療效果,增加患者醫療負擔。研究顯示膝下流出道不良影響ASO 患者支架通暢率,增加靶血管再狹窄風險[5]。糖尿病足患者ASO 往往累及腓動脈末段和足弓的動脈,踝下流出道病變程度是否影響膝下動脈球囊擴張療效尚不清楚。本研究回顧性分析糖尿病足患者不同踝下流出道病變程度對膝下動脈球囊擴張療效的影響,以期為臨床治療提供參考。
1 材料與方法
1.1 臨床資料
選擇2020 年10 月至2021 年10 月福建醫科大學附屬閩東醫院介入血管外科收治的糖尿病膝下ASO 患者153 例。納入標準:①2 型糖尿病,診斷符合《中國2 型糖尿病防治指南(2020 年版)》[6];②經B 超、CTA、MRA 或DSA 診斷為膝下動脈ASO;③Rutherford 分級3~5 級;④膝下TASCⅡ分級C、D 級;④同側髂股動脈病變已經處理,膝下動脈靶血管開通成功。排除標準:①造影劑過敏;②Rutherford分級6 級,已經發生肢體缺血壞死;③晚期腫瘤;④合并腘動脈、髂股動脈病變影響到膝下動脈血流;⑤靶病變血管遠端沒有流出道;⑥嚴重心、腦、腎重要臟器疾病影響腔內治療;⑦孕婦或不能接受X 線檢查的患者;⑧隨訪失聯。本研究已經獲得醫院倫理委員會批準,患者及其家屬均知情同意簽署同意書。
1.2 踝下流出道病變程度評估
術前采用全球血管指南(GVG)提出的全球肢體解剖分期系統(GLASS)評估患者踝下流出道(包括腓動脈末段和足弓的動脈)病變程度。分為3 級,P0:目標動脈經踝關節進入足部,且足弓動脈完整;P1:目標動脈經踝關節進入足部,但足弓動脈缺如或嚴重病變;P2:無目標動脈經踝關節進入足部[7]。
1.3 膝下動脈球囊擴張治療
參考《下肢動脈硬化閉塞癥診治指南》[8]治療原則,所有患者符合手術指征,無明顯手術禁忌。膝下動脈球囊擴張成型術:患者仰臥于DSA 操作臺上,于左側腹股溝采用2%利多卡因局部浸潤麻醉,Seldinger 技術穿刺,置入5-6 F 股動脈鞘,全身肝素化(100 U/kg),經鞘推注對比劑,確定病變部位、程度及遠端流出道情況。泥鰍導絲配合導管到達腘動脈,0.014 英寸導絲配合微導管開通堵塞血管,開通成功后再次造影明確是否在真腔內。根據血管直徑及狹窄長度選擇合適球囊,球囊完全覆蓋狹窄病變部位,盡量一次擴張成功,以防引起血管痙攣;管腔嚴重狹窄病變部位,先采用小直徑球囊導管預擴張,再送較大直徑球囊導管逐級擴張(由遠及近擴張壓力6~8 amt,每次3 min),注意避免血管夾層及破裂。擴張結束血管造影確定擴張效果,以目標血管血流恢復、遠端小腿動脈3 支中有1 支以上通暢并到達足部(脛前至足背動脈、脛后至足底內外側動脈)、殘余狹窄<30%為技術成功。拔除血管鞘管,穿刺點紗布覆蓋后彈力繃帶加壓包扎。術后術側患肢制動6 h,觀察穿刺口滲血及遠端血供等情況。口服利伐沙班2.5 mg,2 次/d,阿司匹林100 mg,1 次/d,連續服用至出院后6 個月,囑患者戒煙,控制血糖。術后3、6、12 個月電話隨訪配合門診復查,統計術后3、6、12個月靶血管通暢率以及隨訪期間靶血管再狹窄情況。靶血管通暢率:一期通暢率,術后病變血管無明顯狹窄或閉塞,無需干預;二期通暢率,管腔殘余狹窄>50%,且出現典型臨床癥狀(間歇性跛行或靜息痛),需要至少1 次管腔內介入治療[9]。靶血管再狹窄定義為血管多普勒超聲檢查提示收縮期流速峰值比(peak systolic velocity ratio,PSVR)>2.4,PSVR=最窄部位收縮期流速峰值/相對正常段流速×100%[10]。
1.4 相關臨床資料收集
收集患者年齡、性別、吸煙史、飲酒史、基礎疾病(高血壓、冠心病、高脂血癥)、Fontaine 分期、TASC Ⅱ分級、踝肱指數(ankle brachial index,ABI)、球囊類型(藥物涂層球囊、普通球囊)、潰瘍愈合情況、支架置入數量、支架總長度、踝下流出道病變程度。ABI 指踝部動脈收縮壓與上臂(肱動脈)收縮壓的比值,通過肢體的節段性壓力測量獲得。
1.5 統計學分析
應用SPSS 25.00 軟件進行數據分析。計量資料符合正態分布以±s 表示;計數資料以例(%)表示,比較采用χ2檢驗,兩兩比較采用校正χ2檢驗。繪制Kaplan-Meier 生存曲線,Log-rank 檢驗不同踝下流出道病變程度糖尿病足患者靶血管再狹窄率。單因素和多因素Cox 回歸分析糖尿病足患者接受膝下動脈球囊擴張術后靶血管再狹窄的影響因素。檢驗水準α=0.05,校正檢驗水準α=0.017。
2 結果
2.1 糖尿病足患者基線資料
153 例糖尿病足患者男性82 例,女性71 例,年齡(55.3±8.2)歲(46~68 歲);吸煙史98 例,飲酒史49 例;高血壓101 例,冠心病42 例,高脂血癥77 例;Rutherford 分級3 級46 例,4 級60 例,5 級47 例;下肢潰瘍47 例;膝下TASC Ⅱ分級:C 級101 例,D 級52 例。ABI(0.62±0.21);藥物涂層球囊擴張62 例,普通球囊擴張91 例;支架置入數量(2.15±0.69)枚(1~4枚);支架總長度(19.51±3.26)cm(14~25 cm)。
2.2 不同踝下流出道病變程度糖尿病足患者靶血管通暢率和潰瘍愈合情況比較
所有患者技術成功率為100%。患者中P0 組34 例,P1 組61 例,P2 組58 例。P0 組術后3、6、12 個月一期、二期靶血管通暢率高于P1 組、P2 組(P<0.017),P1組和P2 組術后3、6、12 個月一期、二期靶血管通暢率比較差異無統計學意義(P>0.017),見表1、2。P0組2 例潰瘍均愈合,P1 組21 例潰瘍愈合5 例,P2組24 例潰瘍,愈合6 例,3 組潰瘍愈合情況比較差異無統計學意義(χ2=5.471,P>0.017)。
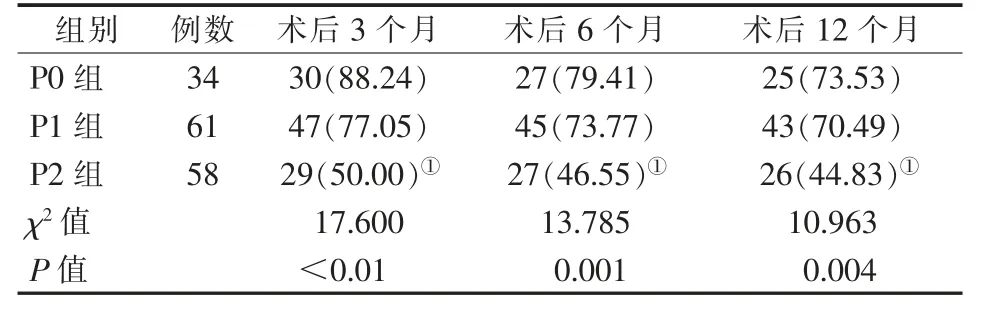
表1 不同踝下流出道病變程度患者一期靶血管通暢率[例(%)]
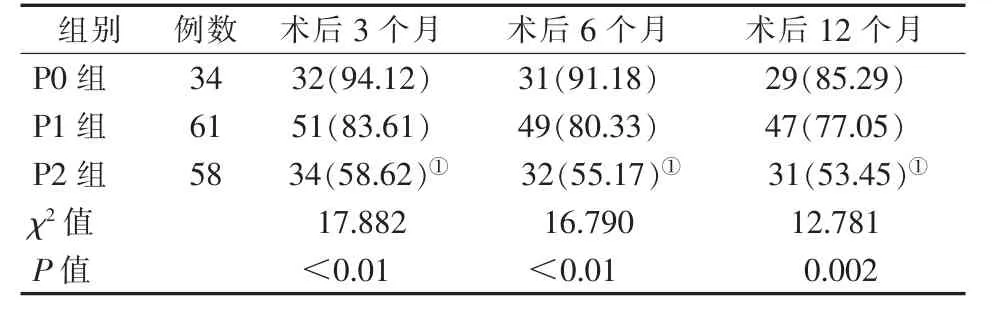
表2 不同踝下流出道病變程度患者二期靶血管通暢率[例(%)]
2.3 不同踝下流出道病變程度糖尿病足患者隨訪期間靶血管再狹窄發生情況
隨訪期間153 例糖尿病足患者發生靶血管再狹窄46 例,P0 組5 例,P1 組14 例,P2 組27 例,靶血管再狹窄率分別為14.71%、22.95%、46.55%,3 組隨訪期間靶血管再狹窄率差異有統計學意義(χ2=12.330,P<0.05),見圖1。
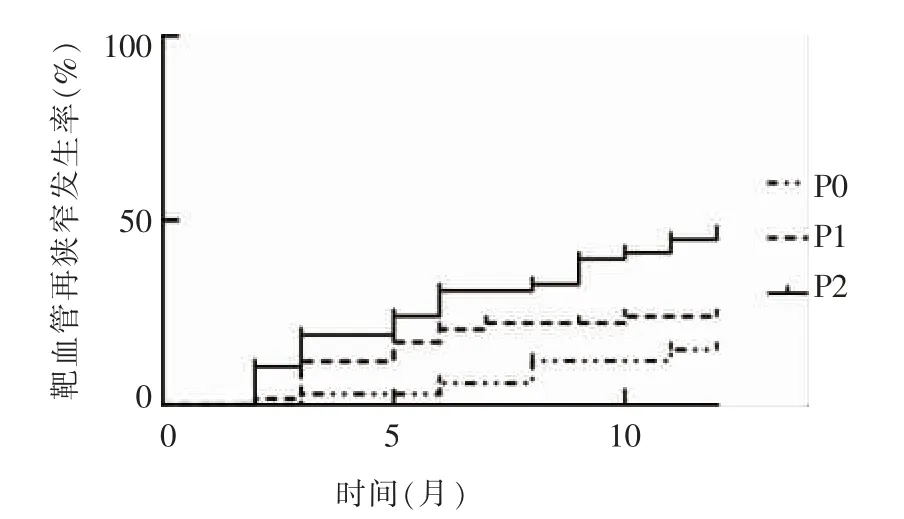
圖1 隨訪期間不同踝下流出道病變程度糖尿病足患者靶血管再狹窄的Kaplan-Meier 曲線圖
2.4 糖尿病足患者接受膝下動脈球囊擴張術后靶血管再狹窄的因素
以性別、年齡、吸煙史(賦值:0=否,1=是)、飲酒史(賦值:0=否,1=是)、高血壓(賦值:0=否,1=是)、冠心病(賦值:0=否,1=是)、高脂血癥(賦值:0=否,1=是)、Rutherford 分級(賦值:0=3 級,1=4~5 級)、TASCⅡ分級(賦值:0=C 級,1=D 級)、ABI、球囊類型(賦值:0=藥物涂層球囊,1=普通球囊)、支架置入數量、支架總長度、踝下流出道病變程度(賦值:0=P0、P1,1=P2)為自變量,以糖尿病足患者接受膝下動脈球囊擴張術后是否發生靶血管再狹窄為因變量(賦值:0=否,1=是),建立Cox 回歸方程。單因素分析結果顯示Rutherford 分級、TASCⅡ分級、ABI、球囊類型、踝下流出道病變程度與糖尿病足患者接受膝下動脈球囊擴張術后靶血管再狹窄有關(P<0.05)。多因素分析結果顯示TASCⅡ分級D 級、踝下流出道病變程度是糖尿病足患者接受膝下動脈球囊擴張術后靶血管再狹窄的危險因素(P<0.05),藥物涂層球囊是保護因素(P<0.05),見表3。
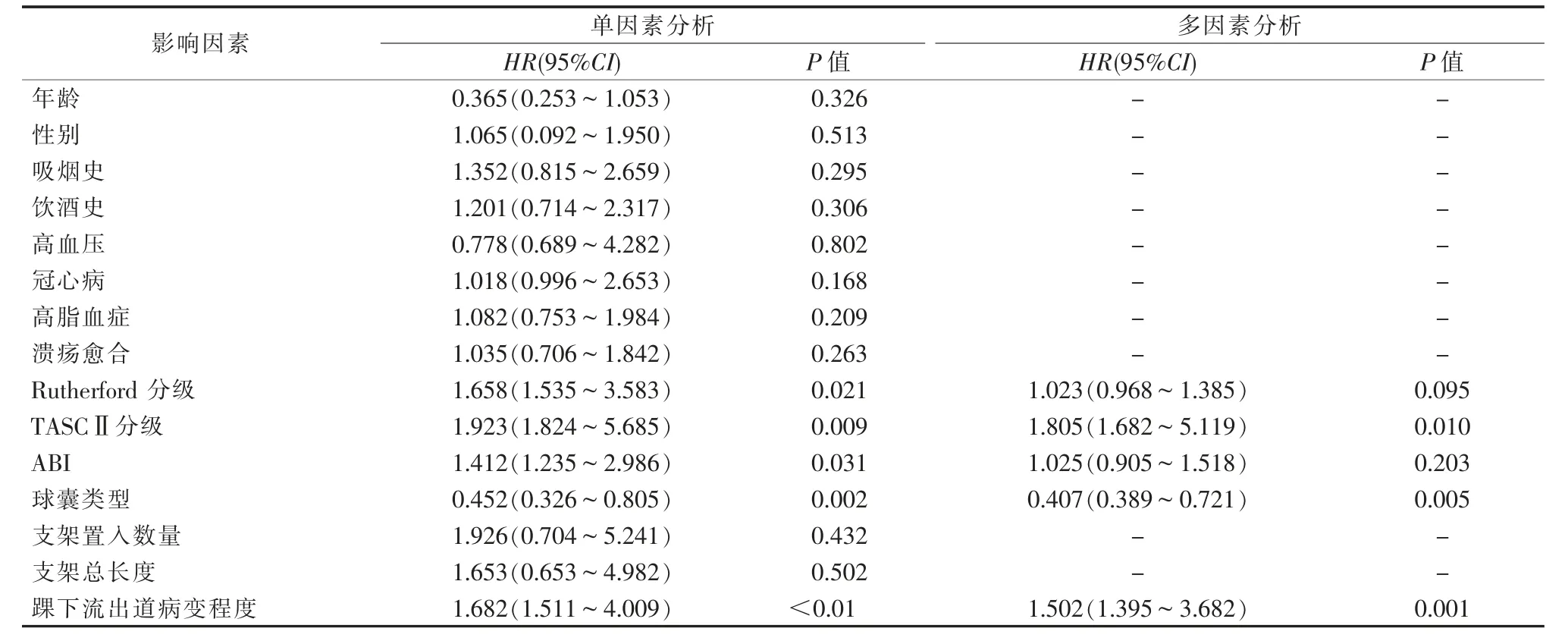
表3 單因素和多因素Cox 回歸分析糖尿病足患者接受膝下動脈球囊擴張術后靶血管再狹窄的影響因素
3 討論
糖尿病足合并下肢ASO 所致缺血性血管病變特點為同時累及多節段,即累及股淺動脈的同時往往合并腘動脈和小腿動脈病變,尤其是小腿動脈很容易受累,可發展成嚴重肢體缺血,若不進行手術干預,截肢及死亡的風險極大[11]。球囊擴張術是腔內治療股腘及膝下動脈病變的首選方案,但術后再狹窄高,隨著腔內裸金屬支架的出現,解決了術后血管彈性回縮等問題,短期療效有所改善,長期通暢率可達60%~75%;但由于下肢ASO 累及動脈血管直徑細小,裸支架置入易引起血管損傷和內膜新生,造成支架內再狹窄與閉塞以及支架斷裂等并發癥,影響病變動脈遠期通暢率[12]。
研究報道,膝下動脈通暢性與藥物涂層球囊擴張術后1 年血管通暢率有關,通暢膝下動脈條數>1 條的股腘動脈硬化閉塞性病變患者血管通暢率高于通暢膝下動脈條數≤1 條的患者;此外,膝下流出道不良是TASC ⅡA、C 和D 級股腘動脈病變患者血管內治療后再狹窄的預測因子[13-14]。以上研究表明膝下流出道不良可能與球囊擴張術靶血管是否通暢有關,但踝下流出道狀態是否影響糖尿病足患者球囊擴張療效尚未見報道。糖尿病足患者由于大血管和微血管病變,動脈灌注不足,往往出現足部微循環障礙和踝下流出道不良,超聲影像學研究發現糖尿病患者足部血流峰值強度較健康對照組顯著降低,達峰時間顯著延長[15]。《慢性肢體威脅性缺血治療的全球血管指南》[16]指出對于伴組織損傷的慢性肢體威脅性缺血患者,腔內球囊擴張治療成功血運重建往往需要恢復足部動脈的血流供應。推測踝下流出道病變程度可能對腔內球囊擴張治療存在一定影響。
GLASS 是一種評價慢性肢體威脅性缺血患者腹股溝以下動脈病變嚴重程度的新型系統評價方法,包括主髂動脈、股腘動脈、腘下動脈和踝下動脈分級,可預測下肢血運重建后截肢、再狹窄、再住院等主要不良肢體事件以及慢性肢體威脅性缺血患者血管內治療的成功率[17-19]。本研究基于GLASS 系統踝下動脈分級評估糖尿病足患者踝下流出道病變嚴重程度,分析其與膝下動脈球囊擴張療效的關系,發現P0 組術后3、6、12 個月靶血管通暢率高于P1 組和P2 組,靶血管再狹窄率低于P1 組和P2組,表明踝下流出道病變越輕術后靶血管通暢率越高,再狹窄率越低。分析原因為腔內球囊擴張治療過程中,血管受機械牽拉和壓力影響發生不同程度損傷,引起血管壁內膜增生和狹窄,影響血管腔內血流動力學,引起血流速度減慢,當血流經過管腔狹窄處流速加快而形成渦流,進一步加重血管壁內膜增生和管腔狹窄,導致靶血管再狹窄[20]。當踝下流出道狹窄或阻塞時,血流少量或無法到達足弓動脈,血流速度減慢,管腔內形成渦流,從而加劇靶血管損傷,加速管腔狹窄進程,導致術后靶血管再狹窄。
回歸分析結果顯示,TASCⅡ分級D 級、藥物涂層球囊與糖尿病足患者接受膝下動脈球囊擴張術后靶血管再狹窄也有關,TASCⅡ分級D 級提示膝下血管閉塞或嚴重鈣化,且缺乏側支循環,因此TASCⅡ分級D 級患者術后靶血管通暢率低,再狹窄率高。藥物涂層球囊表面有抗內膜增生藥物和賦形劑,抗內膜增生藥物可阻止血管內皮細胞有絲分裂,抑制平滑肌和成纖維細胞增殖,穩定微管,抑制靶血管再狹窄的發生,賦形劑則穩定抗內膜增生藥物附著于球囊表面并允許其釋放有效藥物成分,因此采用藥物涂層球囊擴張手術治療可降低術后靶血管再狹窄的發生[21]。
綜上所述,GLASS 踝下流出道P2 級糖尿病足患者治療后靶血管通暢率低,再狹窄發生率高,踝下流出道病變程度是影響動脈球囊擴張治療后靶血管再狹窄的因素之一,藥物涂層球囊可能有助于降低靶血管再狹窄發生風險。臨床對于踝下流出道不良患者,在膝下動脈球囊擴張治療時應考慮改善踝下流出道,以提高術后靶血管通暢率。

