Impella或主動脈內球囊反搏對高危經皮冠狀動脈介入治療及心源性休克支持治療的Meta分析
林 鑫,范春雨
進行高風險經皮冠狀動脈介入治療(percutaneous coronary intervention,PCI)以及急性心肌梗死合并心源性休克(acute myocardial infarction complicated by cardiogenic shock,AMI-CS)的病人通常預后較差,且常常因血流動力學不穩定或心功能差而喪失血運重建的機會[1]。循環輔助是有效維持血流動力學穩定的措施,主動脈內球囊反搏(intra-aortic balloon pump,IABP)具有普及性廣、操作和使用簡單、安全性較高和費用相對低廉等優點,是我國目前應用最廣泛的機械輔助裝置[2]。但在Thiele等[3]研究中,IABP組和對照組的30 d死亡率及1年死亡率差異均無統計學意義。IABP無法取得短期生存率獲益的原因可能是IABP增加心排血量的能力有限,僅為500 mL/min[4]。Impella是一類微型的軸流泵,通過介入的方式經由股動脈放置在左心室中,將左心室的血液通過導管泵入主動脈,能夠有效降低左心室負荷,目前,應用Impella進行支持治療急性心肌梗死(AMI)心源性休克病人呈上升趨勢[5]。因此,本研究通過薈萃分析,對比分析使用Impella或IABP對高危PCI和心源性休克病人的療效及安全性,并探究可能影響預后結果的相關因素。
1 資料與方法
1.1 文獻檢索
檢索 PubMed、EMbase、the Cochrance Library、Web of Science、中國知網、萬方數據庫、維普數據庫,檢索時限為建庫至 2022年3月31日。中文檢索策略以中國知網為例,檢索式:((主題=心源性休克)OR 主題=經皮冠狀動脈介入)AND((主題=Impella)AND 主題=IABP)。英文檢索以Web of Science數據庫為例,檢索策略如下:
#1 TS=("mechanical circulatory support" OR "mechanical circulation support " OR "mechanic circulation support" OR "left ventricular assist device" OR "left ventricular assistance device" OR "left ventricular assist devices" OR "Heart Assist Device" OR "heart-assist pump " OR "vascular assist device" OR "artificial ventricle" OR "ventricle assist device" OR "right-sided heart assist devices" OR "LVAD" OR "RVAD")
#2 (TS=(intra-aortic balloon pump))OR TS=(IABP)
#3 TS=(impella)
#4 #3 AND #2
#5 #1 AND #4
#6 (((TS=(cardiac arrest))OR TS=(cardiac shock))OR TS=(heart failure))OR TS=(cardiogenic shock)
#7 ((TS=(high-risk percutaneous coronary intervention))OR TS=(HR-PCI))OR TS=(high risk PCI)
#8 #6 AND #7 AND #5
1.2 文獻納入與排除標準
1.2.1 納入標準
1)研究對象為接受IABP或Impella支持治療的心源性休克及擬進行高風險PCI術的病人。心源性休克定義為:收縮壓(SBP)<90 mmHg持續30 min及以上,或需要采取支持措施如血管活性藥物、正性肌力藥物及循環輔助裝置以維持SBP≥90 mmHg伴或不伴終末器官灌注不足(四肢冰涼,尿量<30 mL/h,心率≥60次/min)。高風險PCI術目前尚缺乏統一標準的定義,既往研究中有學者將其定義為對左心室功能嚴重受損及存在支配大量心肌的靶血管狹窄的病人進行的PCI術[6],故在該研究中將其定義為:患有3支冠狀動脈病變和/或無保護左主干冠狀動脈疾病且左心室射血分數(left ventricular ejection fraction,LVEF)<35%的病人進行的PCI。2)干預措施,試驗組及對照組分別在PCI過程中植入Impella及IABP,兩組病人皆予常規藥物治療。3)結局指標為術后隨訪臨床結果(如30 d死亡率、主要出血事件、血管并發癥、出血及缺血性腦卒中、再次心肌梗死及敗血癥)。
1.2.2 排除標準
1)重復的文獻資料;2)實驗對象為動物的研究;3)干預措施不包含Impella與IABP之間對比的文獻;4)研究未報告30 d或住院結果中的至少一項,如全因死亡率、大出血(大出血定義為GUSTO評分中度或重度,血紅蛋白下降> 50 g/L,或兩個及以上單位的輸血)或血管并發癥(血管并發癥定義為需要干預的肢體缺血、假性動脈瘤、動靜脈瘺、股動脈閉塞或截肢);5)綜述、薈萃分析、信件、社論材料、會議記錄等。
1.3 文獻篩選
1.4 數據提取及文獻質量評價
兩位研究者分別獨立審查搜索結果,以根據目前的納入與排除標準選擇研究,提取納入文獻的相關信息,并交叉核對。如遇爭議時,通過討論或由第3名研究者裁定,審查者之間關于研究選擇、數據提取或質量評估的任何分歧都要與第三方審查者討論,并通過協商解決。信息提取內容包括基本信息(第一作者、發表時間等)、方法學及文獻質量信息、病例特征(樣本量、研究類型、年齡等)、結局指標等。使用 Cochrane 系統評價員手冊 5.1.0 推薦的偏倚風險評估工具評價納入的隨機對照試驗文獻的質量,評價內容包括從選擇(包括隨機序列產生和分配隱藏)、實施(包括對研究者和受試者施盲)、測量(研究結局盲法評價)、隨訪(結局數據的完整性)、報告(選擇性報告研究結果)及其他(其他偏倚來源)這6個方面總計7個條目對偏倚風險進行評價。對每個條目依據偏倚風險評估準則做出“低風險偏倚”“高風險偏倚”和“不清楚”的判定結果[8]。采用紐卡斯爾-渥太華量表(the Newcastle-Ottawa Scale,NOS)評價納入的非隨機對照試驗文獻,具體包括研究人群選擇(selection)、可比性(comparability)、暴露(exposure)評價或結果(outcome)評價。紐卡斯爾-渥太華量表對文獻質量的評價采用了星級系統的半量化原則,滿分為9顆星[9]。
1.5 終點臨床結局指標
主要結局指標包括短期死亡率(30 d死亡率),次要結局指標包括主要出血事件、血管并發癥、出血及缺血性腦卒中、再次心肌梗死及敗血癥。
1.6 統計學處理
對納入Meta分析的所有研究結果進行可靠性分析[10]。I2和Q檢驗評估研究的異質性,P≥0.1及I2<50%提示各研究間異質性可接受,采用固定效應模型合并效應量;P<0.1,I2> 50%提示研究間存在異質性,采用隨機效應模型合并效應量,并通過亞組分析及敏感性分析探究異質性來源。常用的亞組分類有研究方案、樣本量、質量、人群的特征和發表的年代等,探究研究之間異質性的可能來源,并通過敏感性分析尋找異質性的主要來源文獻,對其進行合理控制和解釋。將統計指標錄入Cochrane協作網提供的Review Manager 5.4軟件進行Meta分析,采用比值比(OR)描述二分類變量結果,加權均方差(MD)描述連續性變量合并結果,采用 95% 置信區間(confidence interval,CI)描述,以P<0.05為差異有統計學意義。通過繪制漏斗圖以評價納入的文獻是否存在發表偏倚,當無偏倚時,將形成對稱的倒置漏斗。
2 結 果
2.1 文獻檢索流程與結果
檢索國內外7個數據庫初次篩選出文獻641篇,剔除重復文獻528篇,通過數據庫的分類功能,剔除綜述、社論材料、信函、會議摘要共54篇。在快速瀏覽標題及摘要后剔除薈萃分析及動物實驗6篇,最后詳細閱讀全文對照納入與排除標準復篩排除文獻49篇,最終納入10項[5,11-19]研究進行Meta分析,其中中文文獻1篇,英文文獻9篇;隨機對照試驗 4篇,觀察性研究6 篇。篩選流程詳見圖1。

圖1 文獻篩選流程與結果
2.2 納入研究的基本情況及質量評價
納入文獻的發表時間為2008-2020年,共涉及觀察對象1 377 例,其中 Impella組661例,IABP組716例,文獻特征見表1。采用 Cochrane 系統評價員手冊5.1.0推薦的偏倚風險評估工具評價納入的隨機對照試驗文獻的質量,所有研究均被認為是低風險(見圖2),但在Ouweneel等[14]研究中,未對分配隱藏狀態進行說明,且研究過程中出現交叉。采用紐卡斯爾-渥太華量表評價納入的非隨機對照試驗文獻的質量,所有的非隨機對照研究均獲得8分,偏倚風險較低。詳見表2。

表1 納入研究的基本特征

表2 基于紐卡斯爾-渥太華量表對非隨機對照研究的質量評估 單位:分

圖2 納入文獻偏倚風險評估圖
2.3 Meta分析結果
2.3.1 30 d死亡率
本研究納入的10項[5,11-19]研究均報道了病人30 d死亡率,經過異質性檢驗:P=0.35,I2=10%,認為各研究間異質性可接受,故使用固定效應模型,Meta分析結果顯示:OR=1.13,95%CI(0.87,1.45),P=0.36,提示Impella組與IABP 組病人30 d內死亡率差異無統計學意義(P>0.05)。詳見圖3。

圖3 Impella組與IABP組30 d死亡率比較的Meta分析森林圖
2.3.2 主要出血事件
納入的研究中有8項[11-17,19]研究報道了病人發生的主要出血事件,經過異質性檢驗:P=0.45,I2=0%,認為各研究之間異質性可接受,故應用固定效應模型,Meta分析結果顯示,OR=2.04,95%CI(1.45,2.87),P<0.001,提示Impella組與IABP組相比出現了更多的出血事件。詳見圖4。

圖4 Impella組與IABP組主要出血事件比較的Meta分析森林圖
2.3.3 血管并發癥
納入的研究中有8項[11-17,19]研究報道了病人發生的血管并發癥,經過異質性檢驗:P=0.78,I2=0%,認為各研究之間異質性可接受,故應用固定效應模型,Meta分析結果顯示:OR=2.92,95%CI(1.59,5.37),P=0.000 5,提示Impella組與IABP組相比出現了更多的血管并發癥。詳見圖5。

圖5 Impella組與IABP組血管并發癥發生率比較的Meta分析森林圖
2.3.4 腦卒中
納入的研究中有8項[5,11,13-17,19]研究報道了病人發生的腦卒中事件,經過異質性檢驗:P=0.88,I2=0%,認為各研究之間異質性可接受,故應用固定效應模型,Meta分析結果顯示:OR =0.65,95%CI(0.31,1.35),P=0.25,提示Impella與IABP對病人腦卒中發作的影響差異無統計學意義。詳見圖6。

圖6 Impella組與IABP組腦卒中發生率比較的Meta分析森林圖
2.3.5 再發心肌梗死
納入的研究中有5項[5,11,14,16,19]研究報道了病人發生的再次心肌梗死事件,Impella組與IABP組的再發心肌梗死發生率分別為7.2%和6.3%,經異質性檢驗:P=0.70,I2=0%,認為各研究之間異質性可接受,故應用固定效應模型,Meta分析結果顯示:OR=1.15,95%CI(0.72,1.84),P= 0.57,提示Impella與IABP對病人再發心肌梗死發作影響相當。
2.3.6 敗血癥
納入的研究中有4項[11-12,15-16]研究報道了病人發生的敗血癥事件,經過異質性檢驗:P=0.24,I2=29%,認為各研究之間異質性可接受,故應用固定效應模型,Meta分析結果顯示:OR=1.64,95%CI(1.11,2.40),P=0.01,提示Impella組與IABP組相比出現了更多的敗血癥。
2.3.7 LVEF
納入的研究中有9項[5,11-18]研究報道了病人未植入設備前的LVEF,經過異質性檢驗:P=0.000 6,I2=71%,認為各研究之間異質性高,故應用隨機效應模型,Meta分析結果顯示:MD=-3.01,95%CI(-5.14,-0.88),P=0.006,提示Impella組與IABP組病人相比植入設備前LVEF較低。詳見圖7。
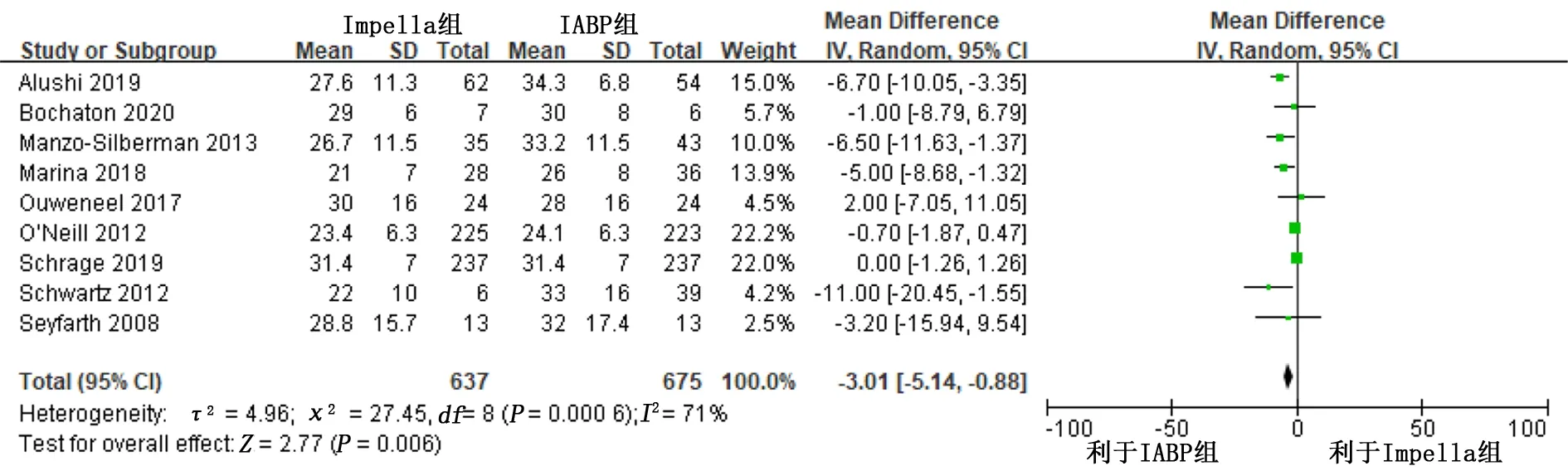
圖7 Impella組與IABP組LVEF比較的Meta分析森林圖
2.4 亞組分析及敏感性分析
在對上述7個指標進行Meta分析時,發現病人植入設備前射血分數的異質性顯著,對該組數據進行按注冊地區及研究類型研究亞組分析,歐洲組:P=0.000 04,I2=78%,美國組:P=0.10,I2=57%;隨機對照試驗組:P=0.92,I2=0%;回顧性研究組:P<0.000 1,I2=84%,提示異質性可能由研究類型與地區的差異產生,這種差異主要體現在歐洲地區組與回顧性研究組之間。詳見圖8。

圖8 LVEF亞組分析的Meta分析森林圖
對該組數據進行敏感性分析。逐一剔除需排除的文獻后發現,剔除O′Neill等[5]研究與Schrage等[16]研究后異質性下降(P=0.42,I2=1%),其中O′Neill等[5]研究為非緊急植入循環輔助設備,Schrage等[16]研究根據LVEF等因素將研究對象進行匹配,且樣本量較其他組內研究量大,具有特殊性[5,16],故將二者剔除,剔除后Meta分析結果:MD=-5.46,95%CI(-7.47,-3.45),P<0.000 01,與之前結果相同,提示Impella組與IABP組病人相比植入設備前LVEF較低。詳見圖9。

圖9 剔除后Impella組與IABP組LVEF比較的Meta分析森林圖
2.5 發表偏倚
通過RevMan 5.4軟件繪制漏斗圖對各研究間是否存在發表偏倚進行評估。30 d死亡率及主要出血事件漏斗圖右下角存在獨立游離點,提示可能存在小樣本IABP不良事件未被報道,猜測可能是因為較重的病人往往選擇了Impella作為循環輔助支持,而與干預效果帶來的異質性有關。其余各研究在各個評價指標中均位于置信區間內,且漏斗圖基本對稱,大致均勻分布于效應線左右兩側。詳見圖10。

圖10 30 d死亡率漏斗圖
3 討 論
心臟的機械循環支持是代替或輔助心臟功能、提供血液灌注、改善機體缺氧狀態、促進器官功能恢復的人工器械[20]。雖然循環輔助裝置廣泛應用于心力衰竭程度嚴重、合并癥復雜以及急性心肌梗死或心搏驟停的心源性休克病人,但仍然無法確定哪些群體會在循環支持治療中獲益[21-24]。
本研究計劃通過薈萃分析的形式,對Impella及IABP在對心源性休克及高危PCI病人的支持中獲益與風險,并對可能影響試驗結果的相關因素加以分析。盡管多項研究結果提示,在急性心肌梗死及高風險PCI病人中使用Impella是安全的,且能夠有效降低心肌耗氧量及提供更為穩定的血流動力學支持并有效地降低了病人的血清乳酸水平[25],但本研究結果表明,與IABP相比,Impella并不能降低短期全因死亡率,這與其他學者的結論[26-27]是相同的。此外,Impella組較IABP組出現主要出血事件、血管并發癥及敗血癥的風險顯著增加。另一方面,Impella組的腦卒中與再發心肌梗死發生率與IABP組差異無統計學意義。Impella組病人LVEF水平較IABP組明顯下降,在Marina等[15]研究中也得到Impella組病人較IABP組病情更重,而在O′Neil等[5]研究中,Impella組相比IABP組有更多的病人進行了完全血運重建與血管旋磨術,這提示Impella組未能展示出更多的獲益可能與Impella組病人基礎更差,更多的操作如反復注射造影劑、球囊擴張、動脈斑塊切除術通過,導致短暫阻斷流向目標冠狀動脈的血液流動而使冠狀動脈缺血加劇有關[5]。
IABP對急性心肌梗死心源性休克病人預后的改善在此前的一項多中心隨機對照試驗中未能得到證實[28],這被認為是因為IABP增加心排血量能力有限,僅有500 mL/min[29]。而Impella可提供多種不同的心排血量,如Impella 2.5可以提供2.5 L/min的心輸出量,Impella CP可以提供3.7 L/min的心輸出量,Impella 5.0將這一數值提高至5 L/min,使用Impella與心排血指數的改善、更好的心肌修復和更快的停用兒茶酚胺相關[11,13,15,30];另一方面,在Kapur等[31]動物實驗提示在急性心肌梗死中應用軸流泵能夠明顯減少心肌梗死面積。本研究提示,Impella未能得到理想的獲益,其原因可能在于,Impella組病人病情更重,心功能更差,更多的操作導致的冠狀動脈缺血與血栓負荷加重有關。此外,部分病人設備植入發生在血運重建后,而據底特律心源性休克計劃表明,在沒有發生心搏驟停的病人中,在PCI前使用Impella與結果改善相關[32]。出血事件、血管并發癥及敗血癥是使用循環輔助裝置的主要不良事件。IABP要求7-8F鞘管,而Impella 2.5、Impella CP分別要求13F、14F鞘管,既往的研究認為Impella血管并發癥的風險和較高的出血率與其所需的更大口徑的血管通路相關[33]。2020年6月美國食品和藥品管理局(FDA)批準Impella ECP可以進行臨床試驗,這是至今為止世界上最小的血流動力學支持型心臟泵,其直徑僅有9F,流量可達到3.5 L/min以上,有望進一步降低相關不良事件發生的風險[34]。而既往的研究認為,敗血癥的出現不能完全歸因于輔助裝置的使用,因為需要循環輔助裝置的病人往往病情危重,通常有多種潛在的感染源,包括機械通氣、動靜脈置管術、導尿和額外的外科干預等[35]。本研究納入的10項研究中僅有3項報道了敗血癥病例的研究,且樣本量集中于回顧性研究,在這些數據中,病人往往因病情較重而選擇了Impella作為循環輔助的器械,例如Schrage等[16]研究中盡管使用了傾向匹配評分的方式以增加兩組的可比性,但Impella組病人平均動脈壓仍顯著低于IABP組,因此,對于該項結果應謹慎解釋。
本研究存在的局限性有:首先,Impella對比IABP的隨機對照試驗數量較少,本研究有一半以上的文獻為回顧性研究;其次,由于無法獲得個體病人的數據,疾病的嚴重程度及病人基線數據存在差異,對本研究提供的數據應該謹慎地進行解釋。第三,納入研究中未提及對血管通路進行穿刺切開或壓迫的裝置,這可能影響血管并發癥的差異。第四,盡管在納入的文獻中有提及冠狀動脈病變數量及位置,但病變的嚴重及復雜程度少有報道,僅有1篇文獻報道了SYNTEX評分[14],此外,僅有少數文獻報道在PCI后是否實現完全血運重建及支架類型及數量,這可能影響研究的結果。
本研究表明,盡管Impella組病人的并發癥更多,病情更重,但在心源性休克及高危PCI病人中使用Impella進行循環支持,仍獲得了與使用IABP相當的療效。通過更加嚴格的試驗設計及病人篩選標準,發現真正能夠從新一代循環輔助裝置支持治療中獲益的人群,并通過技術創新降低相關并發癥的發生,從而真正體現新一代循環輔助裝置的血流動力學優勢,是其應用過程亟待解決的重要問題。

