強心湯對OMA1封閉心力衰竭大鼠心肌組織Caspase-3、Bax、Bcl-2表達的影響
陳文鵬,盧健棋,龐 延,朱智德,潘朝鋅,溫志浩,梁逸強,盧俊燊,許志亮
慢性心力衰竭(chronic heart failure,CHF)是心臟結構和(或)功能異常導致肺循環和(或)體循環淤血,以活動耐量下降、水鈉潴留和呼吸困難為表現的一種臨床綜合征,是各種心血管事件的終末階段。隨著人口老齡化、肥胖等心血管疾病危險因素不斷突出,心力衰竭的死亡率和再住院率居高不下,被認為是21世紀心血管領域的重大公共衛生挑戰[1]。2021年《中國心血管健康與疾病報告2020》[2]指出目前我國心力衰竭的患病率為1.3%,較2000年增加了44.0%,根據推算目前我國約有890萬例心力衰竭病人,眾多的心力衰竭病人給社會和家庭帶來了沉重的經濟負擔和養護負擔。中藥多途徑、多靶點、多機制的作用在防治CHF方面取得了一定成效,中藥通過保護心臟線粒體功能,參與線粒體能量代謝和保護心肌得到了眾多研究驗證。強心湯作為廣西名中醫盧健棋教授臨床治療CHF的有效驗方,長期應用于廣西中醫藥大學第一附屬醫院心血管科CHF的臨床防治中[3-4],并且取得了較滿意的臨床療效。本課題組前期動物實驗研究已證實,強心湯能夠抑制金屬蛋白酶相關蛋白1(OMA1)表達,降低線粒體內膜蛋白酶1(OPA1)水解,保護心肌細胞的線粒體形態和功能從而改善心功能[5]。半胱氨酸天冬氨酸蛋白酶3(Caspase-3)、Bcl-2家族相關x蛋白(Bax)、B細胞淋巴瘤/白血病-2(B-cell lymphoma/leukemia-2,Bcl-2)等相關調控蛋白在強心湯調控心肌線粒體代謝,改善心功能可能作用機制發揮著重要作用。本研究以急性心肌梗死后大鼠為CHF動物模型,初步探討強心湯防治CHF可能作用及機制,為益氣溫陽、活血利水法防治CHF提供科學依據。
1 材料與方法
1.1 動物與病毒
選取清潔級5~6周齡健康雄性Sprague-Dawley(SD)大鼠50只,體質量200~230 g,購自湖南思萊克景達實驗動物有限公司,生產許可證號:SCXK(湘)2019-0004。OMA1 RNAi腺病毒質粒由上海吉凱基因科技有限公司提供。
1.2 藥物
強心湯藥物組方:黃芪30 g,黨參15 g,柏子仁(打碎)12 g,白附片(先煎)、桂枝、川芎、丹參、葶藶子、茯苓、白術、玉竹各10 g,炙甘草6 g。以上藥物由廣西中醫藥大學第一附屬醫院藥學部中藥房提供,并由中藥煎藥室通過水煮醇沉標準工藝制成生藥含量為1 mg/mL的濃縮煎劑。
1.3 試劑與儀器
Trizol regent(Solarbio公司,貨號:R1100);TB GreenTMPremix Ex TaqTMⅡ、PCR Forword Primer、PCR Reverse Primer(Takara公司,貨號:RR820A);高效RIPA組織裂解液(Solarbio公司,貨號:R0010);蛋白酶抑制劑混合液(Solarbio公司,貨號:P6730);Loading Buffer(Solarbio公司,貨號:P1016);脫脂奶粉(Solarbio公司,貨號:D8340);增強型化學發光(ECL)底物(超敏)(Biosharp公司,貨號:BL523A)。低溫離心機(德國Eppendorf公司,貨號:5418R);水平搖床(中國其林貝爾公司,貨號:TS-3D);小型動物呼吸機(中國普升科技有限公司,型號:RSP-1002);超微量核酸檢測儀(中國遂真公司,貨號:FC-1100);VeritiTM96-Well Thermal Cycler(美國Applied Biosystems?,貨號:4375786);蛋白轉印模塊(美國Bio-Rad公司,貨號:Mini Trans-Blot Cell);凝膠成像系統(中國上海天能公司,貨號:Tanon 5200);二維超聲心動圖儀(美國Esaote公司,型號:Mylab 50)。
1.4 建立CHF大鼠模型
參照文獻[6]方法,采用結扎SD大鼠冠狀動脈左前降支中上段建立CHF模型,假手術組大鼠冠狀動脈前降支穿線但不結扎,其余操作同CHF造模方法。成功造模后將大鼠送回籠中常規飼養,2周后心臟彩超檢查提示左室射血分數(left ventricular ejection fraction,LVEF)下降20%~30%可判斷為造模成功。
1.5 實驗分組及干預方法
參考文獻[5],按隨機數字表法將50只大鼠平均分為5組,分別為假手術組、模型組、OMA1封閉組、強心湯組、OMA1封閉+強心湯組,分組完成后采用結扎冠狀動脈方法進行造模,其中封閉組在建立模型前第1天和建模后第7天各尾靜脈注射2×1010pfu OMA1干擾腺病毒對大鼠OMA1表達封閉,CHF大鼠模型建立成功后第2天開始,強心湯組、OMA1封閉+強心湯組給予強心湯混懸液臨床等效劑量每次1.62 g/kg灌胃[7],其余各組給予生理鹽水2 mL灌胃,每日2次。各組均灌胃觀察28 d。
1.6 觀察指標及方法
1.6.1 心功能指標
用心臟彩超檢測各組大鼠的左室舒張末期內徑(left ventricular end-diastolic diameter,LVEDD)、左室收縮末期內徑(left ventricular end-systofic diameter,LVESD)、LVEF心功能指標,具體方法參見文獻[5]內容。
1.6.2 心肌組織OMA1及Caspase-3、Bax、Bcl-2相關蛋白表達
各組SD大鼠干預4周經處死后取出心肌組織,包埋、切片處理后采用二喹啉甲酸法測定蛋白含量,再通過膠層分離→轉膜→封閉(5% 脫脂奶粉)→抗體稀釋→抗體孵育→TBST洗膜→ECL顯色后曝光成像,經Image J 1.52對條帶定量分析,各指標灰度值經β-actin均一化,計算蛋白相對表達量,具體步驟參照文獻[7]。
1.6.3 心肌組織 OMA1及Caspase-3、Bax、Bcl-2 mRNA表達
根據Trizol試劑盒說明書提取大鼠心肌組織RNA,按PrimeScriptTMRT Master Mix操作指示進行反轉錄聚合酶鏈式反應(qRT-PCR)。引物序列,OMA1:正向 CGCGCTCACGATAACCAAG,反向GCCAGCGTAT-TCACTCCAGA,片段長度:97 bp;Caspase-3:正向GAAAGCATCCAGCAATAGGC,反向AGCGATGACTCAGCACCTCC,片段長度:125 bp;Bax:正向TGCTACAGGGTTTCATCCAGG,反向GAGACACTCGCTCAGCTTCTTG,片段長度:113 bp;Bcl-2:正向TGTGGCCTTCTTTGAGTTCG,反向CATCCCAGCCTCCGTTATCC,片段長度:97 bp;ATCB(內參):正向CGTAAAGACCTCTATGCCAACA,反向TAGGAGCCAGGGCAGTAATC,片段長度:100 bp。引物由廣西醫科大學睿谷醫學檢驗有限公司提供。各基因表達的相對定量采用2-△△Ct法進行計算。
1.7 統計學處理
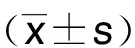
2 結 果
2.1 各組大鼠心功能指標比較
與假手術組比較,模型組大鼠LVEDD、LVESD均升高(P<0.05),LVEF降低(P<0.05);與模型組比較,OMA1封閉組、強心湯組、OMA1封閉+強心湯組大鼠LVEDD、LVESD均降低(P<0.05),LVEF升高(P<0.05);強心湯組大鼠LVEDD、LVESD高于OMA1封閉組、OMA1封閉+強心湯組(P<0.05),LVEF低于OMA1封閉組、OMA1封閉+強心湯組(P<0.05);與OMA1封閉組比較,OMA1封閉+強心湯組大鼠LVEDD、LVESD低于OMA1封閉組(P<0.05),LVEF高于OMA1封閉組(P<0.05)。詳見表1。

表1 各組大鼠心功能指標比較
2.2 各組大鼠心肌組織OMA1及Caspase-3、Bax、Bcl-2 mRNA表達水平
與假手術組比較,模型組大鼠心肌組織中OMA1、Bax、Caspase-3 mRNA表達明顯升高(P<0.05),Bcl-2 mRNA表達明顯降低(P<0.05);與模型組比較,OMA1 封閉組、強心湯組、OMA1 封閉+強心湯組大鼠心肌組織OMA1、Bax、Caspase-3 mRNA表達降低(P<0.05),Bcl-2 mRNA表達升高(P<0.05);與強心湯組比較,OMA1封閉組、OMA1封閉+強心湯組大鼠心肌組織OMA1、Bax、Caspase-3 mRNA表達降低,Bcl-2 mRNA表達升高(P<0.05);與OMA1封閉組比較,OMA1封閉+強心湯組大鼠OMA1、Caspase-3、Bax mRNA表達水平降低(P<0.05),Bcl-2 mRNA表達升高(P<0.05)。詳見表2。

表2 各組大鼠心肌組織OMA1及Caspase-3、Bax、Bcl-2 mRNA表達
2.3 各組大鼠心肌組織OMA1、Caspase-3、Bax、Bcl-2蛋白表達水平
與假手術組比較,模型組大鼠心肌組織OMA1、Caspase-3、Bax 蛋白表達升高(P<0.05),Bcl-2蛋白表達降低(P<0.05);與模型組比較,OMA1封閉組、強心湯組、OMA1封閉+強心湯組大鼠心肌組織 OMA1、Caspase-3、Bax蛋白表達降低(P<0.05),Bcl-2蛋白表達升高(P<0.05)。與強心湯組比較,OMA1封閉組、OMA1封閉+強心湯組大鼠OMA1、Caspase-3、Bax蛋白表達降低(P<0.05),Bcl-2蛋白表達升高(P<0.05);與OMA1封閉組比較,OMA1封閉+強心湯組大鼠OMA1、Caspase-3、Bax 蛋白表達低于OMA1封閉組(P<0.05),Bcl-2蛋白表達高于OMA1封閉組(P<0.05)。詳見表3、圖1。

圖1 各組大鼠心肌組織OMA1、Caspase-3、Bax、Bcl-2蛋白表達電泳圖

表3 各組大鼠心肌組織OMA1及Caspase-3、Bax、Bcl-2蛋白表達比較
3 討 論
中醫學根據CHF臨床癥狀將其歸為“心水”“喘證”“水腫”等中醫疾病范疇,中醫學認為“心者君主之官,主血主脈”,心衰日久,其氣必虛,虛則血行無力,神形失養,血不行則瘀,瘀停則水飲聚,血瘀、水飲皆為陰邪,易滯氣機,氣機運化不調遂出現水腫、喘咳、乏力、納差等癥,最終發為心衰病。陳可冀專家組在《慢性心力衰竭中西醫結合診療專家共識》[8]中提出CHF的病性為本虛標實,基本病機概括為“虛”“瘀”“水”,心氣虛為病之本,基本治法為“益氣溫陽、活血利水”。強心湯是廣西中醫藥大學第一附屬醫院治療CHF的有效經驗方,方中黃芪、白附片、黨參、桂枝補氣溫陽統攝全方,茯苓、玉竹、白術養陰健脾益氣,丹參、川芎活血行氣化瘀,柏子仁寧神養心,葶藶子利水瀉肺,炙甘草調和諸藥,各藥共奏益氣溫陽、活血利水之效。
近年來,國內外發表的相關文獻報道顯示,當前CHF治療早已不是簡單局限在傳統的強心、利尿、擴張血管方案,CHF的研究已向神經激素拮抗劑、延緩心室重塑、多靶點治療理念轉變[9-10]。隨著沙庫巴曲纈沙坦等血管緊張素受體腦啡肽酶抑制劑(angiotensin receptor neprilysin inhibitor,ARNI)、依帕列凈、恩格列凈等鈉-葡萄糖共轉運體2抑制劑(sodium-dependent glucose transporters 2,SGLT2)等新型藥物的研發應用,CHF的治療方案由“黃金三角”過渡到以血管緊張素轉換酶抑制劑(angiotensin converting enzyme inhibitor,ACEI)/ARNI為基礎的“新三角”,再到如今的“新四聯”(ACEI/ARNI、β受體阻滯劑、SGLT2、醛固酮受體拮抗劑)方案,CHF病人的癥狀控制與預后得到了明顯改善,但這些藥物治療仍然受到低血壓、心動過緩、肝腎功能異常等因素影響,臨床應用常受到一定限制[11-13]。
水液潴留、血流動力學異常、神經內分泌異常這些機制并不能完全解釋CHF病理生理的復雜性,心肌線粒體功能和能量代謝與CHF的關系逐漸受到重視,保護心肌線粒體功能,改善心肌能量代謝成為防治CHF新思路[14]。線粒體是心肌細胞中含量最多、功能最重要的細胞器,被稱為細胞的“動力源”,心肌線粒體通過不斷地分裂、融合和形態改變,適應各種應激條件為心臟的收縮和舒張提供能量[15]。以三磷酸腺苷(adenosine triphosphate,ATP)合成減少、活性氧生成增加、Ca2+穩態失衡、線粒體分裂與融合失調為主要特征的線粒體功能障礙會導致廣泛的心肌細胞損傷甚至凋亡,引起心肌的能量供需失調,最終導致心力衰竭[16-18]。據研究報道,OMA1在線粒體融合和分裂過程中扮演著重要角色,當心肌缺血缺氧時,OMA1能夠促進心肌線粒體裂解并激活Bax、Caspase-3細胞凋亡因子表達,誘導心肌細胞凋亡,促進了心肌纖維化和心室重塑的進程[19-20]。此外,處于心肌細胞線粒體上游的Bcl-2、Bax通過調控線粒體的形態與功能,介導調控細胞凋亡相關活性物質釋放,進而參與心肌細胞凋亡,Bcl-2在此過程中發揮抑制凋亡作用,而Bax起到促凋亡作用,二者相互制約、相互聯系。綜上可見,OMA1、Bcl-2、Bax、Caspase-3在調控心肌細胞凋亡過程中發揮著重要的作用。
線粒體在心臟中含量豐富,約占心肌細胞器近30%,通過氧化磷酸化為心肌收縮和舒張功能提供約90%的ATP能量供應,此外,心肌細胞的生長和凋亡的調節同樣與心肌線粒體相關[21-22]。在心肌線粒體中Bcl-2家族蛋白Bcl-2、Bax的表達水平與心肌細胞凋亡調控有關,在線粒體能量代謝平衡的條件下,抗凋亡蛋白Bcl-2能夠阻斷Bax的促凋亡作用,當這種穩態被打破后,促凋亡Bax蛋白寡聚化后在線粒體外膜聚集使得線粒體外膜通透性發生改變導致細胞色素C(Cyt-C)過度釋放,與此同時OMA1被激活后切割OPA1,OPA1切割觸發線粒體嵴重構,使嵴內的更多的Cyt-C被釋放[23]。OMA1作為調節線粒體融合與分裂的一種金屬內肽酶,在線粒體膜間的空間中具有蛋白水解活性,當心肌發生缺血缺氧時,OMA1以依賴應激的方式在S1裂解位點裂解OPA1生成可溶性短鏈蛋白S-OPA1,過量的S-OPA1生成會導致線粒體裂解,促進Bax寡聚化,干擾Bcl-2的生成,改變線粒體外膜通透性,促進Cyt-C釋放到細胞質中,激活下游Caspase級聯反應,Caspase-3活化,最終誘導細胞凋亡;而且OMA1裂解OPA1離不開Bcl-2、Bax等凋亡因子的特異性激活,在參與線粒體凋亡和細胞凋亡的機制中OMA1、Bcl-2、Bax相互影響,與CHF的發生密切相關[24-26]。本實驗結果顯示,強心湯和OMA1封閉均能夠下調OMA1、Bax、Caspase-3的mRNA和蛋白表達,上調Bcl-2的mRNA和蛋白的表達,從而改善心功能,其中OMA1封閉+強心湯組療效最明顯,據此推測強心湯可能與OMA1基因封閉在調節心肌細胞凋亡中能夠發揮協同作用。
本研究中通過采用結扎冠狀動脈左前降支方法建立大鼠CHF模型,強心湯灌胃、基因封閉干預處理后應用超聲檢測各組大鼠心功能,結果顯示:相比假手術組,模型組大鼠LVEDD、LVESD升高,LVEF降低,與模型組比較,其他各干預組大鼠LVEDD、LVESD均下降,LVEF均升高;各干預組相比,OMA1封閉+強心湯組LVEDD、LVESD最小,LVEF最高,OMA1封閉組次之,強心湯組心功能指標改善情況差于OMA1封閉組,表明強心湯可改善CHF模型大鼠心功能。
綜上所述,強心湯可以明顯改善CHF模型大鼠的左室心功能指標,能夠顯著下調CHF模型大鼠心肌組織中OMA1、Bax、Caspase-3表達,上調Bcl-2表達,揭示了強心湯調控心肌線粒體代謝,改善心功能可能的作用機制,為強心湯的開發及臨床應用提供了依據。但由于本研究樣本量和基因數量較少,通路單一,未來仍需進一步增大樣本量和延長干預時間期限,從多分子、多基因、多蛋白、多通路等方面對強心湯治療CHF做進一步深入研究。

