FAERS中免疫檢查點抑制劑相關嚴重皮膚不良反應數據挖掘Δ
龍 霞 ,黃孟文 ,蒲詩云 ,王利辰 ,唐夢蛟 ,周后鳳 #(.成都市第五人民醫院藥劑科,成都 60;.成都中醫藥大學藥學院,成都 67;.川北醫學院藥學院,四川 南充 6700;.西南醫科大學藥學院,四川瀘州 66099)
腫瘤免疫治療為近年來腫瘤治療的突破性進展之一,其中最常應用的藥物是免疫檢查點抑制劑(immune checkpoint inhibitors,ICIs)[1]。ICIs可通過阻斷細胞毒性T 淋巴細胞相關抗原4(cytotoxic T lymphocyte-associated antigen-4,CTLA-4)、程序性死亡受體1(programmed death-1,PD-1)或程序性死亡受體配體1(programmed death-ligand 1,PD-L1)等相關信號通路來解除免疫抑制狀態,恢復機體免疫監控功能,重建T 淋巴細胞對腫瘤細胞的殺傷能力[2]。目前,美國FDA批準上市了多種ICIs,包括CTLA-4抑制劑(伊匹木單抗和替西木單抗)、PD-1抑制劑(納武利尤單抗、帕博利珠單抗和西米普利單抗等)和PD-L1抑制劑(阿替利珠單抗、阿維魯單抗、度伐利尤單抗)等。其中,伊匹木單抗、納武利尤單抗、帕博利珠單抗、阿替利珠單抗和度伐利尤單抗已在我國上市[1,3]。患者在應用ICIs時,常會出現免疫相關不良事件(immune-related adverse events,irAEs),以皮膚系統較為常見,且最早出現[4―5]。皮膚irAEs表現形式多樣,較為常見的是斑丘疹、瘙癢癥及白癜風[6―7]。皮膚irAEs 的嚴重程度通常是輕至中度,但也有部分皮膚irAEs 較為嚴重,如史-約綜合征(Stevens-Johnson syndrome,SJS)/中毒性表皮壞死松解癥(toxic epidermal necrolysis,TEN)等[8―10]。SJS/TEN 會伴發一系列系統癥狀,包括多器官功能衰竭綜合征等,具有較高的死亡率,其中SJS 為4.8%,TEN 為14.8%,SJS/TEN 為19.4%[11]。醫護人員需要早期識別并正確處置這些嚴重皮膚不良反應,這對改善腫瘤患者預后和防范藥物不良反應風險具有重要的意義。為此,本研究基于美國FDA不良事件報告系統(FDA adverse events reporting system,FAERS),對在國內外均已上市的5種ICIs(伊匹木單抗、納武利尤單抗、帕博利珠單抗、阿替利珠單抗和度伐利尤單抗)致嚴重皮膚不良反應進行信號挖掘與分析,以期為ICIs的安全應用提供參考。
1 資料與方法
1.1 數據來源與處理方法
從FAERS 數據庫中收集伊匹木單抗、納武利尤單抗、帕博利珠單抗、阿替利珠單抗和度伐利尤單抗自美國上市至2022年第4 季度的藥物不良事件(adverse drug events,ADEs)報告進行分析。利用Microsoft Office Access 2017對相關信息進行提取;采用國際醫學用語詞典(Medical Dictionary for Regulatory Activities,MedDRA)25.0 版中ADEs 術語集的首選術語(preferred terms,PT)對ADEs進行編碼;根據MedDRA 25.0版中的“標準MedDRA 分析查詢(standardized MedDRA queries,SMQ)”,將術語集定義為嚴重皮膚不良反應(代碼20000020)的相關72個PT作為研究對象。
去除重復報告,得到總的相關ADEs 報告。通過PubMed數據庫以主題詞和自由詞相結合的方式進行查詢,以5種藥品的名稱為檢索詞,并限定藥品角色為“首要懷疑藥品”,即得首要懷疑藥品為上述5種藥品的嚴重皮膚不良反應報告。
1.2 信號檢測方法
為盡可能減少使用單一算法帶來的結果偏倚,本研究采用頻數法中的報告比值比(reporting odds ratio,ROR)法和貝葉斯法中的貝葉斯置信區間遞進神經網絡(Bayesian confidence propagation neural network,BCPNN)法進行信號挖掘。ROR 法是一種常用的藥物不良反應信號挖掘方法,其陽性信號生成條件為報告數≥3 且95%置信區間(confidence interval,CI)下限>1。ROR及其95%CI下限的數值越大,說明信號強度(關聯度)越強[12]。而BCPNN 法的信號檢測指標為信息成分(information component,IC)值,其陽性信號生成條件為IC 下限(即IC-2SD,SD 為標準差)>0。其中,IC 是BCPNN 法的一種統計度量,是一種強有力的信號檢測指標,具有避免假陽性的能力,特別是在報告數較少的情況下[13]。本研究將兩種方法同時檢出的陽性信號判定為可疑信號,提示該藥物與目標ADE報告的關聯具有統計學意義。采用Microsoft Office Excel 2017對數據進行處理,各方法計算公式參考文獻[14]。
2 結果
2.1 嚴重皮膚不良反應報告的基本情況
本研究共在FAERS數據庫收集到5 726份嚴重皮膚不良反應報告,其中納武利尤單抗3 037份、帕博利珠單抗1 465份、度伐利尤單抗130份、阿替利珠單抗429份、伊匹木單抗665份。結果見表1。

表1 5種ICIs信號檢測結果
2.2 信號檢測情況
5 種ICIs 均生成了陽性信號,其關聯度由強到弱依次是帕博利珠單抗>阿替利珠單抗>納武利尤單抗>伊匹木單抗>度伐利尤單抗,具體見表1和圖1。
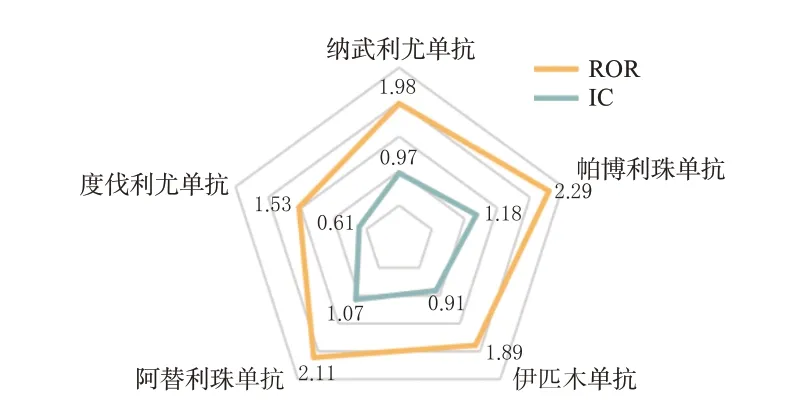
圖1 5種ICIs相關嚴重皮膚不良反應信號檢測雷達圖
納武利尤單抗、帕博利珠單抗、度伐利尤單抗、阿替利珠單抗、伊匹木單抗在嚴重皮膚不良反應方面分別形成的信號數為15、13、4、7、9個,具體見表2。
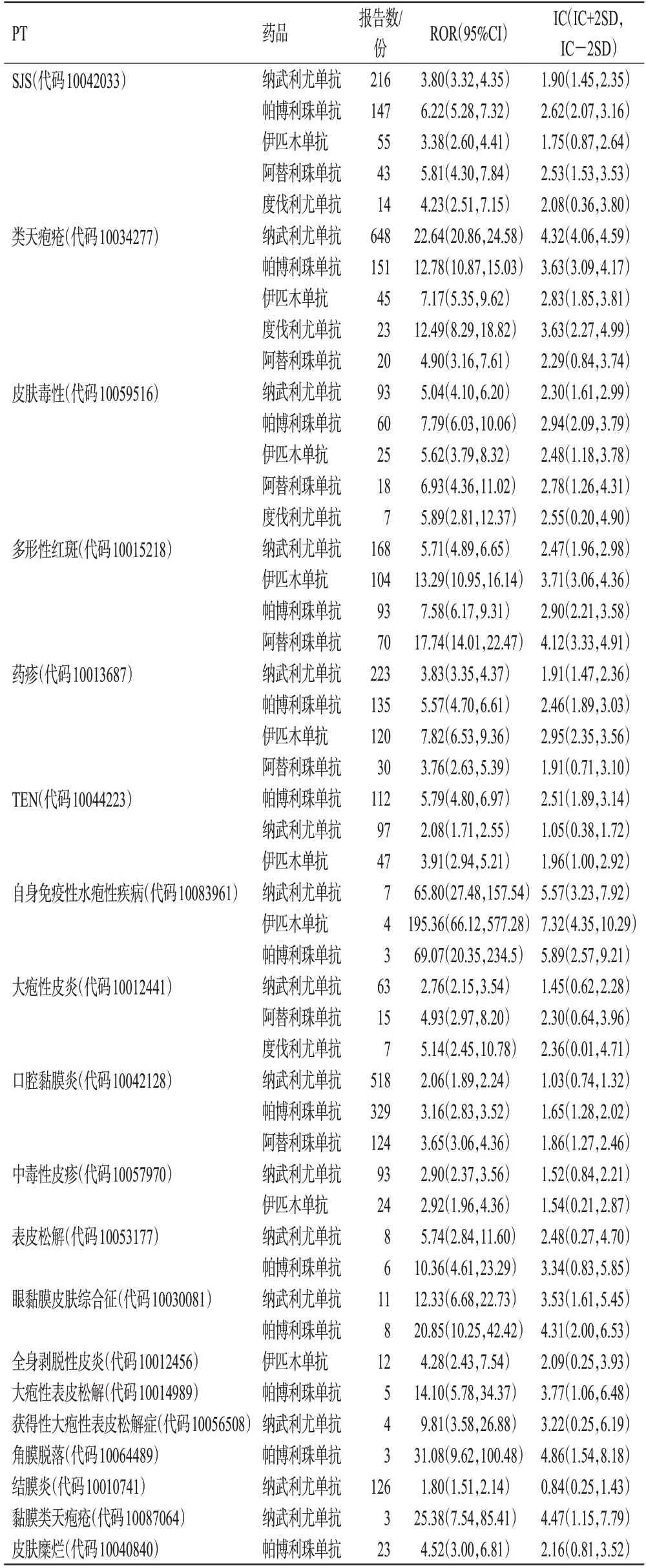
表2 5 種ICIs 在嚴重皮膚不良反應方面的PTs 信號檢測結果
2.3 SJS和TEN信號相關情況
2.3.1 SJS的ADEs信號情況
納武利尤單抗、帕博利珠單抗、伊匹木單抗、阿替利珠單抗、度伐利尤單抗致SJS 的報告分別為216、147、55、43、14 份,均形成了陽性信號。SJS 患者的基本特征見表3,其結局見圖2,其中導致患者死亡比例最高的是帕博利珠單抗(35.37%,52/147)。
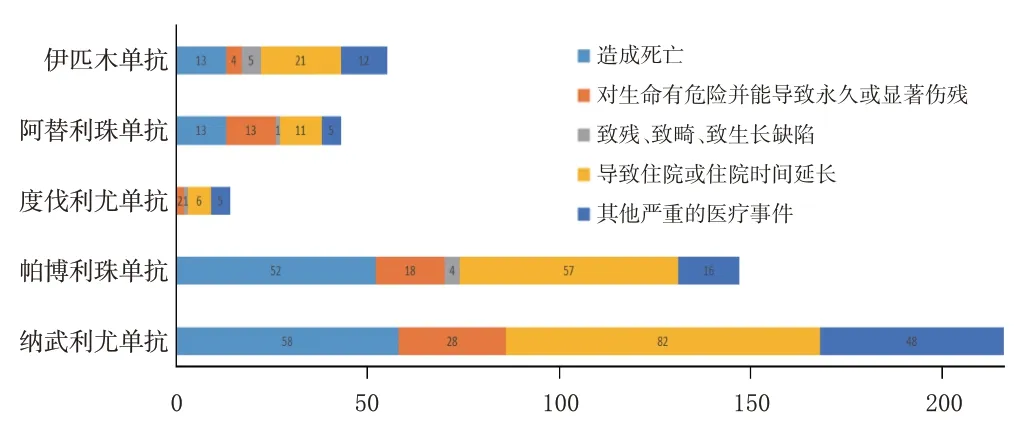
圖2 5種ICIs致SJS患者的結局
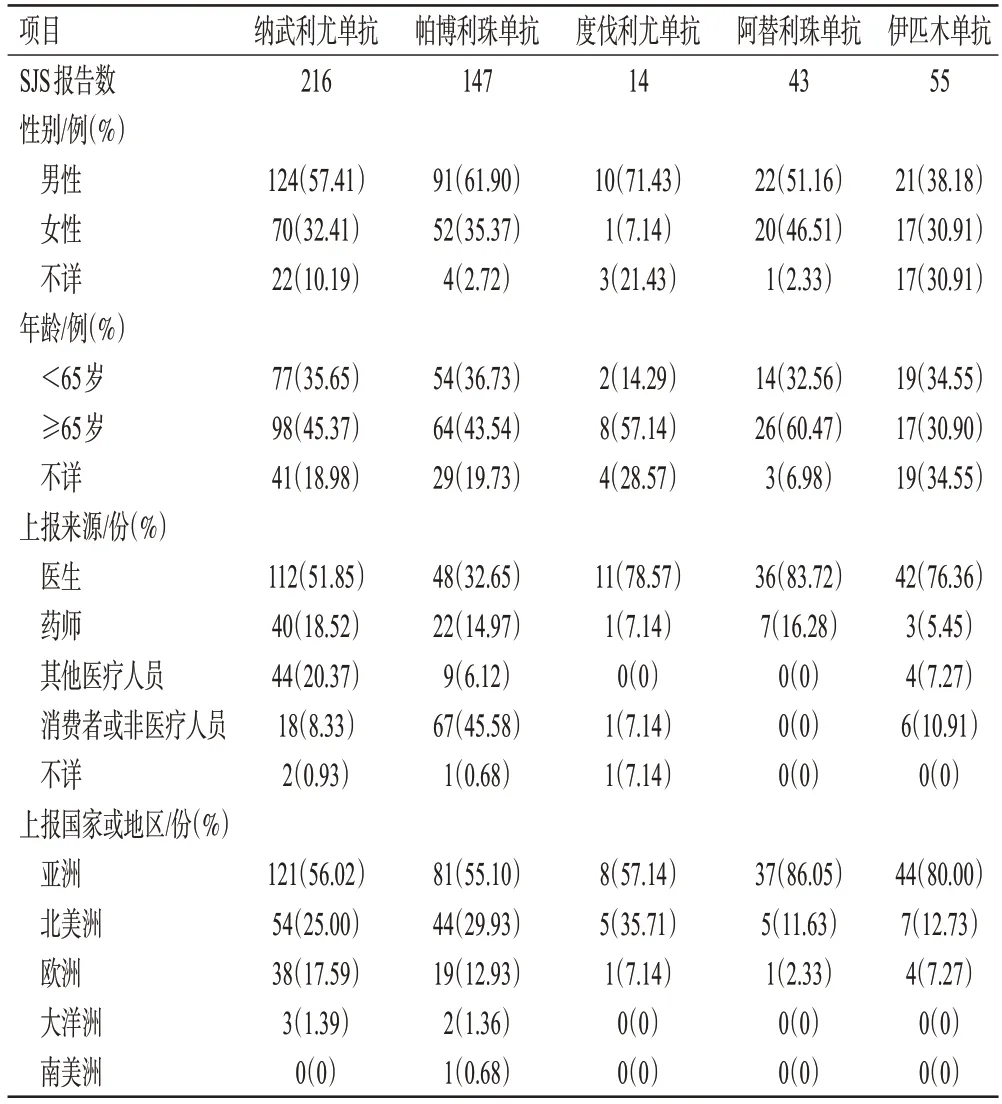
表3 5種ICIs致SJS患者的基本特征
2.3.2 TEN的ADEs信號情況
納武利尤單抗、帕博利珠單抗、伊匹木單抗、阿替利珠單抗、度伐利尤單抗致TEN 的報告分別為97、112、47、18、7 份,其中,阿替利珠單抗、度伐利尤單抗未形成陽性信號。TEN患者的基本特征見表4,其結局見圖3,其中死亡比例最高的為帕博利珠單抗(66.96%。75/112)。
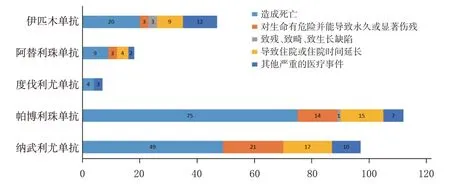
圖3 5種ICIs致TEN患者的結局
3 討論
3.1 ICIs的作用機制
腫瘤細胞通過招募免疫抑制性細胞、下調腫瘤抗原表達、誘導T 細胞凋亡或功能耗竭,并產生誘導抑制性免疫檢查點表達的免疫抑制分子,從而形成高度免疫抑制的腫瘤微環境,以逃避免疫監視[15―16]。在腫瘤微環境中,免疫檢查點如CTLA-4、PD-1及其配體PD-L1顯著過表達[17],從而可抑制T細胞的激活,導致“免疫耗竭”。因此,這些免疫檢查點是重要的免疫治療靶點,阻斷這些免疫檢查點可以“解除”這種免疫抑制,并重新激活能夠摧毀腫瘤細胞的細胞毒性T 細胞[18―19]。基于該機制,ICIs類藥物應運而生。
3.2 ICIs與irAEs
ICIs用于多種惡性腫瘤的療效顯著,使免疫治療成為除手術、放化療和靶向治療外極具潛力的腫瘤新療法[16]。ICIs類藥物顯著提高了黑色素瘤、非小細胞肺癌、肝細胞癌等多種晚期惡性腫瘤患者的生存率[20],但其潛在的irAEs 風險不容小覷。研究指出,在接受ICIs 治療的患者中,有70%~90%的患者會發生irAEs,其中嚴重irAEs 的發生率為10%~15%[21],這些反應可導致1.3%的患者死亡[22]。
3.3 ICIs致嚴重皮膚不良反應的風險
本研究著重對5 種ICIs 導致嚴重皮膚不良反應的ADEs 報告進行了分析,結果顯示,5 種ICIs 均可在嚴重皮膚不良反應方面生成陽性信號,信號與藥物的關聯度從強到弱依次為帕博利珠單抗>阿替利珠單抗>納武利尤單抗>伊匹木單抗>度伐利尤單抗。有學者收集并逐篇查閱公開發表的關于ICIs 致嚴重皮膚不良反應的20項隨機對照試驗,結果發現,帕博利珠單抗共導致84 例嚴重皮膚不良反應,其發生率高于伊匹木單抗[23];結合本研究可以看出,帕博利珠單抗致嚴重皮膚不良反應的發生率大于其余4種ICIs,關聯度最強。
3.4 ICIs致SJS/TEN的風險
SJS/TEN是以皮膚-黏膜損害為主的系統性危重癥,臨床病死率較高,以水皰及泛發性表皮松解為特征,可累及多個系統。目前學界普遍認為,SJS/TEN代表了一組疾病譜,SJS 為輕型(表皮松解面積<10%體表總面積),TEN為重型(表皮松解面積>30%體表總面積),介于兩者之間為重疊型SJS-TEN(表皮松解面積占10%~30%體表總面積)[11]。
本研究中,5 種ICIs 均可導致SJS 和TEN 的發生。分析SJS相關報告可知,5種ICIs均可形成陽性信號,且關聯度強弱依次為帕博利珠單抗>阿替利珠單抗>度伐利尤單抗>納武利尤單抗>伊匹木單抗。分析TEN相關報告可知,阿替利珠單抗和度伐利尤單抗均未形成陽性信號,其余3 種ICIs 的關聯度強弱依次為帕博利珠單抗>伊匹木單抗>納武利尤單抗。從上述結果可以看出,帕博利珠單抗與SJS、TEN 均有關聯,且關聯度在5種ICIs中是最強的。PD-L1抑制劑阿替利珠單抗和度伐利尤單抗與SJS 的關聯度僅次于帕博利珠單抗,但其致TEN并非陽性信號,說明PD-L1抑制劑導致SJS的可能性大,與TEN 關聯度不高。有研究表明,分別有90%和70%接受CTLA-4 抑制劑和PD-1/PD-L1 抑制劑治療的患者會出現irAEs,幾乎所有接受多種方案聯合治療的患者均會出現irAEs[24]。在使用ICIs過程中,如果確需聯用多種ICIs,可考慮將PD-L1 抑制劑與CTLA-4 抑制劑聯用,盡量避免帕博利珠單抗與其他ICIs聯用。
通過分析發生SJS 和TEN 的患者基本特征可知:(1)患者普遍以65 歲及以上居多,除使用阿替利珠單抗者外,其余均是男性發生率更高;(2)亞洲國家上報的病例數普遍居首位;(3)因SJS死亡的患者比例從大到小依次為帕博利珠單抗(35.37%)>阿替利珠單抗(30.23%)>納武利尤單抗(26.85%)>伊匹木單抗(23.64%)>度伐利尤單抗(0),因TEN 死亡的患者比例從大到小依次為帕博利珠單抗(66.96%)>度伐利尤單抗(57.14%)>納武利尤單抗(50.52%)>阿替利珠單抗(50.00%)>伊匹木單抗(42.55%),均大于文獻報告[11]。從上述結果可以看出,≥65 歲的男性患者在使用ICIs時,其SJS/TEN的發生風險更高,臨床醫生應提高警惕,重視嚴重皮膚不良反應的發生。本研究收集到的ADEs報告以亞洲病例居多,故上述結果對國內臨床用藥的參考價值較大。
3.5 ICIs在嚴重皮膚不良反應報告中的獨特信號
5種ICIs以PTs進行信號檢測,結果顯示,帕博利珠單抗在大皰性皮膚松解、角膜脫落和皮膚糜爛中單獨形成信號,納武利尤單抗在獲得性大皰性表皮松解癥、結膜炎和黏膜類天皰瘡中單獨形成信號,伊匹木單抗在全身剝脫性皮炎中單獨形成信號(表2)。SJS和TEN可導致嚴重的眼科后遺癥。有研究表明,SJS/TEN患處體表面積剝離度≥10%、患者年齡≥60 歲、血清生物標志物S100 鈣結合蛋白A8/A9 復合物和顆粒溶素水平升高等因素均與急性嚴重眼部并發癥相關[25]。當具有上述高危因素的患者使用帕博利珠單抗時,臨床醫生應特別警惕并及時干預,最大限度降低視力喪失等慢性眼部后遺癥的發生風險。
綜上,5 種ICIs 均可在嚴重皮膚不良反應方面生成陽性信號,信號與藥物的關聯度從強到弱依次為帕博利珠單抗>阿替利珠單抗>納武利尤單抗>伊匹木單抗>度伐利尤單抗,且帕博利珠單抗致嚴重皮膚不良反應的發生率高于其余4 種ICIs,關聯度最強。建議臨床在使用ICIs 時,無論是何種藥品,都應考慮相關嚴重皮膚不良反應的可能性。帕博利珠單抗與SJS 和TEN 的關聯度均最高,且發生SJS/TEN后導致患者死亡的風險也最高,因此患者(尤其是≥65歲的男性患者)在使用帕博利珠單抗時要尤為警惕,同時應盡量避免ICIs之間的聯用。

