基于美國FAERS的伊沙佐米風險信號挖掘Δ
楊 莉,趙新才,徐 嶸,張劍萍 (上海交通大學醫學院附屬第六人民醫院藥劑科,上海 200233)
多發性骨髓瘤(multiple myeloma,MM)是克隆漿細胞異常增殖的血液系統惡性腫瘤,多發于老年人,常見癥狀包括骨髓瘤相關器官功能損傷,如血鈣增高、腎功能損害、貧血、骨病、繼發淀粉樣變性等[1]。目前,該病相關治療方案的顯著進展是引入了蛋白酶體抑制劑(proteasome inhibitor,PI)、免疫調節劑、針對骨髓瘤細胞表面抗原的單克隆抗體和自體造血干細胞移植[2]。
伊沙佐米是全球首個口服PI,主要通過抑制蛋白酶體的生物功能來發揮殺傷腫瘤細胞的作用,現多與來那度胺和地塞米松聯合(即“IRd 方案”),用于既往接受至少1種藥物治療的MM成人患者[3]。該藥于2015年在美國獲批上市,于2018年在我國上市并于同年進入國家醫保目錄,使得我國MM患者的用藥可及性大大提高。然而在臨床廣泛應用的同時,該藥的安全性也備受重視。研究指出,伊沙佐米會增加患者3級以上血小板減少、腹瀉、皮疹、周圍神經病變的發生率;除此之外,該藥還可引起惡心、嘔吐、便秘、周圍水腫和背痛等常見的不良反應[4―5]。上述安全信息雖已被藥品說明書收錄,但為更好、更全面地了解和評估伊沙佐米的安全性,本研究擬對美國FDA 不良事件報告系統(FDA adverse event reporting system,FAERS)數據庫收錄的相關藥品不良事件(adverse drug event,ADE)報告進行提取和分析,進一步為臨床規范、合理使用該藥提供參考。
1 資料與方法
1.1 數據來源
本研究的原始數據來源于FAERS 數據庫,利用Open Vigil 2.1 在線工具(http://h2876314.stratoserver.net:8080/OV2/search/)進行相關數據查詢、清洗及提取。FAERS 數據庫是自發呈報數據庫,由美國FDA 每季度更新1 次[6]。Open Vigil 2.1 是一種公開且免費的、可在線使用以解析FAERS數據庫數據的藥物警戒分析工具,會自動剔除信息不完整和重復的報告,可一定程度地提高納入報告的整體質量[7]。
本研究數據提取起始時間為伊沙佐米在美國獲批上市的時間(2015年11月20日),截止時間為Open Vigil網站最近更新的時間(2023年3月31日)。目標藥物的檢索通用名限定為“ixazomib”,同時將“role of drug”限定為“首要懷疑藥物(primary subject)”。
對于從網站中提取到的原始數據,以1例“個人安全報告(individual safety reports,ISR)”作為1 例ADE 來進行統計。
1.2 信號挖掘與分析
本研究基于比例失衡法的2×2列表(表1),采用報告比值比(proportional reporting ratio,PRR)法和貝葉斯置信區間遞進神經網絡(Bayesian confidence propagation neural nework,BCPNN)法對伊沙佐米的風險信號進行挖掘[8]。PRR 法陽性信號的判定標準為:在目標藥物ADE 發生數(DE)≥3 的情況下,若PRR≥2 且χ2≥4,則記作1個陽性信號;PRR值越大,陽性信號則越強,即伊沙佐米與該ADE 之間的相關性越強[9]。BCPNN 法陽性信號的判定標準為:計算信息成分(information component,IC)值及其下限(IC-2SD),0<IC-2SD≤1.5為弱信號,1.5<IC-2SD≤3 為中信號,IC-2SD>3 為強信號[10―11]。數據分析采用WPS表格(2023版)軟件。同時,原始數據采用國際人用藥品注冊技術協調會編制的國際醫學用語詞典(Medical Dictionary for Regulatory Activities,MedDRA)25.1 版對信號的系統器官分類(system organ class,SOC)和首選術語(preferred term,PT)進行標準化編碼。
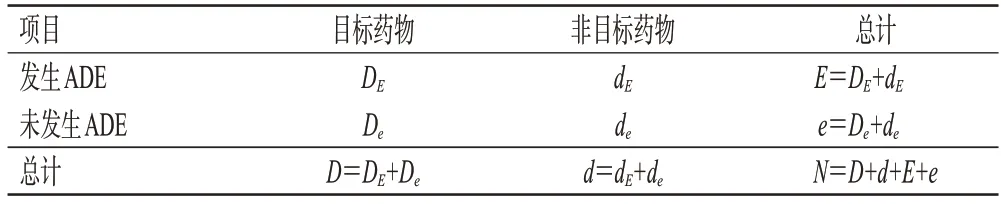
表1 比例失衡法的2×2列表
2 結果
2.1 伊沙佐米相關ADE報告的基本情況
本次研究共提取到13 841份以“伊沙佐米”為“首要懷疑藥物”的ADE報告。其中,男性占比(49.53%)略高于女性(45.52%);在排除年齡缺失的數據(6 221例)后,65 歲及以上患者居多(72.48%);報告分別來自57 個國家/地區,上報最多的是美國(52.90%),隨后依次是加拿大(14.11%)、日本(9.15%)、英國(6.57%)、法國(5.12%)、中國(3.53%)等。結果見表2。
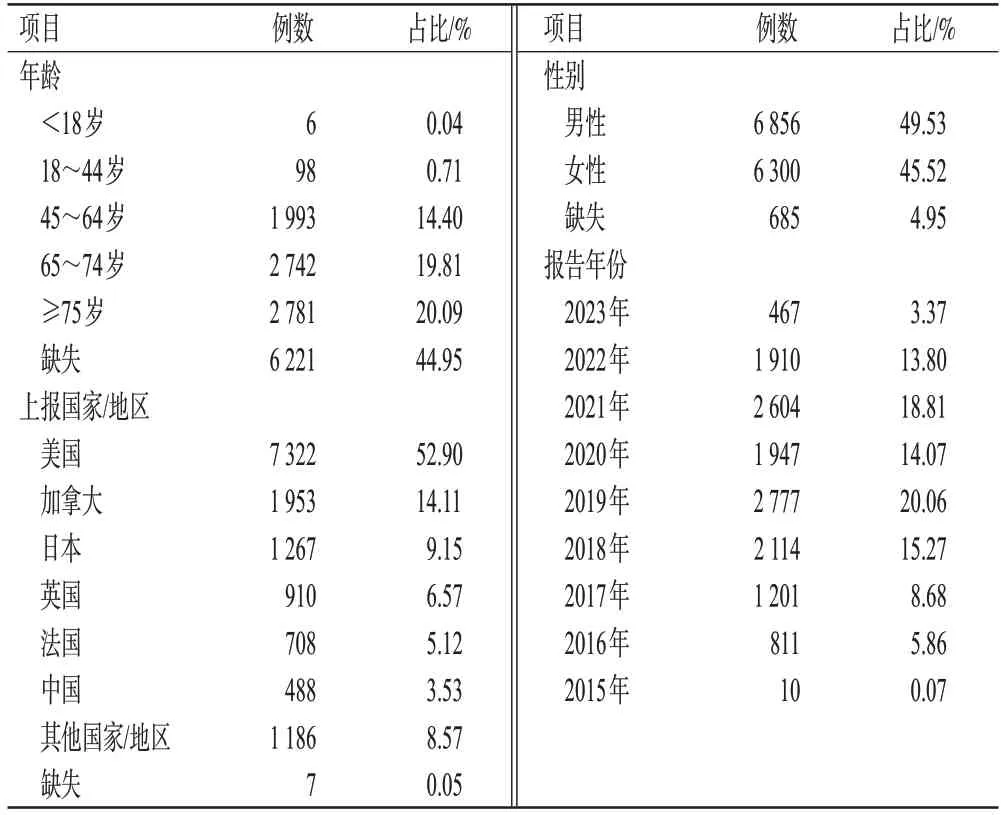
表2 伊沙佐米相關ADE報告的基本情況(n=13 841)
2.2 伊沙佐米陽性信號分析結果
排除適應證相關和完全不相關的PT 后,本研究共獲得以伊沙佐米為“首要懷疑藥物”且經PRR、BCPNN法判定均為陽性的信號共186 個,涉及患者13 538 例。其中,周圍神經病、血小板計數降低、血小板減少癥、血細胞減少癥、神經病學癥狀的發生頻次和PRR信號強度均排在前50位,具體見表3。

表3 伊沙佐米ADE 發生頻次和PRR 信號強度均排前50位的陽性信號
伊沙佐米186個陽性信號PT中,包含強信號51個、中信號99 個、弱信號36 個,累及SOC 共19 個。其陽性信號主要集中在全身性疾病及給藥部位各種反應(2 687例)、胃腸系統疾病(2 588例)、感染及侵染類疾病(1 705例)等。結果見表4。

表4 伊沙佐米信號累及SOC情況和對應PT信號強度等級劃分
3 討論
3.1 伊沙佐米陽性信號分析
本研究發現,伊沙佐米在周圍神經病(414 例,PRR=9.713,強信號)、血小板計數降低(379 例,PRR=8.413,強信號)、血小板減少癥(360 例,PRR=8.537,強信號)、血細胞減少癥(75 例,PRR=11.436,強信號)、神經病學癥狀(41 例,PRR=19.347,強信號)這5 個PT 的發生頻次和信號強度均排在前50 位內,主要累及SOC為各類神經系統疾病、各類檢查、血液及淋巴系統疾病,與目前各項真實世界研究中常見的不良反應基本相符[12―13]。此外,上述各類神經系統疾病和血液及淋巴系統疾病2 個SOC 還包含一些未被藥品說明書記載但呈中/強度的陽性信號PT,如癡呆、共濟失調、肌陣攣、舞蹈病、脊髓壓迫、異常感覺、感覺減退、認知障礙、味覺障礙、多發神經病、發熱性骨髓再生障礙、貧血,對于這些相關癥狀,臨床應予以關注。
3.1.1 累及胃腸系統疾病的陽性信號分析
伊沙佐米相關ADE 發生頻次最多的是全身性疾病及給藥部位各種反應(2 687 例),但強信號死亡和ADE的定義過于寬泛,討論意義不大。排除這2 個PT 后,伊沙佐米致ADE 發生頻次最多的是胃腸系統疾病(2 588例)。其中,發生頻次較多的有腹瀉(1 077例,強信號)、惡心(737 例,中信號)、嘔吐(459 例,中信號)、便秘(275例,中信號),上述信號均已被藥品說明書收錄。值得注意的是,腸梗阻(機能性)(12 例,中信號)可能是伊沙佐米的重度胃腸道安全事件,也可能是其新的潛在不良反應。
3.1.2 累及感染及侵染類疾病的陽性信號分析
感染及侵染類疾病陽性信號包含的PT 較多且大多尚未被藥品說明書收錄。其中,強信號PT 有12 個(1 030例)、中信號PT有30個(627例),主要涉及肺部感染、上呼吸道感染、胃腸道感染、膿毒癥、帶狀皰疹等。國內一項多中心真實世界研究報道了多例伊沙佐米引起肺部感染、上呼吸道感染和腸道感染的病例[14];另一項多中心臨床Ⅱ期研究也提及,肺炎是伊沙佐米使用者常見的嚴重ADE[15],這些報道與本次研究結果基本相符。可見,在使用伊沙佐米時,臨床應重點關注該藥致感染的相關ADE,尤其是肺部感染的發生。
3.1.3 累及心臟器官疾病的陽性信號分析
MM患者通常年齡較大,且攜帶心血管毒性累積的危險因素,增加了PI的心臟毒性負荷[16]。在本研究收集到的心臟器官疾病中/強度陽性信號中,心臟淀粉樣變性(7例,強信號)和急性冠脈綜合征(14例,強信號)均未在中文藥品說明書中被提及,臨床需予以重視。
雖然伊沙佐米作為可逆性PI,其心血管毒性事件并不常見,但國外學者曾報道過1例患者在接受伊沙佐米治療后出現急性失代償性心力衰竭,且停藥后左心室功能未能恢復正常[16];國內的一項真實世界研究也報道了2 例患者接受IRd 方案治療后,因出現3~4 級心力衰竭且并發心臟淀粉樣變性而停藥[14]。可見,上述2 個心臟器官疾病強信號可能是伊沙佐米新的潛在不良反應,有必要進一步評價其實際臨床意義。
3.1.4 累及腎臟及泌尿系統疾病和其他的陽性信號分析
本研究收集到腎臟及泌尿系統中/強度陽性信號只有1個,即腎功能損害(91例,中信號),在各類檢查中還收集到了51例血肌酐升高(中信號)的病例報告。腎功能損害本身是MM 的并發癥之一,根據相關研究,伊沙佐米的腎清除率較低,當復發/難治性MM 患者的肌酐清除率低于30 mL/min 時,需選擇較低的起始劑量(3 mg)[17]。2017、2018年相關研究分別報道了2 例與伊沙佐米相關的藥物致血栓性微血管病的病例,這2例患者均表現出了急性腎損傷癥狀[18―19],可能與PI免疫介導和劑量依賴性毒性等因素所致的內皮細胞損傷及微血管病變有關[20]。國內一項回顧性研究也報道了1例接受伊沙佐米方案治療后出現短暫肌酐升高,予保腎治療后回落的病例[13]。可見,伊沙佐米有導致MM患者腎功能損害的可能,但兩者的關聯還需更多臨床研究予以證實。
另外值得一提的是,超說明書使用(1 306 例)在伊沙佐米相關ADE發生頻次中排第2位,臨床需進一步關注該藥的實際應用情況,保證其應用的合理性、規范性。
3.2 數據挖掘的局限性
數據挖掘作為一種廣泛應用于藥物不良反應監測的方法,可在數據量龐大的ADE報告中檢測風險信號,有利于藥物潛在不良反應的發現。但由于FAERS 數據庫中的信息是自發上報的,且參與上報的人員并非全是醫務人員,上報質量也參差不齊,故常存在上報數據缺失、漏報,患者實際臨床信息缺失,難以排除其他風險因素等不足[21]。Open Vigil 在線工具雖已對不完整的上報數據進行了篩選,但也一定程度地導致了樣本脫落,這些因素最終都會不可避免地對數據挖掘結果產生不利影響。另外,本研究以PRR 法和BCPNN 法所挖掘出的陽性信號僅能說明藥物與ADE信號之間存在統計學關聯,但其明確的臨床意義還需真實世界研究予以驗證。
綜上所述,基于FAERS數據庫挖掘的伊沙佐米風險信號中,上報頻次較多的ADE基本與藥品說明書記載相符,也與目前各真實世界研究的常見不良反應相符,主要涉及胃腸系統疾病、各類神經系統疾病和血液及淋巴系統疾病;感染及侵染類疾病中出現中/強度陽性信號PT最多,且多數未被藥品說明書記載,主要表現在肺部感染、上呼吸道感染、胃腸道感染、膿毒癥、帶狀皰疹等方面;心臟器官疾病中的強信號急性冠脈綜合征、心臟淀粉樣變性可能是該藥新的潛在不良反應;腎功能損害與伊沙佐米ADE的關系還需進一步討論。可見,除需常規關注的伊沙佐米相關胃腸系統疾病、各類神經系統疾病、血液及淋巴系統疾病等常見ADE外,臨床還需關注患者在治療期間可能出現的各種感染,密切監測其心血管毒性和腎功能損害的發生,保證患者用藥的安全、有效。

