幾種環境因子對IHHNV在凡納濱對蝦體內增殖的影響
張麗 馬文婷 姚洪旺 李娜 包海巖
摘要:為闡明在凡納濱對蝦(Litopenaeus vannamei)養殖過程中影響傳染性皮下及造血組織壞死病毒(IHHNV)增殖的關鍵因子,在實驗室條件下,研究了溫度、鹽度、氨氮、亞硝酸鹽氮等環境因子變化對凡納濱對蝦體內IHHNV增殖的影響。結果顯示:在同樣條件下,水溫25 ℃和30 ℃凡納濱對蝦體內IHHNV病毒數具有明顯差異,且在30℃時最大;2.5‰、10.0‰、20.0‰三個鹽度梯度IHHNV增殖組間差異顯著,且增殖速度與鹽度呈正相關;在氨氮0.05、3.00、7.00 mg/L三個濃度梯度下,IHHNV在凡納濱對蝦體內增殖數量的變化未表現出線性關系,但氨氮0.05 mg/L濃度組凡納濱對蝦體內病毒數明顯低于3.00、7.00 mg/L濃度組;在亞硝酸鹽氮0.05、5.00、10.00 mg/L三個濃度梯度下,IHHNV在凡納濱對蝦體內增殖數的變化組間差異不顯著。
關鍵詞:凡納濱對蝦(Litopenaeus vannamei);環境因子;傳染性皮下及造血組織壞死病毒(IHHNV);增殖
隨著凡納濱對蝦(Litopenaeus vannamei)養殖業的迅猛發展,養殖疾病逐年增多,造成了極大的經濟損失。環境因子作為養蝦池塘生態系統的主要部分,對對蝦病毒病的暴發起著重要作用。環境因子超出對蝦的適應范圍就會成為脅迫因子,這種脅迫既影響生物體也影響病原體。養殖環境涉及的脅迫因子包括水質理化因子(溫度、鹽度、pH、溶解氧、環境污染物等)、生物因子(媒介生物等)。近年來環境脅迫因子對養殖生物的生理病理影響受到越來越多國內外科研工作者的重視。已有研究表明:疾病暴發主要是宿主、環境和病原體三者經過復雜的相互作用的結果,在一定環境條件下,宿主與其攜帶的病原體可以共存,當某些環境條件發生了大的變化,可能會導致疾病的暴發。黃燦華等[1]對養蝦水體環境因子變化與對蝦病毒病之間的關系進行了實驗分析,結果表明某些環境因子(如高鹽、低溶氧)的變化能明顯誘發對蝦發病死亡。
對蝦被病毒感染后是否發病是多種因素相互作用、相互影響的結果。包括機體自身的抗病力水平、病原微生物以及環境條件等[2]。徐麗美等[3]通過研究發現了每毫克組織含103個病毒粒子可作為疾病暴發的危險臨界數值。本試驗研究了部分環境因子變化對傳染性皮下及造血組織壞死病毒(IHHNV)在對蝦體內增殖的影響,在室內條件下,模擬自然養殖環境,研究溫度、鹽度、氨氮、亞硝酸鹽氮等環境因子變化對凡納濱對蝦體內IHHNV增殖的影響,分析不同影響因子對IHHNV在對蝦體內增殖的影響力大小,以期闡明在對蝦養殖過程中影響IHHNV在對蝦體內增殖情況的關鍵因子,為綜合防治IHHN的發生提供科學依據。
1材料與方法
1.1材料
1.1.1供試陽性組織陽性組織取自天津地區某發病養殖場池塘采集樣品,試驗用陽性凡納濱對蝦經PCR方法進行多種病毒檢測,根據檢測結果取傳染性皮下及造血組織壞死病毒(IHHNV)陽性,而白斑綜合征病毒(WSSV)、致急性肝胰腺壞死細菌(VPAHPND)、偷死野田村病毒(CMNV)、蝦肝腸胞蟲(EHP)均陰性的樣品用于制備攻毒實驗用病毒粗提液。
1.1.2病毒粗提液病毒提取方式參照孔杰等[4]和吳昊等[5]的方法進行,于超凈臺內無菌條件下取感染IHHNV的凡納濱對蝦的鰓絲,加入三倍體積TNM緩沖液[5] (配方:Tril-HCl 20 mmol/L;NaCl 100 mmol/L;MgCl 5 mmol/L,121 ℃高壓滅菌15 min),冰浴勻漿,勻漿液4 ℃、13 000 rpm/min離心10 min;離心后取上清液再4 ℃、13 000 rpm/min離心5 min,分裝到1.5 mL離心管中,-80 ℃冰箱中保存備用。每管分別取1 μL用RT-PCR測量IHHNV的濃度。
1.1.3試驗用凡納濱對蝦試驗凡納濱對蝦取自天津濱海新區某對蝦養殖廠,體長10 cm左右,平均體重約15 g。經檢測,白斑綜合征病毒(WSSV)、致急性肝胰腺壞死細菌(VPAHPND)、偷死野田村病毒(CMNV)、傳染性皮下及造血組織壞死病毒(IHHNV)、蝦肝腸胞蟲( EHP)均為陰性,暫養3 d,無死亡。
1.1.4試驗場地、設備試驗池為長方體玻璃缸,每個缸水體約80 L,具備循環水養殖系統,每個組設置3個平行,每個平行養殖對蝦20尾。試驗用水為自來水兌鹵水調節鹽度。水溫25 ℃,鹽度2‰,氨氮0.01 mg/L,亞硝酸鹽氮0.01 mg/L,pH值 7.6~8.6,暫養3 d。
1.2方法
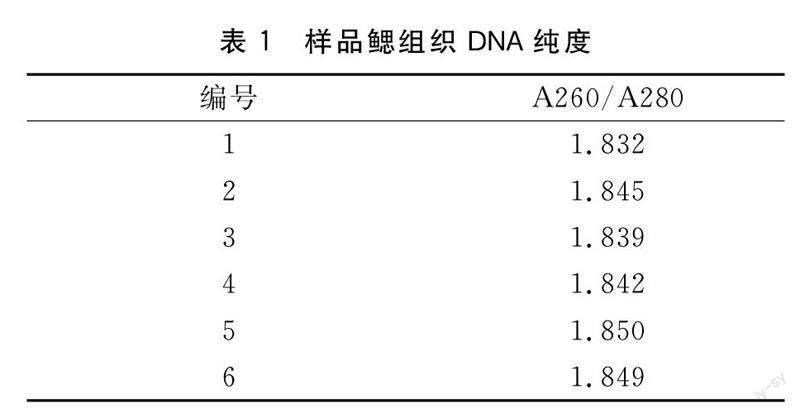
1.2.1陽性樣品病毒濃度測定隨機取6管病毒粗提液,用天根生化科技(北京)有限公司生產的血液/細胞/組織基因組DNA提取試劑盒,分別提取對蝦鰓組織DNA并測定所提取的DNA的A260/A280 比值和IHHNV的濃度。
1.2.2人工感染預試驗
設病毒粗提液106、103copies/μL兩個梯度,采用注射感染,每個梯度注射20尾蝦,設1組平行試驗組。從對蝦倒數第2腹節側面連接處的淺層肌肉進行注射,每尾注射量為10 μL,對照組注射TNM緩沖液。在注射后48 h、72 h、168 h、216 h取樣,樣品暫存于-20 ℃冰箱中。用DNA提取試劑盒提取對蝦鰓組織DNA,用RT-PCR方法檢測IHHNV濃度。
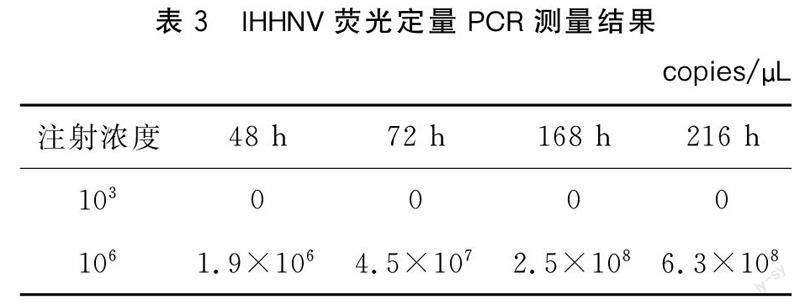
本試驗選擇肌肉注射,可以嚴格控制進入對蝦體內病毒的數量,便于后期對蝦體內病毒量的測定和分析。本次試驗結果顯示病毒濃度為103 copies/μL時注射后48 h、72 h、168 h、216 h鰓組織中未檢測到IHHNV;而病毒濃度為106 copies/μL注射后,從48 h到168 h病毒濃度呈增長趨勢;從168 h到216 h,病毒濃度趨于緩慢增長趨勢,故后期試驗病毒的注射濃度選定為106 copies/μL,檢測時間≤168 h。
1.2.3病毒檢驗方法取對蝦鰓組織10 mg提取DNA,得到100 μL的DNA模板,采用熒光定量PCR方法進行檢測。
1.2.4不同環境因子對IHHNV在感染對蝦體內增殖的影響
暫養后,采用人工感染預試驗的方法,肌肉注射感染IHHNV。試驗中觀察記錄對蝦發病及死亡數,根據實際情況設定取樣起始時間點,每隔24 h取2~3尾蝦鰓組織,-20 ℃冷凍保存,用于病毒檢測。人工感染后每天投喂1次人工配合飼料,換水20%~50%,排出殘餌和糞便,試驗過程中24 h充氣,保證溶解氧濃度。
溫度變化試驗時,將三組試驗水體通過自動控溫系統,把溫度分別控制在(19±1)℃、(25±1)℃、(30±1)℃,在96 h、120 h、144 h、168 h、192 h取樣;鹽度變化試驗時,將三組試驗水體通過添加鹵水,將鹽度調節到2.5‰±1‰、10.0‰±1‰、20.0‰±1‰,在96 h、120 h、144 h、168 h取樣;氨氮濃度變化試驗時,氨氮濃度用氯化銨調節使濃度分別為 0.05、3.00、7.00 mg/L,為保持氨氮的濃度,每天換水50%左右,在72 h、 96 h、120 h、144 h、168 h取樣;進行亞硝酸鹽濃度變化試驗時,亞硝酸鹽濃度用亞硝酸鈉調節使濃度分別為0.05、5.00、10.00 mg/L,為保持硝酸鹽氮的濃度,每天換水50%左右,在72 h、 96 h、120 h取樣。
2結果
2.1陽性樣品病毒濃度測定
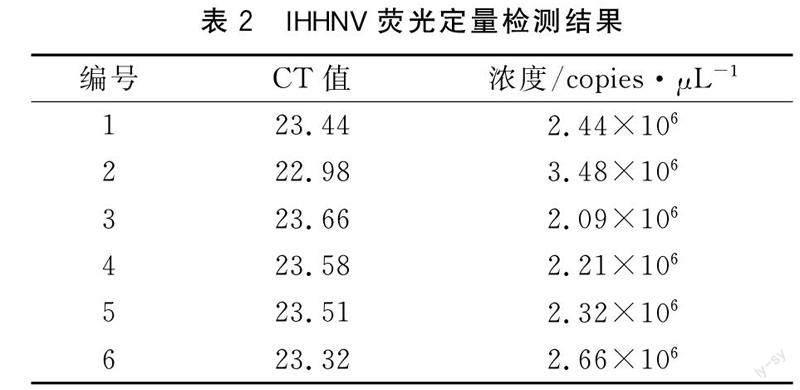
測定提取對蝦鰓組織DNA的A260/A280 比值,均在1.8~2.0之間,結果見表1。用RT-PCR方法測量IHHNV的濃度,結果見表2。
2.2IHHNV的人工感染試驗
濃度為103、106 copies/μL病毒粗提液攻毒試驗后不同時間體內病毒含量測定結果見表3。
2.3溫度變化試驗
表4為攻毒后三個溫度組對蝦在96~192 h內五次取樣并進行病毒濃度測定的結果。通過SPSS軟件進行雙因素方差分析,結果顯示病毒增殖總量在溫度組20 ℃、25 ℃、30 ℃組間P<0.05,說明不同水溫組病毒增殖數量有顯著差異。通過表4可以看出,在30 ℃時病毒增殖數量高于20 ℃和25 ℃。而在同一組內,96~192 h對蝦體內IHHNV拷貝數呈增長趨勢。
2.4鹽度變化試驗
表5為攻毒后不同鹽度組對蝦在96~168 h內四次取樣并進行病毒濃度測定的結果。通過SPSS軟件進行雙因素方差分析顯示,不同鹽度組間P<0.05,差異顯著。說明在不同鹽度組病毒增殖數量有顯著差異。不同鹽度組Pearson(皮爾遜)相關性系數為0.651,且顯著性水平小于0.05,說明IHHNV在凡納濱對蝦體內增殖的速度與鹽度呈正相關,即在鹽度2.5‰~20.0‰范圍內,凡納濱對蝦體內IHHNV增殖速度隨著鹽度的升高而提高。
2.5氨氮變化試驗
表6為攻毒后不同氨氮濃度組對蝦在72~168 h內五次取樣并進行病毒濃度測定的結果。
通過SPSS軟件進行雙因素方差分析,結果顯示不同氨氮組間P>0.05,說明在不同氨氮濃度組病毒增殖數量差異不顯著。不同氨氮組Pearson(皮爾遜)相關性系數為0.274,說明IHHNV在凡納濱對蝦體內增殖的數量與水體中氨氮的濃度相關性低。
2.6亞硝酸鹽氮變化試驗
表7為攻毒后不同氨氮濃度組對蝦在72~120 h內三次取樣并進行病毒濃度測定的結果。通過SPSS軟件進行雙因素方差分析,結果顯示不同氨氮組間P>0.05,說明在不同氨氮濃度組病毒增殖數量差異不顯著。不同氨氮組Pearson(皮爾遜)相關性系數為 -0.218,說明IHHNV在凡納濱對蝦體內增殖的數量與水體中亞硝酸鹽氮濃度相關性低。
3分析與討論
3.1病毒粗提液制備
陽性樣品在病毒粗提過程采取13 000 rpm離心10 min,消除細菌的影響。對凡納濱對蝦進行WSSV、IHHNV、EHP、CMNV、VPAHPND五種病原PCR檢測,保證試驗用凡納濱對蝦陽性樣品只攜帶IHHNV,確保感染后病毒的單一性。病毒提取過程中均在冰水中操作,確保病毒的活性。對粗提后的病毒,進行熒光定量PCR的檢測,確定病毒濃度,再用不同濃度的病毒進行人工感染預試驗,確定人工感染濃度,以證明粗提液的感染性。本試驗病毒粗提液的方法參考吳昊等[5]病毒提取的方法,并根據試驗需求進行適當調整。本試驗人工感染預試驗結果滿足試驗要求,故病毒未進行再次提純,直接用于攻毒試驗。
3.2對蝦的IHHNV人工感染技術
本試驗采用了肌肉注射方法進行攻毒試驗,而未采用投喂病料、病毒浸泡等方法,雖然投喂感染更接近自然狀況,但與注射感染相比較,由于個體攝食行為差異,攝入的病毒量不同,因而后期試驗研究時可比性較差。注射感染的可控性強,能夠準確記錄每尾蝦個體中攻入的病毒劑量,更準確地對比病毒在不同對蝦個體中數量的變化。
3.3不同環境因子對IHHNV在感染對蝦體內增殖的影響
3.3.1溫度對IHHNV在感染對蝦體內增殖的影響溫度是養殖環境中重要的環境因子,對蝦的新陳代謝、抗病力、生長、發育及進食等都會受到影響,李侃等[6]對白斑病毒進行研究,結果顯示病毒在溫度為21~30 ℃之間增殖最快,而當溫度低于20 ℃或超過30 ℃時,病毒的增殖速度受到部分抑制。Du H等[7]發現蝦體內病毒攜帶量在(10±1)℃條件下明顯低于(24±1)℃條件下。Dee Montgomery-Brock等[8]研究發現高水溫可以抑制凡納濱對蝦體內 IHHNV 的增殖。柴超[9]研究了23.87~26.8 ℃范圍內溫度對IHHNV復制的影響,研究結果表明溫度增高可以增加IHHNV 的復制。本試驗結果顯示,在同一時間點,對蝦體內病毒增殖數量在水溫25 ℃和30 ℃具有明顯差異。在同一時間采集樣品組織中IHHNV拷貝數在30 ℃時最大,與柴超的研究結果具有一致性,但本試驗時間設定范圍較大,如果想要得到更加細致的結果,需要增加多個溫度點開展進一步的研究。
3.3.2鹽度對IHHNV在感染對蝦體內增殖的影響Bray等[10]發現高鹽度和IHHN病毒感染之間有明顯的相互作用。柴超[9]也發現鹽度與 IHHNV 拷貝數具有低相關性。管越強[2]研究發現鹽度可顯著影響蝦類的免疫反應,超出適鹽范圍免疫反應下降。本試驗研究了2.5‰、10.0‰、20.0‰三個鹽度梯度內對蝦體內IHHNV增殖的數量變化,結果表明IHHNV在凡納濱對蝦體內增殖的速度與鹽度呈正相關,即在鹽度2.5‰~20.0‰范圍內,凡納濱對蝦體內IHHNV增殖速度隨著鹽度的升高而提高。
3.3.3氨氮對IHHNV在感染對蝦體內增殖的影響氨氮是對蝦養殖池塘中最主要的無機污染物,張輝[11]以日本囊對蝦(Marsupenaeus japonicus)為實驗動物開展研究,發現經氨氮脅迫處理后的對蝦感染WSSV后,體內病毒復制水平明顯高于未處理組。郝晨光[12]通過研究發現在氨氮脅迫下,氨氮濃度越高,協迫時間越長,實驗組克氏原螯蝦鰓絲內WSSV增殖越快。向赟[13]研究氨氮濃度突變對攜帶WSSV對蝦的影響,發現濃度 0.05 mg/L感染組病毒含量明顯低于1.25 mg/L和3 mg/L感染組,對于攜帶WSSV的對蝦,不同氨氮濃度突變都給對蝦體內WSSV增殖提供機會。本試驗根據孫國銘等[14]關于氨氮和亞硝酸氮對凡納濱對蝦的毒性研究的結果,研究了在0.05、3.00、7.00 mg/L三個氨氮濃度梯度下,IHHNV在凡納濱對蝦體內病毒增殖數量的變化,結果是差異不顯著。Pearson相關性顯示氨氮濃度變化與IHHNV在凡納濱對蝦體內病毒增殖數量不相關。但本試驗結果顯示氨氮濃度0.05 mg/L濃度組對蝦體內病毒數量明顯低于3.00、7.00 mg/L濃度組。本試驗結果顯示氨氮濃度與對蝦體內病毒數量未表現出具體的線性關系,可能與養殖試驗過程中氨氮濃度不穩定有關。本試驗使用氯化銨調節氨氮,但發現氨氮調整到所需濃度后第二天會下降到起始濃度的一半以上,為了保證氨氮濃度的穩定,采用換水50%的方法,但氨氮還是不能一直保證穩定在試驗濃度,這或許是造成三個濃度結果不顯著的一個原因。后續研究可考慮用其他方法保證氨氮濃度的穩定。
3.3.4亞硝酸鹽氮對IHHNV在感染對蝦體內增殖的影響管越強[2]研究發現,亞硝酸鹽氮對凡納濱對蝦抗病力相關因子有顯著影響。本試驗根據孫國銘等[14]有關氨氮和亞硝酸氮對凡納濱對蝦的毒性研究結果,研究了在 0.05、5.00、10.00 mg/L三個亞硝酸氮濃度梯度下,IHHNV在凡納濱對蝦體內病毒增殖數量的變化,結果差異不顯著。這可能與為維持亞硝酸鹽氮濃度進行大量換水,對蝦造成應激有關。而且本試驗只進行了120 h,如果再開展類似試驗,應在穩定試驗水體亞硝酸鹽氮濃度的同時增加觀察周期,以獲得更有說服力的數據。
參考文獻:
[1] 黃燦華,石正麗,張建紅,等.養蝦水體環境因子變化與對蝦病毒病之間的關系[J].中山大學學報(自然科學版),2000(S1):159-163.
[2] 管越強.主要環境因子對養殖對蝦抗病力及白斑綜合癥發生的影響[D].青島:中國科學院研究生院(海洋研究所),2003.
[3] 徐麗美,楊豐.利用定量PCR方法研究對蝦白斑桿狀病毒感染與發病的關系[J].高技術通訊,2001(12):9-11.
[4] 孔杰,石拓,劉萍,等.中國對蝦一種C型桿狀病毒的純化技術及形態特征研究[J].海洋與湖沼,1997(3):233-237.
[5] 吳昊,徐麗美,楊豐.對蝦傳染性皮下及造血組織壞死病毒(福建株)基因組的克隆[J].臺灣海峽,2008,100(2):147-151.
[6] 李侃,羅淑婭,徐麗美.溫度影響對蝦白斑綜合癥病毒增殖機制的研究[J].應用海洋學學報,2013,32(1):61-66.
[7] DU H H,DAI W,HAN X Y,et al.Effect of low water temperature on viral replication of white spot syndrome virus in Procambarus clarkii[J].Aquaculture,2008,277(3-4):149-151.
[8] MONTGOMERY-BROCK D,TACON A G J,POULOS B,et al.Reduced replication of infectious hypodermal and hematopoietic necrosis virus (IHHNV) in Litopenaeus vannamei held in warm water[J].Aquaculture,2007,265(1-4):41-48.
[9] 柴超.養殖凡納濱對蝦傳染性皮下及造血組織壞死病毒(IHHNV)的感染率及其基因組學研究[D].上海:上海海洋大學,2014.
[10] BRAY W A,周光正.鹽度對萬氏對蝦生長和存活的影響及IHHN病毒和鹽度相互關系的觀察[J].國外水產,1995,79(1):16-20.
[11] 張輝.氨氮脅迫誘導熱休克因子1促進對蝦白斑綜合征病毒感染[D].濟南:山東大學,2023.
[12] 郝晨光.三種環境因子對克氏原螯蝦體內WSSV增殖的影響[D].秦皇島:河北農業大學,2020.
[13] 向赟.環境因子和弧菌對白斑綜合癥病毒(WSSV)在凡納濱對蝦體內增殖的影響[D].湛江:廣東海洋大學,2014.
[14] 孫國銘,湯建華,仲霞銘.氨氮和亞硝酸氮對南美白對蝦的毒性研究[J].水產養殖,2002(1):22-24.Effects of several environmental factors on IHHNV
proliferation in Litopenaeus Vannamei
ZHANG Li MA Wenting YAO Hongwang LI Na1, BAO Haiyan
(1.Tianjin Animal Disease Prevention and Control Center,Tianjin 300402,China;
2. BeiliZigu Village, Huangzhuang Town, Baodi District, Tianjin 301800,China)
Abstract:In order to elucidate the key factors that affect the proliferation of IHHNV during the cultivation of Litopenaeus vannamei,the effects of environmental factors such as temperature, salinity, ammonia nitrogen and nitrite nitrogen on the proliferation of IHHNV in Litopenaeus vannamei were investigated under laboratory conditions.The experimental results showed that under the same conditions, there were significant differences in the number of IHHNV viruses in the body of Litopenaeus vannamei at water temperatures of 25 ℃ and 30 ℃. And the maximum number of viruses was in the temperature group of 30 ℃; For the salinity gradient experiments of 2.5, 10.0, and 20.0, there were significant differences between the IHHNV proliferation groups, and the proliferation rate was positively correlated with salinity; Under three concentration gradients of 0.05 mg/L, 3.00 mg/L, and 7.00 mg/L of ammonia nitrogen, there was no linear relationship between the changes in virus proliferation quantity of IHHNV in Litopenaeus vannamei. However, the number of virus in the body of Litopenaeus vannamei with an ammonia nitrogen concentration of 0.05 mg/L was significantly lower than that of the 3.00 mg/L and 7.00 mg/L concentration groups; At three concentration gradients of 0.05 mg/L, 5.00 mg/L, and 10.00 mg/L for nitrite nitrogen, there was no significant difference in the number of virus proliferation in Litopenaeus vannamei between groups.
Key words:Litopenaeus vannamei;environmental factor;IHHNV;proliferation
(收稿日期:2023-09-08)

