化學平衡常數在高考試題中的延伸考查
張小波
(張掖市第二中學,甘肅 張掖 734000)
化學平衡常數是化學反應基本原理中的核心內容,是高考熱點知識.近幾年高考化學試題中關于化學平衡常數的考查有所創新,對其進行了延伸,主要涉及壓強平衡常數、標準平衡常數(相對壓力平衡常數)、物質的量分數平衡常數以及平衡常數與其它常數相關聯等.突顯了高考試題源于課本、高于課本的特點,真正體現了變化觀念和平衡思想,證據推理與模型認知的化學核心素養[1].
1 壓強平衡常數

例1(2022年1月浙江卷-29節選)(3)一氧化碳變換反應:

ΔH=-41 kJ·mol-1
①一定溫度下,反應后測得各組分的平衡壓強:p(CO)=0.25 MPa、p(H2O)=0.25 MPa、p(CO2)=0.75 MPa和p(H2)=0.75 MPa,則反應的平衡常數K的數值為____.
②維持與題①相同的溫度和總壓,提高水蒸氣的比例,使CO的平衡轉化率提高到90%,則原料氣中水蒸氣和CO的物質的量之比為____.
答案:(3)①9.0 ②1.8∶1
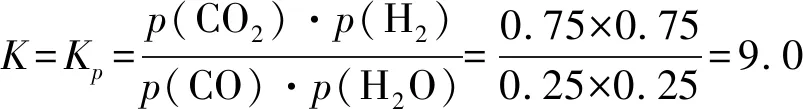
②假設原料氣中水蒸氣為xmol,CO為1 mol,當CO的平衡轉化率為90%時,消耗的CO和H2O的物質的量為0.9 mol,同時生成的CO2和H2的物質的量為0.9 mol,那么,平衡時CO、CO2、H2和H2O的物質的量分別為0.1 mol、0.9 mol、0.9 mol和(x-0.9)mol.此時,假設反應容器的體積為VL,則可逆反應的平衡常數表達式如下:
解得x=1.8,故水蒸氣與CO物質量之比為1.8∶1.
總結這個反應比較特殊,即反應前后氣體分子數不變,所以Kc=Kp.這個知識點在高考備考中學生一定要知曉,否則在考場上學生不僅會不知所措、無法解答,還可能打亂學生思維,影響其他題目的解答.第二問題目告訴要維持與題①相同的溫度和總壓,說明可逆反應達到新平衡后Kp不變.只要巧妙假設出原料其中水蒸氣和一氧化碳的物質的量,然后根據CO的平衡轉化率為90%,就可以根據K的定義式直接求解.
例2(2022年全國甲卷-28節選)(1)



(2)在1.0×105Pa,將TiO2、C、Cl2以物質的量比1∶2.2∶2進行反應.體系中氣體平衡組成比例(物質的量分數)隨溫度變化的理論計算結果如圖1所示[3].
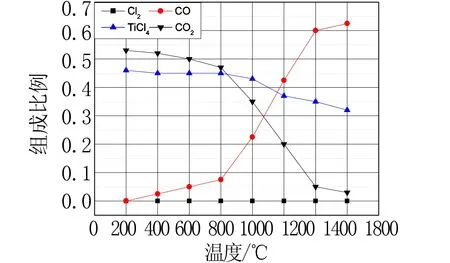
圖1 物質的量分數隨溫度變化圖

答案:(1)① -223 1.2×1014
(2)①7.2×105


總結第一問已知兩個反應的ΔH和Kp,根據蓋斯定律求出第三個反應的ΔH,再按照多重平衡規則就可以求出其Kp.對于多重平衡,處理的規則一般是:若總反應可以看成是幾個分步反應化學方程式經過相加(減)得到的,那么,總反應的平衡常數就等于各分步反應的平衡常數之乘積(商).
2 標準平衡常數(相對壓力平衡常數)

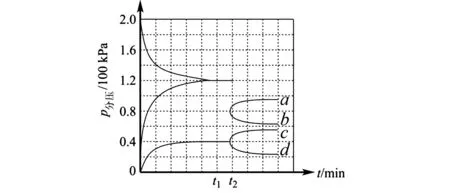
圖2 各物質的分壓隨時間的變化曲線
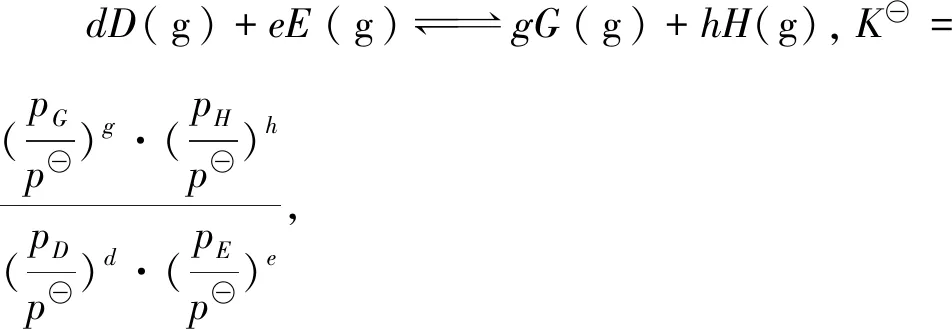
答案:0.48
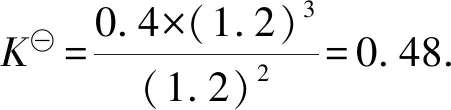
總結標準平衡常數和壓強平衡常數相比較,就是用各氣體分壓和標準壓強的商代替分壓.學生容易理解,難度不大.2021年廣東卷第19題中出現了相對壓力平衡常數,其數學表達式單從形式上來看就是在濃度平衡常數表達式的基礎上,利用平衡時各組分(氣體)的相對分壓代替平衡濃度就可以了.而平衡時氣體的相對分壓等于其分壓(單位為kPa)除以p0(p0=100 kPa),可見,標準平衡常數和相對壓力平衡常數從形式上來看極其相似,只要稍加注意,學生就能實現順利過渡.
3 物質的量分數平衡常數
例4 (2021年山東卷-20節選)
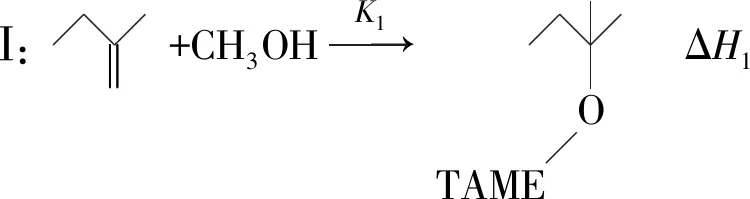
A
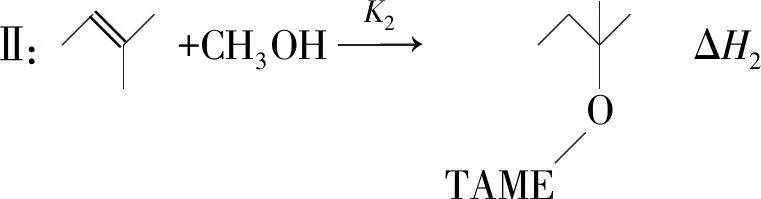
B
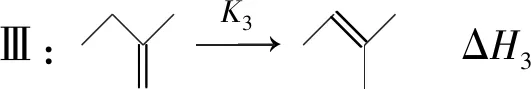
(2)向某反應容器中加入1.0 mol TAME,溫度為353 K時,測得TAME的平衡轉化率為α.已知Kx3=9.0,則平衡體系中B的物質的量為____mol,反應Ⅰ的平衡常數Kx1=____.同溫同壓下,再向該容器中注入惰性溶劑四氫呋喃稀釋,反應Ⅰ的化學平衡將____(填“正向移動”“逆向移動”或“不移動”);平衡時,A與CH3OH物質的量濃度之比c(A)∶c(CH3OH)=____.
(3)向盛有四氫呋喃的另一容器中加入一定量A、B和CH3OH.溫度為353 K,a、b物質的量濃度c隨反應時間t的變化如圖3所示.代表B的變化曲線為____(填“X”或“Y”);t=100 s時,反應Ⅲ的正反應速率v正____逆反應速率v逆(填“>”“<”或“=)[4].
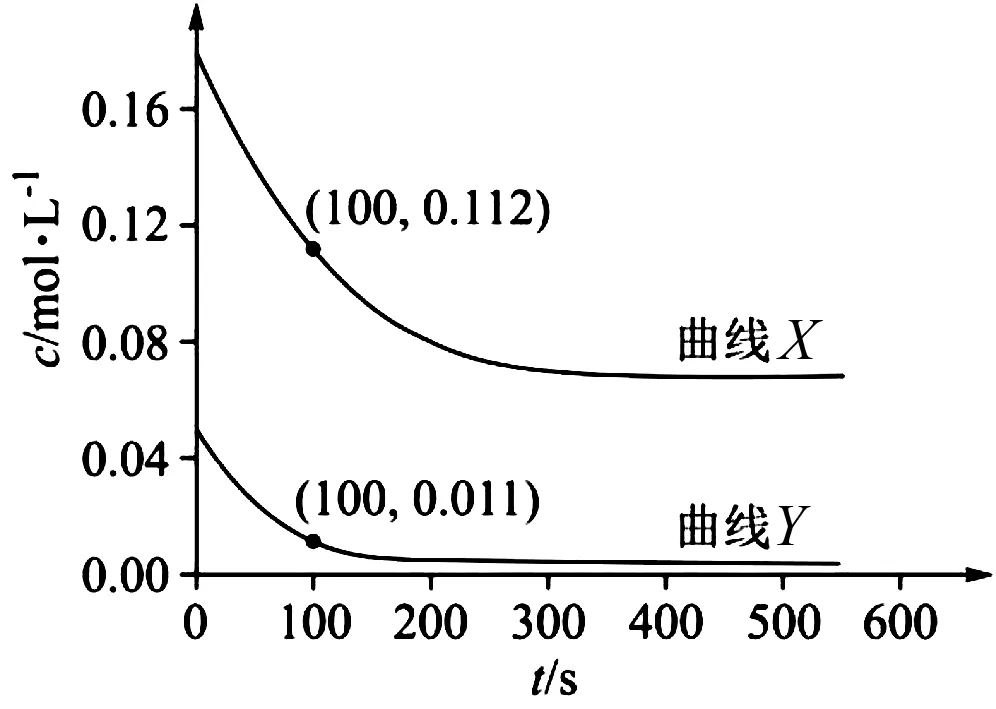
圖3 c與t變化關系
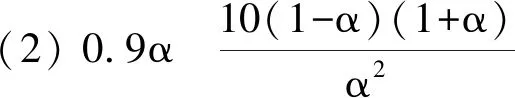
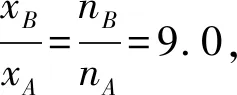
如果在同溫同壓下再向該容器中注入惰性溶劑四氫呋喃進行稀釋,根據平衡移動原理可知,化學平衡Ⅰ將向著分子數增大的方向(逆向)移動.達新平衡時,雖然TAME的轉化率增大了,但是該反應平衡常數不會改變,A與CH3OH物質的量濃度之比也不會改變,即c(A)∶c(CH3OH)=0.1α∶α=1∶10.
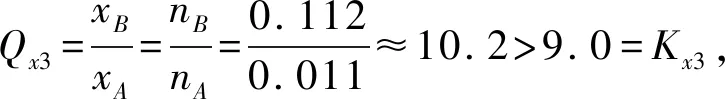
總結學生已經理解了物質的量濃度平衡常數和壓強平衡常數,現在很容易接受新事物——物質的量分數平衡常數.第二問是有關從逆向建立多重平衡的問題,增加了試題的難度,很好地考查了學生對化學平衡的概念、建立過程、特征、多重平衡的特點和規則的理解和掌握情況.要解答好本題,學生需要具備扎實的基本功和靈活的思維.就考查的方向和內容來說比較中規中矩:由反應Ⅲ的平衡常數計算出平衡體系中B的物質的量,再算出反應Ⅰ的平衡常數,即平衡常數與組分物質的量的互算,最后還考查了利用Qx與Kx的相對大小關系來判斷化學反應進行的方向.
4 化學平衡常數與其它常數相關聯
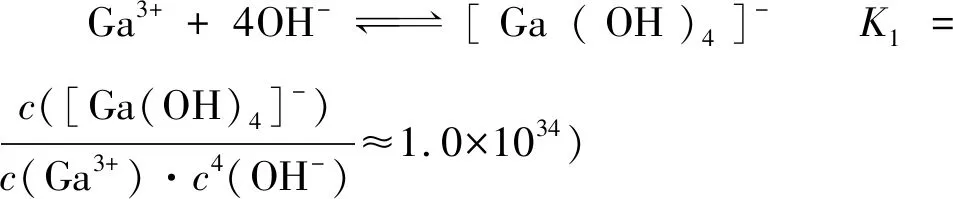
答案: 2.0×10-6
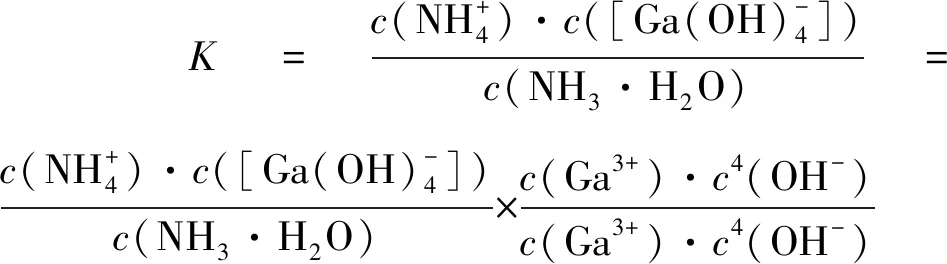
總結此題是一個典型的多重平衡問題,只要心細,找出它們之間的關系,按照多重平衡規則就可以解決,這樣的題目經常訓練,難度不大.可見平衡常數之間是可以相關聯的.
5 化學平衡常數與化學反應速率相關聯

答案:k1/600

總結本題將化學平衡常數與可逆反應的正逆化學反應速率聯系了起來,聯系二者的橋梁和紐帶就是物質的量濃度.題目能很好地考查學生知識遷移應用的能力、學生思維的靈活性、綜合分析和解決問題的能力以及數學推理的能力等等.尤其是最后一步,至關重要.當可逆反應達到平衡狀態時,對同種物質而言,正逆反應速率相等;對不同物質而言,正逆反應速率之比等于化學計量數之比.所以,當這個特殊(化學計量數均為1)的可逆反應達到平衡狀態時,可以得出這樣的結論:v(H2CO3)=v(CO2).
本題表面上看起來很簡單,但對學生而言,要全部想清楚,順利推導出來,還是有一定的挑戰性.這就要求教師在平時教學的過程中要有耐心,循序善誘,最終水到渠成.
綜上所述,高考試題中平衡常數的面孔雖然發生了一些變化,但它的考查方向幾乎沒變:根據平衡常數可以判斷可逆反應進行的程度(若K≤10-5,反應很難進行;若K≥105,反應進行得較完全;若10-5

