柱后衍生離子色譜法測定土壤和沉積物中的六價鉻
王 婷,朱紅霞,周敬峰,姜 麗,金淑聰,胡佳欣
1.寶雞市環境監測中心站,陜西 寶雞 721000
2.中國環境監測總站,國家環境保護環境監測質量控制重點實驗室,北京 100012
3.廣西壯族自治區海洋環境監測中心站,廣西 北海 536001
4.福建省生態環境監測中心,福建 福州 350000
5.昌吉州回族自治州環境監測站,新疆 昌吉 831100
鉻(Cr)在自然界中廣泛存在,主要以三價鉻和六價鉻存在[1]。 少量三價鉻對人體有益[2],而六價鉻毒性約為三價鉻的100 倍[3],被認為是主要的人類致癌因素之一[4],可通過皮膚、胃腸道和呼吸系統被人體吸收,引起胃道及肝、腎功能損害等[5]。 六價鉻在制革、紡織品生產、印染以及鍍鉻等行業有廣泛應用,伴生的含鉻廢水若處理不當很容易滲入土壤[6]。 土壤對六價鉻的吸附能力差,極易擴散遷移[7],因此,準確測定土壤中六價鉻對于控制污染具有重要作用。
《土壤環境質量-建設用地土壤污染風險管控標準》(GB 36600—2018)將六價鉻列為建設用地污染風險篩選和管制項目,但推薦的方法僅有堿溶液提取-火焰原子吸收分光光度法[8-9]。 現有對土壤中六價鉻測定的報道主要基于特定技術提取,分光光度法[10-11]、火焰原子吸收法[12-14]和電感耦合等離子體發射光譜法[15-17]進行測定。 由于土壤基質復雜,相應提取液中干擾因素較多,應用分光光度法分析六價鉻,土壤樣品中的色度、還原性物質等易對測定結果產生干擾;應用原子吸收或電感耦合等離子體發射光譜等總鉻的檢測方法,則必須保證前處理提取出的目標物為六價鉻,但目前對于提取液中鉻形態的研究較少,提取液是否只有六價鉻尚不明確,同時原子吸收測定時存在鹽基沉積的問題[18]。 離子色譜法則彌補了這一缺陷[19],對于六價鉻測定具有分離效果好、檢出限低、進樣量少等特點。 應用離子色譜法測定土壤中六價鉻的研究相對較少,張濤等[2]選用超聲輔助提取/離子色譜法測定了鉻污染土壤中的六價鉻,選用的檢測器為電導檢測器,相比紫外檢測器測定六價鉻靈敏度較低,且超聲提取相比加熱回流提取控溫效果較差。
本研究選用氫氧化鈉和碳酸鈉強堿混合溶液作為提取劑,應用恒溫攪拌回流提取,離子色譜分離,柱后衍生紫外可見檢測器測定土壤六價鉻,方法操作簡便、靈敏度高、特異性強,是土壤中六價鉻測定方法的有力補充。
1 實驗部分
1.1 儀器、試劑與材料
1.1.1 試劑
氫氧化鈉(優級純,日本);碳酸鈉(優級純,德國);氯化鉀(純度≥99.8%,國藥集團化學試劑有限公司);硝酸(55%,德國);氨水(25%,優級純,國藥集團化學試劑有限公司);碳酸氫鈉(分析純,國藥集團化學試劑有限公司);濃硫酸(98%,優級純,國藥集團化學試劑有限公司);甲醇(色譜純,德國);1,5-二苯基碳酰二肼(優級純,國藥集團化學試劑有限公司);六價鉻標準儲備液100 mg/L(生態環境部標準樣品研究所);土壤六價鉻質控樣(ERA D113-921,美國)。
1.1.2 儀器和設備
柱后衍生離子色譜儀(紫外檢測器,ELSpe-2型,廣州譜臨晟科技有限公司);加熱回流裝置(德潤環保科技有限公司);水浴鍋(BT47 型,yamato);超聲波清洗器(KQ2200DE 型,昆山市超聲儀器有限公司); 臺式高速冷凍離心機(H2050R 型,長沙湘儀離心機儀器有限公司);電子天平(精確至0.1 mg,瑞士梅特勒公司);0.22 μm 親水PTFE 針式濾器(上海安譜實驗科技股份有限公司)。
1.1.3 條件實驗用土壤樣品
為提升方法普適性,選用7 種不同類型土壤或沉積物樣品進行條件實驗,編號為1 ~7 號,即:1 號GBW 07405(GSS-5)黃紅壤,2 號GBW 07407(GSS-7)磚紅壤,3 號GBW 07447(GSS-18)鹽堿土, 4 號 GBW 07454 ( GSS-25 ) 黃土, 5 號GBW 07455(GSS-26)淮河沉積物,6 號承德市某地黃棕土,7 號承德市某地棕土。
1.2 實驗方法
1.2.1 色譜條件
色譜柱為Prin-cen GF2108 六價鉻快速分析柱4.1 mm×50 mm,5 μm;柱溫為室溫;流動相為0.1 mol/L HNO3+0.133 mol/L NH3·H2O,流速為1.2 m L/min;柱后衍生試劑為0.4 g 二苯碳酰二肼溶于50 m L 甲醇+50 m L 2 mol/L 硫酸定容到500 m L,流速為0.7 m L/m in;進樣量為50 μL;檢測器為紫外可見檢測器;檢測波長為540 nm。
1.2.2 樣品前處理
篩分:參照《土壤環境監測技術規范》(HJ/T 166—2004),將土樣風干后過孔徑為0.150 mm 篩。
提取:稱取2.5 g(精確至0.001 g)篩分后的試樣于玻璃樣品杯中,放入磁子,加入25.0 m L 提取劑(0.5 mol/L NaOH +0.28 mol/L Na2CO3),在樣品杯外壁標記液面刻線,磁攪拌條件下120 ℃回流1 h,自然冷卻后備用。 若冷卻后提取液液面低于刻線,可用純水補充至刻線后混勻待測。
凈化:將樣品杯中試樣全量轉入50 m L 塑料離心管,5 000 r/min 離心5 min。 將上清液用0.22 μm 的微孔濾膜過濾,棄去1 m L 初濾液,取適量稀釋后上機待測。
2 結果與討論
2.1 提取劑種類的選擇
根據現有研究,選擇4 種提取劑進行比對實驗:第1 種,常用的氫氧化鈉-碳酸鈉溶液(0.5 mol/L NaOH +0.28 mol/L Na2CO3);第2 種,柱后衍生離子色譜法測定環境空氣顆粒物中六價鉻時使用碳酸氫鈉溶液(20 mmol/L NaHCO3)[20];第3種,蔡曄等綜合多種提取劑優選后的氫氧化鈉-氯化鉀溶液(0.5 mol/L NaOH +0.5 mol/L KCl)[21];第4 種,與實驗室離子色譜測定六價鉻條件一致的淋洗液(0.1 mol/L HNO3+0.133 mol/L NH3·H2O)。選用1.1.3 節中列出的7 種不同風干土壤或沉積物,向其中滴加適量六價鉻標準溶液,待自然風干后制成7 種加標樣品。 由于使用的實際樣品為液體加標的土壤或沉積物樣品,且風干后立即進行提取實驗,其中的Cr(Ⅵ)與土壤或沉積物的結合并不牢固,故實驗初期選擇常用且操作便捷的超聲提取,在不控溫條件下使用4 種提取劑將7 種加標樣品超聲提取1 h,樣品信息及加標回收率見表1。
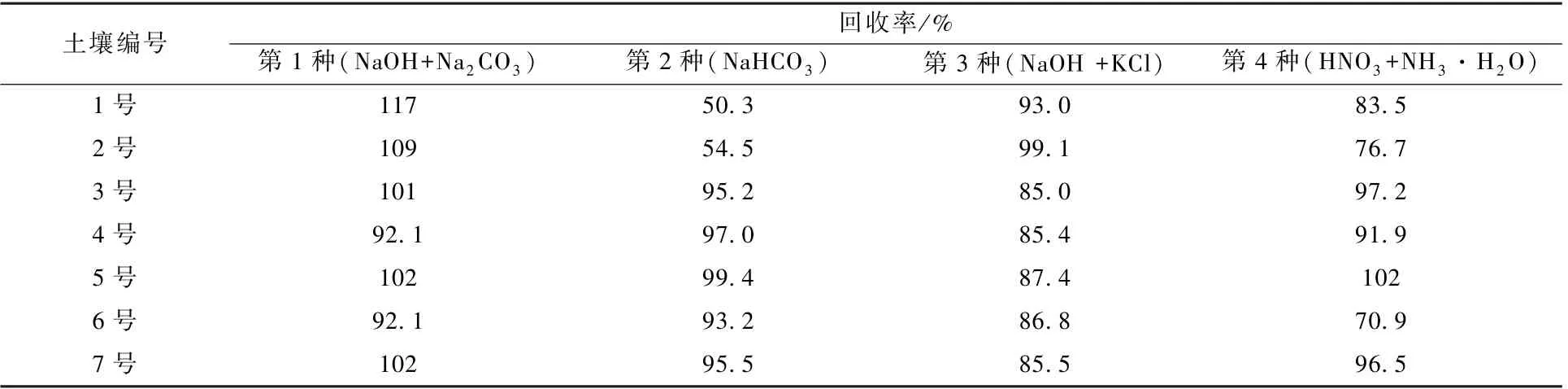
表1 不同提取劑回收率Table 1 Recovery of different extractants
由表1 可以看出:第2 種提取劑測定1 號、2號2 種土壤中六價鉻時,回收率低至50%;第4 種提取劑測定2 號、6 號2 種土壤時,六價鉻回收率低至70%。 第1 種(NaCO3+NaOH) 和第3 種(KCl+NaOH)2 種提取劑提取的7 種土壤的加標回收率為85%~120%,考慮到高濃度的KCl 易引起離子色譜柱飽和,故優選碳酸鈉和氫氧化鈉混合溶液作為提取劑。
2.2 提取方式的選擇
常用可以滿足混勻加熱功能的提取方式包括超聲提取、水浴振蕩提取、恒溫磁力攪拌回流提取。 參照《土壤和沉積物 六價鉻的測定 堿溶液提取-火焰原子吸收分光光度法》(HJ 1082—2019)中對土壤六價鉻的前處理條件,提取過程中至少需要將提取液加熱至90 ℃,然而超聲提取時水溫波動較大,恒溫的條件不易控制,且部分儀器水微沸時極易導致超聲斷開,故溫度和超聲的限制導致附著在土壤和沉積物晶格內的六價鉻不易提取。 故僅比較了水浴振蕩提取和恒溫磁力攪拌回流裝置對非加標樣品的提取效果,在相同溫度(90 ℃)和時間(60 m in)內提取并測定了7 種土壤中六價鉻的本底含量,結果如圖1 所示。
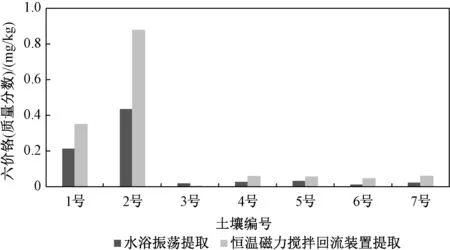
圖1 2 種提取方式提取7 種土壤中六價鉻Fig.1 Extraction of hexavalent chromium from 7 kinds of soil by 2 extraction methods
由圖1 可以看出,恒溫磁力攪拌回流提取出的六價鉻含量明顯高于水浴振蕩提取,可能是實驗室內的水浴振蕩器對提取樣的振動頻率低于磁力攪拌,土壤中六價鉻不能完全溶解在提取液中,故最終選用恒溫磁力攪拌回流提取。
2.3 提取時間的選擇
對2.1 節中制備的7 種加標樣品進行實驗,討論提取時間。 參照現行方法標準或文獻在10 ~60 min 內改變提取時間,比較測定回收率,結果見圖2。
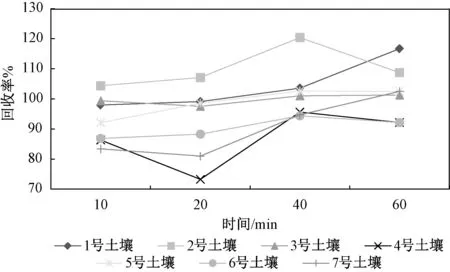
圖2 提取時間對不同土壤加標回收率的影響Fig.2 Effect of extraction tim e on recovery rate of different soils
由圖2 可以看出,提取時間超過40 min 時,7種土壤中添加六價鉻標準溶液后的回收率均高于90%,考慮到土壤基質復雜,故仍參照HJ 1082—2019,加熱回流提取60 m in。
2.4 提取溫度的選擇
應用上述7 種不同土壤和沉積物樣品進行提取溫度的討論。 改變加熱回流裝置的底部加熱溫度,分別在常溫(約25 ℃)、60 ℃、95 ℃、120 ℃、190 ℃條件下,比較各溫度下樣品本底中提取出的六價鉻含量,結果見圖3。 由圖3 可以看出,提取溫度對六價鉻的提取效率影響較大,隨溫度升高,提取量逐漸增加。 在95 ℃時,實驗所選的大部分樣品中六價鉻的測定值趨于穩定,但仍有2種樣品的六價鉻提取量未達到最大值。 在加熱溫度超過120 ℃后7 種樣品均達到了最大提取量,故最終選取的提取溫度為120 ℃。
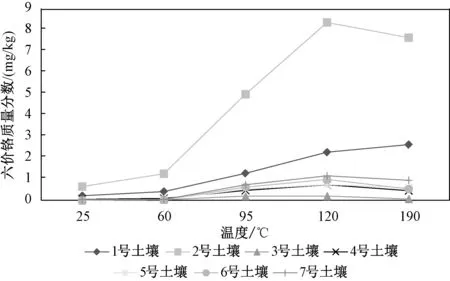
圖3 不同的提取溫度下不同土壤中六價鉻的提取量Fig.3 The extraction amount of hexavalent chromium in different soil under different extraction temperature
2.5 提取劑用量的選擇
通過改變提取劑體積和土壤質量比的方式選擇最佳的提取劑用量,如圖4 所示。 由圖4 可以看出,固定土壤稱樣量和固定提取劑體積2 種方式得到的提取量較為一致,且提取劑體積和稱樣量的比大于10 ∶1 后,提取的土壤中的六價鉻濃度趨于穩定,故最終選擇提取劑體積和稱樣量比為 10 ∶1,根據本實驗儀器設備規格,最終確定稱取 2.5 g 土壤用25 m L 提取劑提取。
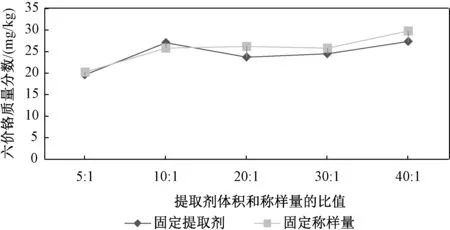
圖4 提取劑體積和土壤的質量比對六價鉻提取量的影響Fig.4 Effect of extractant volume and soil mass ratio on the extraction amount of hexavalent chromium
2.6 提取液的保存
選用3 號和6 號2 種土壤的提取液進行保存時間的影響實驗,4 ℃冷藏14 d 內測定,結果如表2 所示。 從表2 可以看出,2 種土壤提取液冷藏時,14 d 內六價鉻濃度變化不大,說明提取后可以在14 d 內完成測定。
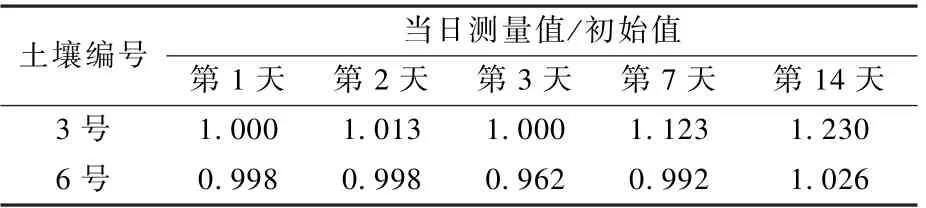
表2 提取劑保存時間對六價鉻濃度的影響Table 2 Effect of storage time of extractant on concentration of hexavalent chromium
2.7 線性方程和檢出限
用提取液配制0.0、2.0、5.0、10、30、50 μg/L的六價鉻標準系列,應用離子色譜進行測定,標準曲線方程為y=60 852.736 8x+341.869 4,相關系數r=0.999 9,線性關系良好。
按照《環境監測分析方法標準制訂技術導則》(HJ 168—2020)中空白實驗未檢出目標物的檢出限測定要求,向25 m L 提取液中添加20 μL的1 mg/L 的標準溶液,配制成0.8 μg/L 的混合溶液,按照實際樣品的測定步驟進行加熱回流提取和測定,重復測定7 次,結果分別為0.762、0.780、0.815、0.754、0.907、0.880、0.849 μg/L,均值為0.821 μg/L,標準偏差為0.059 7 μg/L,該方法提取液中六價鉻的檢出限為0.2 μg/L。 以2.5 g 土壤稱樣量和25 m L 提取液體積計算,土壤中六價鉻的方法檢出限為0.002 mg/kg,遠低于《土壤環境質量 建設用地土壤污染風險管控標準》(GB 36600—2018)中土壤六價鉻的第一類用地篩選值(3.0 mg/kg)的限值要求,同時也低于李恒[17]用堿溶液提取-ICP 法測定土壤中的六價鉻的方法檢出限0.08 mg/kg;煉曉璐等[14]用堿消解-火焰原子吸收光譜法測定土壤中六價鉻的方法檢出限0.20 mg/kg;唐愛玲[18]用FAAS 和ICPMS 法測定污染土壤中六價鉻,FAAS 法(火焰原子吸收分光光度法)測得的污染土壤中六價鉻的方法檢出限為0.44 mg/kg,ICP-MS 測得的檢出限為0.003 mg/kg。 說明本方法適用于土壤中低含量六價鉻的測定。
2.8 實際樣品的測定
選擇河北承德某地2 種實際土壤樣品(編號為6 和7 的土壤)及編號為ERAD113-921[標準值為(25.5±1.5 )mg/kg]的六價鉻標準土壤樣品,按上述優化好的提取和離子色譜條件進行實際樣品以及加標樣品實驗,平行測定6 次,具體結果如表3 所示,相對標準偏差為1.3%~3.7%,實際樣品的回收率為93.6%~100%,標準樣品的測定均值在給定范圍內,對應離子色譜圖如圖5 和圖6 所示,本方法適用于土壤中六價鉻的測定。
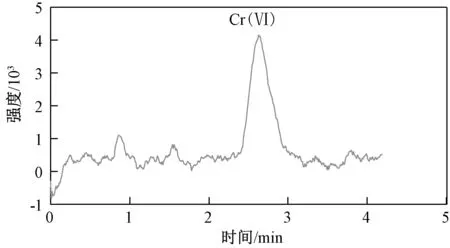
圖5 樣品6 的離子色譜圖Fig.5 Ion chromatogram of sample 6
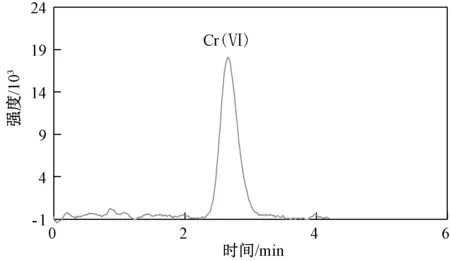
圖6 樣品7 的離子色譜圖Fig.6 Ion chromatogram of sample 7
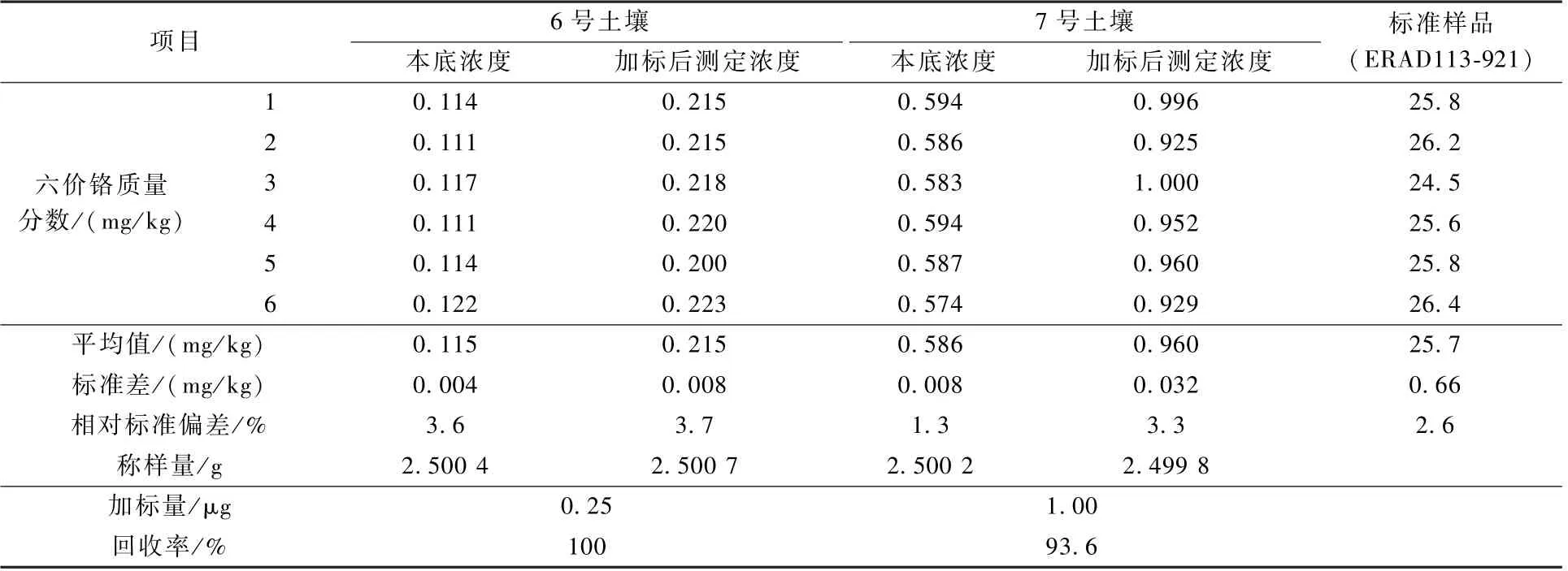
表3 實際樣品和質控樣測定結果Table 3 Test results of actual samples and quality control samples
3 結論
本文建立的加熱回流提取、柱后衍生離子色譜法用于土壤中六價鉻測定,檢出限低至0.002 mg/kg,提取液損耗小,運行成本低,特異性強,準確度、精密度良好。 相比目前常用的原子吸收等土壤中鉻(Ⅵ)測定方法,柱后衍生離子色譜法對于低含量土壤樣品的測定更具優勢,可滿足土壤中低含量鉻(Ⅵ)的測定需求。

