FBXW7/MCM7信號軸介導(dǎo)肝癌細胞增殖的研究*
李英, 王興, 李永寧, 劉鵬, 劉松柏, 潘耀振
(貴州醫(yī)科大學(xué)附屬腫瘤醫(yī)院 肝膽外科, 貴州 貴陽 550000)
肝細胞肝癌(hepatocellular carcinoma, HCC)是消化系統(tǒng)常見的惡性腫瘤之一,每年約超過 905 000例新發(fā)病例和830 000例死亡病例,是全球第六位常見的惡性腫瘤和第三大癌癥相關(guān)的死亡原因[1]。隨著肝移植、放化療、靶向免疫等治療方法的發(fā)展,肝癌的臨床預(yù)后有所改善[2-4]。但由于早期檢測手段缺乏、病程進展迅速、腫瘤細胞惡性程度高及增殖能力強,多數(shù)肝癌發(fā)現(xiàn)時已處于中晚期階段,喪失根治性手術(shù)時機,且傳統(tǒng)放化療效果較差[5],故探討肝癌發(fā)生發(fā)展的分子機制對肝癌的臨床診治具有重要意義。含F(xiàn)-box和WD重復(fù)結(jié)構(gòu)域蛋白7(F-box and WD repeat domain-containing protein 7,FBXW7)作為腫瘤抑制因子已在多種類型腫瘤的研究中被報道,FBXW7可抑制腫瘤細胞的增殖與轉(zhuǎn)移,與患者的臨床預(yù)后呈正相關(guān)[6]。本課題組前期研究表明,FBXW7在肝癌組織中的表達高于癌旁非腫瘤組織,過表達FBXW7后顯著抑制了肝癌細胞的遷移侵襲能力[7]。結(jié)合近期實驗結(jié)果及預(yù)測分析發(fā)現(xiàn),微小染色體維持蛋白-7 (minichromosome maintenance complex component 7, MCM7)可能作為FBXW7的潛在靶點,在肝癌生物學(xué)功能的調(diào)控中發(fā)揮重要作用。Qu等[8]研究也表明MCM7可促進肝癌細胞增殖并可作為肝癌不良預(yù)后的預(yù)測因子,但其具體的調(diào)控機制仍鮮有研究。本研究將主要探討肝癌細胞中FBXW7對MCM7的調(diào)控作用及對肝癌細胞增殖的影響。
1 材料與方法
1.1 實驗材料
1.1.1細胞株 人肝癌細胞系MHCC-97H購自上海生科院細胞資源中心。
1.1.2主要試劑 胎牛血清、DMEM培養(yǎng)基及胰蛋白酶購自Gibco公司;青、鏈霉素雙抗購自Hyclone公司;FBXW7抗體購自Abcam公司;MCM7抗體購自武漢三鷹公司;GAPDH抗體、羊抗鼠及羊抗兔二抗購自博士德公司;Alexa Fluor 488和CoraLite594熒光二抗購自賽默飛公司;Protein A+G Agarose Beads購自碧云天公司;CCK-8試劑盒為日本同仁產(chǎn)品;siRNA轉(zhuǎn)染試劑盒購自銳博生物公司;FBXW7及MCM7過表達慢病毒質(zhì)粒由吉凱基因構(gòu)建及包裝。
1.2 研究方法
1.2.1細胞培養(yǎng)與分組 MHCC-97H細胞用含10%胎牛血清和1%青、鏈霉素雙抗的DMEM培養(yǎng)基,于37 ℃、5%CO2的恒溫培養(yǎng)箱中常規(guī)培養(yǎng)。首先,通過感染過表達慢病毒質(zhì)粒及對照空載體病毒將細胞分為4組:對照空載體組(Vector組)、FBXW7過表達組(FBXW7組)、對照空載體與MCM7過表達病毒質(zhì)粒共感染組(Vector+MCM7組)、FBXW7過表達病毒質(zhì)粒與MCM7過表達病毒質(zhì)粒共感染組(FBXW7+MCM7組)。其次,siRNA轉(zhuǎn)染MHCC-97H細胞下調(diào)FBXW7和(或)MCM7的表達,將細胞分為4組:空載體組(NC組)、FBXW7下調(diào)組(siFBXW7組)、空載體與MCM7下調(diào)序列共轉(zhuǎn)染組(NC+siMCM7組)、FBXW7與MCM7表達同時下調(diào)組(siFBXW7+siMCM7組)。
1.2.2FBXW7與MCM7蛋白互作關(guān)系檢測 采用免疫共沉淀(co-immunoprecipitation,Co-IP)實驗,細胞中加入NP40裂解液(含10 μL蛋白酶抑制劑500 μL、磷酸酶抑制劑10 μL、PMSF 5 μL )提取總蛋白。蛋白提取物加入 Protein A+G Agarose Beads 20 μL于4 ℃搖床孵育2 h進行預(yù)純化。將純化后的提取物分為3份,分別為IgG純化抗體孵育組(IP-IgG組)、FBXW7抗體孵育組(IP-FBXW7組)及對照組(Input組),置于4 ℃搖床孵育過夜。IgG組和FBXW7組各自加入Protein A+G Agarose Beads 40 μL 于4 ℃孵育4 h,離心收集沉淀,加入2×蛋白上樣緩沖液,100 ℃變性5 min。采用SDS-PAGE凝膠電泳對結(jié)合蛋白進行檢測。
1.2.3FBXW7與MCM7共定位分析 采用免疫熒光(immunofluorescence staining, IF)共定位實驗,收集細胞進行細胞爬片,待貼壁后PBS洗3遍,4%多聚甲醛固定30 min,破膜劑室溫破膜20 min,5%牛血清白蛋白封閉30 min,加入FBXW7和MCM7一抗溶液于4 ℃孵育過夜。PBST洗3遍后加入Alexa Fluor 488和CoraLite594熒光二抗,室溫避光孵育1 h,滴加DAPI染料室溫避光孵育5 min,洗去多余的染料后滴加封片劑封片,熒光顯微鏡下觀察FBXW7和MCM7在肝癌細胞中表達分布情況。
1.2.4MCM7蛋白表達檢測 通過Western blot實驗分析FBXW7對MCM7表達的影響。采用RIPA裂解液提取細胞總蛋白,BCA法測定蛋白濃度。行10% SDS-PAGE凝膠電泳分離蛋白,電泳結(jié)束將蛋白條帶濕轉(zhuǎn)至PVDF膜上,用5%脫脂牛奶室溫封閉2 h。封閉后分別將目的條帶放入對應(yīng)的一抗溶液中4 ℃搖床孵育過夜。TBST洗去膜表面一抗后,放入二抗溶液中室溫孵育1 h。采用ECL法對條帶進行顯影,以GAPDH作為內(nèi)參計算目的蛋白的相對表達量。
1.2.5CCK-8細胞活性檢測 細胞消化計數(shù),96孔板內(nèi)每孔接種4 000個細胞,每組設(shè)5個復(fù)孔。分別于細胞貼壁后的24 h、48 h及72 h檢測各組細胞的吸光度值。檢測時每孔加入110 μL經(jīng)無血清培養(yǎng)基稀釋的CCK-8液(無血清培養(yǎng)基∶CCK-8液=10∶1),37 ℃溫箱孵育2 h后在酶標(biāo)儀下檢測波長450 nm處的吸光度值,觀察各組細胞增殖活性的變化。
1.2.6EdU細胞增殖檢測 按操作說明將細胞接種于96 孔板中,待細胞貼壁后加入EdU試劑(50 μmol/L)孵化2 h,4%多聚甲醛固定30 min,再加入Apollo Dye Solution染色30 min,細胞核用DAPI染色5 min。于熒光顯微鏡下觀察并采集圖片,計算EdU陽性細胞百分比。
1.2.7細胞集落形成數(shù)檢測 采用平板克隆實驗,細胞消化計數(shù),按2×103個/孔接種于6孔板中,補加培養(yǎng)基至2 mL。使細胞均勻的分布于孔板中,放于細胞培養(yǎng)箱常規(guī)培養(yǎng),定期觀察細胞集落形成情況。培養(yǎng)10~14 d后,4%多聚甲醛固定30 min,1%結(jié)晶紫染色30 min,PBS清洗后烘干拍照,統(tǒng)計細胞集落形成數(shù)量。
1.3 統(tǒng)計學(xué)分析
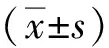
2 結(jié)果
2.1 FBXW7與MCM7在蛋白水平存在結(jié)合關(guān)系
結(jié)果顯示,用FBXW7抗體特異性免疫沉淀FBXW7蛋白時,可同時檢測到MCM7蛋白的表達(圖1A);FBXW7與MCM7在細胞中的表達主要共定位在細胞核(圖1B)。上述結(jié)果表明FBXW7與MCM7之間存在相互作用的可能。

注:A為Co-IP實驗結(jié)果;B為IF共定位結(jié)果 (400×)
2.2 過表達FBXW7對肝癌細胞中MCM7蛋白表達的影響
與Vector組比較,過表達FBXW7后,FBXW7組細胞中MCM7的表達水平明顯降低(P<0.001);與Vector+MCM7組相比,在MCM7表達水平上調(diào)的基礎(chǔ)上同時過表達FBXW7后,FBXW7+MCM7組細胞中MCM7蛋白的表達明顯降低(P=0.002);結(jié)果提示過表達FBXW7可抑制肝癌細胞中MCM7的蛋白表達水平。見圖2。

注:A為蛋白免疫印跡實驗結(jié)果;B為蛋白相對表達量統(tǒng)計圖;與Vector組比較, (1)P<0.01,(2) P<0.001;(3)與Vector+MCM7比較, P<0.01。
2.3 敲低FBXW7對肝癌細胞中MCM7蛋白表達的影響
與NC組相比,下調(diào)FBXW7后,siFBXW7組細胞中MCM7的表達水平顯著增加(P<0.001);與NC+siMCM7相比,抑制MCM7表達的同時下調(diào)FBXW7的表達后,siFBXW7+siMCM7組細胞中MCM7的表達水平明顯增加(P=0.004);結(jié)果提示在肝癌細胞中FBXW7可調(diào)控靶蛋白MCM7的表達。見圖3。

注:A為蛋白免疫印跡實驗結(jié)果;B為蛋白相對表達量統(tǒng)計圖;與NC組比較, (1)P<0.01,(2) P<0.001;(3)與NC+siMCM7比較,P<0.01。
2.4 過表達FBXW7調(diào)控MCM7對肝癌細胞增殖的影響
與Vector組相比,過表達FBXW7后,FBXW7組細胞增殖活性、EdU陽性細胞比例及集落形成數(shù)量均降低,差異具有統(tǒng)計學(xué)意義(P<0.05);Vector + MCM7組細胞的增殖活性、EdU陽性細胞比例及集落形成數(shù)量均增加,差異具有統(tǒng)計學(xué)意義(P<0.05);與Vector+MCM7組相比,FBXW7+MCM7組細胞的增殖能力降低,差異具有統(tǒng)計學(xué)意義(P<0.05)。見表1及圖4。

表1 CCK-8實驗比較各組細胞的增殖活性Tab.1 Analysis of the proliferation activity of cells in each group by CCK-8

注:A為EdU實驗結(jié)果;B為平板克隆實驗結(jié)果;與Vector組比較,(1)P<0.05, (2)P<0.01;與Vector+MCM7組比較,(3)P<0.05, (4)P<0.01。
2.5 敲低FBXW7調(diào)控MCM7對肝癌細胞增殖的影響
與NC組相比,siFBXW7組細胞的增殖活性、EdU陽性細胞比例及集落形成數(shù)量均增加(P<0.05);NC+siMCM7組細胞的增殖活性、EdU陽性細胞比例及集落形成數(shù)量均下降,差異均具有統(tǒng)計學(xué)意義(P<0.05)。與NC+siMCM7組對比,在抑制MCM7表達的同時干擾FBXW7的表達可增強siFBXW7+siMCM7組細胞的增殖能力,差異具有統(tǒng)計學(xué)意義(P<0.05)。上述結(jié)果提示FBXW7可調(diào)控MCM7的表達影響肝癌細胞的增殖能力。見表2、圖5。

表2 CCK-8實驗比較各組細胞的增殖活性Tab.2 Analysis of the proliferation activity of cells in each group by CCK-8

注:A為EdU實驗結(jié)果;B為平板克隆實驗結(jié)果;與NC組比較,(1)P<0.05, (2)P<0.01,(3)P<0.001;(4)與NC+siMCM7組比較, P<0.01。
3 討論
HCC是肝癌最主要的組織學(xué)亞型,雖然通過臨床和基礎(chǔ)上的不斷研究,發(fā)現(xiàn)了誘發(fā)HCC的多種風(fēng)險因素和遺傳變異[9-10],但由于治療方法有限,其預(yù)后仍然較差,術(shù)后5年生存率僅達18%左右[1]。HCC相關(guān)的疾病癥狀通常直到疾病中晚期才出現(xiàn),這也進一步限制了患者獲得有效治療的機會和降低了患者的存活率。因此,在表觀分子水平上理解HCC的發(fā)生及發(fā)展,或有望發(fā)掘出新型潛在的藥物靶點,為開發(fā)治療肝癌的新型療法提供理論基礎(chǔ)。
FBXW7作為Cullin-RING E3泛素連接酶中SCF復(fù)合體(SKP1-CUL1-F-box)的成員之一,主要參與底物蛋白的特異性識別和結(jié)合[11]。FBXW7可抑制一系列關(guān)鍵癌基因的表達發(fā)揮抑癌作用,如c-Myc、cyclinE1、mTOR和Notch1等[12-15]。眾多編碼F-box蛋白的相關(guān)基因在臨床腫瘤中的檢測結(jié)果表明,在人類腫瘤細胞中FBXW7是這些基因中突變最頻繁的[6]。在結(jié)直腸癌中FBXW7的突變率達10%,FBXW7突變或缺失的腫瘤組織中相關(guān)促癌基因的表達豐度增加、腫瘤細胞的惡性表型增強[16]。與之對應(yīng)的在其他多種類型的腫瘤中也發(fā)現(xiàn)FBXW7的表達降低或功能缺失[17-19],進一步說明了FBXW7在腫瘤發(fā)生發(fā)展中有著重要的抑癌作用。
本研究基于前期數(shù)據(jù)進一步分析FBXW7影響肝癌細胞增殖的分子機制,Co-IP實驗及IF共定位分析結(jié)果證實,MCM7是FBXW7的分子靶點。既往研究表明,MCM是DNA復(fù)制前復(fù)合物的重要組成部分,在DNA復(fù)制啟動過程和DNA損傷修復(fù)中發(fā)揮著重要作用[20]。MCM復(fù)合體由6個高度保守的MCM蛋白組成,即MCM2~MCM7,與腫瘤的發(fā)生密切相關(guān)[21-23]。研究發(fā)現(xiàn)MCM7在近半數(shù)以上的臨床肝癌樣本中表達升高,并與肝內(nèi)轉(zhuǎn)移、血管侵犯及化療耐藥顯著相關(guān)[24-25]。近期研究報道MCM7通過cyclin D1的信號轉(zhuǎn)導(dǎo)促進腫瘤進展,可作為肝癌患者預(yù)后不良的標(biāo)志物[8]。越來越多的證據(jù)表明MCM7在肝癌中起著重要作用,但MCM7發(fā)揮促癌功能和影響臨床預(yù)后的分子機制仍有待闡明。
本研究通過基因干擾技術(shù)及功能學(xué)實驗,初步探索了肝癌細胞中FBXW7對靶點MCM7 的表達及功能的調(diào)控作用。實驗結(jié)果表明過表達FBXW7可顯著抑制細胞中MCM7表達水平,發(fā)揮著抑制肝癌細胞增殖活性、EdU陽性細胞比例及集落形成能力的作用,而該抑制作用可被MCM7過表達而削減;敲低FBXW7后細胞中MCM7的表達明顯增加,功能上表現(xiàn)為促進細胞增殖活性、EdU陽性細胞比例及集落形成能力,而同時下調(diào)MCM7后細胞的增殖能力被明顯抑制。
綜上所述,FBXW7可抑制肝癌細胞增殖能力,其機制可能與靶向MCM7并抑制其蛋白水平表達有關(guān)。本研究首次發(fā)現(xiàn),FBXW7/MCM7信號軸對肝癌細胞增殖具有調(diào)控作用,為臨床上肝癌的分子診斷和靶向治療提供了新的思路和理論依據(jù)。

