早產兒視網膜病與母體因素及胰島素樣生長因子-1 的關系研究
盧煜明 張愛民 盧彥 鄭迅風 徐國明 李芳
隨著醫學技術的不斷進步,早產兒的生存率顯著提高,但與之相應的是早產兒視網膜病(ROP)的發病率也呈上升趨勢[1]。ROP 是一種與早產兒生長發育不成熟相關的疾病,其可能導致嚴重的視力障礙甚至失明。盡管ROP 的確切發病機制尚未完全明了,但研究表明母體因素和生長因子的異常可能與其發生相關。母體在胚胎發育過程中扮演著至關重要的角色,而母體因素如宮內感染、胎盤異常、母體妊娠期疾病(如高血壓或糖尿病)以及羊水異常等,可能直接影響早產兒的發育進程[2]。胰島素樣生長因子-1(IGF-1)是一種對胚胎和新生兒生長發育至關重要的激素。IGF-1 水平的異常可能與ROP 的發生有關,但其與ROP 之間的確切關系仍需深入研究[3]。鑒于以上背景,本研究旨在深入探討早產兒ROP 與母體因素以及IGF-1 水平之間的關系,探討IGF-1 在ROP 發病機制中的可能作用。
1 材料與方法
1.1 一般資料選取2021 年1 月~2022 年12 月我院兒科收治的胎齡<34 周的早產兒40 例,依據我國現行的早產兒ROP 篩查標準[5],于出生后4~6 周或矯正胎齡32 周開始進行眼底篩查,隨訪至周邊視網膜血管化。根據眼底檢查結果,發生ROP 的20 例設為ROP 組,未發生ROP 的20 例設為對照組。ROP 組男10 例,女10 例,胎齡31~34 周,平均(33±0.7)周,對照組男15 例,女5 例,胎齡31~34周,平均(33±0.84)周。兩組患兒性別和胎齡比較差異無統計學意義(P>0.05),具有可比性。納入標準:①胎齡<34 周的早產兒;②符合ROP 診斷標準;③監護人知情同意,且自愿參加本研究。排除標準:①不符合上述納入標準者;②母體除妊娠期疾病外還有其他基礎疾病者;③病情危重,曾經接受有創機械通氣,吸氧時間較長者;④重要器官或眼部存在先天畸形或缺陷者。本研究通過我院倫理委員會審核。
1.2 方法所有早產兒均采用常規綜合管理治療,包括呼吸支持、營養支持、感染對抗、循環支持等。ROP 的診斷及篩查按我國現行的ROP 篩查標準,于生后4~6 周或糾正胎齡32 周開始進行眼底篩查,由新生兒科醫師確定第1 次篩查時間,同時由經過專科培訓的高級眼科醫師進行眼底照相方法進行眼底篩查,隨訪至周邊視網膜血管化。在出生后1 周以及糾正胎齡34 周、36 周、40 周時于清晨采集患兒外周靜脈血1mL。血樣靜置30~60min 后,以2 000 轉/min 離心15min,分離血清后,保存在-70℃冰箱中待測。血清中IGF-1 的測定采用雙抗夾心ELISA 法,試劑盒選擇使用德國DRG 公司提供的進口試劑盒。
1.3 觀察指標觀察兩組患兒母體宮內感染、胎盤異常、母體妊娠期疾病(高血壓或糖尿病)、羊水異常情況和生后不同時間外周血IGF-1 的濃度。早產兒出生后,IGF-1 濃度通常較低,為30~170ng/mL;出生后第1~3 周IGF-1 濃度通常會達到峰值,為50~200ng/mL,隨后,IGF-1 濃度會逐漸下降,直到達到成人水平。
1.4 統計學方法采用SPSS 22.0 軟件進行統計分析。計量資料以表示,行配對t檢驗;計數資料以%表示,行χ2檢驗。P<0.05 為差異有統計學意義。
2 結果
2.1 兩組母體因素對比在母體因素方面,ROP 組中宮內感染、胎盤異常、母體妊娠期疾病(高血壓或糖尿病)和羊水異常的發生率均顯著高于對照組(P<0.05)。見表1。
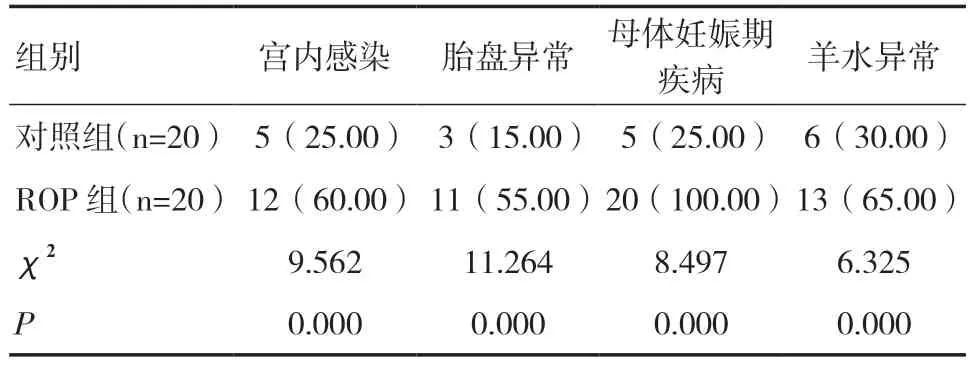
表1 兩組患兒母體因素對比[n(%)]
2.2 兩組患兒各周期血清IGF-1 水平對比ROP 組患兒出生后1 周、糾正胎齡34 周、糾正胎齡36 周時外周血IGF-1 水平明顯低于對照組(P<0.05),在糾正胎齡40 周時兩組患兒外周血IGF-1 水平差異無統計學意義(P>0.05)。見表2。
表2 兩組患兒各周期血清IGF-1 水平對比(,ng/mL)

表2 兩組患兒各周期血清IGF-1 水平對比(,ng/mL)
2.3 多因素分析經Logistic 回歸分析顯示,母體有宮內感染、胎盤異常、妊娠期疾病、羊水異常,早產兒IGF-1 水平較低是ROP 發生的危險因素。見表3。

表3 Logistic 多因素分析
3 討論
早產兒ROP 是一種發生于早產兒(胎齡低于37 周)的視網膜血管增殖性病變,其發病基礎是早產兒視網膜血管發育未完全[6]。通常,正常的視網膜發育在妊娠的最后幾周,而早產兒的視網膜發育可能不夠完善,尤其是在極度早產的情況下。ROP的發病機制與未成熟的視網膜血管系統有關。早產兒視網膜血管的生長和發育可能受到影響,特別是在早產兒被置于高氧環境時,可能導致異常的血管發育[7]。當早產兒需要在孵化器中接受高濃度氧氣治療時,血管生長可能受到抑制,但停止氧氣治療時,血管生長就會受到限制[8]。ROP 的嚴重程度可以分為五個階段,從輕微的病變到嚴重的病變,最終可能導致視網膜脫落。定期眼底檢查對于早產兒是非常重要的,可及時發現和干預ROP 的進展,有助于預防患兒出現嚴重的視力問題。
本研究結果顯示,ROP 組患兒母體因素中宮內感染、胎盤異常、母體妊娠期疾病(高血壓或糖尿病)和羊水異常的發生率均顯著高于對照組(P<0.05)。宮內感染可導致炎癥反應,炎性因子和細胞因子的釋放可能影響胚胎期間的血管發育,炎癥狀態會干擾正常的血管生成和維持過程,可能導致異常的血管發育,增加ROP 的風險[9]。胎盤在胚胎發育中發揮著關鍵的供血和營養作用,而胎盤異常可能導致胎兒供血和氧氣供應不足,從而影響眼睛的正常發育[10]。缺血和營養不足可能引發胚胎期間血管發育的異常,易引發ROP。母體妊娠期疾病,尤其是高血壓和糖尿病,也被認為是與ROP 發生密切相關的因素[11]。高血壓和糖尿病可能導致母體循環系統的異常,影響胎兒的供血。這可能導致胚胎期間的血管發育受到干擾,為ROP 的發生創造條件。羊水異常可能通過影響胎兒環境而對ROP 產生影響。羊水的成分對胎兒的發育至關重要,異常的羊水成分可能影響眼睛的正常發育[12]。羊水異常可能引發了胚胎期間血管發育的紊亂,增加了ROP 的發生風險。綜上,母體因素通過多種途徑影響了早產兒的視網膜發育。這些因素可能通過炎癥反應、胎兒供血和氧氣供應不足、循環系統異常以及羊水成分的變化等機制,干擾了正常的血管生成和維持過程,易導致ROP 的發生。
IGF-1 是一種由肝臟和其他組織合成的蛋白質激素,其在胚胎發育和生長過程中扮演著重要角色[13]。IGF-1 與細胞生長、分化和代謝調控密切相關,同時對于血管系統的發育也有著至關重要的影響。在早產兒ROP 的發病機制中,IGF-1 的水平與ROP 的發生密切相關,較低的IGF-1 水平可能增加早產兒患上ROP 的風險。IGF-1 是由生長激素刺激產生的,其生物學功能主要通過結合IGF 受體來實現[14]。IGF-1 通過與受體結合,激活多條信號通路,包括細胞內的酪氨酸激酶通路,從而調控細胞的增殖、生長和分化。這對于胚胎和新生兒的正常生長發育至關重要。IGF-1 在ROP 中的作用機制:①促進視網膜血管生長。IGF-1 對血管系統的發育具有刺激作用[15]。在正常的生長過程中,IGF-1 通過促進血管內皮細胞的增殖和遷移,有助于形成健康的血管網絡。在早產兒中,IGF-1 水平的下降可能導致血管生成受到抑制,增加了ROP 的發生風險。②維持視網膜的正常生理狀態。IGF-1 通過調節視網膜細胞的生理活動,維持視網膜的正常結構和功能[16]。低IGF-1 水平可能導致視網膜細胞代謝和功能的紊亂,使其更容易受到外界因素的干擾,從而影響視網膜的健康[17]。③抗炎作用。炎癥狀態是ROP 發生的一個重要因素,而IGF-1 水平的降低可能減弱這種抗炎作用,使得視網膜更容易受到炎癥的影響,進而促使ROP 的發生[18]。④抗氧化作用。IGF-1 被認為具有一定的抗氧化作用,有助于減輕細胞受氧化應激的損傷[19]。氧化應激可能是ROP 發生的另一個重要機制,而低IGF-1水平可能降低了細胞對氧化應激的抵抗力,使視網膜更容易受到氧化損傷[20]。
綜上所述,對早產兒母體因素充分了解,并及時監測早產兒IGF-1 水平,有助于早期發現和干預早產兒ROP,為臨床預防和治療提供更為全面的依據。在早產兒的綜合管理中,需重視母體因素的干預,提高早產兒的整體健康水平。

