雙酶法優化祿豐香醋糖化工藝
陳乾睿 趙銳環 徐志強 谷大海
DOI:10.3969/j.issn.1000-9973.2024.05.014
引文格式:陳乾睿,趙銳環,徐志強,等.雙酶法優化祿豐香醋糖化工藝[J].中國調味品,2024,49(5):80-88.
CHEN Q R, ZHAO R H, XU Z Q, et al.Optimization of saccharification process of Lufeng aromatic vinegar by double-enzymatic method[J].China Condiment,2024,49(5):80-88.
摘要:為提高祿豐香醋的生產效率,通過添加α-淀粉酶與糖化酶,對祿豐香醋生產過程中糖化工藝進行優化。糖化工藝包括液化工藝與糖化工藝兩部分:液化實驗以還原糖為指標;糖化實驗以還原糖為主要指標,黃酮類物質、氨基酸態氮為次要指標。在單因素實驗的基礎上,采用響應面分析法對祿豐香醋糖化過程中的參數進行優化。研究結果表明,祿豐香醋的最佳糖化工藝參數為α-淀粉酶添加量2.272%、液化pH 4.9、液化溫度50 ℃、液化時間43 min,此條件下還原糖含量為5.372 g/100 g。結合實際生產情況,當糖化酶添加量為2.336%、糖化pH為4、糖化溫度為55 ℃、糖化時間為60 min、蒸煮時間為1 h、料液比為1∶3時得到還原糖含量為13.614 g/100 g,黃酮含量為6.867 mg/L,氨基酸態氮含量為0.101 724 g/dL。
關鍵詞:祿豐香醋;糖化;工藝優化;雙酶法;響應面法
中圖分類號:TS264.22????? 文獻標志碼:A????? 文章編號:1000-9973(2024)05-0080-09
Optimization of Saccharification Process of Lufeng Aromatic
Vinegar by Double-Enzymatic Method
CHEN Qian-rui1,2, ZHAO Rui-huan1,2, XU Zhi-qiang1,2*, GU Da-hai1,2
(1.College of Food Science and Technology, Yunnan Agricultural University, Kunming 650201,
China; 2.Engineering Technology Research Center for Processing of Livestock Products in
Yunnan Province, Yunnan Agricultural University, Kunming 650201, China)
Abstract: To improve the production efficiency of Lufeng aromatic vinegar, α-amylase and glucoamylase are added to optimize the saccharification process during the production of Lufeng aromatic vinegar. The saccharification process includes two parts: liquefaction process and saccharification process. In the liquefaction experiment, reducing sugar is used as the index. In the saccharification experiment, reducing sugar is used as the main index, and flavonoids and amino acid nitrogen are used as the secondary indexes. On the basis of single factor experiment, response surface analysis method is used to optimize the parameters in the saccharification process of Lufeng aromatic vinegar. The results show that the optimal process parameters for saccharification of Lufeng aromatic vinegar are as follows: the addition amount of α-amylase is 2.272%, the liquefaction pH is 4.9, the liquefaction temperature is 50 ℃ and the liquefaction time is 43 min. Under these conditions, the content of reducing sugar is 5.372 g/100 g. According to practical production conditions, when the addition amount of glucoamylase is 2.336%, the saccharification pH is 4, the saccharification temperature is 55 ℃, the saccharification time is 60 min, the cooking time is 1 h and the solid-liquid ratio is 1∶3. the content of reducing sugar is 13.614 g/100 g, the flavonoid? content is 6.867 mg/L, and the amino acid nitrogen content is 0.101 724 g/dL.
Key words: Lufeng aromatic vinegar; saccharification; process optimization; double-enzymatic method; response surface method
收稿日期:2023-11-09
基金項目:云南省許正宏專家工作站,云南省重大專項及重點研發計劃(202105AF150062);科技入滇專項資金(202105AF150062)
作者簡介:陳乾睿(1999—),女,碩士,研究方向:食品科學。
*通信作者:徐志強(1974—),男,副教授,博士,研究方向:畜產品品質控制。
醋是中國傳統的酸性調味品。中國傳統食醋是以糧食為主要原料,經多種微生物共同發酵,再經長時間陳釀而成的酸性液體調味料,在我國已有3 000多年的歷史[1]。
祿豐香醋是一種具有云南風味的傳統名醋。史書記載,明朝中葉,祿豐當地以糯米為原料,經20余味中藥制曲,釀制成醋,將醋吸附在清潔的布帛上,名曰“干醋”,曾作為貢品送進京城。近年來,許坤一等[2]對傳統技藝重點進行微生物菌種學和發酵方式的技術改造,形成了一套新的固態生產程序。在不同地區,因為地理環境與氣候不同,食醋的釀造工藝與使用的原料具有不同的特點。采用傳統工藝,出醋率較低,原材料的利用率較低,成本較高。
生產食醋一般有4個過程:液化、糖化、酒精發酵、醋酸發酵。原料需經糖化酶或糖化菌分解(一般用米曲菌和黑曲菌等)才能成為可被酵母菌利用的糖類,再進一步進行酒精發酵和醋酸發酵,最終轉化成醋[3]。
糖化階段是一個重要的階段,因為在原料進行加熱蒸煮時會導致部分成分損失,以及加熱過程中溫度變化會影響微生物的生長代謝,會直接影響后續發酵,從而影響產品的品質[4]。
采用糖化酶與α-淀粉酶可以生產出水解糖[5]。現已有制醋工藝直接采用酶、純種酵母、純種醋酸菌代替糖化曲法發酵生產食醋[6-8],這表明用酶來代替傳統的糖化曲生產食醋具有可實施性。
1? 材料與方法
1.1? 材料與試劑
糯米:產自云南省祿豐市;α-淀粉酶(10萬U/g);糖化酶(10萬U/g);檸檬酸;檸檬酸鈉、鹽酸、硫酸銅、亞甲藍、乙酸鋅、氫氧化鈉、冰乙酸、酒石酸鉀鈉、亞鐵氰化鉀、葡萄糖標準品(純度≥99%)、甲醛、酚酞、乙醇、鄰苯二甲酸氫鉀(基準物質)、亞硝酸鈉、氯化鋁、蘆丁標準品(純度≥99%):昆明賽捷生物科技有限公司。
1.2? 儀器與設備
DZKW-S-4水浴鍋? 北京市永光明醫療儀器有限公司;UV-9000S紫外可見分光光度計? 上海元析儀器有限公司;SZCL-2型智能數顯控溫磁力攪拌器? 鞏義市予華儀器有限責任公司;LC22006368 pH計? 上海力辰邦西儀器科技有限公司。
1.3? 實驗方法
1.3.1? 工藝流程
原料→浸泡→蒸煮→料液比→調節pH→添加α-淀粉酶→水浴加熱→冷卻1→調節pH→添加糖化酶→水浴加熱→冷卻2。
1.3.2? 測定方法
1.3.2.1? 還原糖的測定
參照GB 5009.7—2016《食品安全國家標準 食品中還原糖的測定》中的方法。
1.3.2.2? 黃酮的測定
參照DB34/T 2743—2016《槐米及其制品中總黃酮含量的測定 分光光度法》中的方法。
1.3.2.3? 氨基酸態氮的測定
參照GB 5009.235—2016《食品安全國家標準 食品中氨基酸態氮的測定》中的方法。
1.3.3? 單因素研究
在液化實驗中,以還原糖為指標,在保持研究中工藝條件不變的基礎上,取25 g糯米,浸泡8~12 h[9],料液比為1∶3,α-淀粉酶添加量分別為0.5%、1%、1.5%、2%、2.5%、3%;pH分別為3,4,5,6,7;液化溫度分別為30,40,50,60,70 ℃;液化時間分別為20,30,40,50,60 min。
在糖化實驗中,以還原糖為主要指標,氨基酸態氮、黃酮為次要指標,在保持研究中工藝條件不變的基礎上,糖化酶添加量分別為1%、1.5%、2%、2.5%、3%;pH分別為3,4,5,6,7;糖化溫度分別為30,40,50,60,70 ℃;糖化時間分別為30,40,50,60,70 min。
1.3.4? Box-Behnken實驗
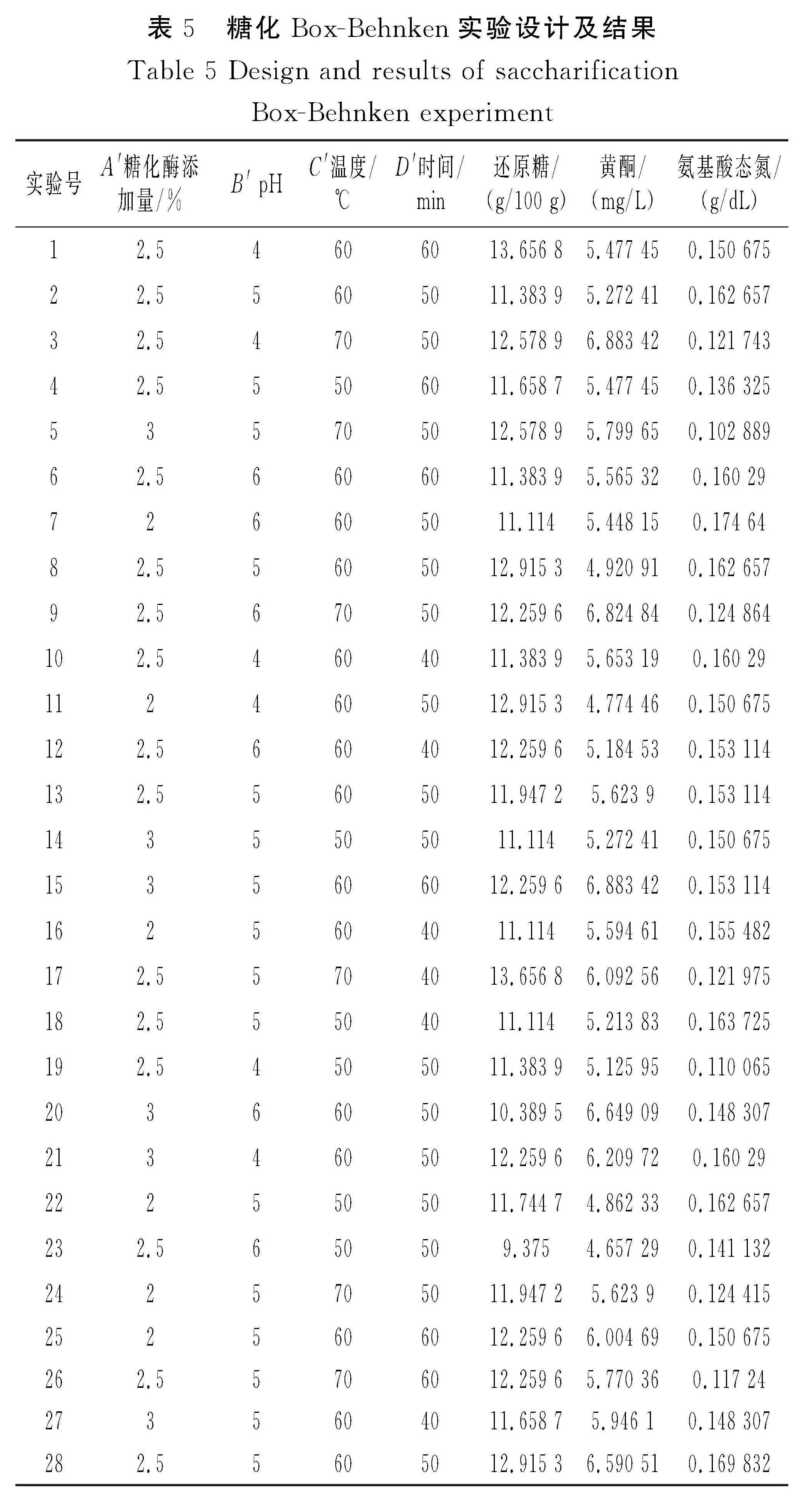
在單因素實驗結果的基礎上,確定各因素的范圍,在液化實驗中選取α-淀粉酶添加量、pH、溫度、時間4個影響顯著的因素,以還原糖含量為響應值。在糖化實驗中選取糖化酶添加量、pH、溫度、時間4個影響顯著的因素,以還原糖、氨基酸態氮和黃酮含量為響應值。響應面實驗設計見表1和表2。
1.3.5? 數據處理
采用Design-Expert 10、Origin 2018、Excel軟件處理數據。
2? 結果與分析
2.1? 單因素實驗結果
2.1.1? α-淀粉酶添加量、液化pH、液化溫度、液化時間的確定
由圖1中a可知,其余因素一定時,隨著α-淀粉酶添加量的增加,還原糖含量逐漸上升。當α-淀粉酶添加量達到2%時,糖化液中還原糖含量達到最大值,然后隨著α-淀粉酶添加量的增加,還原糖含量下降。陳磊等[10]的研究發現,釀醋原料中含有一定量的黃酮類物質,而黃酮類物質可通過疏水作用、氫鍵或范德華力與α-淀粉酶結合在一起,當黃酮類物質結合到α-淀粉酶的非活性中心部位時,對α-淀粉酶表現出非競爭性抑制。基于此原理,當黃酮含量增加時,對α-淀粉酶的抑制性也會增強,從而使還原糖含量呈現下降或平穩趨勢。
由圖1中b可知,隨著pH在3~7范圍內增加,還原糖含量先上升后下降,這是因為在一定的酸堿條件下,α-淀粉酶的活性受到了影響[11-12]。在液化過程中,pH為5時,酶活性最佳。大部分真菌α-淀粉酶在生產中的最適作用溫度在 50~55 ℃之間,最適pH一般在5.2~5.6之間[13-14]。所以,在本實驗中,pH為5時還原糖含量最高是合理的。
由圖1中c可知,隨著溫度的上升,還原糖含量呈現上升趨勢,當溫度達到60 ℃時,還原糖含量最高,繼續升溫,還原糖含量開始下降。從α-淀粉酶的最適作用溫度來看,溫度一旦超過60 ℃或pH小于5時,酶的活性開始迅速下降,從而導致催化反應速率降低[15-17]。
由圖1中d可知,當時間為20~40 min時,還原糖含量的上升速度十分迅速,但時間超過40 min后,還原糖含量呈現下降趨勢。由解華東等[18]的研究可知,這是由于淀粉的液化分為兩個階段:第一階段,α-淀粉酶作用于直鏈淀粉使其迅速分解;第二階段,α-淀粉酶作用于支鏈淀粉產生葡萄糖等,同時促進寡糖分解為葡萄糖,第二階段的反應速度比第一階段慢。隨著時間的延長,底物濃度的降低也會減緩酶反應的效率。大多數酶促反應都是可逆反應,酶反應速度受底物濃度的影響,也受生成物濃度的影響,生成物濃度升高會抑制酶的活性。隨著時間的延長,酶活性降低,所以導致還原糖含量下降。
2.1.2? 糖化酶添加量、糖化pH、糖化溫度、糖化時間的確定
由圖2中a可知,糖化酶添加量影響氨基酸態氮、還原糖、黃酮的含量。隨著糖化酶添加量的增加,氨基酸態氮含量先下降后升高,在糖化酶添加量為2%時,氨基酸態氮含量達到最高,隨著糖化酶添加量的繼續升高,氨基酸態氮含量下降。還原糖含量隨著糖化酶添加量的增加而升高,當糖化酶添加量為2.5%時達到最高,隨著糖化酶添加量的繼續增加,還原糖含量下降。孫潔心等[19]的研究表明,糖化酶添加量低于2.5%時,糖化酶與底物充分反應導致糖化反應受酶添加量的影響較大,當糖化酶添加量大于2.5%時,糖化酶添加量已過量,高濃度底物降低了水的有效濃度和分子的擴散性,從而降低了酶促反應速度。黃酮含量隨著糖化酶添加量的增加而增加,當糖化酶添加量為2.5%時,黃酮含量達到最高,隨著糖化酶添加量的繼續增加,黃酮含量下降,原因是隨著糖化酶添加量的增加,逐漸將黃酮水解為異黃酮苷。
由圖2中b可知,隨著pH的增加,氨基酸態氮含量和還原糖含量均呈現先上升后下降的趨勢,黃酮含量呈現先上升后下降再上升的趨勢,于pH為5時達到峰值,其原因是pH過高或過低均會抑制酶的活性。pH使酶制劑變性失活的原理主要是能破壞其空間結構[20],引起酶構象的改變,使酶活力喪失。
由圖2中c可知,隨著糖化溫度的上升,黃酮含量和氨基酸態氮含量均呈現先上升后下降的趨勢,于50 ℃時達到峰值,之后隨著溫度的上升而下降。其原因是溫度對酶的影響較大,從而影響了氨基酸態氮含量與黃酮含量。隨著溫度升高,還原糖含量也呈現先上升后下降的趨勢,于60 ℃時達到峰值。其原因主要與溫度對酶的影響有關。絕大多數糖化酶的最適酶解溫度在40~60 ℃范圍內,世界上糖化酶最適反應溫度最高為65 ℃[10]。李多川[21]報道過一株嗜熱真菌最適溫度為70 ℃,最適pH值為5.7,在60 ℃條件下保溫24 h后酶活性基本無損失,是目前為止我國發現的熱穩定性最高的糖化酶。
由圖2中d可知,隨著糖化時間的延長,黃酮含量和還原糖含量均呈現先上升后下降的趨勢,氨基酸態氮含量呈現先上升后下降再上升的趨勢。氨基酸態氮含量于30~40 min急速上升,之后趨于平穩。黃酮含量于40 min時達到峰值,之后下降。還原糖含量于50 min時達到峰值,之后下降。其原因為糖化酶作用的底物濃度逐漸降低,使得還原糖含量增長變緩,這時糖化酶對黃酮進行水解,導致黃酮含量下降。
2.2? 響應面實驗結果
2.2.1? 液化響應面實驗結果
以還原糖含量為響應值,采用Box-Behnken實驗和響應面分析對實驗結果進行處理和分析,見表3。液化工藝方差分析表見表4。
由表4可知,該模型回歸關系顯著,各因素對還原糖含量的影響大小為α-淀粉酶添加量>液化時間>液化pH>液化溫度。
各因素交互作用對還原糖含量的影響結果可以通過響應面圖直觀地反映出來,其中圖像底部的等高線可以反映兩因素交互作用的強弱,若是橢圓形則表示交互作用較強,圓形則表示交互作用較弱[22]。
由回歸方程擬合得到液化工藝的最優工藝條件為α-淀粉酶添加量2.272%、液化pH 4.922、液化溫度50 ℃、液化時間42.837 min,此條件下還原糖含量為5.274 g/100 g。
結合實際生產情況進行重復實驗,將工藝條件調整為α-淀粉酶添加量2.272%、pH 4.9、液化溫度50 ℃、液化時間43 min,此時還原糖含量為5.372 g/100 g。由此說明該模型的擬合程度良好,得到的液化工藝參數可靠。
2.2.2? 糖化響應面實驗結果
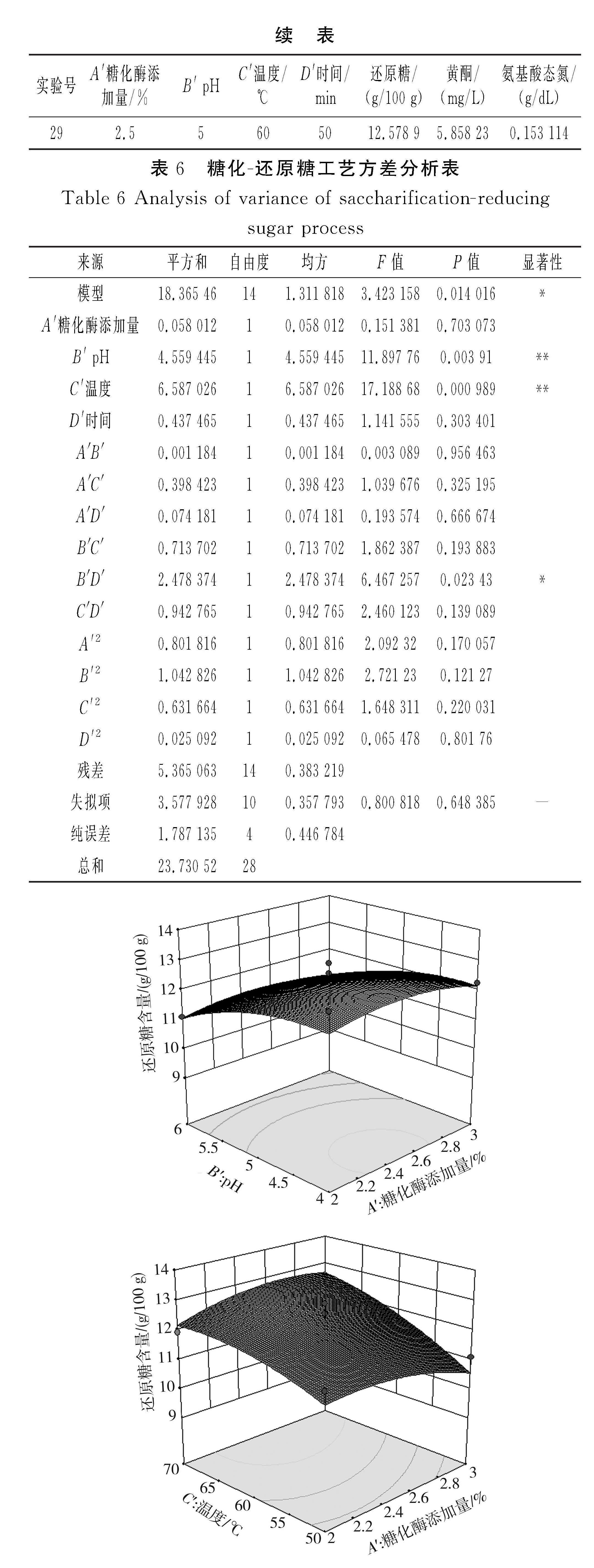
以還原糖、黃酮與氨基酸態氮含量為響應值,采用Box-Behnken實驗和響應面分析對實驗結果進行處理和分析,見表5。糖化-還原糖工藝方差分析表見表6。
由回歸方程擬合得到的糖化工藝的最優工藝條件為糖化酶添加量2.336%、糖化pH 4.008、糖化溫度55.653 ℃、糖化時間59.851 min,此條件下還原糖含量為13.660 g/100 g,黃酮含量為6.883 42 mg/L,氨基酸態氮含量為0.022 486 4 g/dL。
結合實際生產情況進行重復實驗,將工藝條件調整為糖化酶添加量2.336%、糖化pH 4、糖化溫度55 ℃、糖化時間60 min,此時還原糖含量為13.614 g/100 g,黃酮含量為6.867 mg/L,氨基酸態氮含量為0.101 724 g/dL。由此說明該模型的擬合程度良好,得到的糖化工藝參數可靠。
3? 結論
該實驗對祿豐香醋生產過程中糖化工藝進行了優化,添加α-淀粉酶與糖化酶代替原本生產工藝中的大曲。在單因素實驗的基礎上進行Box-Behnken實驗,篩選出α-淀粉酶添加量、液化時間、液化pH、液化溫度、糖化酶添加量、糖化時間、糖化溫度、糖化pH的顯著因素。采用響應面法優化了糖化工藝,得出α-淀粉酶添加量為2.272%、液化pH為4.922、液化溫度為50 ℃、液化時間為42.837 min時還原糖含量為5.274 g/100 g。糖化酶添加量為2.336%、糖化pH為4.008、糖化溫度為55.653 ℃、糖化時間為59.851 min、蒸煮時間為1 h、料液比為1∶3時還原糖含量為13.660 g/100 g,黃酮含量為6.883 42 mg/L,氨基酸態氮含量為0.022 486 4 g/dL。
在此之前,對于祿豐香醋的研究較少,未發現關于祿豐香醋生產工藝優化的相關研究。本實驗采用α-淀粉酶與糖化酶對工藝進行優化,為祿豐香醋后續生產工藝的改進提供了理論基礎。
參考文獻:
[1]鄭宇,程程,劉靜,等.中國傳統固態發酵食醋主要特征風味物質組成分析[J].中國食品學報,2020,20(8):237-247.
[2]許坤一,劉勇,楊麗源,等.祿豐香醋的生產及其工藝特點[J].食品科學,1988(4):38-41.
[3]周永治.食醋的生產原理[J].江蘇調味副食品,2007,24(4):21-24.
[4]文明,王毛毛,王雪婷,等.小米綠豆醋的糖化工藝研究[J].中國調味品,2022,47(4):102-108.
[5]施安輝,趙正溪,刑圓林,等.利用新型復合酶提高固態食醋風味和出品率的研究[J].江蘇調味副食品,2003(3):1-3.
[6]王傳榮.TH-AADY和糖化酶在食醋生產中的應用試驗[J].中國釀造,2001(1):23-24.
[7]李樹立,李娜,楊虹,等.酶法生料制醋新工藝的研究[J].食品研究與開發,2007(8):90-93.
[8]薛茂云,畢靜,鄭萍.鎮江香醋糖化工藝的研究[J].中國調味品,2018,43(1):125-127.
[9]吳宗亮.如何用糯米釀醋[J].農村百事通,2010(1):20-21.
[10]陳磊,劉輝,邱國棟.類黃酮和α-淀粉酶相互作用特性及機理的研究概述[J].廣東化工,2016,43(8):91-92,82.
[11]葉永菁,張云.“pH對α-淀粉酶活性的影響”探究活動的實驗優化[J].生物學通報,2014,49(12):44-46.
[12]范淑秋.pH影響淀粉酶活性的探究[J].生物學通報,2008,43(10):49-50.
[13]錢瑩,段鋼.新型耐酸真菌淀粉酶在麥芽糖生產上的應用[J].食品與發酵工業,2008(2):87-89.
[14]沈微,林麗珍,黃雯雯,等.一種酸性真菌α-淀粉酶的異源表達與重組酶性質[J].食品與發酵工業,2013,39(8):1-6.
[15]李松,王正祥.真菌α-淀粉酶的研究進展[J].生物技術通報,2011(3):66-71.
[16]DEY T B.Improvement of microbial α-amylase stability: strategic approaches[J].Process Biochemistry,2016,51(10):1380-1390.
[17]楊倩.米根霉α-淀粉酶pH與溫度耐受性相關氨基酸結構研究[D].蕪湖:安徽工程大學,2018.
[18]解華東,劉鄰渭,陳德經,等.低溫α-淀粉酶液化板栗淀粉的工藝研究[J].食品科技,2007,32(3):80-83.
[19]孫潔心,張永忠.糖化酶水解大豆異黃酮[J].食品與發酵工業,2012,38(12):91-94.
[20]高兆建,許祥,王先鳳,等.深綠木霉嗜酸性阿魏酸酯酶酶學性質及生物質轉化分析[J].食品科學,2019,40(10):121-128.
[21]李多川.利用嗜熱真菌生產熱穩定糖化酶的方法:中國,CN03112567.0[P].2003-11-19.
[22]呂歡,劉瑤,樊迎,等.響應面法優化壺瓶棗醋的工藝研究[J].中國調味品,2019,44(7):14-19,24.

