達格列凈中特定雜質分析及穩定性研究
范祥元 杜陳俠
摘 要:為建立達格列凈中的特定雜質DGL301分析方法,采用十四酸丙酰胺基團鍵合硅膠為填充劑(Poroshell 120Bonus-RP,100 mm×4.6 mm,2.7 μm或效能相當的色譜柱);流動相A:0.085%的磷酸水溶液;流動相B:乙腈;控制體積流量為1.0 mL/min進行梯度洗脫;檢測波長為225 nm;柱溫為25℃;進樣體積10 μL。在優化的色譜條件下,主峰、特定雜質DGL301及其他雜質分離度符合要求;特定雜質DGL301在0.16~0.79 μg/mL的濃度范圍內,呈現良好的線性關系,回歸方程為A =24.869 C+0.5787,r =0.9992,檢測限為17.56 ng·mL-1,定量限為59.85 ng·mL-1,RSD=0.9%(n =6),平均回收率為98.37%(n =9)。本方法可用于達格列凈中特定雜質DGL301的檢測。
關鍵詞:達格列凈,特定雜質,高效液相色譜法
DOI編碼:10.3969/j.issn.1002-5944.2024.05.036
0 引 言
達格列凈原研企業為百時美施貴寶公司和阿斯利康公司,其為SGLT2抑制劑,于2012年12月在歐盟獲批上市,臨床適應證為2型糖尿病,國家藥品監督管理局已批準國內上市的生產企業僅有3家。研究表明,達格列凈降糖通過二個途徑實現降糖作用[1-2]:第一,通過調節抑制腎臟對葡萄糖的重吸收作用,第二、通過增加腎臟對葡萄糖的排泄作用。通過文獻檢索發現,關于達格列凈的研究方向主要集中在臨床領域,針對達格列凈雜質分析研究報告很少,截至投稿,國內外針對達格列凈雜質分析公開發表的文章不足10篇[3-7]。研究人員通過對合成工藝的深入研究,將產生可能性最大的DGL301定為特定雜質,而此雜質在進口標準未進行控制,已發表的文獻中也未對此雜質進行報道。本實驗建立了達格列凈雜質分析方法,試驗結果表明,該方法準確度高、專屬性強、重復性好,可作為達格列凈原料藥雜質評價方法。
1 儀器與試藥
氣相色譜儀;梅特勒XS105電子天平。
達格列凈原料藥(宣城美諾華藥業有限公司,批號為DGBB-9-210901、DGBB-9-210902、DGBB-9-210903);DGL301對照品(批號07-APR-20-16-01,純度97.8%),達格列凈對照品(宣城美諾華藥業有限公司自制,批號D009-200402KB)。
鹽酸、氫氧化鈉、30%過氧化氫為分析純,乙腈為色譜純,水為純化水,其他試劑為分析純。
2 方法與結果
2.1 色譜條件
色譜柱:Agilent In f inity L ab Poroshell120Bonus-RP(100 mm×4.6 mm,2.7 μm);流動相A:0.085%的磷酸水溶液;流動相B:乙腈;梯度洗脫;流速為1.0 mL /min;檢測波長為225 nm;柱溫為25℃;進樣體積10 μL。
2.2 溶液制備
稀釋劑∶乙腈∶水=50∶50(V/V)
雜質儲備溶液:稱取DGL301雜質對照品3 mg,取稀釋液溶解并稀釋至濃度為0.03 mg/mL雜質儲備溶液。
系統適用性溶液:稱取達格列凈對照品15 mg及雜質DGL301儲備溶液0.5 mL,取稀釋液溶解并稀釋至DGL301濃度為0.03 μg/mL雜質儲備溶液(達格列凈:0.03 μg/mL)。
標準溶液: 稱取達格列凈對照品15 mg,取稀釋液溶解并稀釋至濃度為0.03 μg/mL。
樣品溶液: 在50 mL容量瓶中加入本品15 mg,加入稀釋劑超聲處理至完全溶解,定容至刻度,搖勻。平行配制2份。
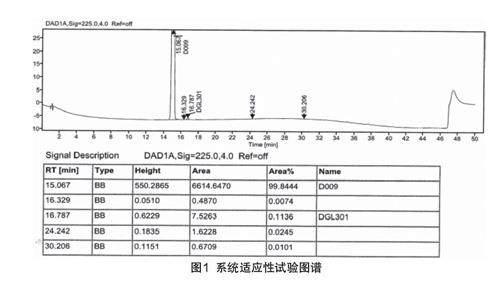
2.3 系統適應性試驗
取系統適應性溶液按照規定的色譜條件進樣,系統適應性試驗圖譜如圖1所示。結果表明,主峰與雜質DGL301依次出峰,分離度為4.3,符合分析要求。
2.4 檢測方法
測定法:精密量取供試品溶液和對照品溶液,分別注入液相色譜儀,記錄色譜圖。限度:按外標法以對照品溶液主峰峰面積計算,DGL不得大于0.10%,其他單個雜質不得大于0.10%,各雜質的和不得大于1.0%。供試品溶液色譜圖中小于0.05%的雜質忽略不計。
2.5 專屬性試驗
(1)酸破壞。50 mL量瓶中加入精密稱定的達格列凈原料藥15 mg(批號:DGBB-9-210901),移取1.0 mL鹽酸溶液(濃度為5 mol/L)加入量瓶,搖勻后靜置,調節水浴鍋溫度至60℃恒定,將其放置24小時后,取出并放至室溫,加入1.0 mL氫氧化鈉溶液(濃度為5 mol/L)作為中和試劑,加乙腈-水(50∶50)溶解并稀釋至刻度,搖勻。
(2)堿破壞。50 mL量瓶中精密稱定達格列凈原料藥15 mg(批號:DGBB-9-210901),移取1.0 mL氫氧化鈉溶液(濃度為5 mol/L),搖勻后靜置,調節水浴鍋溫度至60℃恒定,將其放置24小時后,取出并放至室溫,加入1.0 mL鹽酸溶液(濃度為5 mol/L)作為中和試劑,加乙腈-水(50∶50)溶解并稀釋至刻度,搖勻。
(3)氧化破壞。50 mL量瓶中精密稱定達格列凈原料藥(批號:DGBB-9-210901)15mg,加入30%過氧化氫,室溫條件下放置24小時,加乙腈-水(50:50)溶解并稀釋至刻度,搖勻。
(4)高溫破壞。50 mL量瓶中精密稱定達格列凈原料藥15 mg(批號:DGBB-9-210901),置50 mL量瓶中,加乙腈-水(50∶50)30 mL使溶解,調節水浴鍋溫度至60℃恒定,將其放置24小時后,取出并放至室溫,加乙腈-水(50∶50)稀釋至刻度,搖勻。
(5)光照破壞 。50 mL量瓶中精密稱定達格列凈原料藥(批號:DGBB-9-210901)15 mg,加乙腈-水(50∶50)溶解并稀釋至刻度,搖勻,于4500 Lx光照條件下放置3天。
精密量取上述溶液,分別注入液相色譜儀。結果顯示,DGL301在高溫、酸、堿等條件下均能與主峰及降解產物實現有效分離,此方法可以用于特征雜質DGL301的測定。
2.6 線性和范圍
精密量取標準溶液和DGL301對照品貯備液,用乙腈-水(50∶50)逐步稀釋,制成不同濃度的混合溶液作為系列線性溶液。
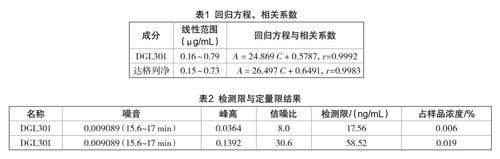
精密量取上述溶液各10 μL注入液相色譜儀,記錄色譜圖。結果見表1。
2.7 校正因子
對表3 中的數據進行計算的到特定雜質DGL301的校正因子為1.07。
2.8 檢測限與定量限
取標準溶液及特定雜質DGL301儲備溶液,用乙腈-水(50∶50)逐級稀釋,計算結果見表2。
2.9 精密度試驗
2.9.1 重復性
按照“2 . 2”項規定,制備6 份平行樣,按照“2.1”項下規定的色譜條件檢測,考察6份加標樣品溶液中各雜質測試結果的相對標準偏差,RSD為0.9%,結果表明重復性好。
2.9.2 中間精密度
另一人按照“2. 2”項規定,制備6份平行樣,按照“2.1”項下規定的色譜條件檢測。計算2未測定人員中間精密度相對標準偏差R SD(n =12)為1.13%,因此,該分析方法具有良好的中間精密度。
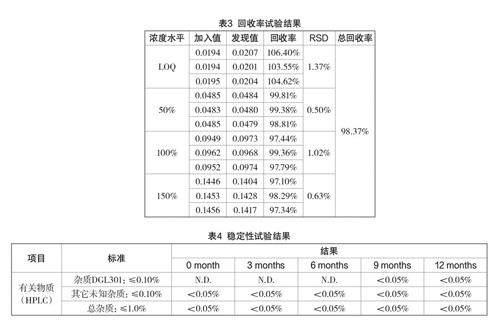
2.10 加樣回收率(見表3)
從上述結果分析,在LOQ~150%濃度水平下,DGL301在各濃度下3份加標樣品溶液中的回收率和回收率的相對標準偏差均在可接受標準范圍內。
2.11 溶液的穩定性試驗
標準溶液在常溫下放置不同時間,0小時,5小時,10小時…25小時,48小時,比較不同時間點樣品溶液和加標樣品溶中各雜質結果與初始結果的絕對差異值,以及不同時間點標準溶液中主峰峰面積的相對偏差,結果總雜含量的RSD為6.08%,表明溶液在測試條件下穩定性良好。
2.12 耐用性試驗
本試驗考察了流速、檢測波長、流動相比例對測定結果的影響。從結果來看,流動相中磷酸比例(±0.01%)、流速(±0.1 mL/min)、柱溫(±2℃)、波長(±2 nm)的細微變化沒有影響各雜質含量的檢測,且滿足可接受標準的要求。
2.13 穩定性研究
考察樣品在室溫條件下的長期穩定性,定期檢測雜質成分,結果如表4所示。
3 結 論
本試驗建立了達格列凈特定雜質的分析方法,其H PL C檢測方法通過方法學驗證。結果表明,該方法簡單易操作、靈敏度、專屬性好,穩定性研究結果理想,可用于達格列凈的特定雜質DGL301的測定。
參考文獻
[1]COLE P, VICENTE M, CASTANER R. Dapagliflozin.SGLT2 inhibitor, Antidiabetic agent [J]. Drugs Future,2008,33(9):745-751.
[2]MENG W, ELLSWORTH B A, NIRSCHL A A, et al.Discovery of dapagliflozin: a potent, selective renal sodiumdependent glucose cotransporter 2 (SGLT2) inhibitor for the?treatment of type 2 diabetes [J]. J Med Chem, 2008, 51(5):1145-1149.
[3]陳穩,鄭津津,王晨.HPLC法測定達格列凈原料藥中有關物質[J].現代藥物與臨床,2015,30(9):1068-1071.
[4]周浩, 孟繁華, 孫磊,等. L C - M S / M S 法定量檢測恩格列凈原料藥中雜質的含量[ J ] .國際藥學研究雜志,2016,43(4):753-756.
[5]戴震,朱麗君.反相高效液相色譜法測定達格列凈的有關物質[J].臨床合理用藥雜志,2017,10(23):100-101.
[6]鄭云峰,吳高鑫,羅海榮.達格列凈·(S)-(+)-1, 2-丙二醇·一水合物的合成及其有關物質的分離與結構鑒定[J].山東化工, 2018,47(15):48-50.
[7]白彥川,張孟孟,劉蕊,等.HPLC法測定達格列凈起始物料有關物質[J].海峽藥學.2022,34(4):83-88.
作者簡介
范祥元,碩士研究生,研究方向為藥物合成及藥品質量標準研究。
杜陳俠,通信作者,本科,主管藥師,研究方向為藥事管理及藥品質量分析。
(責任編輯:袁文靜)

