學科大概念統領下發展模型認知的單元教學實踐
譚湘湘 何彩霞
摘要:? 以學科大概念為統領,以“水處理過程的化學”為例開展主題教學,整體考慮水的凈化、硬水軟化、含鉻污水處理3個情境任務,引導學生自主建構并應用拓展“水處理”認知模型,促進學科知識結構化,發展解決問題的能力,提升化學學科核心素養。
關鍵詞:? 學科大概念; 認知模型; 物質的分離與轉化; 水處理; 單元教學
文章編號: 1005-6629(2024)05-0042-07
中圖分類號: G633.8
文獻標識碼: B
1? 問題的提出
《普通高中化學課程標準(2017年版2020年修訂)》[1](以下簡稱“課標”)主張“素養為本”的化學教學,倡導“真實問題情境的創設,重視教學內容的結構化設計”“通過分析、推理等方法認識研究對象的本質特征、構成要素及其相互關系,建立認知模型,并能運用模型解釋化學現象,揭示現象的本質和規律”。知識關聯,認識思路、核心觀念的結構化是實現學科知識向學科核心素養轉化的關鍵。教學中需要選擇合適的主題情境,以學科大概念為統領,實現知識結構化,注重思維方法建構,切實提高解決實際問題的能力[2,3]。
水處理的過程包含水的凈化、硬水軟化、污水處理等任務,其核心在于利用混合物中組分的性質及其差異進行物質的分離與轉化,這是中學化學學習的重要內容,對于發展學生綜合運用化學知識分析解決問題,發展學生化學學科核心素養具有重要作用。現各版本高中化學教材沒有集中編排“水處理”的內容,暫未見中學教學中對水的凈化、硬水軟化、污水處理等幾個任務整合的文獻。
本文針對高二學生設計“水處理過程的化學”主題學習,以“物質的分離與轉化”學科大概念為統領,建構并應用認知模型,形成解決此類問題的一般思路。
2? 學科大概念統領下的單元知識分析與認知模型
2.1? 單元知識結構分析
利用物質的性質及反應進行物質的分離、轉化是中學化學學習的重要內容。高中化學必修課程[4]要求:“能根據物質性質的差異選擇物質分離的實驗方法”,了解通過化學反應可以實現物質轉化,認識物質及其轉化的重要價值。高中化學選擇性必修1課程[5]強調,“選取典型案例,能從限度、平衡等角度對化學反應和化學工業生產條件進行綜合分析”,了解水溶液中的離子反應及平衡在物質分離、轉化中的應用,認識化學反應的調控在生產、生活和科學研究中的重要作用。
就“水處理過程”相關學科知識而言,自然界中的水、工業生產排放的廢水屬于混合物,為滿足生活和生產需要,人們需要根據水質的不同進行分離、轉化等處理,以達到凈化、安全和可持續利用的目的。盡管水的凈化、硬水軟化和含鉻污水處理等“水處理過程”各有其獨特的原理和技術,但它們都蘊含共同的道理,即根據混合物中組分性質的差異選擇合適的方法和程序來進行物質的分離、轉化和提純。也就是說,解決這類問題需要關注兩類關鍵知識:概念原理與方法程序[6]。因此,“水處理”過程的關鍵是要考慮依據什么原理、采用什么方法和程序來分離除去水中的雜質,其分離的路徑大致有以下情形:一是利用物理性質差異直接分離,如利用過濾的方法進行分離,除去水中的不溶物;二是依據化學性質差異通過反應將其轉化為可直接分離的狀態再進行分離,或利用化學方法將雜質轉化成符合要求的成分,以達到去除和凈化的目的,如加沉淀劑使雜質轉化成沉淀后再利用過濾來分離,或加消毒劑進行殺菌消毒等。
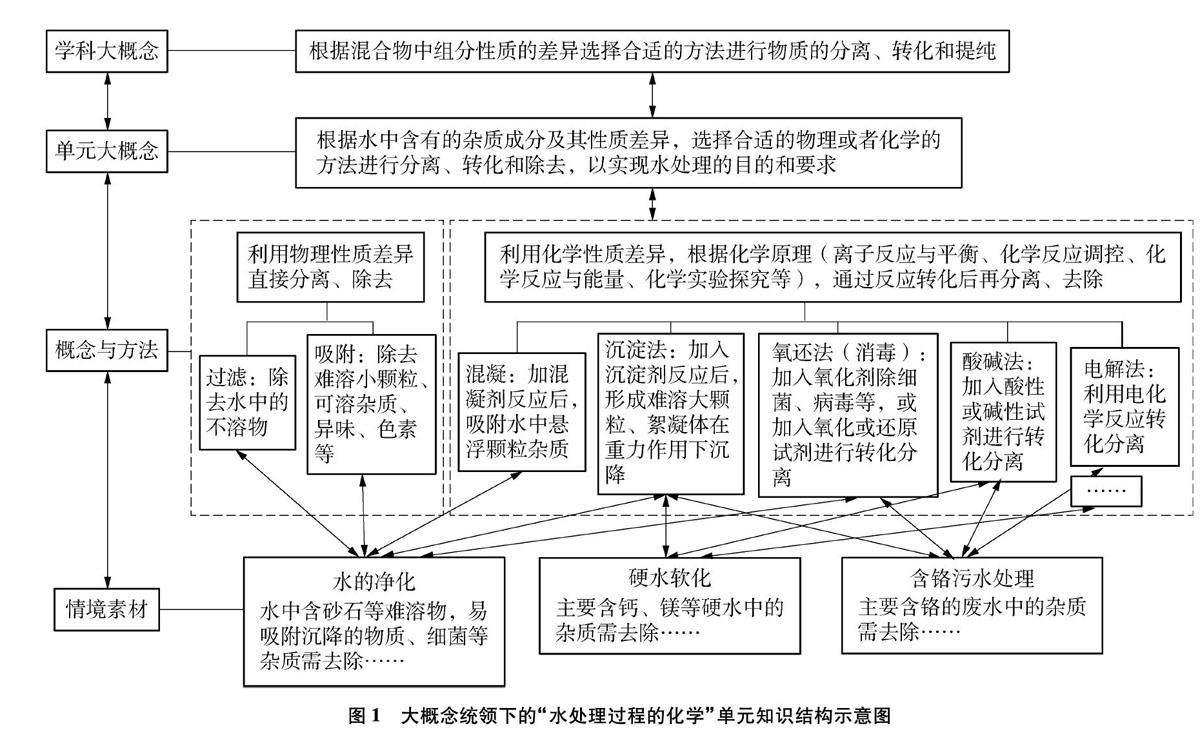
基于上述分析,在學習人教版選擇性必修1化學反應原理后設置“水處理過程的化學”主題單元,學科大概念統領下的知識結構如圖1所示。學生認識進階側重于:綜合運用學科知識,根據物質的性質與反應,選擇合適的試劑,利用化學方法將雜質轉化為易于除去的物質進行分離,以達到凈化、除雜的目的,即能從水溶液中離子反應與平衡的角度、運用化學實驗的核心思路,融合多學科知識思考問題,發展學生從離子、平衡、能量、調控等角度認識溶液中物質的性質和反應,形成分析“水處理”這類問題的方法策略并能應用于解決實際問題。
2.2? 認知模型
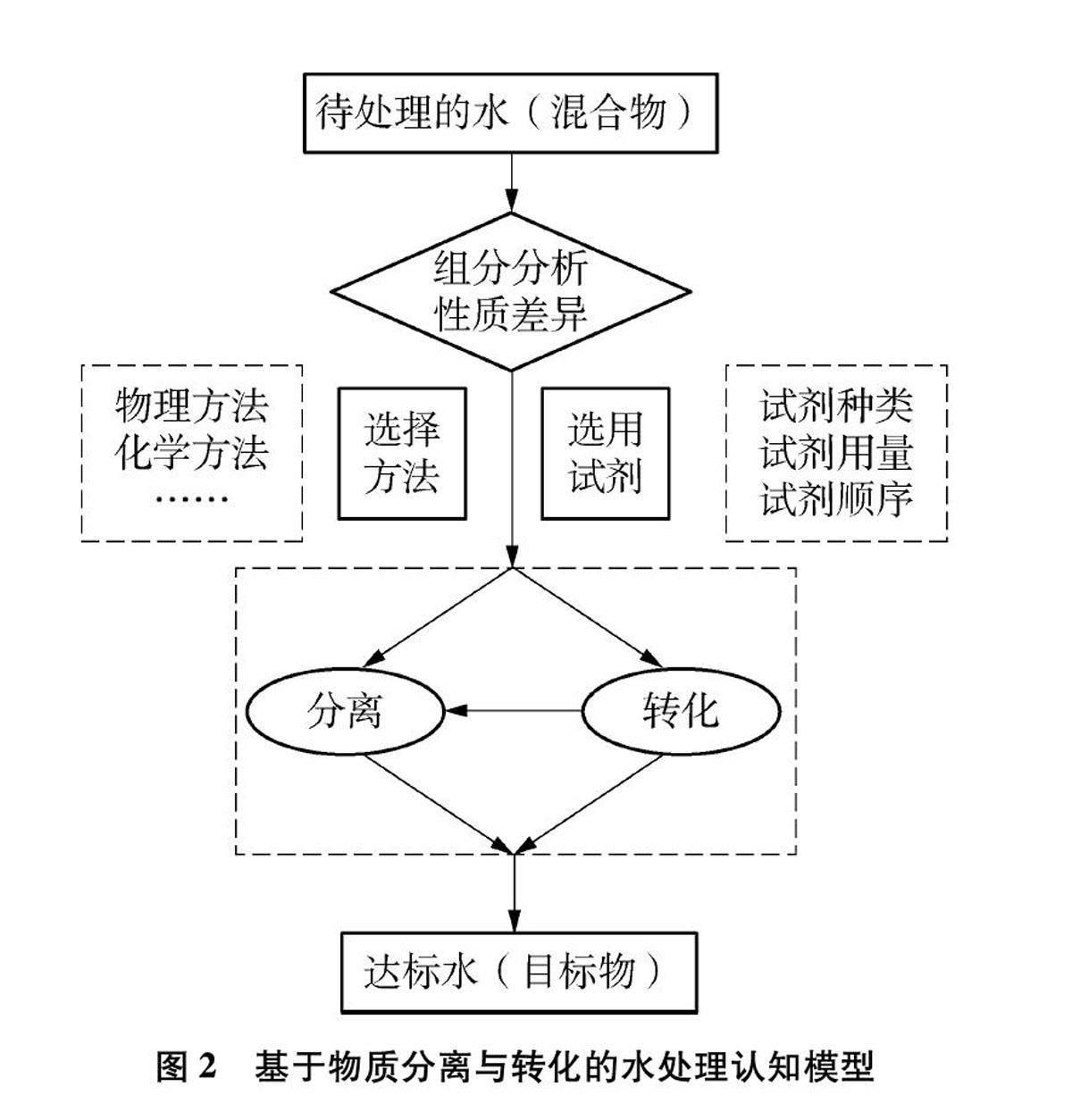
實際工業生產中,“水處理”這類問題都是通過一系列的處理步驟和方法來完成的,其綜合性較強,比較復雜。基于圖1所示結構化知識構建“基于物質分離與轉化的水處理認知模型”(見圖2):首先,明確研究對象和分離除雜的目的和要求;其次,分析混合物的組分及其性質差異;再次,按照“易分”“除盡”“環保”“最優”的基本原則,選擇方法和選用試劑。對于難溶等易分離雜質可直接過濾或吸附分離,對于不易分離的雜質選用化學方法將其轉化為易于除去或無毒害物質等來實現分離和除雜,過程中要結合化學反應原理等知識考慮試劑的選擇、用量、順序、使用條件等,從速率、限度的角度調控化學反應,從能量等角度綜合分析,最終獲得目標產物。
3? “水處理過程的化學”單元教學目標與教學流程
3.1? 單元教學目標
(1) 通過對水的凈化工藝流程的分析,初步建構混合物(待凈化的水)分離與轉化的認知模型,能應用于硬水軟化、含鉻廢水處理等實際問題的分析,完善混合物分離與轉化的認知模型,形成解決這類問題的一般思路。
(2) 針對凈化水中的混凝、消毒及硬水軟化中的沉淀轉化等問題,能依據組分性質差異,從離子反應與平衡、氧化還原反應等角度進行試劑的選擇及反應條件的調控,能用化學反應與能量等知識解決含鉻污水的處理問題,拓展對水處理過程的原理和常見方法的認識,提升解決實際問題的能力。
(3) 通過水的凈化、硬水軟化及含鉻廢水等真實問題的分析,體會學科知識間的內在聯系和系統解決問題的基本思路的重要性,增進對化學學科知識價值的理解,提高節約資源的責任意識。
3.2? 單元教學流程
聚焦水的凈化處理,教學流程共分3個課時任務,如圖3所示,具體如下:
任務1:建構模型。以“水的凈化”為載體創設實際問題情境,根據自來水廠凈水過程示意圖,思考程序,小結方法,初步構建認知模型;探討混凝和消毒環節的原理和方法,通過數據、設計并實驗等,認識選擇思路;討論野外凈水方案,互評方案可取性,獲取實用策略;分析完善待凈化水的認知模型,復習反應原理知識的同時,形成水凈化的一般思路方法。
任務2:應用模型。創設硬水軟化情境,根據資料學生討論交流硬水的危害,先行應用模型,根據鈣、鎂不同的存在形式,探討除雜方法,教師跟進評價:加熱法,先轉化為難溶物再實現沉淀轉化除雜;藥劑軟化法,考慮多重因素間接轉化為沉淀,并能用化學用語表達;離子交換法,根據電荷守恒去除雜。
任務3:拓展模型。創設含鉻廢水情境,分析含鉻
廢水的危害及鉻元素常見的轉化形式,探討鋇鹽沉淀轉化法;加Na2SO3還原沉淀法,尋求最佳工業條件;電解法等特殊手段。梳理特殊水質問題的解決思路,拓展模型解決問題,樹立環保能耗意識。
4? 單元視角下的課時教學舉例
“水處理過程的化學”主題教學的3個任務中,任務1聚焦于一般水質的凈化問題,建構水的凈化認知模型;任務2和任務3聚焦于解決特殊水質的問題,應用并拓展模型。其中任務1的主要教學活動見下文。
4.1? 活動1:水凈化工藝流程
[問題1]從自然界獲得的水,不能完全滿足人類生產、生活的需要,根據水體、用途的不同,需要對水進行處理。有哪些處理方法呢?
[學生]海水淡化、水的凈化、硬水軟化、污水處理等。
[追問]水的凈化處理方法復雜且多樣,請結合粗鹽精制[7],應具體考慮哪些問題?
[學生主要觀點](1)先過濾掉砂石,再加入試劑將雜質離子轉化為沉淀去除;(2)還要考慮試劑用量、順序、檢驗等。
[展示前測]我們是否可以類似考慮待凈化的水呢?課前,同學們根據初中自來水凈水圖,對流程進行了描述。你認同哪個觀點?請分析水凈化工藝的流程,思考主要環節、目的及順序,并說出你的依據(見圖4)。
[學生主要觀點](1)認同2號(沉淀-過濾-吸附-消毒);(2)認同3號(混凝-沉淀-過濾-吸附-消毒),應先將懸浮物吸附,與大顆粒難溶物在重力作用下沉淀并過濾,活性炭吸附色素及異味等,最后細菌消殺等。
[共同小結]程序方法:先大后小,先易后難。初步構建認知思路:組成分析-性質差異。
設計意圖與認知發展:針對水的凈化問題,類比粗鹽精制,能依據混合物中的組分及其性質差異選擇分離方法和程序,初步建構水的凈化的認知模型。
4.2? 活動2:水凈化的原理和方法
[教師]為達到凈水目標,進一步探討混凝、消毒環節的原理方法。
[問題2-1]選擇什么試劑除去不易沉降的物質,它們有什么共同特點?為什么常常同時加入少量NaHCO3?
[學生]可選明礬、鐵鹽等吸附除去,因為能發生鹽類的水解產生膠體;可促進水解程度。
[問題2-2]常選用什么試劑可除去水中細菌?為什么可以消毒?
[學生]含氯消毒劑,如氯水、次氯酸鹽等,因為它們具有強氧化性。
[教師]類比漂白粉,國內自來水廠大多用Cl2對水進行消毒,其原理是什么?使用時加氨可延長處理時間,提高消毒效果,結合化學用語解釋原因。
[學生]產生HClO起殺菌作用;書寫解釋水解反應可逆,不斷釋放成分并吸收。
[追問]Cl2消毒有什么弊端?
[學生]Cl2有毒,副產物。
[教師]保存:陰暗處密封,否則容易失效,用化學用語解釋原因。
已知(見表1):
[學生]根據電離常數信息及已學知識書寫方程式。
[討論]實驗室通過測定不同條件NaClO的細菌殺滅率,以探究“84”消毒液殺菌能力影響因素,實驗結果見表2:
(1) 結合上表數據推斷,相同條件下,HClO與NaClO哪個殺菌能力更強?
(2) NaClO的殺菌能力與哪些因素有關?使用時應注意什么?
[學生主要觀點](1)認為HClO更強,并與濃度、pH、溫度等有關;(2)對金屬制品有腐蝕作用,不可長期使用;噴灑后保持一段時間效果會更好。
[共同小結提升](見圖5)
[教師]ClO2被國際公認為安全、無毒、綠色消毒劑,消毒效率是Cl2的2.6倍,對生物細胞壁有很強的吸附穿透能力。
[實驗展示]大腸桿菌是水處理的常用指標,這是ClO2對大腸桿菌滅活前后的對照實驗,ClO2符號是用棉簽蘸取大腸桿菌寫的,培養1天后的生長情況。經ClO2處理后,僅有少量菌生長(見圖6)。
[追問]ClO2較強的消毒殺菌能力是由什么決定的,能否預測,你的依據是什么?
[學生]強氧化性,+4價。
[實驗探究]如何設計實驗證明ClO2有氧化性?
資料:ClO2是一種黃綠色氣體,避光保存,低溫光解,為易爆炸的物質,易溶于水但不與水反應。
實驗藥品:ClO2消毒片、維生素C溶液、水
[學生主要觀點](1)ClO2固體溶于水呈黃綠色,加入維生素C溶液后退色;(2)退色有可能是因為加入溶液稀釋的結果,應再加一個對照試管:ClO2固體溶于水后,加等量的蒸餾水。
[小結提升]在進行多因素對照試驗時變量控制很重要。ClO2有強氧化性,所以有較強的消毒能力,性質決定用途。
[教師]能否找到消毒、凈水兩者功能兼備的試劑?
[學生]應找高價態且能水解吸附的物質,如K2FeO4等。
[拓展]介紹預處理、深度處理工藝。
設計意圖與認知發展:認識混凝劑、消毒劑的工作原理和方法,并基于離子反應與平衡、氧化還原反應、化學實驗探究等認識化學反應調控的重要性。
4.3? 活動3:凈化水實踐
[問題3]如果在野外,如何凈水?
[學生主要觀點](1)就地取材,制作簡易裝置,雜質由大到小依次除掉;(2)對水進行蒸餾或用海藻吸附凈水;(3)帶好混凝劑、消毒劑,如ClO2、 K2FeO4等;(4)用含黏液質的野生植物吸附懸浮物質沉降凈水,再加消毒劑。
設計意圖與認知發展:創設野外情境,思考凈水原理和方法,考慮采用混凝和消毒相結合的方法,或就地取材選擇試劑,提升解決實際問題的能力。
4.4? 活動4:總結提升
[問題4]在水凈化過程中,我們是如何思考問題的,你還有哪些補充和完善建議?
[學生主要觀點](1)先分析水源成分,如懸浮物可以吸附,難溶物可以沉降,細菌等可以消毒,再根據雜質的性質差異選擇合適的方法進行過濾分離或轉化為沉淀、無毒成分后分離;(2)應選擇合適的混凝劑、消毒劑;(3)細節上應關注試劑用量,優化除雜順序,考量是否除盡等因素,與粗鹽提純方法類似。
[共同小結]建立“待凈化的水”認知模型(見圖7)。
設計意圖與認知發展:通過互動交流,從組成分析、性質差異、選擇方法等角度,總結水凈化的一般思路與方法,構建凈化水的認知模型,為特殊水質處理做鋪墊。
5? 教學反思與感悟
本單元以水的凈化、硬水軟化、含鉻廢水處理為情境素材,從知識間的內在聯系和系統解決問題的基本思路[8]兩方面,引導學生認識基于物質分離與轉化的原理、方法和程序,提升學生分析解決相關問題的能力。在教學設計中,以下兩點較為關鍵:
第一,關注學生認知基礎,做好新舊知識間的關聯與遞進。利用前測,了解學生對于水的凈化工藝流程的認知程度,課堂上通過部分學生的作品展示與分析,喚醒學生的已有認知,厘清初中階段所學的“水凈化”知識,再類比粗鹽精制實驗,激活學生對除雜試劑、順序、用量等問題的考量,初步構建水凈化的認知模型;將認知模型遷移應用于解決硬水軟化的問題,如學生通過運用藥劑軟化法,能從微觀角度較快討論出:除Mg2+選擇OH-、除HCO-3選擇OH-和Ca2+、除多余Ca2+選擇CO2-3,同時還考慮到試劑的用量(過量)、順序(CO2-3加在Ca2+之后)和除盡等問題。面對復雜的實際問題,學生一旦有了認知模型作為抓手,思路方法更為順暢清晰。
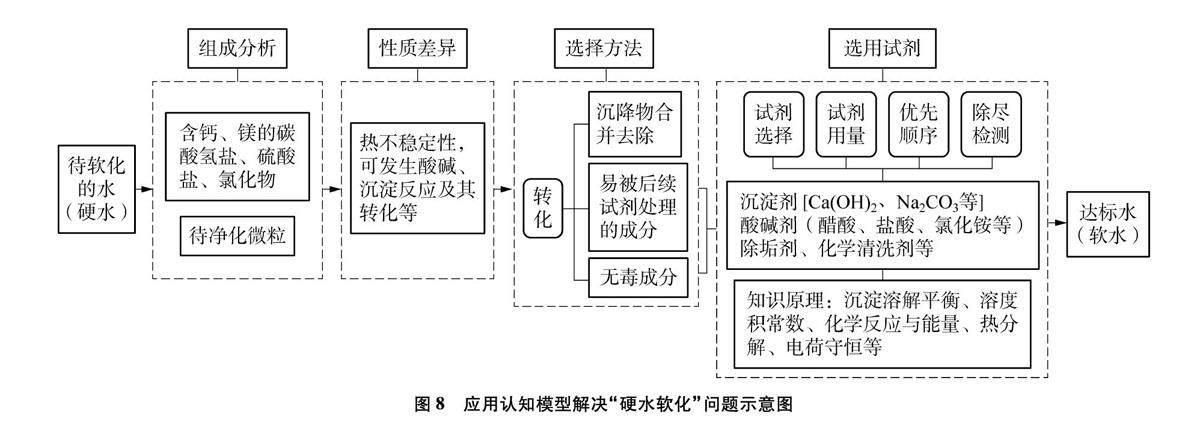
第二,利用問題引導學生思考,建構并應用模型,注重發展學生思維和能力。例如在水的凈化基礎上,進一步考慮硬水軟化問題,可提出問題鏈:“硬水中含哪些雜質、它們具備哪些性質差異、可以選擇什么方法進行分離、具體選用什么試劑”等,問題有導向性,使不同層次學生均能參與其中。在探討分離方法時,學生提出可利用碳酸氫鹽的熱不穩定性,通過加熱法轉化為易于除去的碳酸鹽沉淀,或加沉淀劑將碳酸氫鹽轉化,或加入易于轉化沉淀的試劑,如將硫酸鹽轉化為易于除去的碳酸鹽沉淀等。此時,學生對雜質轉化的認識更加豐富深入,順利建構起“硬水軟化”的認知模型(見圖8)。
在探討含鉻污水的分離時,學生依據組成及性質差異進行分析,在教師的啟發下能夠猜想到將六價鉻直接轉化為鉻酸鋇沉淀而分離,并考慮殘留離子的去除;或先用還原劑將六價鉻轉變為三價鉻,再轉化為沉淀除去;并綜合設備成本等因素,選擇最佳pH調控反應,或設計為電化學裝置,形成分析解決“含鉻污水處理”實際問題的基本思路。
從“待凈化的水”到“硬水軟化”再到“含鉻污水處理”,學生不僅拓展和豐富了對于水處理問題的認識,更為重要的是學生以認知模型作為思考工具,有助于提升思維層次和認知水平,發展在新情境下分析解決實際問題的能力[9]。
參考文獻:
[1][4][5]中華人民共和國教育部制定. 普通高中化學課程標準(2017年版2020年修訂)[S]. 北京: 人民教育出版社, 2020: 2~4, 14~15, 30~33, 96~97.
[2][8]何彩霞主編. 核心素養導向的化學教學探索[M]. 北京: 北京教育出版社, 2019: 8, 2~3,
[3][7]譚湘湘, 何彩霞. 促進化學學科理解的單元教學實踐——以“離子反應”單元為例[J]. 化學教學, 2022,(11): 49~54.
[6]何彩霞. “促進學生問題解決思路形成”的遞進式教學——以“實驗探究化學反應發生的證據”為例[J]. 化學教學, 2018,(10): 51~57.
[9]陳鍵等. 物質分離的思維模型建構及其應用建議——基于混合物狀態組合轉化的視角[J]. 化學教學, 2023,(4): 91~93,97.

