基于學科大概念的高中化學單元教學設計與實施
化學是探索物質變化本質與規律的學科,高中化學課程致力于培養學生的科學素養和創新能力,基于學科大概念的高中化學單元教學設計可以更有效地實現這一目標。學科大概念涵蓋了化學的基本概念、原理和規律,是理解化學現象和解決問題的關鍵。本文以魯教版高中化學必修2“元素周期表的應用”為例,探討了基于學科大概念的教學設計與實施策略,期望為高中化學教師提供參考。
一、明確核心概念,引入新課內容
核心概念既是構建教學框架的基礎,也是學生掌握周期表應用的關鍵,教師在明確了核心概念后,需要構建邏輯清晰、層次分明的單元教學框架,這一框架應包括以下幾個層次:回顧原子結構和元素周期律的基礎知識;深入剖析元素周期表的編排規律和元素性質的周期性變化;通過具體案例和實驗,引導學生學習如何利用元素周期表預測元素性質;指導化學反應等實際應用,總結歸納周期表的應用方法和技巧。
在教學“元素周期表的應用”時,教師首先帶領學生回顧了元素周期表的基本結構。周期表是按照原子序數遞增的順序排列,每一橫行構成一個周期,每一縱列形成一個族,這樣的編排方式不僅清晰地展示了元素的排列順序,還揭示了元素性質的周期性變化規律。緊接著,教師提出問題,引導學生思考:“什么是元素性質的周期性變化規律呢?為什么元素性質會呈現出這樣的周期性變化規律?”通過這些問題,教師成功激起了學生的好奇心和求知欲。隨后,教師詳細解釋了元素性質的周期性變化規律。教師指出,隨著原子序數的遞增,元素的性質會呈現出周期性的變化,這種變化不僅體現在元素的物理性質上,如熔沸點、密度等,還體現在元素的化學性質上,如化合價、化學反應活性等。元素性質會呈現這種周期性的變化規律,與其原子結構有著密切聯系,隨著原子序數的遞增,原子核外電子的排布也會發生變化,這直接影響了元素的性質。最后,教師表示本節課將通過一系列的實驗,深入學習元素周期表的應用,并鼓勵學生認真聽講,積極參與討論,共同掌握這一強大的化學工具。通過這樣的教學過程,教師成功地引出了“元素性質的周期性變化規律”這一核心概念。
二、整合教學資源,提高實踐能力
為了有效實施單元教學,教師需整合教學資源,采用多樣化教學手段,激發學生的學習興趣,幫助學生深入理解學科大概念,進而提升化學素養和綜合能力。在教學“元素周期表的應用”時,教師可借助教材、多媒體課件、網絡資源等,將抽象的元素周期表知識以直觀、生動的形式呈現給學生,利用圖片、動畫等方式展示元素周期表的構成和規律,幫助學生形成直觀認識,同時,通過小組討論、案例分析等多樣化的教學手段,引導學生積極參與課堂活動,發揮主體作用。針對實驗探究環節,教師可以設計一系列實驗,通過實驗操作、觀察和分析,學生可以加深對元素周期表的理解,這里通過比較鈉、鎂和鋁的金屬性強弱,以及氯、溴和碘的非金屬性強弱,來探索同周期、同主族元素的遞變規律。
實驗一:比較鈉、鎂和鋁的金屬性強弱實驗
教師:在之前的學習中,大家已經了解了鈉與水反應的現象,現在請大家回憶一下,鈉與水反應時會出現什么現象呢?
學生:鈉與水反應時會迅速浮在水面上,并發出“嘶嘶”的響聲,同時產生大量氣泡,這些氣泡就是氫氣(見圖1、表1)。
教師:那么鎂與冷水和熱水反應的現象又有什么不同呢?實驗中為什么要將鎂條用砂紙打磨至光亮?請大家認真觀察并記錄實驗現象(見圖2、表2)。
學生:Mg是強氧化劑,放置在空氣中有MgO生成,MgO是氧化物,氧化反應的速度比較慢,把鎂條打磨至光亮,是為了讓單質鎂能以最大的面積接觸空氣中的氧氣。
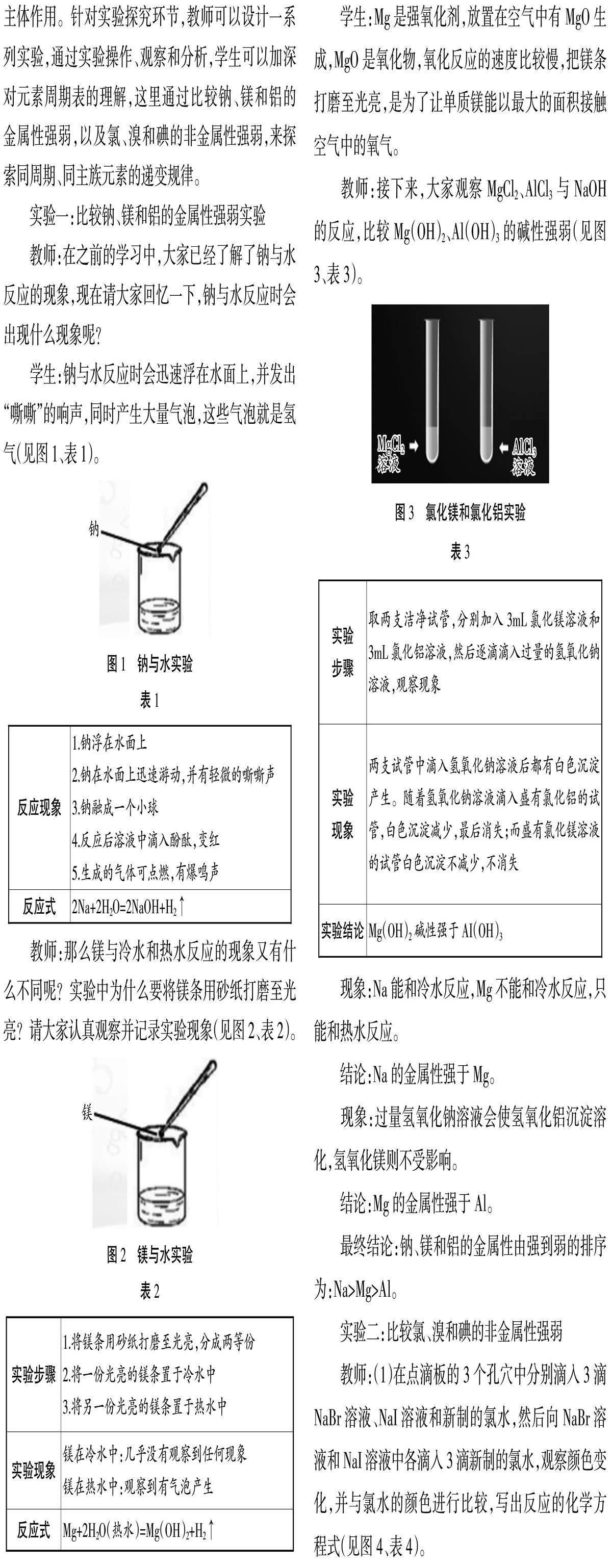
教師:接下來,大家觀察MgCl2、AlCl3與NaOH的反應,比較Mg(OH)2、Al(OH)3的堿性強弱(見圖3、表3)。
現象:Na能和冷水反應,Mg不能和冷水反應,只能和熱水反應。
結論:Na的金屬性強于Mg。
現象:過量氫氧化鈉溶液會使氫氧化鋁沉淀溶化,氫氧化鎂則不受影響。
結論:Mg的金屬性強于Al。
最終結論:鈉、鎂和鋁的金屬性由強到弱的排序為:Na>Mg>Al。
實驗二:比較氯、溴和碘的非金屬性強弱
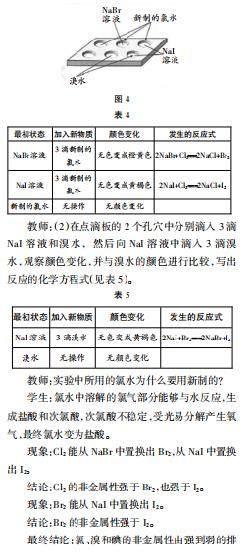
教師:(1)在點滴板的3個孔穴中分別滴入3滴NaBr溶液、NaI溶液和新制的氯水,然后向NaBr溶液和NaI溶液中各滴入3滴新制的氯水,觀察顏色變化,并與氯水的顏色進行比較,寫出反應的化學方程式(見圖4、表4)。
教師:(2)在點滴板的2個孔穴中分別滴入3滴NaI溶液和溴水,然后向NaI溶液中滴入3滴溴水,觀察顏色變化,并與溴水的顏色進行比較,寫出反應的化學方程式(見表5)。
教師:實驗中所用的氯水為什么要用新制的?
學生:氯水中溶解的氯氣部分能夠與水反應,生成鹽酸和次氯酸,次氯酸不穩定,受光易分解產生氧氣,最終氯水變為鹽酸。
現象:Cl2能從NaBr中置換出Br2,從NaI中置換出I2。
結論:Cl2的非金屬性強于Br2,也強于I2。
現象:Br2能從NaI中置換出I2。
結論:Br2的非金屬性強于I2。
最終結論:氯、溴和碘的非金屬性由強到弱的排序為:Cl2>Br2>I2。
通過實驗,學生得出了鈉、鎂和鋁的金屬性遞變規律,以及氯、溴和碘的非金屬性遞變規律,這些規律不但適用于這些特定的元素,而且在整個元素周期表中都有廣泛應用。
三、建立評價體系,促進持續發展
在單元教學的實施過程中,建立科學的評價體系是至關重要的,評價體系不僅是對學生學習成果的檢驗,還是對教學質量的反饋和提升。一個完善的評價體系應關注學生的學習過程、理解程度以及應用能力等多個維度,以全方位地衡量學生的學習狀態。
從學習過程來看,教師需要建立一種過程性評價機制,通過觀察學生在課堂上的表現、參與討論的情況、合作完成任務的能力等方面評價學生的學習狀態,這種評價方式能夠更真實地反映學生的學習情況,幫助學生發現自己的優點和不足,從而調整學習策略。從學生對知識的理解程度來評價學生的學習成果時,教師可以設置一些開放性問題或案例分析題來考查學生的思考深度和廣度,從而更全面地評價學生的學習成果。從應用能力來評價學生的學習成果時,教師應注重考查學生的應用能力,可以通過組織一些實踐活動或項目任務讓學生應用所學知識,并通過觀察學生的表現來評價學生的應用能力。
為了建立這樣一個評價體系,教師可以采用多種評價方式:課堂表現可以作為評價學生學習態度、參與度和表達能力的一個重要依據,作業完成情況則可以反映學生對課堂知識的理解和掌握程度,實驗報告則可以考查學生的實驗技能和科學思維等方面。此外,教師還可以采用問卷調查、個別談話等方式來獲取更全面的評價信息。需要注意的是,評價體系的建立不僅僅是為了給學生打分,更重要的是通過評價結果的反饋教學和學習:教師應根據評價結果及時調整教學策略,針對學生的不足進行有針對性的指導,幫助學生克服學習困難,增強學習效果;學生應根據評價結果了解自己的不足和進步方向,調整學習策略,努力提升自己的學習水平。
四、教學總結
基于學科大概念的高中化學單元教學設計與實施策略,有助于提升學生的化學學科素養。通過這一教學策略,教師得以將復雜的化學知識系統化、結構化,使學生能夠在更廣闊的視野下理解化學現象。在未來的教學實踐中,教師應繼續探索和完善這一策略,結合具體的教學內容和學生特點,靈活運用各種教學方法和手段,以實現教學效果的最優化。
(作者單位:山東省曹縣第一中學)
編輯:陳鮮艷
作者簡介:胡華(1970—),男,漢族,山東曹縣人,大學本科,一級教師,研究方向:高中化學教學。

