環丙烯酮及其衍生物反應研究

摘 要: 環丙烯酮擁有著最小的芳香環結構,因此具有十分特殊的結構性質,能通過開環釋放環張力斷裂碳碳鍵,該反應特性在有機合成方面得到很大的發展。闡述了環丙烯酮及其衍生物作為反應底物于不同條件下進行開環反應的方法,并對該方法存在的優缺點進行了總結。
關 鍵 詞:環丙烯酮;催化劑;開環反應;環加成反應
中圖分類號:TQ224.23文獻標志碼: A 文章編號:文章編號: 1004-0935(2024)09-1462-04
環丙烯酮擁有著最小的芳香環結構,因此具有十分特殊的結構性質,通過開環釋放環張力斷裂碳碳鍵這一反應特性得到科學界廣泛關注和研究[1-2]。環丙烯衍生物存在于許多天然的脂肪酸中,例如錦葵酸等常被用作動物異常產生的病原體[3]。和環丙烯一樣,環丙烯酮同樣也是構建眾多骨架的重要選擇[4],近5年來在對于環丙烯酮及其衍生物的合成與反應方面取得了許多新的進展,盡管自然界中環丙烯酮的起源尚未完全闡明,但是已有部分天然產物已經被分離、合成并用來研究構效關系,用于細胞毒性以及抑制劑等[5]。
1 環丙烯酮及其衍生物的研究進展
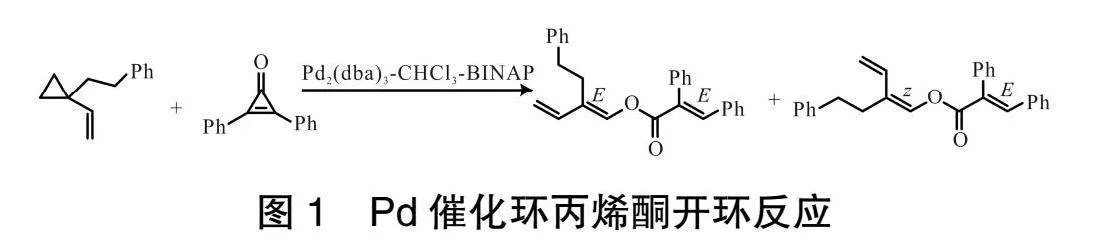
2022年,WU課題組[6]報道了通過Pd催化環丙烯酮與環乙烯基衍生物的選擇性開環反應,通過市售的Pd(dba)·CHCl-BINAP催化劑能夠實現可觀的產率以及優異的區域選擇性,得到系列共軛醇二烯羧酸酯,實現了兩性離子Π-烯丙基鈀中間體在有機合成中的新應用,如圖1所示。
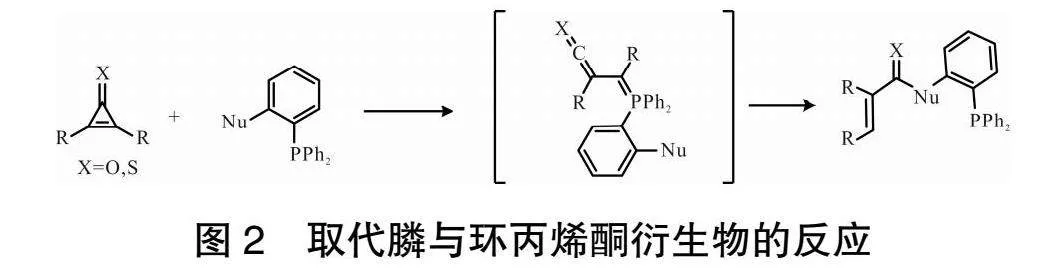
2018年,DAVID等[7]通過取代的芳香叔膦與烷基取代的環丙烯酮進行反應,生成了對應的硫羰基化合物,該產物在生物環境中十分穩定,可用于體外和細胞裂解液中的生物分子標記,并且環丙烯酮的反應快速性以及生物相容性表明了這類產物將成為十分有效的細胞研究中的探針。取代膦與環丙烯酮衍生物的反應如圖2所示。
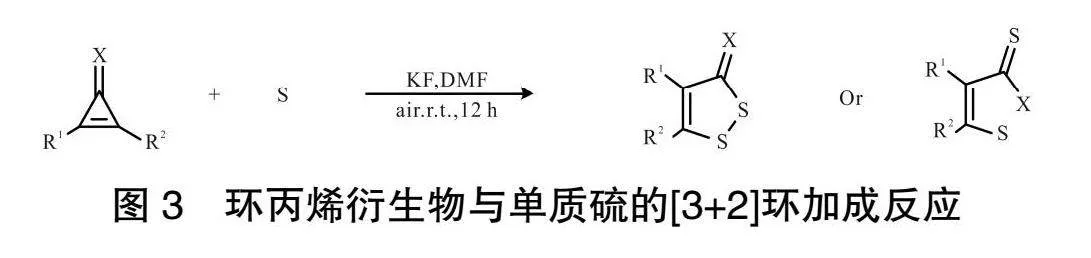
2020年,WU課題組[8]通過取代的環丙烯酮與單質硫進行反應,實現特殊的[3+2]環化過程,如圖3所示。與其他環丙烯酮衍生物有所不同,環丙烯酮會在與硫的作用下發生特殊的重排反應,高效合成了系列1,2-二硫雜環。該方案反應條件溫和,產率表現優異,有著優秀的原子經濟性以及區域選擇性好。
2020年,WU團隊[9]開發了一種銠(Ⅲ)催化環丙烯酮和 β-酮磺酰硫葉立德的[3+3]環加成反應,來制備一系列2-吡喃酮類衍生物。該方法通過 C—C 鍵斷裂使金屬卡賓插入來獲得中等至優異的產率的三取代 2-吡喃酮。
NGUYEN等[10]在2019年報道了醇取代的環丙烯酮在三苯基膦催化下在甲醇中自身開環并環合的反應,得到了對應的取代丁烯內酯。該方法能兼容廣泛的官能團,產生各種對應的α-以及γ-取代的丁烯內酯。
2021年,RAVIKUMAR[11]以醋酸鈀作為催化劑,以二苯基環丙烯酮與苯酚作為反應底物,加入合適的配體以及堿的作用下通過活化C—C鍵后,反應生成了對應的α, β-不飽和酯,并且能通過此條件同樣生成共軛的酰胺。
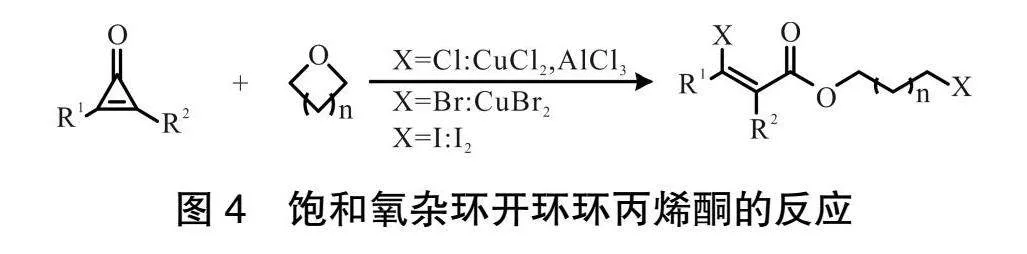
2021年,WU課題組[12]通過鹵化銅或者單質碘促進下實現了通過飽和氧雜環開環環丙烯酮的反應,如圖4所示。該反應為3-不飽和鹵酸酯的合成提供了一種高效的途徑,并且在一鍋法開環后在斷裂了1個C—O鍵以及2個C—C鍵的情況下,為產物結構提供了2個C—X鍵以及1個C—O鍵。
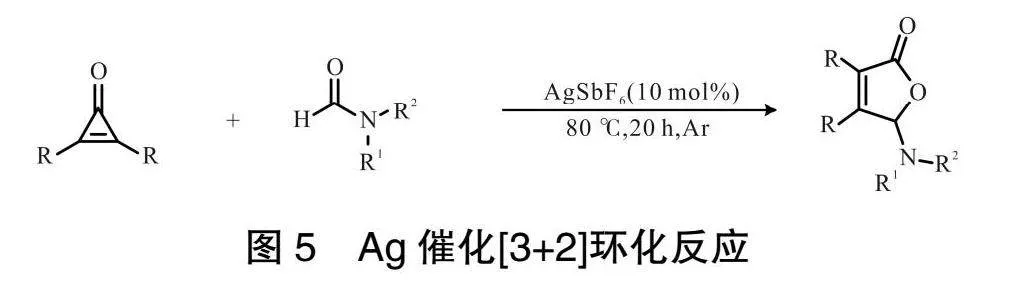
2018年,SUN課題組[13]提出了一種未被研究過的以Ag催化的C—C鍵裂解環化環丙烯酮與DMF(N,N-二甲基甲酰胺)發生[3+2]環化反應,如圖5所示。該方案表現出了優異的化學以及區域選擇性,并且官能團的兼容性優異,開發了一種全新的途徑來構建γ-氨基丁烯內酯,并且酯類化合物也能夠與環丙烯酮反應,得到相應的酯交換結果產物。
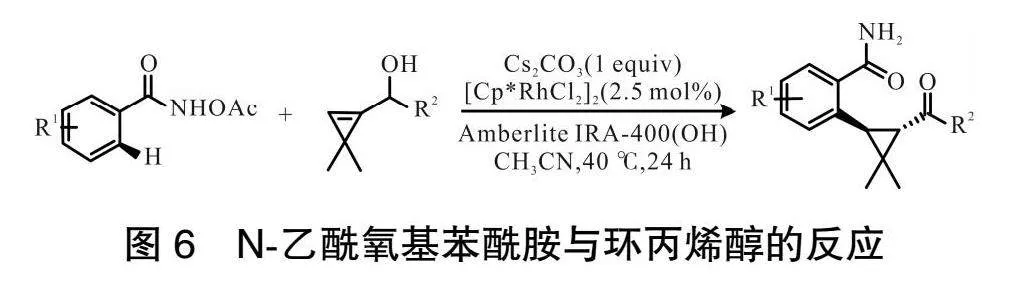
2020年,YI課題組[14]通過使用協同雙定向基團輔助C—H活化的策略,采用類似的反應條件,實現了Cp*Rh(III)催化的N-乙酰氧基苯酰胺與環丙烯醇的C-H環丙基化,為正反式以及順式1,1-二甲基環丙烷功能化苯酰胺提供了區域選擇性、化學選擇性以及對映選擇性的途徑,如圖6所示。
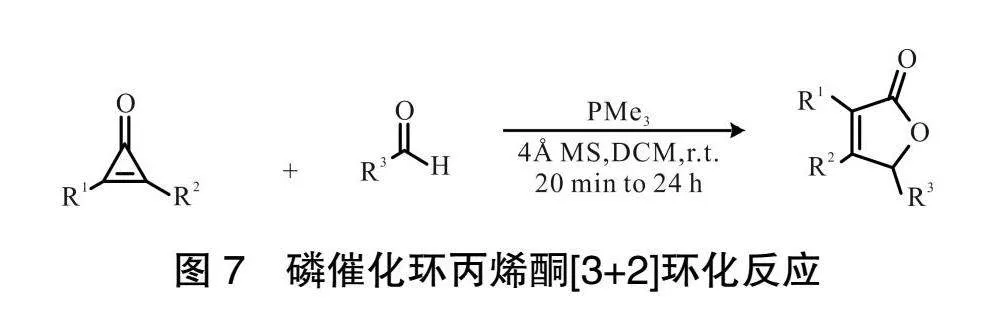
2022年,XU課題組[15]報道了關于膦催化環丙烯酮衍生物的[3+2]環化反應,如圖7所示。其反應產物包括醛類、酮酯類、亞胺類、異氰酸酯類以及碳二亞胺類的反應物,產率高,該反應底物范圍十分廣泛,并且官能團耐受性良好。
2018年,WU課題組[16]發現在室溫條件下鈀催化的環丙烯酮與有機硼酸的開環酰化反應,該方法適用于芳基硼酸和乙烯基硼酸,并且有良好收率和優異立體選擇性,為合成α,β-二芳基不飽和酮提供了新的策略。研究表明,在該反應中生成了乙烯基鈀中間體。
2018 年,ZHAO 團隊[17]研發了環丙烯酮的C—C鍵斷裂與(苯并)硅環丁烷的C—Si鍵之間的第一個分子間鍵交叉交換反應。這種簡單的[3+4]環加成方法,合成了多種硅(苯并)二環衍生物,并且考慮到(苯并)二環和(苯并)氧雜環戊烯酮的結構在藥物化學和天然產物中的重要性。
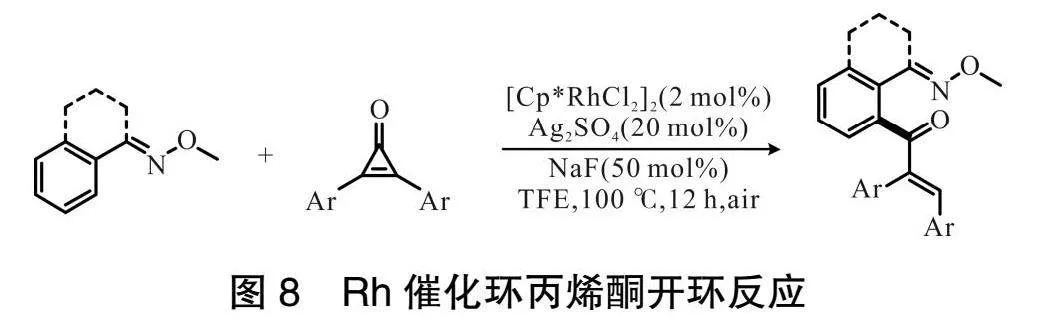
2020 年,CHEN 課題組[18]描述了通過 Rh 催化 O-甲基酮肟鄰位 C—H 鍵活化與環丙烯酮合成查耳酮的丙烯酸酯化反應,如圖8所示。這種交叉偶聯反應展現出高的官能團耐受性和區域選擇性,并且在溫和的條件下可以得到多種查爾酮衍生物。
XU等[19]開發了一種Ag催化下的環丙烯酮與硝酮加成的反應,通過C—C鍵的斷裂來合成酰亞胺,如圖9所示。此外,該方案不僅為由不同的硝酮合成各種酰亞胺提供了一種新的合成方法,而且拓寬了環丙烯酮作為3C合成子的應用。
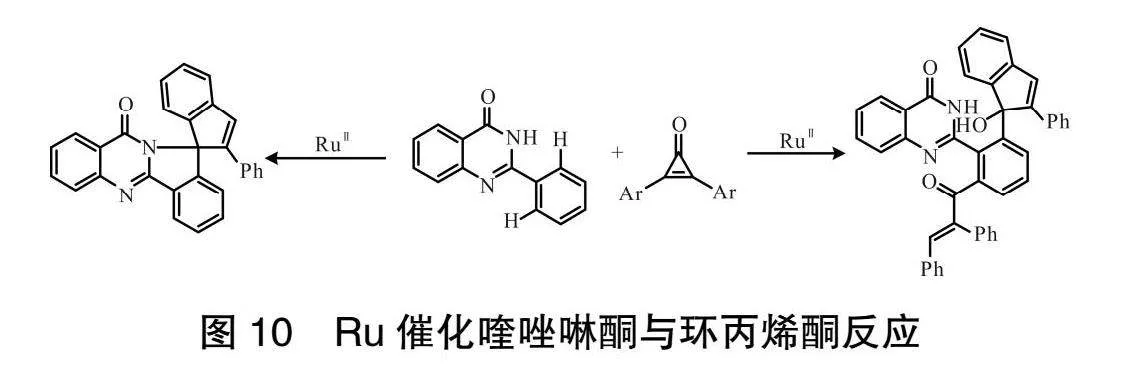
WU 課題組[20]報道了貴金屬釕催化喹唑啉酮的C—H 活化與環丙烯酮快速構建多種喹唑啉酮衍生物,如圖10所示。其中,催化劑在反應的轉化中起著重要作用。此外,該方法能得到高效率和良好的化學區域選擇性目標產物,并具有廣泛的底物范圍。
2019年,HAITO等[21]利用Rh(I)催化的環丙烯酮與酰胺[3+2]環化反應,來制備高度取代的 α,β-不飽和γ-內酰胺衍生物。酰胺上氮原子上的烷基對反應的成功至關重要,且反應表現出高的官能團相容性。
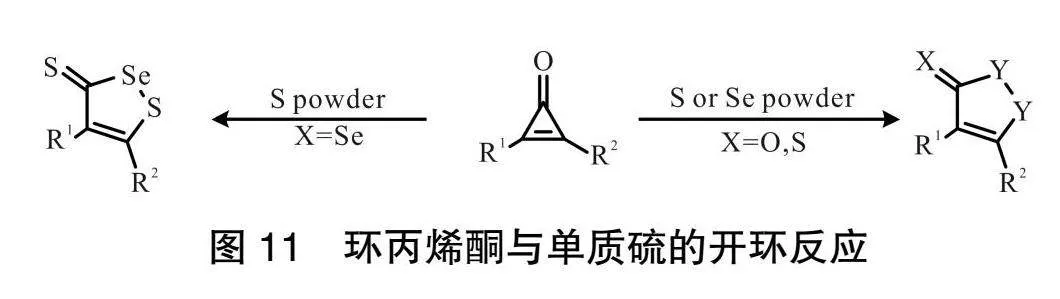
2020 年,WU課題組[8]研究發現通過環丙烯酮衍生物和單質硫或者單質硒的[3+2]環加成合成 1,2-二氫雜環的高效方法,如圖11所示。與其他環丙烯酮衍生物不同,環丙烯酮與單質硫會經歷前所未有的重排。該方法特點包括反應條件溫和、效率高、原子經濟性好、克級能力和良好的區域選擇性。
2018年,SHI等[22]通過環丙烯酮和環丙烯硫酮與酰胺在堿的促進下發生[3+3]環加成反應來制備 6H-1,3-噁嗪-6-酮和6H-1,3-噻嗪-6-酮衍生物。這些反應在無金屬和溫和條件下表現出極好的收率和良好的官能團耐受性。
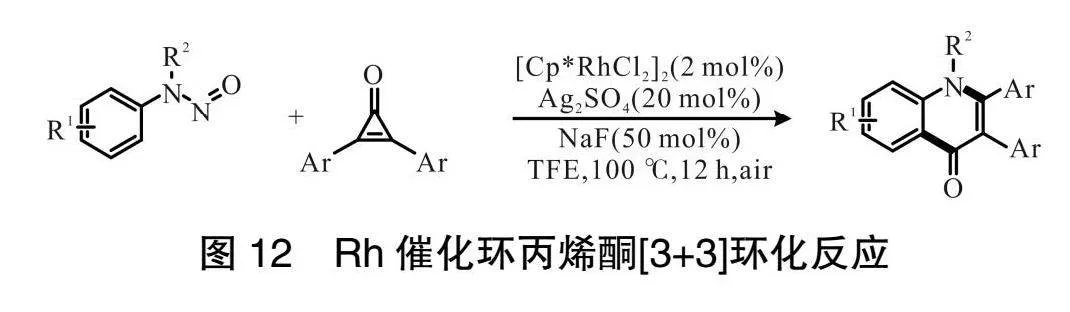
2019 年,CHEN 課題組[23]報告了Rh(Ⅲ)催化 N-亞硝基苯胺和環丙烯酮通過[3+3]環加成反應來制備功能化的4-喹諾酮類藥物,如圖12所示。該反應允許 C—C 鍵斷裂,并通過 N-亞硝基導向的 C—H 活化作用構建 C—C 和 C—N 鍵。通過使用不對稱的間位取代的 N-亞硝基苯胺達到良好的區域選擇性。用這種方法,在溫和的條件下以中等到良好的產率得到各種4-喹諾酮衍生物。
2020 年,WU課題組[24]利用廉價金屬 AgO 促進環丙烯酮與肟的[3+3]環加成反應來制備 1,3-惡嗪酮的衍生物。該方法突出了環丙烯酮的新反應性,該環丙烯酮與肟進行1,4-加成,然后通過β-碳消除反應原位生成α-羰基乙烯酮中間體。
2 結束語
環丙烯酮作為最小的芳香環化合物,其特殊的 骨架以及性質成了有機化合物中最特別的結構之一,對于環丙烯酮結構特點的研究以及合成路徑的開發對于各類藥物中間體的合成都有著一定的意義。對于其C—C鍵的斷裂手段以及更加綠色的反應條件的探索,仍需要有機化學家們的不懈研究與努力。
參考文獻:
[1] GREENBERG A, TOMKINS R P T, DOBROVOLNY M, et al. The strain energy of diphenylcyclopropenone: A reexamination[J]. , 1983, 105(23): 6855-6858.
[2] BUDZELAAR P H M, KRAKA E, CREMER D, et al. Long interbridge- head bonds in acceptor-substituted bicyclobutanes[J]. , 1986, 108(4): 561-567.
[3] SHENSTONE F S, VICKERY J R. Occurrence of cyclo-propene acids in some plants of the order Malvales[J]. , 1961, 190: 168-169.
[4] KOMATSU K,KITAGAWA T. Cyclopropenylium cations, cyclopro- penones, and heteroanaloguesrecent advances [J]. ., 2003, 103: 1371-1427.
[5] REBER K P, GILBERT I W, STRASSFELD D A, et al. Synthesis of (+)-lineariifolianone and related cyclopropenone-containing sesquiterpenoids[J]. , 2019, 84(9): 5524-5534.
[6] LU L G, CHEN J H, HUANG X B, et al. Palladium-catalyzed ring-opening reaction of cyclopropenones with vinyl epoxides[J]. , 2022, 87(24): 16851-16859.
[7] ROW R D, PRESCHER J A. A cyclopropenethione-phosphine ligation for rapid biomolecule labeling[J]. , 2018, 20(18): 5614-5617.
[8] WU J,GAO W X,HUANG X B,et al.Selective [3 + 2] cycloaddition of cyclopropenone derivatives and elemental chalcogens [J].2020, (14: 5555-5560.
[9] ZHOU P, YANG W T, RAHMAN A U, et al. Rh(Ⅲ)-catalyzed[3+ 3]annulation reaction of cyclopropenones and sulfoxonium ylides toward trisubstituted 2-pyrones[J]. , 2020, 85(2): 360-366.
[10] NGUYEN S S, FERREIRA A J, LONG Z G, et al. Butenolide synthesis from functionalized cyclopropenones[J]. , 2019, 21(21): 8695-8699.
[11] NANDA T, BISWAL P, PATI B V, et al. Palladium-catalyzed C-C bond activation of cyclopropenone: modular access to trisubstituted -unsaturated esters and amides[J]. , 2021, 86(3): 2682-2695.
[12] MIAO W H, GAO W X, HUANG X B, et al. Cascade ring-opening dual halogenation of cyclopropenones with saturated oxygen heterocycles[J]. , 2021, 23(24): 9425-9430.
[13] REN J T, WANG J X, TIAN H, et al. Ag(I)-catalyzed[3+2]-annulation of cyclopropenones and formamides via C—C bond cleavage[J]. , 2018, 20(21): 6636-6639.
[14] WU M, LIN S, ZHU G X, et al. Synergistic dual directing groups-enabled diastereoselective C—H cyclopropylation Rh(Ⅲ)- catalyzed couplings with cyclopropenyl alcohols[J]. , 2020, 22(4): 1295-1300.
[15] HE X, MA P, TANG Y, et al. Phosphine-catalyzed activation of cyclopropenones: a versatile Csynthon for (3+2) annulations with unsaturated electrophiles[J]., 2022, 13(43): 12769-12775.
[16] SHAN L D, WU G, LIU M C, et al. Α, β-Diaryl unsaturated ketonespalladium-catalyzed ring-opening of cyclopropenones with organo-boronic acids[J]., 2018, 5(10): 1651- 1654.
[17] ZHAO W T, GAO F, ZHAO D. Intermolecular Σ-Bond cross-exchange reaction between cyclopropenones and (Benzo)silacyclobutanes: straightforward access towards Sila(benzo)cycloheptenones[J].(.), 2018, 57(21): 6329-6332.
[18] LIU Y F, TIAN Y, SU K X, et al. Rhodium-catalyzed-acrylation of aryl ketone-methyl oximes with cyclopropenones[J]., 2020, 18(20): 3823-3826.
[19] XU J L, TIAN H, KANG J H, et al. Ag(I)-catalyzed addition of cyclopropenones and nitrones to access imides[J]., 2020, 22(17): 6739-6743.
[20] SHI Y, HUANG T,WANG T, al et. Divergent construction of diverse scaffolds through catalyst-controlled c [J].. 2021, 27:13346-13351.
[21] HAITO A, CHATANI N. Rh(I)-Catalyzed[3+2]annulation reactions of cyclopropenones with amides[J]., 2019, 55(40): 5740-5742.
[22] NIU B, JIANG B, YU L Z, et al. Base-promoted[3+3]cyclization of cyclopropenones and cyclopropenethiones with amides for the synthesis of 6H-1, 3-oxazin-6-ones and 6H-1,3-thiazin-6-ones[J]., 2018, 5(8): 1267-1271.
[23] LIU Y F, TIAN Y, SU K X, et al. Rhodium(Ⅲ)-catalyzed[3+ 3]annulation reactions of-nitrosoanilines and cyclopropenones: an approach to functionalized 4-quinolones[J]., 2019, 6(24): 3973-3977.
[24] YANG Y F, HUANG X B, GAO W X, et al. AgO-promoted ring- opening reactions of cyclopropenones with oximes[J]., 2020, 18(30): 5822-5825.
Study on Reaction of Cycloallenone and Its Derivatives
CHEN Zhibin,LIANG Chen
(College of Chemistry and Material Engineering, Wenzhou University, Wenzhou Zhejiang 325035, China)
Abstract:Cycloallenone has the smallest aromatic ring structure, possessinga very special structural property. It can cleave carbon-carbon bond by ring opening and releasing ring tension. This reaction property has been greatly developed in organic synthesis. In this paper, application of cycloallenone and its derivatives as substrates to synthesize various kinds of characteristic compounds by ring-opening reaction under different conditions wassummarized, and itsadvantages and disadvantages werediscussed.
Key words: Cycloallenone; Catalysis; Ring-opening reaction;Cycloaddition reaction

