葉黃素對大鼠骨髓間充質干細胞成骨分化的影響分析

[摘要]目的:研究葉黃素對大鼠骨髓間充質干細胞成骨分化的作用。方法:挑選5周齡SPF級健康雌性SD大鼠,在體外分離培養大鼠骨髓間充質干細胞傳至第三代后進行細胞流式鑒定;細胞增殖實驗觀察不同濃度葉黃素(1.25、2.5、5 μmol/L)對大鼠骨髓間充質干細胞增殖的影響,以確定葉黃素的最終使用濃度。后續實驗分三組:對照組(α-MEM培養基)、成骨培養基組和結合組(成骨培養基+葉黃素)。成骨誘導分化第7、21天時,分別用堿性磷酸酶及茜素紅染色法研究成骨細胞礦化過程中不同時間點礦化結節生成;成骨誘導第5天,蛋白免疫印跡法觀察骨髓間充質干細胞成骨分化相關基因核心結合蛋白因子2(Runt-related transcription factor 2,Runx2)骨形態發生蛋白2(Bone morphogenetic protein,BMP2)、骨橋蛋白(Osteopontin,OPN)和甘油醛-3-磷酸脫氫酶(Glyceraldehyde-3-phosphate dehydrogenase,GAPDH)蛋白表達水平。結果:第3代細胞表面抗原中CD29、CD90的陽性表達率為97.7%、74.8%,CD34、CD45陰性表達率為0.03%、1.61%;CCK-8細胞增殖實驗發現,隨著葉黃素濃度的增加至5 μmol/L,骨髓間充質干細胞的活力受到抑制,從而影響其正常的生物學功能。由此確定葉黃素最終使用濃度為2.5 μmol/L;堿性磷酸酶染色及茜素紅染色結果顯示,葉黃素能抑制細胞堿性磷酸酶的表達,降低骨礦化能力;Western blot結果顯示,葉黃素可使RUNX2、BMP2、OPN蛋白表達量下降。結論:葉黃素對大鼠BMSCs成骨分化有明顯的抑制作用。
[關鍵詞]葉黃素;骨髓間充質干細胞;成骨分化;創傷性顳下頜關節強直;堿性磷酸酶
[中圖分類號]TQ461" " [文獻標志碼]A" " [文章編號]1008-6455(2025)01-0001-05
Effect of Lutein on Osteogenic Differentiation of Rat Bone Marrow Mesenchymal Stem Cells
GUO Sha1, Maimaitiaili·MAIMAITIMIN2, YAO Zhitao1,3
( 1.Orthognathic Surgery of Oral-maxillofacial Trauma, the First Affiliated Hospital of Xinjiang Medical University, Urumqi 830054, Xinjiang, China; 2. Department of Prosthodontics and Implant, the First Affiliated Hospital of Xinjiang Medical University, Urumqi 830054, Xinjiang, China; 3. Xinjiang Institute of Stomatology, Urumqi 830054, Xinjiang, China )
Abstract: Objective" To study the effect of lutein on osteogenic differentiation of rat bone marrow mesenchymal stem cells. Methods" 5-week-old SPF-grade healthy female SD rats were isolated and cultured in vitro, and then the mesenchymal stem cells were transferred to the third generation for cell flow identification. The effects of different concentrations of lutein (1.25, 2.5, 5 μmol/L) on the proliferation of rat bone marrow mesenchymal stem cells were observed in cell proliferation experiment to determine the final concentration of lutein. The follow-up experiments were divided into 3 groups: control group (α-MEM medium), osteogenic medium group, and combination group (osteogenic medium + lutein). On the 7th and 21st day of osteogenic differentiation, alkaline phosphatase and alizarin red staining were used to study the formation of mineralized nodules at different time points during the mineralization of osteoblasts. On the 5th day of osteogenic induction, runt-related transcription factor 2 of bone marrow mesenchymal stem cells was observed by western blotting. Runx2) bone morphogenetic protein 2 (BMP2), osteopontin (OPN), and glyceraldehyde 3-phosphate dehydrogenase (glyceraldehyde 3-phosphate) dehydrogenase (GAPDH) protein expression levels. Results" The third generation cell surface antigen, the positive expression rates of CD29 and CD90" were 97.7% and 74.8%, and the negative expression rates of CD34 and CD45 were 0.03% and 1.61%. CCK-8 cell proliferation experiment showed that with the increase of lutein concentration to 5 μmol/L, the activity of bone marrow mesenchymal stem cells was inhibited, thus affecting their normal biological function. The final concentration of lutein was determined to be 2.5 μmol/L. The results of alkaline phosphatase staining and alizarin red staining showed that lutein could inhibit the expression of alkaline phosphatase and reduce the mineralization ability of bone. Western blot results showed that lutein decreased the expression levels of RUNX2, BMP2 and OPN proteins. Conclusion" Lutein can significantly inhibit osteogenic differentiation of BMSCs in rats.
key words: lutein; bone marrow mesenchymal stem cells; osteogenic differentiation; traumatic temporomandibular joint ankylosis; alkaline phosphatase
顳下頜關節強直(Ankylosis of temporomandibularjoint,TMJA)是指各種原因引起的一側或雙側關節內發生病變,造成關節內纖維性或骨性粘連,導致患者張口受限、咀嚼困難,創傷是其主要病因[1-2]。目前,創傷性TMJA的發生機制闡述仍未統一。近年來,隨著組織工程學理論和技術的不斷進步,以骨髓間充質干細胞(Bone mesenchymal stem cells,BMSCs)為種子細胞的組織工程技術為骨損傷修復帶來了新的希望。
來源于中胚層的骨髓間充質干細胞(BMSCs),能夠進行自我更新,從而可實現多種不同的發育方式。因其易于在體外擴增、易于外源基因導入,現已成為骨組織修復領域重要的種子細胞[4]。對于TMJA,關節損傷后局部微環境改變,出現局部成骨因子表達增強的“異常骨愈合”現象,其局部微環境發生改變,可能促使TMJ間充質干細胞定向遷移至骨斷端之間并主要向成骨方向分化,破壞了關節區正常骨組織損傷后改建修復的穩態平衡[2]。因此,改善BMSCs成骨分化能力是防治顳下頜關節強直的關鍵。
葉黃素是一種含氧類胡蘿卜素,分子式為C40H56O2,分子量是568.85[6]。天然來源的葉黃素(Lutein),人工合成困難,只能通過天然植物來提取,故又有“植物黃體素”之稱[7]。藥用葉黃素不溶于水,易溶于油脂和脂溶性溶劑,儲存在2℃~8℃,避光防潮密閉干燥。葉黃素的生理功能主要體現在以下幾個方面:延緩動脈粥樣硬化[8];通過抑制活性氧自由基來抗氧化,增強人體免疫力[9];保護視力及預防白內障[10]。近年來的研究還發現其擁有一定的抗腫瘤[11-12]及調控破骨細胞代謝[10],但目前葉黃素對骨髓間充質干細胞的成骨分化影響尚未見報道。本實驗旨在探究葉黃素對大鼠骨髓間充質干細胞成骨分化的影響。
1" 材料和方法
1.1 實驗材料
1.1.1 實驗動物:Sprague Dawley(SD)大鼠(5周齡)購自新疆醫科大學第一附屬醫院醫學實驗動物中心。所有動物實驗均按照國家衛生研究院(NIH)實驗室動物護理原則指南(NIP出版物85-23,1996年修訂)進行,由新疆醫科大學第一附屬醫院實驗動物及應用監督委員會審定,倫理審批號為IACUC-20220442-18。
1.1.2 實驗試劑及儀器:葉黃素(北京索萊寶);大鼠骨髓間充質干細胞成骨誘導分化試劑盒(Oricell);α-MEM培養基、澳洲胎牛血清(Gibco);1%青鏈霉素、0.25%trypsin-0.02%EDTA消化液、PBS(Hyclone);流式細胞儀、CD34、45、29、90抗體(BD);堿性磷酸酶改良鈣鈷法染液(北京索萊寶);茜素紅染色液(北京索萊寶);CCK-8試劑盒(北京博奧森);PAGE凝膠快速制備試劑(Biotides);CO2恒溫培養箱、酶標儀(Thermo),倒置顯微鏡(Zeiss公司)。OPN、GAPDH、BMP2、羊抗鼠IgG、羊抗兔IgG抗體(Proteintech);RUNX2(Abcam)。
1.2 實驗方法
1.2.1 大鼠骨髓間充質干細胞的提取和培養:將5周齡大鼠頸部脫臼處死,置于75%醫用酒精中浸泡60 s,將大鼠股骨從周圍軟組織中取出,置于6 cm的培養皿中,用基礎培養基清洗。轉移至無菌超凈臺,將骨髓切成小塊,用含有20%胎牛血清(胎牛血清;Thermo)、1%青霉素、硫酸鏈霉素的a-MEM進行培養。去除非貼壁細胞,培養貼壁的骨髓間充質干細胞并擴增以供進一步實驗。當細胞培養融合度超過95%時,對粘附的骨髓間充質干細胞進行傳代。使用1~3代骨髓間充質干細胞進行研究實驗。
1.2.2 流式鑒定:將第3代細胞接種于培養瓶,在37℃,5% CO2培養箱內進行培養,當細胞生長至90%左右時,0.25%胰蛋白酶消化細胞,離心(1 500 rpm,3 min);棄上清液,在含有2%胎牛血清的PBS的離心管中重懸1×107細胞,與CD29(PE,1μl),CD34(1μl),CD45(Alexa 647,1μl)和CD90(PE,1μl)常溫避光孵育30 min。孵育結束后用PBS清洗,繼續300μl含有2%胎牛血清的PBS重懸細胞;200目篩網過濾。將上清液轉移到另一個離心管中進行流式細胞儀檢測。根據FlowJo7.7對實驗結果進行分析。
1.2.3 細胞增殖實驗:以每孔2×103為密度的第3代BMSCs接種入96孔板,并在培養基中加入不同濃度(1.25、2.5、5μmol/L)的葉黃素,以檢測其對細胞增殖活性的影響。實驗中采用CCK-8試劑盒來測定葉黃素對BMSCs細胞增殖的抑制作用。同時取出孔板將原液小心吸出,用PBS洗滌2次。將10% CCK-8工作溶液加入96孔板中的每一個含100 μl培養基的小孔中,培養箱避光孵育2 h,動態觀察工作液顏色變化。孵育結束后,將已完全反應的工作液轉移到新的96板中,利用全波長酶標儀,于450 nm處測定吸光度值。所有實驗均重復進行三次。
1.2.4 實驗分組及成骨誘導
1.2.4.1 實驗分組:①對照組(α-MEM)將第3代細胞接種于含α-MEM基礎培養基的T25培養瓶中;②成骨組將第3代細胞接種于含成骨細胞培養基的T25培養瓶中;③聯合組將第3 d細胞接種于含成骨細胞培養基與濃度為2.5 mol/L的葉黃素T25培養瓶中,均置于37℃,5% CO2培養箱內進行培養。
1.2.4.2 成骨誘導:將第3代BMSCs按2×104/孔接種于24孔平板上,每孔5×105接種于6孔板,1×106/皿接種于6 cm皿。每隔3 d更換一次新鮮專用成骨誘導培養基。
1.2.5 堿性磷酸酶染色:在成骨誘導培養第7天,從培養箱中取出6孔板置于超凈工作臺,去除孔內原有培養基后用PBS洗3次。每個孔添加40 g/L的多聚甲醛溶液固定,30 min后,將固定液丟棄,使用PBS清洗3次。根據試劑盒說明書,在每一個小孔中加入相應數量的染液,室溫孵育30 min,完成后用吸液槍將小孔中的染液吸凈,再用PBS沖洗3次,最后一遍保留孔內PBS并在倒置熒光顯微鏡下拍攝照片。
1.2.6 茜素紅染色:茜素紅染色在2.5μmol/L葉黃素濃度處理BMSCs后的第21天進行茜素紅染色測定,評估成骨細胞的骨質礦化情況。將6孔板從培養箱中取出,用吸液槍將原液吸取干凈后用PBS沖洗3遍;在每個孔中添加40 g/L的多聚甲醛溶液,固定15 min后棄固定液,PBS清洗3次。PBS清洗可以去除固定液中的有機成分,防止有機成分污染樣品,從而使樣品的分析結果更加準確可靠。清洗結束后,將500μl茜素紅染色工作液小心加入每孔內,室溫避光孵育30 min;孵育結束后棄染加PBS洗3次,最后一遍保留孔內PBS并在倒置熒光顯微鏡下拍攝照片。
1.2.7 Western Blot印跡法檢測:將1×106個細胞接種于6 cm皿中進行成骨誘導并用2.5μmol/L葉黃素處理后置于培養箱中培養5 d。隨后收集細胞,加入RIPA裂解液進行細胞裂解并在冰上靜置15 min后提取蛋白質。使用BCA蛋白檢測試劑盒(賽默費世爾科學公司)定量蛋白質濃度。用10%十二烷基硫酸鈉-聚丙烯酰胺凝膠制膠完成后,每孔加入等量蛋白質進行電泳,然后轉移到聚偏氟乙烯(PVDF)膜(Merch公司),用5%脫脂奶粉常溫下阻斷2 h;清洗,采用一抗RUNX2、BMP2、OPN、GAPDH在4℃冰箱中孵育過夜,二抗孵育1 h,沖洗曝光。
1.3 統計學分析:所有的實驗都至少進行了3次。實驗數據的處理采用SPSS 26.0軟件。計量數據用均值±標準差表示,用單因素方差分析多組間的差異,用最小顯著性差異進行成對比較,以P<0.05表示差異有統計學意義。
2" 結果
2.1 骨髓間充質干細胞形態及鑒定:分離提取得到的原代BMSCs正常培養狀態下,原代培養首次換液后,可見細胞呈圓形均勻鋪滿瓶底,培養72 h后的大鼠BMSCs細胞伸出偽足,多數細胞為梭形,有少量細胞呈多角形集落生長,
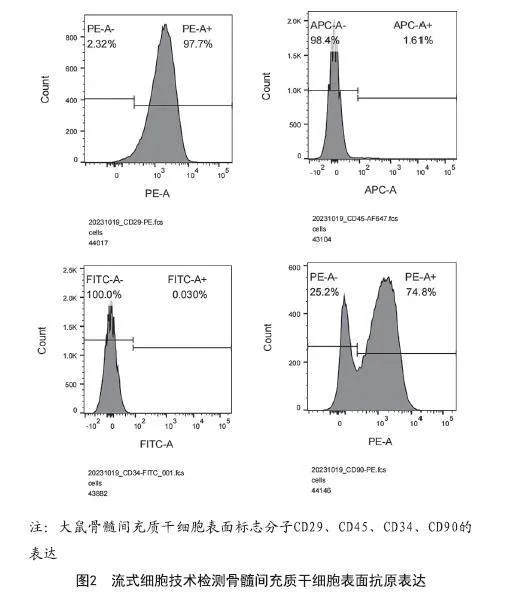
并相互融合成單細胞層(見圖1)。第3代細胞表面抗原中CD29、CD90的陽性表達率為97.7%、74.8%,CD34、CD45陰性表達率為0.03%、1.61%(見圖2)。該流式鑒定結果表明所提取的細胞是大鼠骨髓間充質干細胞。
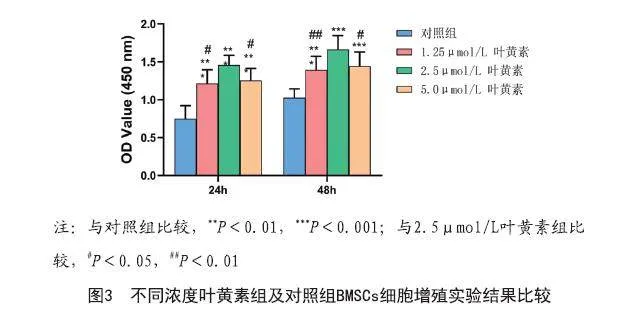
2.2 葉黃素對BMSCs增殖活性的影響:研究葉黃素對BMSCs增殖活性的影響,設定不同濃度的葉黃素(1.25、2.5、5μmol/L)干預BMSCs,采用CCK-8法測定24 h和48 h BMSCs的增殖情況,從而選定應用葉黃素的濃度。結果表明,與對照組相比,不同濃度葉黃素對BMSCs的增殖有明顯的促進作用。當葉黃素濃度大于2.5μmol/L時,隨著葉黃素濃度的升高,細胞的生長速度逐漸減慢。當葉黃素濃度為2.5μmol/L時BMSCs的增殖活性最高。由此,選擇葉黃素濃度2.5μmol/L進行下一步實驗。見圖3。
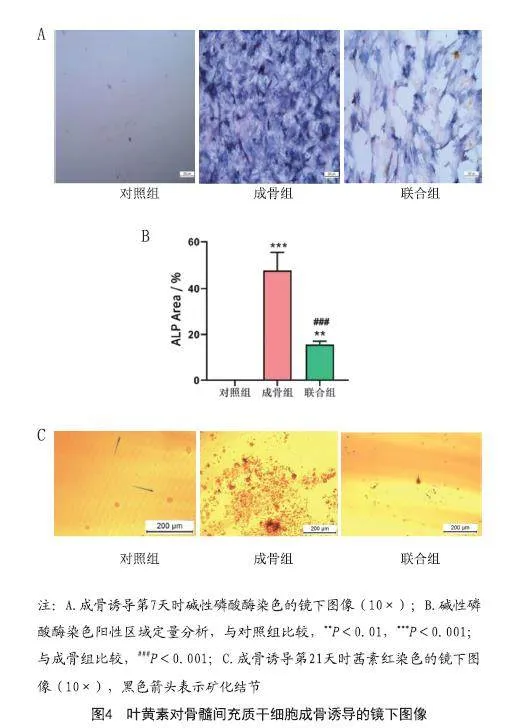
2.3 葉黃素對BMSCs成骨分化的作用:從CCK-8試驗的結果看,選2.5μmol/L葉黃素對骨髓間充質干細胞進行誘導成骨分化。結果顯示。成骨誘導第7天,通過堿性磷酸酶染色及堿性磷酸酶染色陽性區域的定量分析,與成骨組相比,聯合組骨髓間充質干細胞中的堿性磷酸酶表達及活性降低,差異具有統計學意義(P<0.001),見圖4A~B。成骨誘導第21天,通過茜素紅染色結果顯示,成骨組茜素紅特異性紅染的鈣化結節較多,染色最深,紅染斑塊面積最大,鈣化結節形成能力較強,見圖4C。
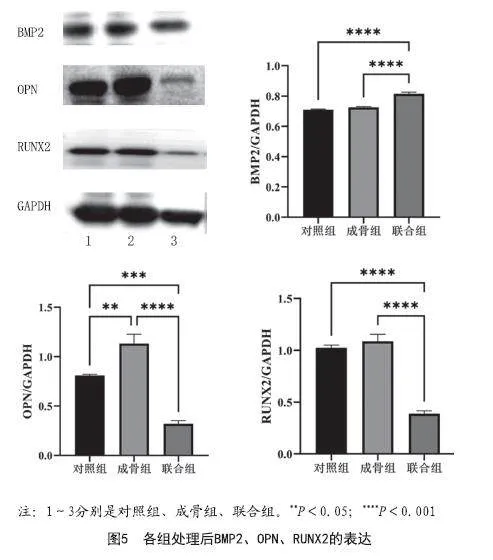
2.4 葉黃素對骨髓間充質干細胞成骨誘導后成骨相關蛋白表達的影響:成骨誘導5 d后,用免疫印跡法檢測成骨相關基因BMP2、OPN、RUNX2的蛋白表達量。根據WB實驗的條帶結果顯示,對照組與成骨組中BMP2、RUNX2的蛋白表達量比較差異均無統計學意義(P>0.05)。聯合組與成骨組相比,聯合組BMP2、OPN、RUNX2的蛋白表達量均低于成骨組,差異有統計意義(P<0.001),見圖5。以上結果證實,葉黃素可以通過某通路抑制骨髓間充質干細胞的成骨分化。
3" 討論
創傷性顳下頜關節(TMJ)強直(TMJA)是指創傷性誘導的髁突和TMJ窩之間的纖維或骨融合,骨損傷必然伴隨骨量缺失。一般情況下,正常骨組織具備強大的自我修復能力,可通過自體分泌骨生長因子與其他細胞因子、激素的協同作用下形成新骨,同時刺激破骨細胞,使新骨不斷塑形改建,從而使受損骨組織的結構和功能都得到恢復。而TMJA則是骨組織過度修復的表現[13]。這種情況可能導致慢性、持續性和進行性無法張開頜骨、面部畸形和阻塞性睡眠呼吸暫停-低通氣綜合征[14-15]。目前,間隙關節置換術截骨是緩解融合TMJ、緩解TMJA臨床癥狀的唯一有效治療方法。然而,由于該區域的神經、血管和顱底非常接近,這種手術具有挑戰性,技術要求很高[16]。但TMJA的確切分子機制尚不完全清楚。骨髓間充質干細胞在骨形成和骨折愈合中至關重要[17]。在修復過程中,這些細胞通過細胞因子和趨化因子,如骨形態發生蛋白(BMP2),從鄰近的骨、骨髓或其他組織被招募到損傷部位形成骨性強直[18-19]。Imai Y等[19]和Hofmann A等[21]發現參與肥厚性骨折不愈合的組織中含有可分化為成骨細胞的間充質干細胞,這進一步表明這些組織可能是骨形成的有效間充質干細胞。在建立TMJA動物模型時,Porto GG等[22]報道,與應用骨移植相比,應用BMSCs在TMJ損傷區域誘導了更多的骨形成和更嚴重的強直癥狀。目前,針對TMJA的防治方法包括切開復位內固定術、復位關節盤、開口牙合墊的使用及藥物干預。而在既往的研究中主要藥物為地塞米松,地塞米松屬于激素類藥物,長期服用可引起許多不良反應,如免疫系統下降、糖尿病、骨質疏松等。
葉黃素是一種含氧類胡蘿卜素,存在于各種瓜果蔬菜中,在萬壽菊中含量非常豐富[5]。近年來的研究還發現其擁有一定的抗腫瘤[11-12]及調控破骨細胞代謝作用[10]。但目前葉黃素對骨髓間充質干細胞的成骨分化影響國內外均未見報道。因此,利用葉黃素改善BMSCs向成骨分化的水平,對于有效預防TMJA的發生有重要的意義。
在本研究中,BMSCs在成骨誘導培養基中分別分化為成骨細胞且第三代細胞表達間充質表面標記物CD29、CD90,而細胞標志物CD34、CD45很少。這些結果表明,所提取的細胞均為骨髓間充質干細胞。BMSCs的成骨過程受到藥物、激素、細胞因子等多種因素的影響,因此相關因子來調控BMSCs的成骨分化可以為臨床上有效預防TMJA提供新策略。堿性磷酸酶是成骨細胞功能性酶,細胞堿性磷酸酶的活性和礦化結節形成是成骨細胞早期和中期成骨細胞分化的標志,也是BMSCs成骨分化的重要指征[23]。通過堿性磷酸酶染色來檢測骨髓間充質干細胞的成骨活性,從而確定其成骨能力。茜素紅染色法測定成骨組織中鈣質結節的數量。兩種染色方法提示,葉黃素可影響BMSCs成骨向分化,可減少ALP的表達,并抑制其骨礦化,因此可推測葉黃素對BMSCs成骨分化具有一定的抑制作用。此外,RUNX2在調節成骨細胞分化中起關鍵作用[24],RUNX-2、OPN、BMP2是調控成骨分化的重要因子,是成骨細胞分化的生物標志物。既往研究表明應用BMSCs在TMJ損傷區域誘導了更多的骨形成和更嚴重的強直癥狀[22]且葉黃素具有調控骨質代謝作用[10],在本實驗中發現成骨培養第5天后,RUNX-2、OPN、BMP2的蛋白表達明顯減少,進一步提示葉黃素影響了間充質干細胞的成骨分化,因此可推測葉黃素可能是防治顳下頜關節強直的有效試劑。
但是本研究也有一些局限性。首先,僅使用骨髓間充質干細胞作為體外成骨細胞分化后葉黃素的作用靶點,具體機制尚未明確,且缺乏破骨細胞和成軟骨細胞的分化。第二,需要進行后續動物實驗進一步了解葉黃素在預防顳下頜關節強直中起到的不同作用,并找到影響關節強直形成的分子機制,以期更好地指導臨床治療,這對于有效預防TMJA的發生有重要的意義。
[參考文獻]
[1]Bello S A, Aluko Olokun B, Olaitan A A, et al. Aetiology and presentation of ankylosis of the temporomandibular joint:report of 23 cases from Abuja,Nigeria[J]. Br J Oral Maxillofac Surg, 2012,50(1):80-84.
[2]Zhao Y P, Zhang Z Y, Wu Y T, et al. Investigation of the clinical and radiographic features of osteoarthrosis of the temporomandibular joints in adolescents and young adults[J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 2011,111(2):e27-e34.
[3]Casado -Díaz A, Santiago -Mora R, Jiménez R, et al. Cryopreserved human bone marrow mononuclear cells as a source of mesenchymal stromal cells: application in osteoporosis research[J]. Cytotherapy, 2008,10(5):460-468.
[4]Friedenstein A J, Petrakova K V, Kurolesova A I, et al. Heterotopic of bone marrow. Analysis of precursor cells for osteogenic and hematopoietic tissues[J]. Transplantation, 1968,6(2):230-247.
[5]宋幼良,吳殿星,錢國壬,等.葉黃素研究進展[J].農業科技通訊,2013,11:138-140,198.
[6]楊文文,邱靜,高貴,等.HPLC法測定加工食品中葉黃素的含量[J].安徽農業科學,2013,24:10108-10109,10214.
[7]Johra F T, Bepari A K, Bristy A T, et al. A mechanistic review of β-Carotene, Lutein, and Zeaxanthin in eye health and disease[J]. Antioxidants (Basel), 2020,9(11):1046.
[8]王彥博,唐慧安,朱元成.紫花苜蓿中葉黃素的提取及純化[J].江蘇農業科學,2013,41(2):229-231.
[9]黃遠英.越橘葉黃素酯軟膠囊緩解視疲勞的保健作用[J].四川生理科學雜志,2013,35(4):164-167.
[10]郎朗,刁磊,陳惠杰.葉黃素口服脂質體的制備[J].黑龍江畜牧獸醫,2013,56(21):150-152.
[11]韋麗嬌,謝祥勇,何碧華.口服葉黃素聯合中藥離子導入治療大齡兒童弱視的療效觀察[J].醫學理論與實踐,2013,26(7):905-906.
[12]王麗,王新雨,胡明月.萬壽菊花中葉黃素的提取方法及其藥理作用研究進展[J].中國民族民間醫藥,2013,22(6):28,30.
[13]羅卓荊,畢龍.我國骨缺損修復的成就與展望[J].空軍軍醫大學學報,2022,43(3):263-267.
[14]He D, Yang C, Chen M, et al. Traumatic temporomandibular joint ankylosis: our classification and treatment experience[J]. J Oral Maxillofac Surg, 2011,69(6):1600-1607.
[15]Zhang Y, He D M. Clinical investigation of early post-traumatic temporomandibular joint ankylosis and the role of repositioning discs in treatment[J]. Int J Oral Maxillofac Surg, 2006,35(12):1096-1101.
[16]Vasconcelos B C, Bessa-Nogueira R V, Cypriano R V. Treatment oftemporomandibular joint ankylosis by gap arthroplasty[J]. Med Oral Patol Oral Cir Bucal, 2006,11(1):E66-E69.
[17]Spagnoli A. Mesenchymal stem cells and fracture healing[J]. Orthopedics, 2008, 31(9):855-856;discussion 856.
[18]Einhorn T A. The cell and molecular biology of fracture healing[J]. Clin Orthop Relat Res, 1998,(355 Suppl):S7-21.
[19]Imai Y, Takaoka K. [Bone fracture and the healing mechanisms. The role of BMP signaling in fracture healing][J]. Clinical Calcium, 2009,19(5):667-672.
[20]Iwakura T, Miwa M, Sakai Y, et al. Human hypertrophic nonunion tissue contains mesenchymal progenitor cells with multilineage capacity in vitro[J]. J Orthop Res, 2009,27(2):208-215.
[21]Hofmann A, Ritz U, Hessmann M H, et al. Cell viability, osteoblast differentiation, and gene expression are altered in human osteoblasts from hypertrophic fracture non-unions[J]. Bone, 2008,42(5):894-906.
[22]Porto G G, Vasconcelos B C, Fraga S N, et al. Development of temporomandibular joint ankylosis in rats using stem cells and bone graft[J]. Int J Oral Maxillofac Surg, 2011,40: 1414-1420.
[23]崔國勝,曾劍玉,張婧,等.神經生長因子對2型糖尿病小鼠骨髓基質細胞體外成骨能力的影響[J].中華口腔醫學雜志,2018,53(2):97-102.
[24]Franceschi R T, Xiao G. Regulation of the osteoblast-specific transcription factor, Runx2: responsiveness to multiple signal transduction pathways[J]. J Cell Biochem, 2003,88(3):446-454.
[收稿日期]2024-03-04
本文引用格式:郭莎,麥麥提艾力·麥麥提敏,姚志濤.葉黃素對大鼠骨髓間充質干細胞成骨分化的影響分析[J].中國美容醫學,2025,34(1):1-6.

