胃腸道間質瘤的診斷及預后探討①
王霖
(昆明結核病防治院 云南昆明 650301)
胃腸道間質瘤(gastrointestinal stromal tumors,GISTS)是指起源于胃腸道壁原始或幼稚間質干細胞(Cajall細胞)的具有多向分化特征的,有別于經典的平滑肌瘤和神經來源腫瘤的一類異質性腫瘤。隨著超微結構和免疫組化研究的深入,經過多年的研究,人們對GISTS有了較明確的認識。基于目前的認識,GISTS的確診還主要依靠病理和免疫組化。本文收集2005年1月至2009年5月GIST患者42例,將其臨床、病理學特征及預后報道如下。
1 材料與方法
1.1 標本來源
收集我院2005年1月至2009年5月GISTS患者42例。全部標本經10%福爾馬林固定,常規石蠟包埋。
1.2 試劑
免疫組化抗體CD117、CD34、Des、Actin、SMA、S-100、Ki-67、bcl-2均購自福州邁新公司。
1.3 免疫組織化學染色
用S-P法免疫組織化學染色,用已知陽性片做陽性對照,PBS液代替一抗做陰性對照。操作過程嚴格按照說明書操作。
1.4 結果判斷
CD117、CD34、Des、Actin、SMA、bcl-2為胞質表達,部分為胞膜和胞質共同表達;Ki-67為胞核表達;S-100為胞核表達,部分為胞核和胞質共同表達。免疫組化結果根據陽性細胞占腫瘤細胞比例≥10%為陽性,反之為陰性。
1.5 良惡性標準
生物學行為分組根據Fletcher CD等[1]:I組(極低度侵襲危險性)、Ⅱ組(低度侵襲危險性)、Ⅲ組(中度侵襲危險性)、Ⅳ組(高度侵襲危險性)。
1.6 統計學方法
采用SPSS 13.0統計軟件對統計資料進行χ2檢驗或校正χ2檢驗及相關分析,以(P<0.05)表示差異有顯著性。
2 結果
2.1 臨床資料
42例GISTS發生于食道2例,胃16例,小腸10例,結/直腸12例,腹腔2例。42例GIST在消化道中分布情況見表1。其中I組(極低度侵襲危險性)4例,Ⅱ組(低度侵襲危險性)2例,Ⅲ組(中度侵襲危險性) 16例、Ⅳ組(高度侵襲危險性)20例。男性26例,女性16例,年齡幾乎在33~67歲,平均50歲,但有1例為6.5歲的兒童。常見癥狀:吞咽不適2例,便血14例,惡心嘔吐10例,腹塊6例,體檢發現4例,其他手術時發現6例。隨訪半年至3年,其中5例復發或轉移(6~24個月),4例轉移到腹腔及肝臟,1例全身轉移,2例死亡。
2.2 病理資料
2.2.1 肉眼檢查 腫塊大小1.0~16.0cm。大多數為境界清楚的包塊,卵圓形,結節狀或分葉狀,部分有包膜。切面灰白、灰紅,實性,質韌,部分腫瘤呈魚肉狀伴出血、壞死及囊性變。I組體積較小,切面質韌;Ⅲ組Ⅳ組質嫩“魚肉樣”;Ⅱ組介于二者之間,部分伴壞死、出血及粘液樣變。
2.2.2 鏡檢 GISTS的組織學表現多種多樣,但主要有梭形及上皮樣細胞兩種基本成分以梭形細胞多見或二者混合存在。梭形細胞漿輕至中度嗜酸性,核長梭形,兩端鈍圓“臘腸樣”染色質分散,核仁不明顯,編織狀或魚骨樣排列,部分核細長,柵欄狀排列。上皮樣細胞形態不一,圓形或多邊形,胞漿豐富,弱嗜酸性,核周空亮或偏位,呈漿細胞樣、印戒樣細胞,核仁明顯,可見瘤巨細胞,片狀、巢狀分布。Ⅲ組Ⅳ組GIST瘤細胞呈浸潤性生長,細胞輕至重度異型,核分裂明顯,腫瘤中央壞死常見。
2.2.3 免疫組織化學檢測 42例GISTS中Des(+)4例(9.5%),SMA(+)14例(33%),Actin(+)12例(28.6%),CD34(+)36例(85.7%),CD117(+)40例(95.2%),S-100(+)12例(28.6%)。以上免疫組化的指標陽性與否與腫瘤的惡性度無關(P>0.05)。Ki-67(+)22例(52.4%),bcl-2(+)28例(66.7%),其中I組GISTS Ki-67均為陰性,隨著危險級別增高,陽性率增高,差異有顯著性(P<0.05)。bcl-2表達與Ki-67相反,差異有顯著性(P<0.05)見表2。
3 討論
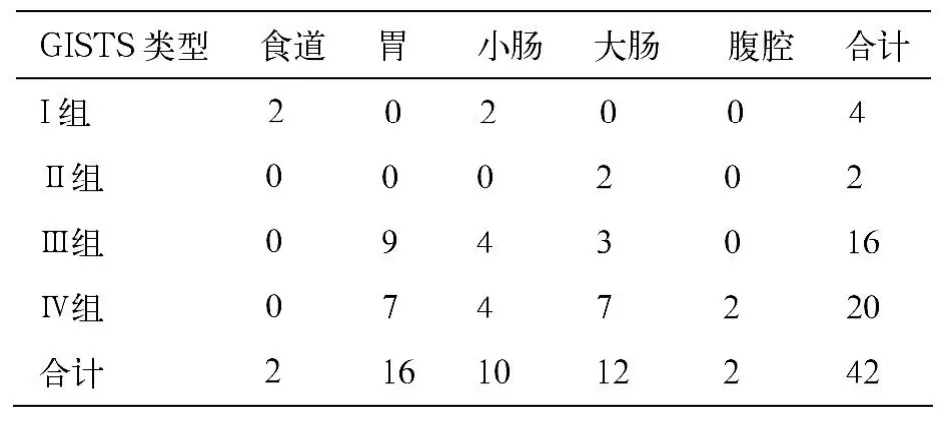
表1 42例GISTS在消化道中的分布情況
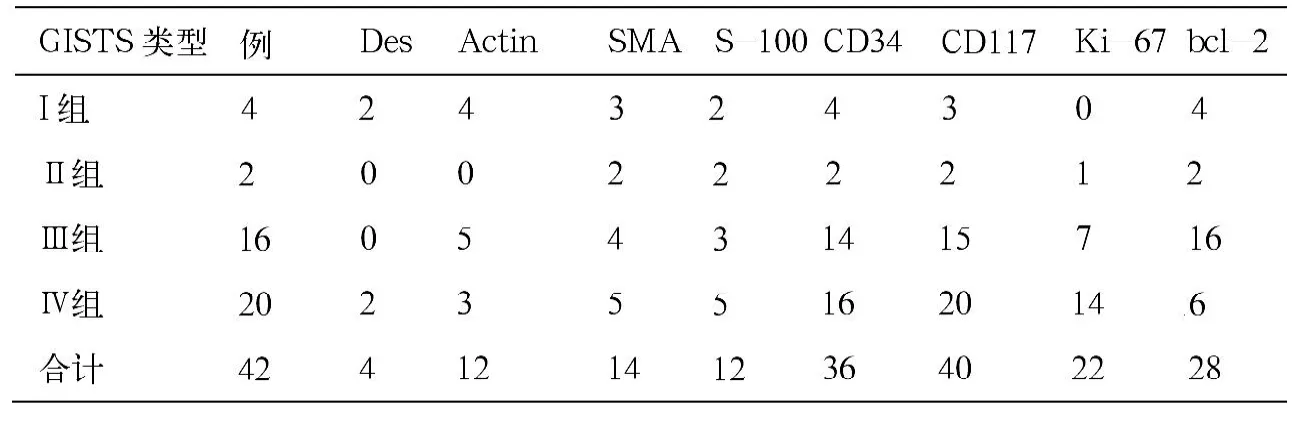
表2 42例GISTS的免疫組化檢測結果
GISTS是一類發生胃腸壁最常見的間葉源性腫瘤,還可累及網膜、腸系膜,以及腹膜后。根據腫瘤的分化特征,形態上表現為梭形和(或)上皮樣細胞,在常規HE染色中很難與典型的平滑肌瘤,神經鞘瘤相鑒別。免疫組化是目前最為有效的診斷手段。臨床上對于發生在消化道的實體腫瘤,光鏡表現為典型的細胞形態,如再獲得CDl17陽性的免疫組織化學結果,則可確診GISTS[2]。
本組42例GISTS以胃、小腸、大腸發生率最高,分別為38%、23.8%、28.6%,食道和其他部位罕見(4.8%)。患者絕大多數為成年人,幾乎在33歲以上,本組最小發病年齡為6.5歲。GISTS偶見兒童,Terada等[3]曾報道過1例發生于4歲女孩的GISTS。
胃腸道間質瘤是一類具有自身形態學特點、特定的免疫表型和遺傳學特征的腫瘤,在光鏡和電鏡形態上它有不恒定的、多變的表現形式。HE染色下的光鏡形態與平滑肌瘤和神經鞘瘤相互間較易混淆,故應用免疫組織化學給予辨別和認識是診斷GIST必不可少的手段。在免疫組織化學標記中,KIT受體酪氨酸激酶(CD117)是GISTS最特異和敏感的標志物。杜春燕等[4]對103例GISTS進行免疫組織化學檢測,發現CD117陽性95例(92.2%)、CD34陽性59例(57.3%)、SMA陽性7例(6.8%)、SIO0陽性9例(8.7%),另有7.8% GISTS為KIT陰性。本組研究CD34陽性率為85.7%,CD117陽性率為95.2%,其中CD34陽性組中有2例CD117陰性,CD117陽性組中有4例CD34陰性。在診斷GISTS中CD117抗體具有較好的敏感性和特異性。研究表明CD34在GISTS的診斷中具有很高的特異性和敏感性,但隨GISTS發生部位不同有所差異,由胃、小腸到大腸其陽性率逐漸有所降低,但對于CDI17陰性病例有補充作用。因此,聯合檢測CD117、CD34的表達有利于提高GISTS的診斷率[5]。本組有14例向平滑肌分化,12例向神經分化。因此,其他免疫組化標記物對判斷GISTS的分化方向和鑒別診斷也有著重要作用。
CD117與GISTS的關系是通過卡哈爾間質細胞(Cajall細胞)發現的。有學者研究認為該細胞具有啟動平滑肌的自發性收縮功能,并可表達c-kit蛋白[6]。c-kit原癌基因位于人染色體4q11-12,它的產物是Ⅲ型酪氨酸激酶生長因子受體,屬免疫球蛋白超家族成員,排列序號為CD117,在黑色素細胞、生殖細胞和造血細胞3個細胞系的發育中起重要作用,研究表明卡哈爾間質細胞和GISTS均表達CD117,不論GISTS的發生部位和細胞組成,CD117都有較高的陽性率[7]。對比研究證明CD117對真性平滑肌瘤和神經鞘瘤全部呈陰性[6~7]。CD34是一種骨髓造血干細胞抗原,在GIST診斷中有很高的特異性和敏感性,真正胃腸道內外平滑肌瘤和神經鞘瘤基本不表達[8],可標記內皮細胞、一些間葉細胞及相應的部分腫瘤,如血管源性腫瘤、隆突性皮膚纖維肉瘤、孤立性纖維性腫瘤等。
因此,以CD117和CD34為主的此組抗體能有效的將GISTS從以往的消化道“平滑肌(肉)瘤、(惡性)平滑肌母細胞瘤、(惡性)神經鞘瘤”中準確地區分開來,提示CD117和CD34在正確認識GISTS的過程中發揮了重要作用,肯定了此組抗體尤其是CD117的輔助診斷價值。
GIST的確診要經過術后病理和免疫組化檢查證實,但是免疫組化的指標陽性率與否與腫瘤的惡性度無關。伍小軍等認為,原發灶大小和核分裂象是判斷腫瘤惡性程度的重要指標,全部的GIST都應視為具有潛在惡性[9]本組Ki-67陽性率為52.4%,隨GIST形態學惡性程度的增加而陽性率增高;bcl-2陽性率為66.7%,隨GIST形態學惡性程度的增加而陽性率減少,差異有顯著性。提示Ki-67和bcl-2可作為GIST的預后參考指標。
對于腫瘤良、惡性方面,國內大多數學者認為腫瘤的大小及核分裂的多少是判斷良惡性的重要指標,而國外學者對所有間質瘤具有潛在惡性這一觀點已達成共識,認為GIST不能簡單以良、惡性劃分,而是應該以風險程度分級。美國國立衛生研究院(NIH)的GIST的風險程度的分級與腫瘤的直徑和細胞核分裂數關系的標準,腫瘤部位和免疫組化抗體蛋白陽性率與腫瘤危險程度無相關性,腫瘤是否浸潤周圍組織與風險程度無顯著相關性[10]。總之,GIST的確診要經過術后病理和免疫組化檢查證實,對于腫瘤的生物學行為雖有較多的認識,但還有待進一步探討。
[1]Fletcher C D,Bem a n J J,Corless C,et a1.Diagnosis O fgastroi Ntestinal Stromal Tumors:a Consensus Approach[J].Hum Pathot,2002,33:459~465.
[2]張信華,何裕隆,詹文華,等.胃腸問質瘤135例臨床診治分析[J].中華胃腸外科雜志,2007,10(1):19~20.
[3]Terada R,Ito S,Akama F,et al.Clinical and histopathological features of colonic stromal tumor in a child[J].Jgastroenterel,2000,35:456~459.
[4]杜春燕,師英強,傅紅,等.胃腸道間質瘤103例預后分析[J].中國實用外科雜志,2007,27(4):297~299.
[5]胡達水,胡海,萬志剛.胃腸間質瘤免疫組織化學特征及臨床診[J].實用臨床醫學,2009,10(5):11~13.
[6]Sircar K,Hew lett BR,Huizinga JD,et al.Interstitial cells of Cajal as precursors for gastrointestinal stromal tumors[J].Am J Surg Pathol,1999,23:377~389.
[7]Graad t van Roggen JF,Velthuysen ML,Hogendoorn PC.The histopathologial differential diagnosis of gastrointestinal stromal tumors[J].J Clin Pathol,2001,54:96~103.
[8]Erlandson RA,K limstra DS,Woodruff JM.Subclassification of gastrointestinal stromal tumors based on evalution by electron m icroscopy and immmunohistochem istry[J].Ultrstruct Pathol,1996,20:373.
[9]伍小軍,萬德森,潘志忠,等.胃腸道間質瘤大小與預后[J].腫瘤研究與臨床,2006,18(8):520~524.
[10]裴靜,汪圣毅,程云生.75例胃腸問質瘤診治分析[J].安徽醫藥,2008,12(8):708~710.

