吡格列酮對胰島素抵抗細胞糖代謝糖異生的影響
韓坤 李德恒 袁磊
(漯河醫學高等專科學校生理教研室,河南 漯河 462002)
胰島素抵抗指胰島素在周圍組織攝取和清除葡萄糖的作用減低,在胰島素抵抗狀態下,肝糖原分解增加,糖異生作用增強,導致肝糖輸出增多[1]。近年來,噻唑烷二酮類藥物(Thiazolidinedionederivatives,TZDs)因其可改善組織的胰島素抵抗狀態,增強組織對胰島素的敏感性而越來越受到重視[2,3]。
本研究采用3T3-L1脂肪細胞復制胰島素抵抗模型[4],觀察TZDs類藥物吡格列酮對胰島素抵抗3T3-L1脂肪細胞葡萄糖消耗及糖異生作用的影響,進一步在細胞水平明確吡格列酮對糖代謝影響的分子機制。
1 材料與方法
1.1 材料和試劑 3T3-L1小鼠前脂肪細胞(中科院上海細胞所),地塞米松與3-異丁基-1-甲基黃嘌呤均(Sigma),胰島素注射液(諾和公司),DMEM培養基(Gibco),乳酸鈉(上海化學試劑總廠上海試劑三廠),考馬斯亮蘭法總蛋白測定試劑盒(南京建成生物工程研究所),葡萄糖臨床檢測試劑盒(四川邁克公司)。
1.2 實驗儀器 酶標儀(Thermo Electron),CO2培養箱(Forma Scientific),超凈工作臺(北京半導體廠),倒置顯微鏡(Olympus IX),BP210S電子天平(賽多利斯有限公司)。
1.3 方法
1.3.1 3T3-L1脂肪細胞細胞培養[5]參考AnilKumar[6]分化前脂肪細胞的方法,對細胞進行分化:將3T3-L1前脂肪細胞置于含10%小牛血清的DM EM 高糖培養基中,37℃、5%CO2、飽和濕度下培養。待細胞融合2d后,加入含0.5 mmol?L-13-異丁基-1-甲基黃嘌呤、0.25μ mol? L-1地塞米松、10mg? L-1胰島素以及10%小牛血清的DM EM高糖培養基培養48h,換含10 mg?L-1胰島素的培養基再培養 48 h,隨后以 10%小牛血清的DMEM高糖培養基繼續培養2d,換培養液1次,誘導分化8~12 d的3T3-L1細胞90%以上呈脂肪細胞表型可用于試驗。
1.3.2 3T3-L1脂肪細胞胰島素抵抗細胞模型的建立[7,8]將上述分化成熟的3T3-L1脂肪細胞調整細胞密度轉入48孔細胞培養板中繼續培養,分為空白組及模型組,空白組加入正常培養基,模型組加入含終濃度為 1μ mol?L-1地塞米松的培養基,孵育48h,孵育結束后,棄去培養液,用PBS輕輕洗滌2次,即為正常對照3T3-L1脂肪細胞和胰島素抵抗3T3-L1脂肪細胞模型。
1.3.3 吡格列酮對胰島素抵抗3T3-L1脂肪細胞細胞葡萄糖消耗量的影響[9]將上述分化成熟的3T3-L1脂肪細胞調整細胞密度轉入48孔細胞培養板中培養,細胞密度為3×105個?孔-1,復制上述胰島素抵抗模型。將細胞分為正常細胞對照組,模型組和吡格列酮組(濃度為 10-5mol?L-1)孵育12h后,再按是否加入生理濃度的胰島素(10-9mol?L-1)將各組均分為兩個平行組,繼續溫浴12h,并設無細胞培養基對照組,取各組上清液用GOD-POD法(葡萄糖氧化酶法)測定葡萄糖含量[10]。細胞所消耗的葡萄糖量(GC)=無細胞對照組培養液中葡萄糖含量-各組細胞培養液中葡萄糖含量。
1.3.4 吡格列酮對胰島素抵抗3T3-L1脂肪細胞細胞糖異生作用的影響 同樣復制上述胰島素抵抗模型之后換以Krebs-Ringer緩沖液,將細胞分為正常細胞對照組,模型組和吡格列酮組(濃度為10-5mol?L-1)加入10-5mol?L-1吡格列酮,再按是否加入生理濃度的胰島素(10-9mol?L-1)以及是否含有底物(終濃度為10 mmol?L-1的乳酸)將上述三組細胞各分一平行組,繼續孵育2h。孵育結束后,取上清測定葡萄糖含量;板中下層細胞用200g?L-1的KOH裂解,用考馬斯亮蘭法測定蛋白含量。糖異生量(μ mol?mg-1)=葡萄糖生成量(μ mol)/蛋白含量(mg)
1.4 統計學處理 實驗各組同批內重復6次,計量數值用表示。采用統計軟件SPSS17.0行統計學分析,兩組間比較采用t檢驗,多組間比較采用單因素方差分析。以P<0.05為有統計學意義。
2 結果
2.1 吡格列酮對胰島素抵抗3T3-L1脂肪細胞細胞葡萄糖消耗量的影響
在無生理濃度胰島素存在條件下,胰島素抵抗3T3-L1脂肪細胞組糖耗與對照組相比并無明顯差異;給予生理胰島素后,對照組和胰島素抵抗3T3-L1脂肪細胞組糖耗均增加,但后者明顯低于前者(0.85±0.03 vs 0.68±0.02,P<0.05)。給予吡格列酮后,僅與細胞孵育12h即可顯著促進胰島素抵抗3T3-L1脂肪細胞組糖耗,與模型組比較差異有統計學意義((0.6±0.01 vs 1.7±0.02,P<0.05);加入生理胰島素時,吡格列酮表現出與胰島素協同的促進胰島素抵抗3T3-L1脂肪細胞糖耗的作用。(圖1)
2.2 吡格列酮對胰島素抵抗3T3-L1脂肪細胞糖異生作用的影響
在無底物乳酸和胰島素存在條件下,吡格列酮對胰島素抵抗3T3-L1脂肪細胞糖異生均沒有表現出明顯抑制作用。底物乳酸存在條件下,生理濃度胰島素可顯著抑制胰島素抵抗3T3-L1脂肪細胞糖異生作用;給予吡格列酮后,胰島素抵抗3T3-L1脂肪細胞的糖異生作用也受到明顯抑制,且吡格列酮與胰島素有協同抑制胰島素抵抗3T3-L1脂肪細胞糖異生的作用(表1)。
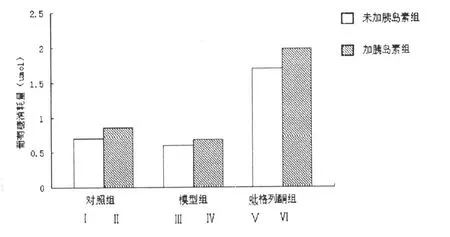
圖1 吡格列酮對胰島素抵抗3T3-L1脂肪細胞細胞葡萄糖消耗量的影響(,n=6)
表1 吡格列酮對胰島素抵抗3T3-L1脂肪細胞細胞糖異生作用的影響(,n=6)

表1 吡格列酮對胰島素抵抗3T3-L1脂肪細胞細胞糖異生作用的影響(,n=6)
注:VS模型組+乳酸,△P<0.05;VS模型組+乳酸+胰島素,▲P<0.05
組別 糖異生量(umol?mg-1)對照組8.3±0.05模型組10.2±0.13吡格列酮組 9.0±0.03△對照組+乳酸 12.0±0.15模型組+乳酸 14.5±0.11吡格列酮組+乳酸 12.2±0.08△對照組+乳酸+胰島素 9.6±0.02模型組+乳酸+胰島素 13.5±0.04吡格列酮組+乳酸+胰島素 10.8±0.03▲
3 討論
胰島素抵抗是糖尿病、肥胖、冠心病、高血壓及脂代謝異常等多種疾病發病的中心環節,IR的發病機理不明,研究其發生機制成為當今的重要課題。胰島素抵抗可以發生在胰島素信號傳導和環境因素等各個環節,我們采用地塞米松誘導3T3-L1脂肪細胞構建的胰島素抵抗模型,對胰島素抵抗前提下細胞水平糖代謝過程中葡萄糖消耗糖異生做了進一步的研究,研究表明:吡格列酮可顯著改善胰島素抵抗狀態下3T3-L1脂肪細胞的糖代謝作用,并且對糖代謝過程中糖異生有明顯的抑制作用,并且該抑制作用在胰島素存在的情況下表現的更明顯,其詳細的分子機制有待進一步的研究。
1 Hideyuki S,Takehide O,M otonobu A,et al.Dexamethasone-Induced insulin resistance in 3T3-L1 adipocy tes is due to inhibition of glucose transport rather than insulin signal transduction[J].Diabetes,2000,49(10):1700-1708.
2 Koh EH,Kim MS,Park JY,et al.Peroxisome proliferator activated receptor(PPAR)apha activation prevents diabetes in O LETF rats comparison with PPAR gamma activation[J].Diabetes,2003,52(9):2331-2337.
3 Guan Y.PPA R family and its relationship to renla complications of the metbaolic syndrome.[J].J Am Soc Nephro1,2004,15(11):2801-2815.
4 SoaresA F,Guichardant M,Cozzone D,et al.Effects of oxidative stress on adiponectin secretion and lactate production in 3T3-L1 adipocytes[J].Free Radic Biol Med,2005,38(7):882-889.
5 Nelson B A,Robinson K A,Buse M G.High glucose and g luosamine induce insulin resistance via different mechanisms in 3T3-L1 adipocytes[J].Diabetes,2000,49(6):981-991.
6 AnilKumarK L,Marita A R.T roglitazone prevents and reverses dexamethasone induced insulin resistance on glycogen synthesis in 3T 3 adipocyte[J].Br J Pharmacol,2000,130(2):351-358.
7 Xu A,Wong LC,Wang Y,et al.Chronic treatment with growth ho rmone stimulates adiponectin gene ex pression in 3T3-L1adipocy tes[J].FEBS Lett,2004,572(2-3):129-134.
8 Palmer RM,Bain PA,Southern BG.Dexamethasone-induced catabolism and insulin resistance in L6 my oblast are reversed by the removel of serum[J].Lomp Biochem physiol C,1990,97(2):369-372.
9 陳秋,夏永鵬,邱宗蔭.吡格列酮對胰島素抵抗 HepG2細胞模型的藥理學評價[J].中國藥理學通報,2006,22(2):248-251.
10 楊桂枝,高小平,晏菊芳,等.GOD-POD法微量化測定的方法建立以及在3T 3-L1脂肪細胞和 HepG2細胞糖攝取中的應用[J].四川解剖學雜志,2003,11(1):12-16.

