阿侖膦酸鈉腸溶片的質量和穩定性研究
曹 雯 ,張 育 ,孫勇兵 ,劉 艷 ,孫 進 ,何仲貴 *
(1.沈陽藥科大學藥學院,遼寧沈陽 110016;2.石藥集團歐意藥業有限公司,河北石家莊 050051)
骨質疏松癥是指單位體積內骨量減少,使骨結構改變,從而導致骨脆性增加甚至骨折[1]。阿侖膦酸鈉(alendronate sodium)是一種新的預防和治療骨質疏松癥的雙膦酸鹽類藥物,因其作用強度高,療效確切,可廣泛用于治療骨質疏松癥、變型性骨炎、糖皮質激素誘導的骨質疏松癥等骨類疾病[2]。隨著人口老齡化,骨質疏松癥和伴隨的骨折越來越受到社會的關注[3]。目前上市的劑型只有普通片劑一種,但阿侖膦酸鈉本身呈酸性,其不良反應主要集中于上消化道,如嘔吐、胃部不適、胃灼熱、食管炎、胃炎或潰瘍等[4],尤其是普通片劑易黏附在消化道壁上造成局部刺激甚至潰瘍。
阿侖膦酸鈉為酸性藥物,在胃酸中溶解度下降,導致一些白色膠狀物質出現,不利于吸收。阿侖膦酸鈉的吸收機制為細胞旁路吸收,主要吸收部位是小腸,且胃部酸性環境不利于吸收時,腸溶制劑可以最大程度地發揮其臨床療效;阿侖膦酸鈉對消化道上部有較強的刺激性,開發腸溶制劑可減少胃部不良反應的發生。因此,非常有必要考慮將其研制成腸溶片劑以減少阿侖膦酸鈉對食道及胃部的強烈刺激,使患者服用更加方便、安全有效。本研究對合作研制的阿侖膦酸鈉腸溶片進行質量和穩定性研究。
1 儀器與試藥
1.1 儀器
WFZ800-D2型紫外-可見分光光度計(北京第二光學儀器廠),RC2-5A智能藥物溶出儀(天津大學精密儀器廠)。
1.2 試藥
阿侖膦酸鈉原料藥(批號:040102,石藥集團華盛制藥);阿侖膦酸鈉腸溶片(石藥集團歐意藥業有限公司);微晶纖維素(MCC,常熟市藥用輔料有限公司);預膠化淀粉(湖州展望化學藥業有限公司);淀粉(廊坊市淀粉廠);十二烷基硫酸鈉(天津市博迪化工有限公司);乳糖(天津市博迪化工有限公司);交聯PVP(上海德祥醫藥技術有限公司);PVP(天津市博迪化工有限公司);歐巴代03B28796、歐巴代OY-P(上海卡樂康包衣技術有限公司)。
2 方法與結果
2.1 檢測波長的選擇
經UV掃描,阿侖膦酸鈉與鉬酸銨形成的衍生物在710 nm處有較大且穩定的吸收,再對空白輔料進行UV掃描,結果顯示其在710 nm處無干擾吸收,確定阿侖膦酸鈉腸溶片含量測定的檢測波長為710 nm。
2.2 對照品溶液的制備
精密稱取經150℃干燥至恒重的阿侖膦酸鈉對照品適量,加水溶解并定容制成每毫升含阿侖膦酸鈉相當于阿侖膦酸0.20 mg的溶液,即得為對照品溶液。
2.3 供試品溶液的制備
取樣品20片,精密稱定,研細,精密稱取適量(約相當于阿侖膦酸40 mg),置200 ml量瓶中,加水適量,充分振搖,使阿侖膦酸鈉溶解,加水至刻度,搖勻,濾過,棄去初濾液,取續濾液作為供試品溶液。
2.4 含量測定方法
精密量取對照品溶液和供試品溶液,各2 ml,分別置25 ml量瓶中,加過硫酸銨溶液(1→100)3 ml,水浴中加熱15 min,冷至室溫,加鉬酸銨溶液(取鉬酸銨5 g,加水100 ml溶解,加 5 mol/L硫酸溶液 100 ml,混勻)2 ml,于 25℃以上放置15 min,加對甲氨基酚硫酸鹽溶液(取對甲氨基酚硫酸鹽0.5 g,加15%亞硫酸氫鈉溶液195 ml,加20%亞硫酸鈉溶液 5 ml,搖勻)1 ml,于 25℃以上放置 15 min,加 34%醋酸鈉溶液5 ml,加水至刻度,搖勻,濾過,照分光光度法(《中國藥典》2000年版二部附錄Ⅳ),在710 nm波長處測定吸收度,計算,即得。方法學實驗得出,方法回收率的平均回收率為100.76%,系統精密度RSD為0.602%,溶液穩定性得出該溶液在實驗4 h內穩定。
2.5 線性關系考察
精密稱取阿侖膦酸鈉對照品適量,以水溶解并稀釋至濃度約1 mg/ml(按阿侖膦酸計)的貯備液。精密量取貯備液適量,用水分別稀釋至濃度(按阿侖膦酸計)為100、140、170、200、230、260 μg/ml,依法操作進行測定。記錄吸收度,線性相關性見圖1。結果表明阿侖膦酸鈉在(按阿侖膦酸計)100~260 μg/ml范圍內呈良好的線性相關性(r=0.9995)。
2.6 樣品含量測定
按含量測定項下的方法對3批樣品(批號:20040401、20040402、20040403)進行含量測定。并另外測定其含量均勻度,方法:取本品1片,置乳缽中,研細,加水適量,研磨,并用水分次轉移至50 ml量瓶中,充分振搖使阿侖膦酸鈉溶解,加水至刻度,搖勻,濾過,棄去初濾液,精密量取續濾液2 ml,置25 ml量瓶中,照含量測定項下的方法依法測定,結果見表1。
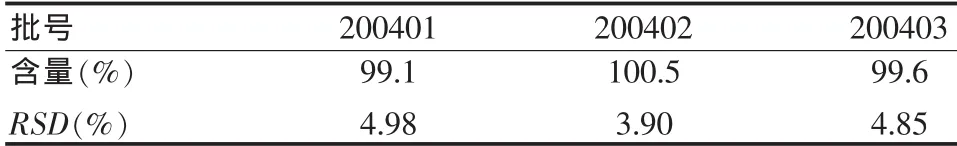
表1 樣品含量測定結果(%,n=3)Tab.1 Content determination results of samples(%,n=3)
由表1可知,所測定的各個批次樣品含量和含量均勻度均符合《中國藥典》相關規定。
2.7 釋放度檢查
2.7.1 測定波長的確定 經UV掃描阿侖膦酸鈉的醋酸鈉緩沖液(pH=6.8),測得在710 nm處有較大且穩定(無干擾)的吸收,確定釋放度測定的檢測波長為710 nm。
2.7.2 測定方法 取本品2片,照釋放度測定法(《中國藥典》2000年版二部附錄ⅩD第二法,儀器裝置采用附錄ⅩC第三法),以0.1 mol/L鹽酸溶液700 ml為溶劑,轉速為75 r/min,依法操作,經2 h,立即棄去酸液,隨即加入醋酸鈉緩沖液700 ml,繼續依法操作,經45 min時,取溶液濾過,精密量取續濾液和對照品溶液各3 ml,分別置25 ml量瓶中,加1 mol/L 硫酸溶液 1.2 ml,加過硫酸銨溶液(1→100)6 ml,水浴中加熱15 min,冷至室溫,加鉬酸銨溶液(取鉬酸銨5 g,加水 100 ml溶解,加 5 mol/L 硫酸溶液 100 ml,混勻)4.5 ml,于25℃以上放置15 min,加對甲氨基酚硫酸鹽溶液(取對甲氨基酚硫酸鹽0.5 g,加15%亞硫酸氫鈉溶液195 ml,加20%亞硫酸鈉溶液 5 ml,搖勻)2 ml,于 25℃以上放置 15 min,加 34%醋酸鈉溶液5 ml,加水至刻度,搖勻,濾過,照分光光度法(《中國藥典》2000年版二部附錄Ⅳ),在710 nm波長處測定吸收度,計算出每片的釋放量,限度為標示量的80%,應符合規定。
2.7.3 釋放度的測定 依據上述測定方法,測定腸溶制劑的釋放行為,見圖1。由圖1可知,該制劑在模擬胃液中2 h內均未出現裂縫、崩解或溶脹的現象,在模擬腸液中45 min后的釋放量大于標示量的80%,所制備阿侖膦酸鈉腸溶片達到了腸溶的目的。
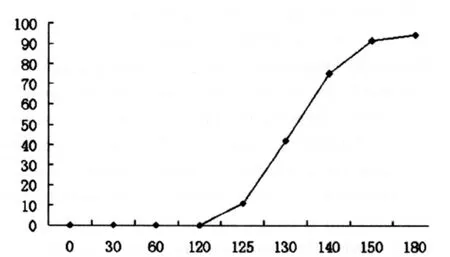
圖1 釋放度曲線Fig.1 The release curve
考察了同一批次內藥物(批號:20040402)釋放的均一性以及批次間的釋放均一性。取同一批次內的6個樣品進行釋放度測定,結果見圖2,結果表明所制備阿侖膦酸鈉腸溶片(批號:20040402)批內均一性良好。另外取3個批次的樣品進行釋放試驗,結果見圖3,各批在模擬小腸液內的釋放均一性良好。總之所制備的阿侖膦酸鈉腸溶片不僅具有腸溶特性,還具有良好的批內和批間均一性。
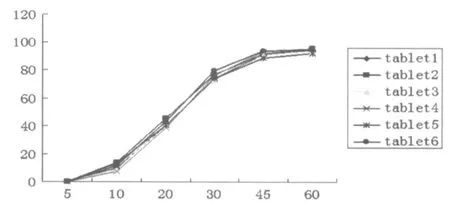
圖2 釋放均一性試驗(批號:20040402)Fig.2 The test of reproducibility of drug release(No.20040402)
2.8 穩定性研究
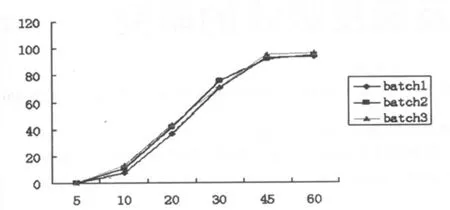
圖3 不同批號釋放均一性試驗Fig.3 The test of reproducibility of drug release for different batch
將各批次樣品進行高溫、強光照和高濕度的影響因素試驗,于第5、10天取樣考察與當天數據比較。實驗結果表明,樣品分別在高溫、強光照以及RH為75%條件下10 d均未見明顯質量改變,在RH=92.3% 放置10 d,仍未見明顯質量改變,但吸濕增重均大于5%,說明本品應采用防潮包裝。加速試驗則將兩種劑量規格的上市包裝樣品各3批,留樣6個月(40℃,RH=75%),并于第 1、2、3、6 個月取樣考察,與 0 個月數據比較,結果見表2。室溫留樣實驗表明,在為期6個月的觀察內,樣品均未見明顯質量改變。

表2 加速穩定性試驗Tab.2 The test of accelerated stability
3 討論
阿侖膦酸鈉為雙膦酸鹽類藥物,其既無紫外吸收又無熒光吸收,國內市售阿侖膦酸鈉片的質量標準中均采用鉬藍比色法進行含量測定及溶出測定,此法準確可靠。應用鉬藍比色法測定阿侖膦酸鈉的原理是將有機膦酸鹽分解氧化成無機磷酸鹽,在酸性溶液中與鉬酸銨反應生成磷鉬黃,再被還原劑還原成磷鉬藍,使溶液呈現深藍色,710 nm波長處比色法測定吸收度。因此,《中國藥典》2000版中采用的人工腸液(磷酸鹽緩沖液pH=6.8)對鉬藍比色法有干擾。考慮到此藥的特殊性,筆者通過試驗并參考《中國藥典》標準配制成醋酸鈉緩沖液pH=6.8模擬人工腸液,試驗結果證明,效果良好,溶出前后pH值基本沒有改變;又因為鉬藍比色法對溶液酸度有一定要求,所以溶出樣品測定前應先消除緩沖液的緩沖能力,通過試驗筆者選擇一定濃度的硫酸溶液中和醋酸鈉緩沖液,并通過正交試驗優化了試劑用量。
阿侖膦酸鹽是一種有效地抑制破骨細胞吸收作用的二磷酸鹽類化合物,能增加骨密度,預防椎骨、髖骨以及其他部位骨病變的發生,總得來說,它是安全的,能廣泛地用于絕經期后婦女骨質疏松癥的治療[5-6],但它也具有比較嚴重的上消化道毒副反應,包括食管和胃部的潰瘍、惡心、腹痛等[7]。據國外文獻報道,在一個隨機、雙盲為期3個月的臨床試驗中,受試者共75人,試驗組分為A組阿侖膦酸鈉片(10 mg/d)、B組阿侖膦酸鈉片(70 mg/周)、C組阿侖膦酸鈉腸溶片(70 mg/周)三組,結果顯示,A、B、C三組療效相當,而胃灼燒的發生率分別為 7例(28%)、3例(12%)、2例(8%)。由此可知,阿侖膦酸鈉腸溶片的胃部不良反應明顯降低[8],將其制成腸溶片能夠有效降低其不良反應,增加用藥安全性,具有非常重要的臨床意義。
市售的阿侖膦酸片有10 mg/d、70 mg/周兩種規格,臨床研究表明兩種劑量療效相等,安全性無明顯差異,但是70 mg/周規格一方面增加了患者的順應性,另一方面可以通過降低給藥次數,使得上消化道的不良反應降低。雖然70 mg/周的給藥方式在一定程度上降低了不良反應,但是它沒有從根本上來消除上消化道刺激性。與之相反的是,腸溶片在原則上降低了消化道刺激性。當然推薦將上述兩個優點合并,即70 mg/周的阿侖膦酸腸溶片。
對于一些具有食道和胃黏膜刺激性大的藥物,包括紅霉素、阿司匹林、雙氯芬酸鈉、吲哚美辛、呋喃妥因等,目前均已制成相應腸溶制劑,原因主要在于可以有效地降低食道和胃黏膜刺激性;同時小腸的刺激性也小。這主要是由于小腸的迅速蠕動(推進)和混合運動,使得藥物與腸黏膜的接觸時間較短,導致對小腸刺激性小;而胃部只有混合運動,使得藥物與胃黏膜的接觸時間較長;再加上小腸具有非常大的比表面積,因此阿侖膦酸鈉腸溶片可以有效降低上消化道刺激性,同時對腸道刺激性也小。
據文獻報道,阿侖膦酸鈉腸溶膠囊及其制備方法,其專利產品在45 min時平均有93%釋放出來,這與筆者研制產品相似(約95%)。阿侖膦酸鈉腸溶膠囊與進口阿侖膦酸鈉片(福善美)生物等效,且不良反應明顯降低[9]。這說明與普通片相比,阿侖膦酸鈉腸溶定位釋放不會影響藥物體內吸收行為,阿侖膦酸鈉腸溶片會表現出與普通片相類似的藥動學和藥效學性質。
綜上所述,阿侖膦酸鈉腸溶片在模擬胃液中2 h不釋放,在模擬腸液(pH=6.8)中45 min釋放度大于標示量的80%,且批間和批內的釋放度均一性良好,藥物含量符合《中國藥典》規定,穩定性試驗表明,樣品質量均未見明顯改變。阿侖膦酸鈉為水溶性良好的藥物,其吸收方式為細胞旁路被動擴散,因而口服生物利用度較低,約為0.7%,且食物和礦物質等可顯著減少其吸收,故可以進一步考慮增加其生物利用度,如制成生物黏附制劑、前體藥物等方式。
[1]王欣榮.骨質疏松癥的發病機理及其治療[J].生物工程進展雜志,2001,21(3):54-56.
[2]商紅.雙膦酸鹽類藥物的研究進展與臨床合理應用[J].中國藥房,2003,14(4):245-247.
[3]賀偉.阿侖膦酸鈉的臨床研究進展[J].社區醫學雜志,2003,1(1):13-14.
[4]曹園.阿侖屈酯可引起胃腸道副作用[J].藥學進展,1999,23(4):250-251.
[5]Pols HAP,Felsenberg D,Hanley DA,et al.Multinational,placebo-controlled,randomized trial of the ects of alendronate on bone density and fracture risk in postmenopausal women with low bone mass:results of the FOSIT study[J].Osteoporos Int,1999,(9):461-468.
[6]Bell NH,Bilezikian JP,Bone HG,et al.Alendronate increases bone mass and reduces bone markers in postmenopausal African-American women[J].J Clin Endocrinol Metab,2002,(87):2792-2797.
[7]Graham DY.What the gastroenterologist should know about the gastrointestinal safety proles of bisphosphonates[J].Dig Dis Sci,2002,(47):1665-1678.
[8]劉紅梅.阿侖膦酸鈉片[J].中國新藥雜志,1996,5(5):340-341.
[9]徐成,胡傳良,秦勇,等.一種阿侖膦酸鈉腸溶膠囊及其制備方法[P].CN101601662:2009,6-30.

