注射用燈盞花素細菌內毒素檢查方法研究
王 璐,張紅宇,劉 勤(云南省食品藥品檢驗所,昆明市 650031)
注射用燈盞花素細菌內毒素檢查方法研究
王 璐*,張紅宇,劉 勤(云南省食品藥品檢驗所,昆明市 650031)
目的:建立注射用燈盞花素細菌內毒素檢查方法。方法:按2005年版《中國藥典》(一部)要求,采用凝膠法和光度測定法,確定合理的注射用燈盞花素內毒素限值(L),并研究注射用燈盞花素對細菌內毒素與鱟試劑反應的干擾情況,以確定無干擾試驗濃度。結果:L=1 EU·mg-1,注射用燈盞花素的無干擾濃度為0.25 g·L-1。結論:該藥品采用細菌內毒素檢查法代替熱原檢查法,方法可行。
注射用燈盞花素;細菌內毒素;凝膠法;光度測定法
燈盞花素是從菊科植物燈盞細辛的干燥全草中分離得到的野黃芩苷,為注射用燈盞花素的原料藥,以野黃芩苷計其純度應達到98%以上[1]。注射用燈盞花素具有活血化瘀、通絡止痛的功效,臨床常用于中風后遺癥、冠心病、心絞痛的治療。云南省食品藥品檢驗所承擔了國家評價抽驗注射用燈盞花素的檢驗及探索性研究任務。在2005年版《中國藥典》增補本中,注射用燈盞花素細菌內毒素值用熱原檢查法控制,該法用實驗動物家兔進行,為一傳統方法。用鱟試劑(TAL)進行細菌內毒素檢查法與之比較,具有靈敏度高、重現性好、標準化試驗過程短,且可完成多批次供試品檢測等優點;同時,國家鼓勵以合理的試劑取代實驗動物的使用。因此,筆者按照2005年版《中國藥典》(一部)細菌內毒素檢查法[2],對注射用燈盞花素的熱原檢查轉化為細菌內毒素檢查進行了研究。
1 儀器與材料
1.1 儀器
DHG-9075A型電熱恒溫鼓風干燥箱(上海一恒科技有限公司);ZH-2型旋渦混合器(天津藥典標準儀器廠);SUB 28型恒溫水浴箱(美國格蘭特公司);BET-32M型細菌內毒素測定儀(天津市天大天發科技有限公司)。
1.2 試藥
1.2.1 TAL 湛江博康海洋生物有限公司,批號:0901190(λ=0.5 EU·mL-1)、0902270(λ=0.25 EU·mL-1),規格均為每支0.1 mL;湛江安度斯生物有限公司,批號:0908281(λ=0.5 EU·mL-1,規格:每支0.1 mL)、0907102(檢測范圍:10~0.03 EU·mL-1,規格:每支1.25 mL)。
1.2.2 細菌內毒素檢查用水(WBET) 湛江安度斯生物有限公司,批號:0902170、0908030,規格均為每支50 mL;湛江博康海洋生物有限公司,批號:W2003-3,規格:每支10 mL。
1.2.3 細菌內毒素工作標準品(WSE) 中國藥品生物制品檢定所,批號:200861,規格:每支150 EU。
1.2.4 注射用燈盞花素 衡陽恒生制藥有限公司,批號:20071003(規格:10 mg)、20090408(規格:20 mg)、20081210(規格:50 mg);昆明龍津藥業股份有限公司,批號:20090210-2(規格:10 mg)、20090106-1(規格:25 mg)、20081124(規格:50 mg)。
2 方法與結果
2.1 凝膠法
2.1.1 TAL靈敏度復核[2]按2005年版《中國藥典》(一部)細菌內毒素檢查法“TAL靈敏度復核試驗”規定進行檢查。結果,TAL靈敏度的測定值(λc)均在0.5λ~2λ之間,所用TAL均可用于細菌內毒素檢查。TAL靈敏度復核結果見表1(表中,+表示凝膠形成;-表示凝膠未形成)。

表1 TAL靈敏度復核結果Tab 1 TALsensitivity check results
2.1.2 細菌內毒素限值(L)的確定 本品臨床用法為肌肉注射及靜脈滴注,最大用量為1次20~50 mg,用500 mL10%葡萄糖注射液稀釋后使用,1日1次。因此,計算靜脈給藥的L時還應考慮扣除大輸液的細菌內毒素值,故L=K/M=(5 EU·kg-1·h-1-250 EU·(60 kg)-1)·h-1/(50 EU·(60 kg)-1·h-1=1 EU·mg-1。
2.1.3 最小有效稀釋濃度(MVC)的計算[3]按公式MVC=λ/L計算(L=1 EU·mg-1,MVC以EU·mL-1表示)。目前,常用TAL最高λ為0.031 25 EU·mL-1,則試驗時注射用燈盞花素的MVC為0.031 25 g·L-1。
2.1.4 干擾試驗預試驗 用WBET對2批注射用燈盞花素進行溶解稀釋,使稀釋濃度為2、1、0.5、0.25、0.125 g·L-1,取相應濃度樣品稀釋液加入WSE,制成內毒素濃度為1、0.062 5、0 EU·mL-1的供試品溶液,取TAL(批號:0901190)與上述系列溶液進行反應,每一濃度重復試驗2管。結果,供試品溶液≥0.5 g·L-1濃度管加入1 EU·mL-1WSE的各試驗管均呈陽性,其余各試驗管均呈陰性,表明本品濃度≤0.5 g·L-1即可能對細菌內毒素與TAL的反應無干擾作用,故筆者選擇了0.25 g·L-1的濃度進行正式干擾試驗。干擾試驗預試驗測定結果見表2(表中,+表示凝膠形成;-表示凝膠未形成)。
2.1.5 正式干擾試驗[2]按2005年版《中國藥典》(一部)細菌內毒素檢查法“供試品干擾試驗”項下規定進行,將2個廠家各3批注射用燈盞花素分別用WBET制成0.25 g·L-1的供試品溶液,用WBET及0.25 g·L-1的供試品溶液將WSE配成濃度為2 λ、λ、0.5λ、0.25λ的試驗液,用2個廠家的TAL進行試驗。結果,Es均在0.5λ~2λ范圍內,且Et也均在0.5Es~2Es范圍內,即0.25 g·L-1供試品濃度對細菌內毒素與TAL的反應無干擾作用(Es、Et表示反應終點濃度的幾何平均值)。正式干擾試驗結果見表3、表4(表中,+表示凝膠形成,-表示凝膠未形成)。
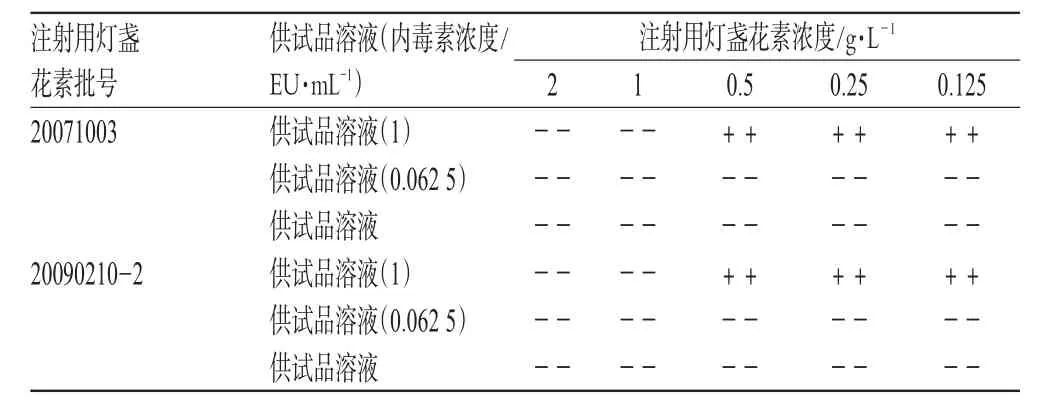
表2 干擾試驗預試驗測定結果Tab 2 Interference pretest results

表3 正式干擾試驗結果(TAL批號:0908281)Tab 3Results of interference test(TALno.0908281)
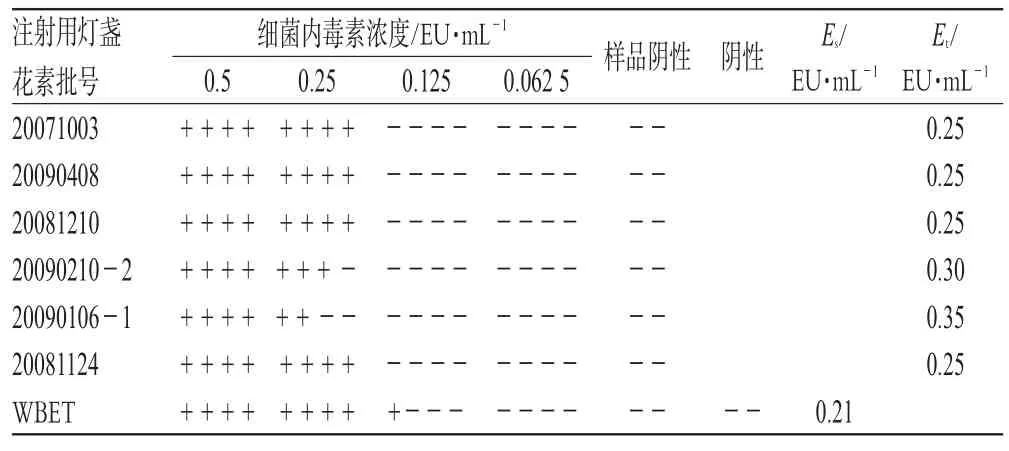
表4 正式干擾試驗結果(TAL批號:0902270)Tab 4Results of interference test(TALno.0902270)
2.2 光度測定法
2.2.1L的確定 按“2.1.2”項下方法進行試驗。
2.2.2 MVC的計算 按“2.1.3”項下方法進行試驗。
2.2.3 檢測波長的確定 注射用燈盞花素溶解后為黃色澄明液體,細菌內毒素測定儀有2種波長可供選擇(450 nm、660 nm)。因黃色物質對檢測光的吸收小,故筆者選擇660 nm為檢測波長。
2.2.4 標準曲線的可靠性試驗 把WSE稀釋為0.24、0.12、0.06、0.03 EU·mL-14個濃度的溶液,制備4個點的標準曲線,進行線性回歸分析。結果,r>0.98、變異系數<10%時符合要求。用WBET稀釋注射用燈盞花素至0.5、0.25、0.125 g·L-1,加入中間濃度為0.12 EU·mL-1的內毒素溶液作標準曲線,摸索供試品溶液在什么濃度下加樣回收率最為理想。結果,回收率均在75%~125%之間,獲得了較為理想的回收率;各稀釋濃度下,樣品細菌內毒素含量均<1 EU·mg-1,細菌內毒素檢查均符合規定,表明可將注射用燈盞花素在660 nm波長處用光度測定法進行試驗。細菌內毒素光度測定法試驗結果見表5(表中,#表示內毒素低于檢測限。TAL批號:0907102)。
3 討論
細菌內毒素檢查法是用TAL與細菌內毒素產生凝聚反應,以判斷供試品中細菌內毒素是否符合規定的一種方法。目前,《美國藥典》絕大多數品種已完成內毒素檢查替代熱原檢查的修訂。英國、日本也正在收集這一替代過程數據,我國也在加速進行試驗研究,以建立更多藥品注射液的細菌內毒素檢查方法。

表5 細菌內毒素光度測定法試驗結果Tab 5 Photometric technical test Results
細菌內毒素檢查法在2005年版《中國藥典》(一部)中收載有凝膠法和光度測定法2種。凝膠法是一限量試驗,操作簡便,主要為檢驗機構判定供試品細菌內毒素限值是否合格的檢驗手段。光度測定法是一定量試驗,主要為藥品生產企業采用,可定量測定供試品中含有的細菌內毒素值,以提高生產質量。注射用燈盞花素目前只有衡陽恒生制藥有限公司和昆明龍津藥業股份有限公司2個生產廠家,筆者對國家評價性抽驗中2個廠家不同規格的6批樣品,使用不同生產廠家和不同靈敏度的TAL進行了干擾試驗。結果表明,高濃度注射用燈盞花素對于TAL與細菌內毒素的凝集反應有干擾(抑制)作用,經稀釋后可以排除;濃度為0.25 g·L-1以野黃芩苷計的注射用燈盞花素對細菌內毒素與TAL的反應無干擾作用。除采用凝膠法進行細菌內毒素檢查,亦可在660 nm波長處用光度測定法進行細菌內毒素檢查。筆者對衡陽恒生制藥有限公司的3批樣品采用光度測定法進行細菌內毒素檢查,昆明龍津藥業股份有限公司的3批樣品采用凝膠法進行細菌內毒素檢查,所有檢查結果與熱原檢查結果一致,均符合規定。結果表明,該藥采用細菌內毒素檢查法代替熱原檢查法,方法可行。
[1]國家藥典委員會編.中華人民共和國藥典(增補本)[S].2005年版.北京:化學工業出版社,2005:6.
[2]國家藥典委員會編.中華人民共和國藥典(一部)[S].2005年版.北京:化學工業出版社,2005:附錄79.
[3]唐元泰.關于注射劑細菌內毒素檢查限值的確定[J].中國藥品標準,2003,4(4):5.
Study on Bacterial Endotoxin Test for Breviscapine for Injection
WANG Lu,ZHANG Hong-yu,LIU Qin(Yunnan Institute for Food and Drug Control,Kunming 650031,China)
OBJECTIVE:To develop bacterial endotoxin test for breviscapine for injection.METHODS:The limit of bacterial endotoxin(L)in this product was confirmed according to the appendix Ⅰ ofChinese Pharmacopoeia(2005 edition).We had studied the interference to bacterial endotoxin test by breviscapine for injection in order to confirm the noninterference concentration with gel clot techniques and photomeric techniques.RESULTS:Lwas 1 EU·mg-1Noninterference concentration of breviscapine for injection for bacterial endotoxin test was 0.25 g·L-1.CONCLUSION:It is feasible for bacterial endotoxin test instead of pyrogen test.
Breviscapine for injection;Bacterial endotoxin;Gel clot techniques;Photometric techniques
R915;R927.12
A
1001-0408(2010)39-3726-03
2010-03-03
2010-05-24)

