催化劑在混酚烷基化中的應用
王 斌,王 慶
(廣州合成材料研究院有限公司,廣東廣州,510665)
催化劑在混酚烷基化中的應用
王 斌,王 慶
(廣州合成材料研究院有限公司,廣東廣州,510665)
將酚鋁、H2SO4和酸性陽離子交換樹脂三種常見酚類催化劑分別添加到異丁烯與混 (間、對)甲酚 (以下簡稱混酚)反應實驗中,比較三者催化效果。實驗結果表明:在反應 2.5h時,以 H2SO4和酸性陽離子交換樹脂為催化劑,混酚的轉化率均達 90%以上,而以酚鋁為催化劑混酚無如此高的轉化率,表明 H2SO4和酸性陽離子交換樹脂的催化活性強于酚鋁。
混酚;烷基化;催化劑;轉化率
對甲酚和間甲酚兩者物理、化學性質都非常相似,常以混合物形式存在。混酚的有效分離一直是生產高純度間甲酚和對甲酚的重要途徑,但由于二者性質接近,沸點也僅相差 0.3℃,通過精餾分離兩者對精餾條件要求高且能耗高。目前國內外都有通過烷基化反應的方法,得到兩者的物理、化學性質有著顯著不同的烷基化產物,再經過精餾等手段分離產物后,通過脫烷基反應還原成對甲酚和間甲酚。此反應需要選擇合適的催化劑將烷基化劑轉變成活潑的烷基正離子,以促進烷基化劑與混酚親電取代反應的進行[1]。本文通過實驗,對比了酚鋁、H2SO4和酸性陽離子交換樹脂三種常用催化劑對混酚烷基化的具體催化效果,并闡述了各自的優點及其不足。
1 混酚烷基化實驗
1.1 反應機理
本次實驗采用異丁烯作為烷基化劑,通過添加不同的催化劑,來研究異丁烯與混酚的反應情況,通過檢測混酚的轉化率來了解不同催化劑的催化活性。由于間甲酚和對甲酚的化學性質非常相似,其烷基化的催化劑也都基本相同。
間甲酚和對甲酚的異丁烯化反應機理如式一、式二:
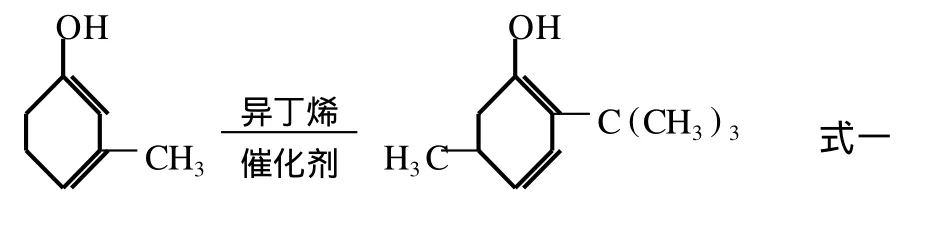
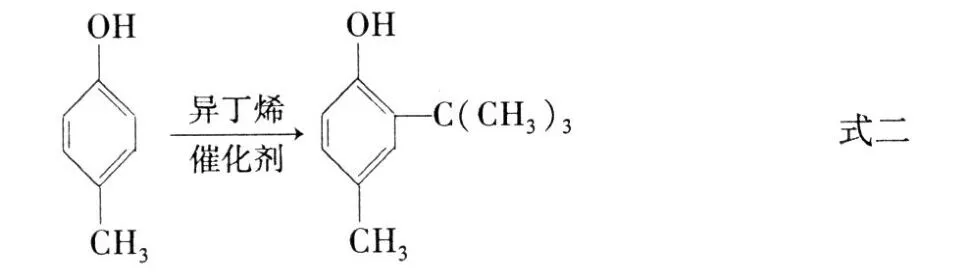
常見可用于酚類的烷基化反應的催化劑有:酸性鹵化物 (如A lB r3、BF3等)、質子酸 (如 H2SO4、HF等)、酸性氧化物 (如 SiO2-A l2O3等)、烷基鋁、樹脂等。本實驗采用了酚鋁、H2SO4和酸性陽離子樹脂三種常用催化劑參與混酚與異丁烯的烷基化反應,固定異丁烯流量為 20L/h,反應溫度選擇各催化劑的最佳催化溫度,添加量選擇各自的有效添加量,通過實驗了解三種不同催化劑的催化效果。
1.2 原料
間甲酚:分析純,純度大于 98%;
對甲酚:分析純,純度大于 98%;
異丁烯:工業級,純度大于 99%,洛陽宏利化工廠提供;
鋁錠:工業級;
H2SO4:分析純,純度 95%;
酸性陽離子交換樹脂:工業級,黑石化提供。
1.3 實驗內容
市場銷售的混酚中間甲酚和對甲酚含量合計約 90%,其中間甲酚與對甲酚的質量比約為 6∶4,另外 10%為它們的同系物或其它雜質。為減少反應的干擾因子,本次試驗用混酚以分析純級的間甲酚和對甲酚自行配制而成,間甲酚與對甲酚的比例為 6∶4。
將配制好的混酚 216g加入連接有溫度計、攪拌槳、放空閥和加溫裝置的四口燒瓶中,加熱攪拌升溫至所需溫度,開始勻速通入異丁烯。反應數小時,并且每隔一定時間取樣檢測混酚的反應情況,至反應中各組分不再有明顯的變化時,停止反應。將不同催化劑在其最佳催化條件下的反應數據進行對比,比較各自的優劣。
2 催化劑的選擇
2.1 酚鋁
酚鋁是一種最常用的烷基鋁類催化劑,實驗時以純的鋁錠顆粒添加到混酚中,高溫成鹽反應得酚鋁,再在合適溫度下通入異丁烯進行烷基化反應。在酚鋁的制備過程中,其它反應條件固定,則催化劑酚鋁的量可用投入金屬鋁的量間接表示,在工業生產中,也直接以鋁的添加量作為催化劑的量。本次實驗鋁錠與混酚的投入質量比為 0.5∶100。分別在 100℃、120℃、140℃三個溫度下進行混酚與異丁烯的烷基化反應,確定最佳反應溫度。
反應條件如下:
催化劑 (鋁)量:1.08g
混酚:216g
異丁烯流速:20L/h
反應溫度:100℃/120℃/140℃
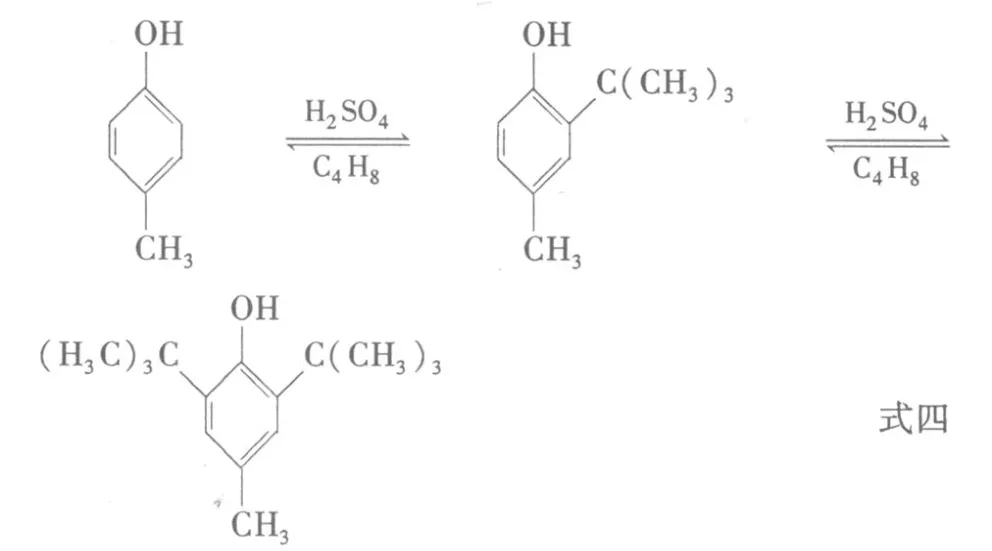
反應結果如圖 1。
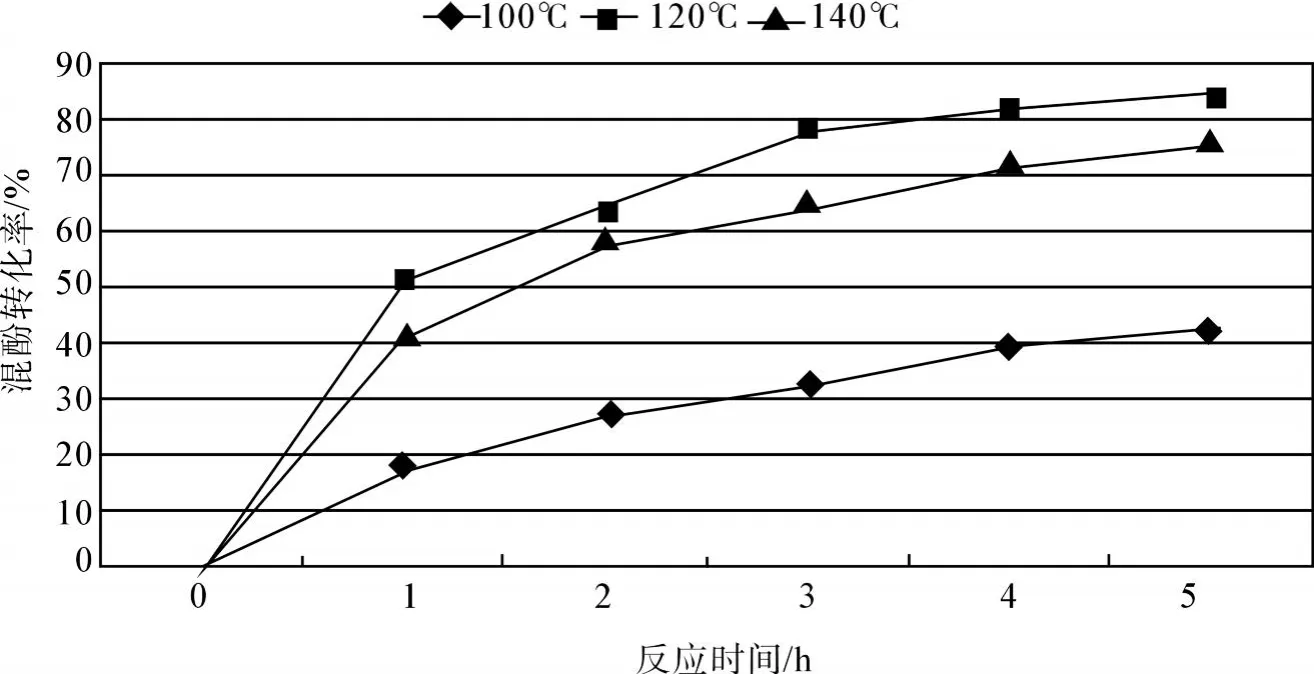
圖 1 酚鋁催化下混酚隨時間轉化率Fig.1 Mixed cresol conversion with action time by Aluminum salt of phenol
由圖 1可以看出,以酚鋁為催化劑,反應溫度為 120℃時混酚各個時段的轉化率都明顯高于其它溫度,說明 120℃為酚鋁的最佳催化溫度。在120℃反應時,前 3h反應劇烈,混酚轉化率迅速達到 78%,之后反應逐漸放緩,在 5h后混酚轉化率達到 85%。
2.2 H SO24
在烷基化反應中,H2SO4是 H+酸中最常用到的催化劑,H2SO4既是酚的烷基化反應的催化劑,也是脫烷基化反應的催化劑。在低溫時促進烷基化反應進行,較高溫度時則促進脫烷基化反應進行,因此以 H2SO4作為烷化反應催化劑時反應溫度的選擇至關重要。作者經過多次實驗,發現在 60℃以下烷基化反應緩慢。參考對甲酚在酸性催化劑催化下生產抗氧劑 BHT的相關文獻報道[2-3],最終確定 65℃作為本次實驗的反應溫度,取得了較好的實驗結果。H2SO4的濃度也需恰當選擇,不同濃度的 H2SO4在反應中所起作用不同,本次實驗選擇濃度系數 95%的濃 H2SO4作為反應催化劑,H2SO4與混酚的質量比為 5∶100。
反應條件如下:
催化劑 (H2SO4)質量:10.8g
混酚:216g
異丁烯流速:20L/h
反應溫度:65℃
反應結果如圖 2。

圖 2 硫酸催化下混酚隨時間轉化率Fig.2 Mixed cresol conversion with action time by H2 SO4
由圖 2可以看出,以 H2SO4為催化劑在 65℃參與反應,前 2h烷基化反應迅速進行,混酚轉化率達到 89%,之后反應趨于緩慢,在反應 5h后混酚轉化率達到最大值 99%,之后反應發生逆轉,混酚轉化率減小,說明有部分已經烷基化的混酚又發生了脫烷基反應。混酚烷基化反應的可逆反應表示如反應方程式三、式四。
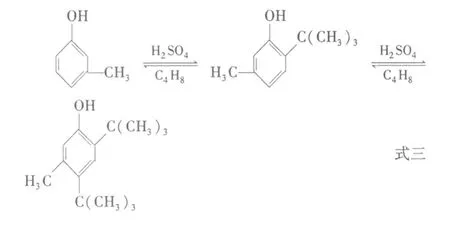
因此在以 H2SO4為催化劑時,除考慮 H2SO4的濃度、添加量外,反應時間也需嚴格控制,在混酚基本完成烷基化反應后,應立即停止反應,若繼續延長反應時間將導致脫烷基化反應進行。
2.3 酸性陽離子樹脂
酸性陽離子樹脂也是一種 H+酸型催化劑,在許多烷基酚的合成中已經被廣泛應用,本次實驗中酸型陽離子樹脂的添加質量參考文獻 [4]中同類反應的添加質量,樹脂與混酚的質量比為 15∶100。分別在 100℃、120℃、140℃三個溫度下進行混酚的烷基化反應,比較在各溫度下反應混酚的轉化率并確定最佳反應溫度。
反應條件如下:
催化劑 (酸性陽離子樹脂)質量:32.4g
混酚:216g
異丁烯流速:20L/h
反應溫度:100℃/120℃/140℃
反應結果如圖 3。
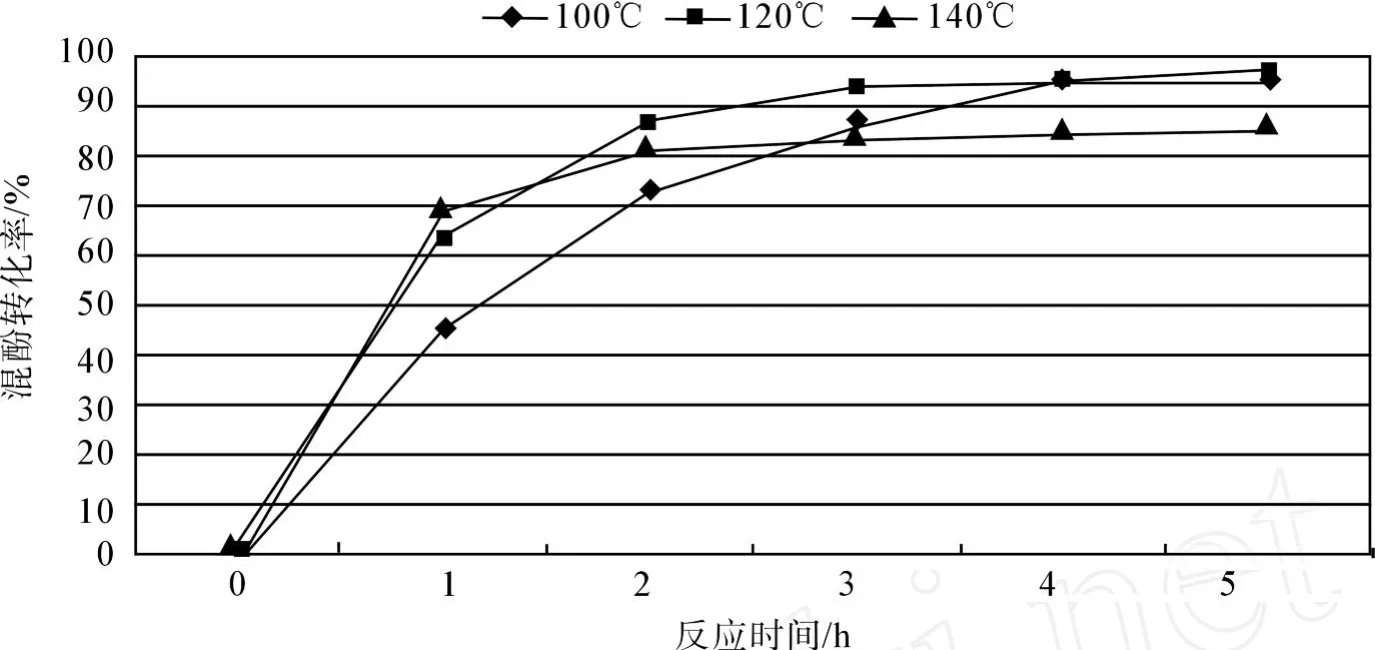
圖 3 酸性陽離子樹脂催化下混酚隨時間轉化率Fig.3 Mixed cresol conversion with action time by acid cation resin
由圖 3可以看出,酸性陽離子樹脂的催化活性非常強,在 100~140℃之間都有較高的轉化率。比較發現在 100℃時溫度低,開始階段反應緩慢,但經過 4h的反應后轉化率也能達到 90%以上。140℃時因反應溫度較高,反應開始至反應 1h階段混酚轉化率最高,反應 2h過后反應進程非常緩慢,可能的原因是反應在較高溫度下較易發生逆反應,達到正逆反應平衡所致。綜合考慮,120℃時樹脂的催化效果最佳,反應前 2h混酚轉化率迅速提高,達到 87%,之后反應緩慢,3h過后反應趨于平衡, 5h后混酚轉化率達 96%。
3 結果分析
在混酚用量、異丁烯流量、壓強都相同的條件下,選擇三種催化劑的最佳催化曲線進行比較,結果見圖 4。
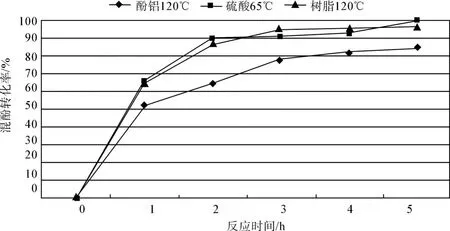
圖 4 不同催化劑催化下的混酚隨時間轉化率Fig.4 Mixed cresol conversion with action time by different catalysts
由圖 4可以看出,在各自的最佳催化條件下,酚鋁的催化效果明顯較差,在各個反應時間段混酚的轉化率都低于 H2SO4和樹脂,反應 3h過后反應速率也明顯下降。H2SO4和樹脂的催化效果相當,都是在大約 2h反應時間后出現拐點,兩小時之前反應迅速進行,兩小時之后反應進程逐漸緩慢下來。以混酚轉化率達到 80%所需反應時間來比較,以酚鋁為催化劑時約需 3.5h,樹脂約為 1.7h, H2SO4約為 1.6h,以 H2SO4和樹脂為催化劑的反應時間比酚鋁快了一倍有余。而在反應至 2.5h時,以 H2SO4和樹脂為催化劑的混酚轉化率同時達到90%,而酚鋁至反應 5h結束時混酚轉化率僅達85%。
4 結論
(1)酚鋁作為一種酚、胺類烷化反應的鄰位催化劑,鄰位催化作用非常強,鄰位催化的專一性是 H2SO4和酸性陽離子樹脂不能取代的。缺點是酚鋁的催化活性不及 H2SO4和酸性陽離子樹脂,回收難,且酚鋁用作混酚的催化劑時,一般都是通過鋁錠與混酚高溫反應制得酚鋁后立即進行烷基化,以保證酚鋁有較高的活性,酚鋁的催化性能也會不可避免地受到此步反應的影響。
(2)H2SO4的催化活性非常強,在足夠的時間內,H2SO4做催化劑可以將混酚轉化 99%以上,而且反應溫度低。H2SO4的不足在于其較大的腐蝕性,這對反應設備損害較大,且在后期需對反應產物進行中和處理。
(3)酸性陽離子樹脂的催化活性與 H2SO4相當,在常用的以烯烴為烷基化劑的反應中,是特別有效的催化劑,副反應少[1]、使用方便、回收簡單、無腐蝕性,一次性投料多次使用,本次試驗用樹脂總共經 23次烷化實驗,催化活性不減。缺點是酸性陽離子樹脂使用溫度有一定限度,脫離有效使用溫度會失效,且一旦樹脂經碰撞、磨損,溶脹等原因破裂受損,影響收率。
(4)綜合考慮,三種催化劑都有各自的優點及不足,在混酚烷化反應中,采用酸性陽離子交換樹脂做催化劑最為合適。
在本次試驗中,未控制反應壓力,反應器與外界連通,勻速通入異丁烯參與反應,異丁烯的總量是過量的,反應壓強為一個大氣壓。作為氣-液反應,反應壓強是一個非常重要的因素,改變壓強,反應的進程很可能產生較大變化,未對這一反應因子進行優化是本次試驗的不足。
[1]田鐵牛.有機合成單元過程 [M].2005,3: 160-162.
[2]李梅,韓偉,蔣魏.混酚制備抗氧劑 264及300[J].吉林化工學院學報,2000,17(3): 26-27.
[3]王正平,任衛東.抗氧劑 264生產工藝的研究[J].化學工程師,1998,4(67):34-36.
[4]王裕康,孫志剛.H型陽離子交換樹脂在催化合成烷基酚中的工業應用 [J].離子交換與吸附,1994,10(2):164-167.
The Application of Catalyst in the Alkylation of the Mixture of M-cresol and P-cresol
WANG Bin,WANG Qing
(Guangzhou Research Institute of Synthetic Materials Co.Ltd.,Guangzhou 510665, Guangdong,China)
Aluminum salt of phenol,H2SO4and acid cation exchange resin are three kinds of common phenolic catalyst.Each catalyst was added to the reaction of is obutene and the mixture of M-cresol and P-cresol(hereinafter referred to as the mixed cresol)to compare the catalytic effectiveness.It show s thatwhen H2SO4o r acid cation exchange resin was added,the conversion of mixed cresol is more than 90%after2.5hours,while Aluminum salt of phenol could'tget90%.The result indicate that the catalytic activity of H2SO4and acid cation resin is better than aluminum salt of phenol.
mixed cresol;alkylation;catalyst; conversion
TQ 02
2010-10-28

