食品添加劑檸檬酸三鈉綠色生產工藝的研究
周本華,張懷紅
(1.鹽城工學院化學與生物工程學院,江蘇鹽城224051;2.東南大學化學化工學院,江蘇南京211189)
食品添加劑檸檬酸三鈉綠色生產工藝的研究
周本華1,2,張懷紅1,2
(1.鹽城工學院化學與生物工程學院,江蘇鹽城224051;2.東南大學化學化工學院,江蘇南京211189)
傳統的檸檬酸三鈉生產工藝存在生產成本高、造成環境污染等缺點。研究了檸檬酸三鈉綠色生產工藝中的影響因素。通過一系列實驗研究,確定了最佳工藝條件:檸檬酸鈣投料結束時,反應液的pH達到10.0以上;碳酸鈉溶液的濃度為20%;反應時間為30min;反應溫度為80℃。在最佳工藝條件下,檸檬酸鈣的轉化率達到99.7%,檸檬酸三鈉的產率達到98.6%。與傳統工藝相比,新工藝遵循發展循環經濟的指導方針,既達到了節能減排與清潔生產的目的,同時又降低了生產成本。
食品添加劑,檸檬酸三鈉,檸檬酸鈣,碳酸鈉,綠色生產工藝
檸檬酸三鈉,又名枸櫞酸鈉,白色立方晶系結晶或粉末,無臭,清涼,味咸;常溫下穩定,加熱到150℃失去結晶水。ADI對本品毒性不作規定(FAO/ WHO,1994),屬無毒品[1-2]。檸檬酸三鈉在工業上是一種非常重要的檸檬酸鹽,用途十分廣泛,可用于食品、醫藥、電鍍、環保、材料及洗滌劑等行業。由于檸檬酸三鈉無毒性,具有pH調節性能及良好的穩定性,因此被大量用于食品工業,主要用作調味劑、緩沖劑、乳化劑、膨脹劑、穩定劑和防腐劑。另外,檸檬酸三鈉同檸檬酸配伍,用作各種果醬、果凍、果汁、飲料、冷飲、奶制品和糕點等的膠凝劑、營養增補劑及風味劑[3-5]生產檸檬酸三鈉的傳統工藝過程是:將檸檬酸發酵液過濾,往濾液里加入碳酸鈣,得到檸檬酸鈣沉淀。用硫酸酸解檸檬酸鈣,然后過濾、脫色、離子交換,得到檸檬酸。檸檬酸與碳酸鈉反應并經過一系列后處理工序,最后得到檸檬酸三鈉。該方法存在明顯的不足:硫酸對環境造成嚴重污染;副產物硫酸鈣對水土造成污染,成為環保一大難題[6]。另外,原料成本高,操作步驟繁多,生產周期長。本工作研究了利用發酵法生產檸檬酸的中間體檸檬酸鈣通過復分解法直接制備檸檬酸三鈉的新工藝。副產物碳酸鈣能夠循環利用,避免污染環境,從而探索一條節能減排、清潔生產的綠色工藝路線。同時,縮短了生產周期,降低了生產成本,提高了檸檬酸三鈉的質量,可以更好地滿足市場對該產品的多種需要。
1 材料與方法
1.1 材料與儀器
檸檬酸鈣 中間體;碳酸鈉 連云港中銘化工有限公司,食品級;檸檬酸,高氯酸 上海實驗試劑有限公司,分析純;活性炭 溧陽竹溪活性炭有限公司;結晶紫 天津市化學試劑一廠,分析純;冰乙酸,乙酸酐 上海凌峰化學試劑有限公司,分析純;酚酞指示劑 天津市科密歐化學試劑有限公司,分析純。
PHS-3C精密pH計 上海雷磁儀器廠;SX2-5-12箱式電阻爐 上海市實驗儀器總廠;JJ-1精密增力電動攪拌器 常州國華電器有限公司;SHZ-3循環水真空泵 上海華光儀器儀表廠;YJ-501型超級恒溫器 上海躍進醫療器械廠;常規玻璃儀器。
1.2 反應原理及工藝路線
檸檬酸鈣和碳酸鈉在適當的條件下發生復分解反應,生成檸檬酸三鈉和碳酸鈣沉淀,反應方程式如下:
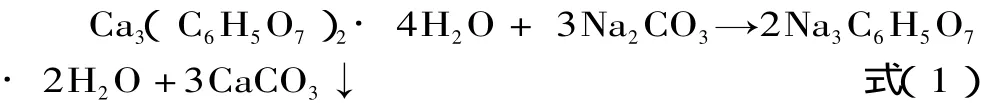
由于碳酸鈣在水中的溶解度遠遠小于檸檬酸鈣的溶解度[7],因此,當檸檬酸鈣與碳酸鈉在水中混合時,檸檬酸鈣與碳酸鈉發生反應,生成檸檬酸三鈉和碳酸鈣。碳酸鈣以沉淀形式從反應體系中不斷析出,從而使反應持續進行下去。工藝路線如下:

圖1 檸檬酸三鈉生產工藝流程
1.3 實驗方法
1.3.1 檸檬酸三鈉的制備 稱取一定量的碳酸鈉,加適量水攪拌溶解,使碳酸鈉溶液的濃度達到20%~30%,加熱升溫至70~90℃。然后在快速攪拌下將檸檬酸鈣料漿分多次逐漸加入碳酸鈉溶液中。在pH接近10.0時,停止投入檸檬酸鈣。恒溫反應一段時間,趁熱過濾,往濾液中加入活性炭微沸10min。趁熱過濾,用少量檸檬酸調整溶液的pH,再依次進行減壓濃縮、冷卻析晶、分離、干燥,最后得到檸檬酸三鈉產品。
1.3.2 產品中Na3C6H5O7·2H2O含量以及產品在180℃干燥失重后Na3C6H5O7含量的分析 分別按照國標GB6782-86及美國FCC-IV實驗方法測定[8-9]。
1.3.3 原料及濾餅中檸檬酸鈣含量的分析 準確稱取干燥過的樣品0.1g左右,置于100mL燒杯里,加30mL蒸餾水,再加適量處理成H型的強酸性陽離子交換樹脂,攪拌均勻,靜置。溶液澄清后,過濾,用蒸餾水洗滌樹脂,直至濾液pH接近蒸餾水的pH(樣品若是濾餅,則此時溶液需要煮沸5min)。往濾液里加兩滴5%酚酞指示劑,用濃度為0.1mol/L的NaOH標準溶液滴定至溶液呈淡紅色,且保持30s不褪色。以質量百分數表示的檸檬酸鈣含量(X)按下式計算:
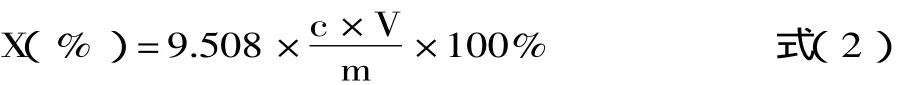
式中:X為檸檬酸鈣的百分比含量,%;c為氫氧化鈉標準溶液的濃度,mol/L;V為氫氧化鈉標準溶液的滴定量,mL;m為樣品質量,g;9.508為根據化學反應方程式得到的換算系數。
1.3.4 檸檬酸鈣轉化率的求算 因檸檬酸鈣在水中微溶,所以極少量未反應的檸檬酸鈣過濾后幾乎全部存在濾餅(主要成分為碳酸鈣)中。根據1.3.3部分求出濾餅中檸檬酸鈣含量,再由原料中檸檬酸鈣的量,按下式求出反應中檸檬酸鈣的轉化率:

式中:T為反應中檸檬酸鈣的轉化率(%);A為原料中檸檬酸鈣的質量(g);B為濾餅中檸檬酸鈣的質量(g)。
1.3.5 檸檬酸三鈉產率的求算 產品在60℃條件下烘干并稱重。按照美國FCC-IV的實驗方法,測定產品在180℃條件下的干燥失重,換算成失重前產品中Na3C6H5O7·2H2O的含量;將原料 Na2CO3換算成Na3C6H5O7·2H2O的量。最后按下式求出產率:

式中:P為檸檬酸三鈉的產率(%);X為反應原料Na2CO3換算成Na3C6H5O7·2H2O的量(g);Y為產品中Na3C6H5O7·2H2O的量(g)。
2 結果與討論
2.1 投料順序
實際操作中加入原料的順序可以有三種:一是將檸檬酸鈣在不斷攪拌條件下加水稀釋溶解,然后加入碳酸鈉;二是將碳酸鈉和檸檬酸鈣兩者各自在攪拌情況下溶解于水,然后混合;三是將碳酸鈉在攪拌下溶解于水,然后加入原料檸檬酸鈣。
經過大量實驗發現,第一種方法即先將檸檬酸鈣稀釋,再逐漸加入碳酸鈉,則得到的產物含量不合格,分析發現有較多的副產物檸檬酸一鈉和檸檬酸二鈉生成。最適宜的投料順序為最后一種,即將碳酸鈉在攪拌下溶解于水,然后加入原料檸檬酸鈣,不僅得到的產品純度高,而且產生的熱量有利于促進復分解反應的進行,同時一定程度上自行提高反應體系的溫度,降低能耗。
2.2 檸檬酸鈣的投料控制
若通過原料的反應比直接控制投料,生產上將很難操作,因為大批量發酵法生產檸檬酸的中間品檸檬酸鈣每個點的含量高低不一,使得反應原料的摩爾比很難通過質量控制,且操作不便。由于反應液的pH與原料反應比之間具有一定關系,因此,完全可以借助反應液的pH來控制投料,而且快速簡便,穩定性好。反應液pH對產品檸檬酸三鈉含量的影響如表1所示。
反應液pH對檸檬酸鈣轉化率的影響如圖2所示。
可見,投料終點反應液的pH大于10.0時,產品檸檬酸三鈉的含量達到99.0%以上,而且檸檬酸鈣的轉化率不低于99.3%。需要指出的是投料終點反應液pH越高,溶液濃縮前調整pH時檸檬酸消耗量就越大,導致生產成本上升。因此,從節約成本角度考慮,投料終點反應液的pH不能太高。
綜合考慮上述情況,檸檬酸鈣投料結束時,反應液的pH宜控制在10.0以上,在此前提條件下,反應液的pH越低越好。

表1 反應液pH對產品檸檬酸三鈉含量的影響
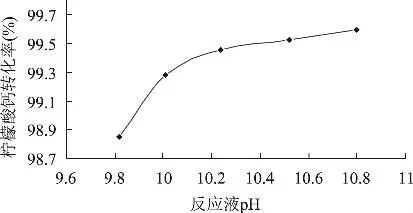
圖2 反應液pH對檸檬酸鈣轉化率的影響
2.3 碳酸鈉濃度對檸檬酸鈣轉化率的影響
將料漿中檸檬酸鈣含量固定在24%,用同批原料進行一組碳酸鈉濃度變化的條件實驗,結果如圖3所示。
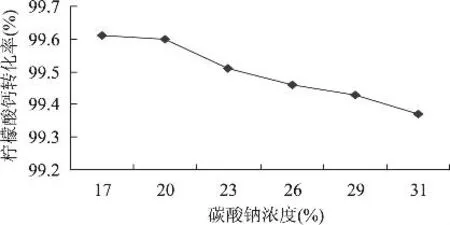
圖3 碳酸鈉濃度對檸檬酸鈣轉化率的影響
可見,檸檬酸鈣的轉化率隨碳酸鈉濃度的降低而上升。另外,若碳酸鈉濃度過低,則后續工段檸檬酸三鈉溶液濃縮慢,將耗費更多時間和能量;相反,若碳酸鈉濃度過高,則攪拌困難,反應時間延長。綜合考慮以上各種因素,碳酸鈉濃度宜取20%。
2.4 反應時間對檸檬酸鈣轉化率的影響
用同批原料進行不同反應時間條件下的一組實驗,結果如圖4所示。由圖4可見,檸檬酸鈣與碳酸鈉直接發生復分解反應,反應程度與反應時間有很大關系。隨著反應時間的增加,檸檬酸鈣的轉化率逐漸增大。反應30min后,增幅開始減緩,說明此時反應漸趨平衡。
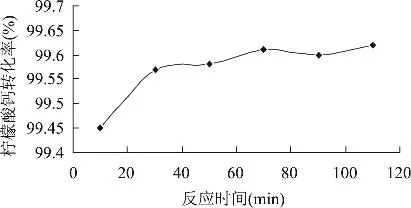
圖4 反應時間對檸檬酸鈣轉化率的影響
2.5 反應溫度對檸檬酸鈣轉化率的影響
用同批原料分別進行60、80、90℃條件下的三組實驗,實驗結果如圖5。
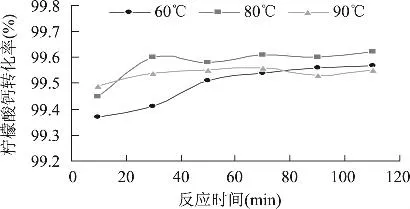
圖5 反應溫度對檸檬酸鈣轉化率的影響
如示。由圖5可見,反應溫度低,則轉化率隨時間增加上升的慢,反應到達平衡需要的時間長;溫度升高,則轉化率隨時間增加上升的快,反應到達平衡需要的時間短,但平衡轉化率上升后又出現略微下降。這可能是由于溫度對檸檬酸鈣和碳酸鈣的溶解度產生不同的影響造成的結果。因為溫度升高,產物碳酸鈣的溶解度增大,而反應物檸檬酸鈣的溶解度卻降低[10]。
檸檬酸鈣轉化率的高低與檸檬酸三鈉收率的高低具有一致性,所以,從生產實際考慮,當然希望檸檬酸鈣的轉化率高。另外,還希望反應時間盡量短,以縮短生產周期;反應溫度盡量低,以降低能耗。綜合考慮上述多種因素,選擇80℃下反應30min比較適宜。
3 結論
通過大量的實驗,在確認新工藝可行的基礎上,對一系列工藝參數進行了研究和優化,得出如下結論:將碳酸鈉在攪拌下溶解于水,然后加入原料檸檬酸鈣;檸檬酸鈣投料結束時,反應液的pH達到10.0以上;碳酸鈉溶液濃度為20%;反應時間為30min;反應溫度為80℃。在此工藝條件下,檸檬酸鈣的轉化率達到99.7%,檸檬酸三鈉的產率達到98.6%,且質量符合GB6782-86及FCC-IV。
以檸檬酸鈣和碳酸鈉為原料經復分解反應生產檸檬酸三鈉的工藝路線,不僅具有工藝簡單、成本低的優點,而且產生的碳酸鈣可直接返回發酵工段,用于檸檬酸鈣的生產,實現了循環經濟。另外,新工藝與傳統工藝相比,不產生污染環境的副產物硫酸鈣,不使用對環境極具污染性的危險品硫酸,達到了節能減排和清潔生產的目的,是一條綠色工藝路線。
[1]任小卉.檸檬酸鈉生產淺談[J].醫藥化工,2006(5):33-35.
[2]孫寶國.日用化工辭典[M].北京:化學工業出版社,2002:454.
[3]張英,周長民.檸檬酸鈉的特性與應用[J].遼寧化工,2007,36(5):350-352.
[4]李炳根,趙博謙.磷酸鹽、檸檬酸鈉、碳酸氫鈉、加熱對梔子紅色素色價的影響[J].現代食品科技,2006,22(4):99-103.
[5]上官新晨,蔣艷.檸檬酸鈉鹽與海藻酸鈉對果汁酸牛乳中酪蛋白穩定協同效應的實驗[J].食品科學,1990(9):25-27.
[6]趙君民,劉榮杰,劉春蓮,等.檸檬酸鈉生產新工藝研究[J].西北大學學報:自然版,1998,28(1):48.
[7]William F L.Solubilities(Inorganic and Metal-organic Compounds)Fourth edition[M].Princeton:D.Van.Nostrand Company,Inc,1958:520,537.
[8]中國食品工業標準匯編-食品添加劑卷選編組編.中國食品工業標準匯編-食品添加劑(上)[M].北京:中國標準出版社,1997:190-194.
[9]美國FCC-IV標準[S].
[10]William F L.Solubilities(Inorganic and Metal-organic Compounds)Fourth edition[M].Princeton:D.Van.Nostrand Company,Inc,1958:520,537.
Study on green technology for food additive sodium citrate production
ZHOU Ben-hua1,2,ZHANG Huai-hong1,2
(1.School of Chemical and Biological Engineering,Yancheng Institute of Technology,Yancheng 224051,China;2.College of Chemistry and Chemical Engineering,Southeast University,Nanjing 211189,China)
The traditional production process for sodium citrate has some shortcomings,such as high production costs and resulting in environmental pollution,etc.Some factors affecting green technology for sodium citrate production were studied.Through a series of experimental studies the optimum conditions were determined in the end.The pH value of reaction solution was more than 10.0 when feeding calcium citrate ended.The appropriate concentration of sodium carbonate was 20%.Suitable reaction time was 30min.Suitable reaction temperature was 80℃.The percentage conversion of calcium citrate was up to 99.7%and the yield percentage of sodium citrate was up to 98.6%under the optimum reaction conditions.Compared with the traditional process,the new technology not only realize the energy saving and clean production,but also cut down the production cost under the guidance of the policy for the development of circular economy.
food additive;sodium citrate;calcium citrate;sodium carbonate;green production technology
TS202.3
A
1002-0306(2010)12-0300-04
2010-06-28
周本華(1969-),男,講師,博士研究生,主要從事精細化學品研究與開發及創新藥物研究工作。

