GC法測(cè)定鹽酸金剛烷胺片中有關(guān)物質(zhì)含量
陳 佩,翟 宇(寧夏回族自治區(qū)藥品檢驗(yàn)所,銀川市 750004)
鹽酸金剛烷胺片用于治療帕金森病、藥物誘發(fā)的錐體外系疾患,也用于防治A型流感病毒所引起的呼吸道感染。《中國(guó)藥典》2005、2010年版[1,2]中未收載鹽酸金剛烷胺片有關(guān)物質(zhì)的測(cè)定方法,《美國(guó)藥典》(USP)[3]和《英國(guó)藥典》(BP)[4]也只對(duì)鹽酸金剛烷胺原料藥有關(guān)物質(zhì)作了規(guī)定。而片劑在制粒、包衣以及貯存過程中均有可能會(huì)導(dǎo)致有關(guān)物質(zhì)產(chǎn)生或增加,影響藥品的療效[5]。故本文參考《中國(guó)藥典》2010年版中鹽酸金剛烷胺原料藥有關(guān)物質(zhì)的測(cè)定方法,建立了氣相色譜(GC)法測(cè)定鹽酸金剛烷胺片中的有關(guān)物質(zhì)含量。該方法靈敏、準(zhǔn)確、專屬性強(qiáng),可用于鹽酸金剛烷胺片的質(zhì)量控制。
1 儀器與試藥
6890N氣相色譜儀及工作站(美國(guó)Agilent公司)。
鹽酸金剛烷胺標(biāo)準(zhǔn)品(中國(guó)藥品生物制品檢定所,批號(hào):100426-200301,含量:100.0%);金剛烷(美國(guó)Chromadex公司,批號(hào):01380-L01,含量:99.9%);41批鹽酸金剛烷胺片(國(guó)內(nèi)8家藥廠提供,批號(hào)略,規(guī)格:每片0.1 g);三氯甲烷為分析純,鹽酸、氫氧化鈉、雙氧水、無水硫酸鈉均為優(yōu)級(jí)純。
2 方法與結(jié)果
2.1 色譜條件
色譜柱為HP-5(30 m×0.32 mm,0.25 μm);載氣為氮?dú)猓粴浠鹧骐x子化檢測(cè)器(FID),進(jìn)樣口溫度為200℃,檢測(cè)器溫度為300℃;柱溫采用程序升溫,初始溫度為80℃,保持4 min,然后以12℃·min-1升溫至280℃,保持15 min;載氣流速為1.0 mL·min-1;溶液進(jìn)樣,進(jìn)樣體積為2 μL。
2.2 溶液的制備
2.2.1 鹽酸金剛烷胺標(biāo)準(zhǔn)品溶液。精密稱取鹽酸金剛烷胺標(biāo)準(zhǔn)品2.000 g,置于分液漏斗中,加5 mol·L-1氫氧化鈉溶液20 mL,用三氯甲烷分次振搖提取(15、10 mL),靜置分層;取三氯甲烷層,加適量無水硫酸鈉振搖脫水,濾過;取濾液置于25 mL容量瓶中,用三氯甲烷稀釋至刻度,搖勻,作為標(biāo)準(zhǔn)品貯備溶液。精密量取貯備液1 mL置于10 mL容量瓶中,用三氯甲烷稀釋至刻度,搖勻,作為標(biāo)準(zhǔn)品溶液。
2.2.2 鹽酸金剛烷胺供試品溶液。取鹽酸金剛烷胺片樣品20片,精密稱定,研細(xì),精密稱取適量(約相當(dāng)于鹽酸金剛烷胺1.25 g),置于分液漏斗中,加5 mol·L-1氫氧化鈉溶液20 mL,用三氯甲烷分次振搖提取(15、10 mL),取三氯甲烷層,加適量無水硫酸鈉振搖脫水,濾過,取濾液置于25 mL容量瓶中,用三氯甲烷稀釋至刻度,搖勻,作為供試品溶液。
2.2.3 金剛烷溶液。精密稱取金剛烷0.5 g,置于10 mL容量瓶中,加三氯甲烷溶解并稀釋至刻度,搖勻。
2.2.4 輔料溶液。按處方量稱取輔料(約相當(dāng)于含鹽酸金剛烷胺1.25 g的量),按“2.2.2”項(xiàng)下方法制備輔料溶液。
2.3 系統(tǒng)適用性試驗(yàn)
精密量取“2.2.3”項(xiàng)下金剛烷溶液1 mL,置于100 mL容量瓶中,加鹽酸金剛烷胺供試品溶液1 mL,用三氯甲烷稀釋至刻度,搖勻,作為系統(tǒng)適用性試驗(yàn)溶液。取此試驗(yàn)溶液及“2.2”項(xiàng)下鹽酸金剛烷胺標(biāo)準(zhǔn)品溶液、鹽酸金剛烷胺供試品溶液、輔料溶液各2 μL,注入氣相色譜儀,記錄色譜,見圖1。
由圖1可知,鹽酸金剛烷胺保留時(shí)間約為14.1 min,金剛烷保留時(shí)間約為11.1 min,鹽酸金剛烷胺峰與金剛烷峰(分離度大于20)及其他物質(zhì)峰的分離度良好。

圖1 系統(tǒng)適用性試驗(yàn)色譜圖A.輔料;B.標(biāo)準(zhǔn)品;C.供試品;D.系統(tǒng)適用性試驗(yàn)溶液;1.鹽酸金剛烷胺;2.金剛烷Fig 1 The chromatogram of system suitability testA.blank excipient;B.reference substance;C.test sample;D.solution of system suitability;1.amantadine hydrochloride;2.adamantane
2.4 專屬性試驗(yàn)
精密稱取鹽酸金剛烷胺片細(xì)粉適量(約相當(dāng)于鹽酸金剛烷胺1.25 g)共5份,進(jìn)行如下處理。(1)酸破壞:加0.1 mol·L-1鹽酸溶液10 mL使鹽酸金剛烷胺溶解,在50℃水浴加熱20 min,放置至室溫,加0.1 mol·L-1氫氧化鈉溶液中和;(2)堿破壞:加1 mol·L-1氫氧化鈉溶液10 mL使鹽酸金剛烷胺溶解,在80℃水浴加熱50 min,放置至室溫,加1 mol·L-1鹽酸溶液中和;(3)氧化破壞:加雙氧水10 mL使鹽酸金剛烷胺溶解,放置過夜;(4)高溫破壞:在105℃烘箱中加熱過夜;(5)光照破壞:在5 000 lx照度下光照過夜。上述5份樣品均加入5 mol·L-1氫氧化鈉溶液20 mL,用三氯甲烷分次振搖提取(15、10 mL),靜置分層;取三氯甲烷層,加適量無水硫酸鈉振搖脫水,濾過,取濾液置于25 mL容量瓶中,用三氯甲烷稀釋至刻度,搖勻。分別取上述5種溶液,按“2.1”項(xiàng)下的色譜條件測(cè)定,記錄色譜。結(jié)果,各破壞條件下均有不同程度的降解產(chǎn)物生成,但均能與主峰達(dá)到完全分離,表明該方法專屬性好,詳見圖2。

圖2 專屬性試驗(yàn)色譜圖A.酸破壞后樣品;B.堿破壞后樣品;C.氧化破壞后樣品;D.高溫破壞后樣品;E.光照破壞后樣品;1.鹽酸金剛烷胺Fig 2 The chromatogram of exclusion inspectionA.sample destroyed by acid;B.sample destroyed by alkali;C.sample destroyed by oxidation;D.sample destroyed by high temperature;E.sample destroyed by high light;1.amantadine hydrochloride
2.5 線性關(guān)系考察
精密量取“2.2.1”項(xiàng)下鹽酸金剛烷胺標(biāo)準(zhǔn)品貯備溶液0.5、1.0、2.0、3.0、4.0、5.0 mL置于5 mL容量瓶中,用三氯甲烷溶液稀釋至刻度,搖勻。分別精密量取上述不同濃度溶液2 μL,按“2.1”項(xiàng)下色譜條件進(jìn)樣測(cè)定,以各溶液濃度(X,mg·mL-1)為橫坐標(biāo),峰面積(A)為縱坐標(biāo),進(jìn)行線性回歸。結(jié)果表明,進(jìn)樣濃度在8.03~80.3 mg·mL-1的范圍內(nèi),與測(cè)定的峰面積呈良好的線性關(guān)系:A=6.489×105X+4.060(r=0.999 9,n=6)。
2.6 穩(wěn)定性試驗(yàn)
取“2.2”項(xiàng)下鹽酸金剛烷胺標(biāo)準(zhǔn)品和供試品溶液,分別在0、1、4、12 h進(jìn)樣測(cè)定。結(jié)果鹽酸金剛烷胺標(biāo)準(zhǔn)品溶液放置12 h穩(wěn)定,鹽酸金剛烷胺峰面積的RSD=0.8%;供試品溶液中雜質(zhì)峰面積未有明顯增加,鹽酸金剛烷胺峰面積的RSD=1.2%。
2.7 精密度試驗(yàn)
精密量取“2.2.1”項(xiàng)下鹽酸金剛烷胺標(biāo)準(zhǔn)品貯備溶液1.0 mL,置于5 mL容量瓶中,用三氯甲烷溶液稀釋至刻度,搖勻。連續(xù)進(jìn)樣6次,測(cè)定。結(jié)果,鹽酸金剛烷胺峰面積值的RSD=1.1%。
2.8 最低檢測(cè)限
精密量取“2.2.1”項(xiàng)下鹽酸金剛烷胺標(biāo)準(zhǔn)品貯備溶液適量,用三氯甲烷逐步稀釋,測(cè)定,以鹽酸金剛烷胺峰的信噪比(S/N)為3計(jì)算,測(cè)得其最低檢測(cè)限為0.22 μg。
2.9 回收率試驗(yàn)
分別精密稱取鹽酸金剛烷胺標(biāo)準(zhǔn)品1.0、1.25、1.5 g各3份,分置于9個(gè)分液漏斗中,分別加入輔料適量,按“2.2.2”項(xiàng)下方法制備成低、中、高3個(gè)濃度的溶液各3份。取上述溶液進(jìn)樣2 μL測(cè)定,記錄色譜。計(jì)算鹽酸金剛烷胺回收率,結(jié)果低、中、高濃度回收率(n=3)分別為92.1%、97.3%、95.5%,RSD分別為2.8%、2.1%、1.9%,表明準(zhǔn)確度良好。
2.10 樣品中有關(guān)物質(zhì)的含量測(cè)定
取鹽酸金剛烷胺片樣品20片,按“2.2.2”項(xiàng)下方法制備供試品溶液,加入金剛烷溶液。精密量取“2.3”項(xiàng)下系統(tǒng)適用性試驗(yàn)溶液2 μL,注入氣相色譜儀,調(diào)節(jié)檢測(cè)靈敏度,使主成分色譜峰的峰高約為滿量程的20%,金剛烷胺峰與金剛烷峰的分離度應(yīng)不小于20。精密量取供試品溶液2 μL,注入氣相色譜儀,記錄色譜。供試品溶液色譜圖中如有雜質(zhì)峰,按歸一化法計(jì)算,單個(gè)雜質(zhì)峰面積不得大于總峰面積的0.5%,各雜質(zhì)峰面積的和不得大于總峰面積的2.0%。
對(duì)全國(guó)8個(gè)生產(chǎn)廠家的41批樣品按擬定的有關(guān)物質(zhì)方法測(cè)定,結(jié)果顯示,41批樣品中均檢查出雜質(zhì)峰,檢出率為100.0%,41批樣品中總雜質(zhì)峰的峰面積均在規(guī)定限度(2.0%)內(nèi),單個(gè)雜質(zhì)峰的峰面積均在規(guī)定限度(0.5%)內(nèi),結(jié)果見表1。
3 討論
3.1 雜質(zhì)限度的選擇
USP及BP收載的鹽酸金剛烷胺原料藥采用氣相色譜法測(cè)定有關(guān)物質(zhì),限度規(guī)定單個(gè)未知雜質(zhì)不得過0.3%,所有雜質(zhì)總量不得過1.0%;《中國(guó)藥典》2010年版二部中鹽酸金剛烷胺原料藥有關(guān)物質(zhì)的限度規(guī)定單個(gè)雜質(zhì)峰面積不得大于總峰面積的0.3%,各雜質(zhì)峰面積的和不得大于總峰面積的1.0%。考慮片劑中有關(guān)物質(zhì)可能增加,故擬定鹽酸金剛烷胺片有關(guān)物質(zhì)的限度為:?jiǎn)蝹€(gè)雜質(zhì)峰面積不得大于總峰面積的0.5%,各雜質(zhì)峰面積的和不得大于總峰面積的2.0%。
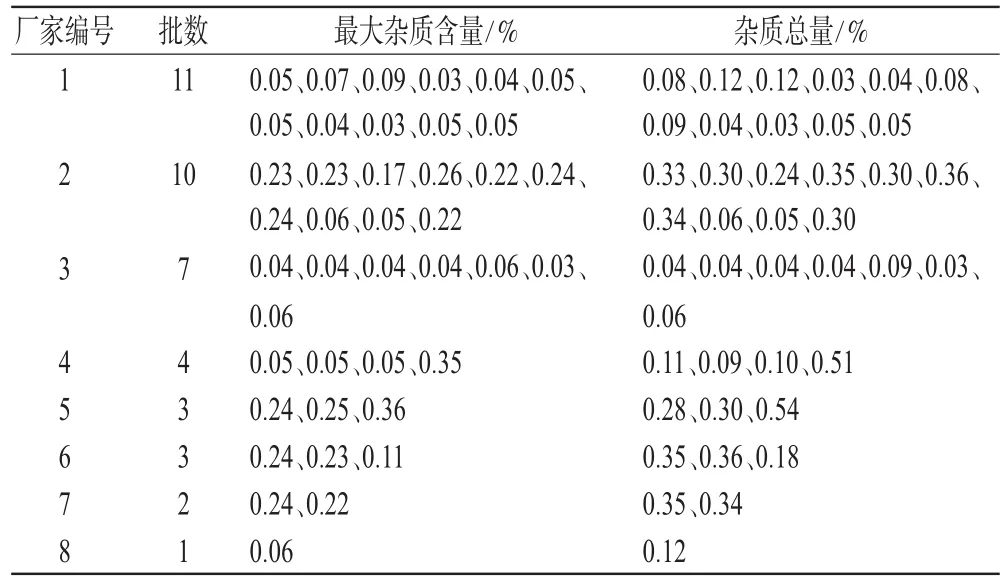
表1 41批樣品中有關(guān)物質(zhì)含量測(cè)定結(jié)果Tab 1 Determination results of related substances in 41 batches of samples
3.2 檢測(cè)方法的選擇
筆者曾嘗試采用高效液相-紫外分光光度法(HPLC-UV法)和高效液相-蒸發(fā)光散射(HPLC-ELSD)法進(jìn)行測(cè)定。但由于鹽酸金剛烷胺紫外最大吸收波長(zhǎng)為210 nm,屬于末端吸收,基線噪音大,故不適合采用HPLC-UV法;鹽酸金剛烷胺為水溶性化合物,采用HPLC-ELSD法測(cè)定,其在色譜柱上的保留時(shí)間短,雜質(zhì)峰與鹽酸金剛烷胺峰不能完全分離。經(jīng)方法學(xué)驗(yàn)證,本文建立的氣相色譜法測(cè)定鹽酸金剛烷胺片的有關(guān)物質(zhì)專屬性強(qiáng)、準(zhǔn)確,可有效地控制產(chǎn)品質(zhì)量。
3.3 測(cè)定結(jié)果分析
鹽酸金剛烷胺片廠家編號(hào)為2、5、6、7的樣品單個(gè)雜質(zhì)量較高,范圍在0.11%~0.36%;廠家編號(hào)為1、4、8的樣品單個(gè)雜質(zhì)量較低,范圍在0.03%~0.09%;廠家編號(hào)為3的樣品單個(gè)雜質(zhì)量總體較低,但有1批較高。說明建立的有關(guān)物質(zhì)測(cè)定方法對(duì)鹽酸金剛烷胺片生產(chǎn)處方的合理性、生產(chǎn)工藝的穩(wěn)定性均可良好監(jiān)控。
[1] 國(guó)家藥典委員會(huì)編.中華人民共和國(guó)藥典(二部)[S].2005年版.北京:化學(xué)工業(yè)出版社,2005:538.
[2] 國(guó)家藥典委員會(huì)編.中華人民共和國(guó)藥典(二部)[S].2010年版.北京:中國(guó)醫(yī)藥科技出版社,2010:737.
[3] The United States Pharmacopeial Convention.The United States Pharmacopeial[S].Rockville:The United States Pharmacopeial Convention,2009:1 054.
[4] The Recommendation of the Commission on Human Medicines.British Pharmacopoeia[S].London:British Pharmacopoeia Commission Office,2009:262.
[5] 許晉星.RP-HPLC法測(cè)定馬來酸桂哌齊特片中有關(guān)物質(zhì)的含量[J].中國(guó)藥房,2009,20(1):59.